文档内容
2024-2025 学年高二化学上学期第一次月考卷
一、选择题:本题共13个小题,每小题3分,共39分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.燃料电池能量转化效率高、环境污染少,运行质量高。下列物质均可用作燃料电池的燃料,其中能实
现碳中和目标的是( )
A.甲醇 B.天然气 C.氢气 D.一氧化碳
【答案】C
【解析】实现碳中和目标需要减少二氧化碳的排放,所以A B D错误,C正确;选C。
2.光合作用是生物体糗以生存和繁衍的基础,其反应为 。下列说法正确的是
( )
A.该反应为置换反应 B.该反应
C. 是还原产物 D.CO 属于电解质
2
【答案】B
【解析】反应物中没有单质参加,该反应不是置换反应,A错误;葡萄糖燃烧放热,因此其逆反应吸收
热量 ,B正确;氧元素化合价升高,是氧化产物,C错误;CO 溶于水不能自身电离,属于非电
2
解质,D错误。
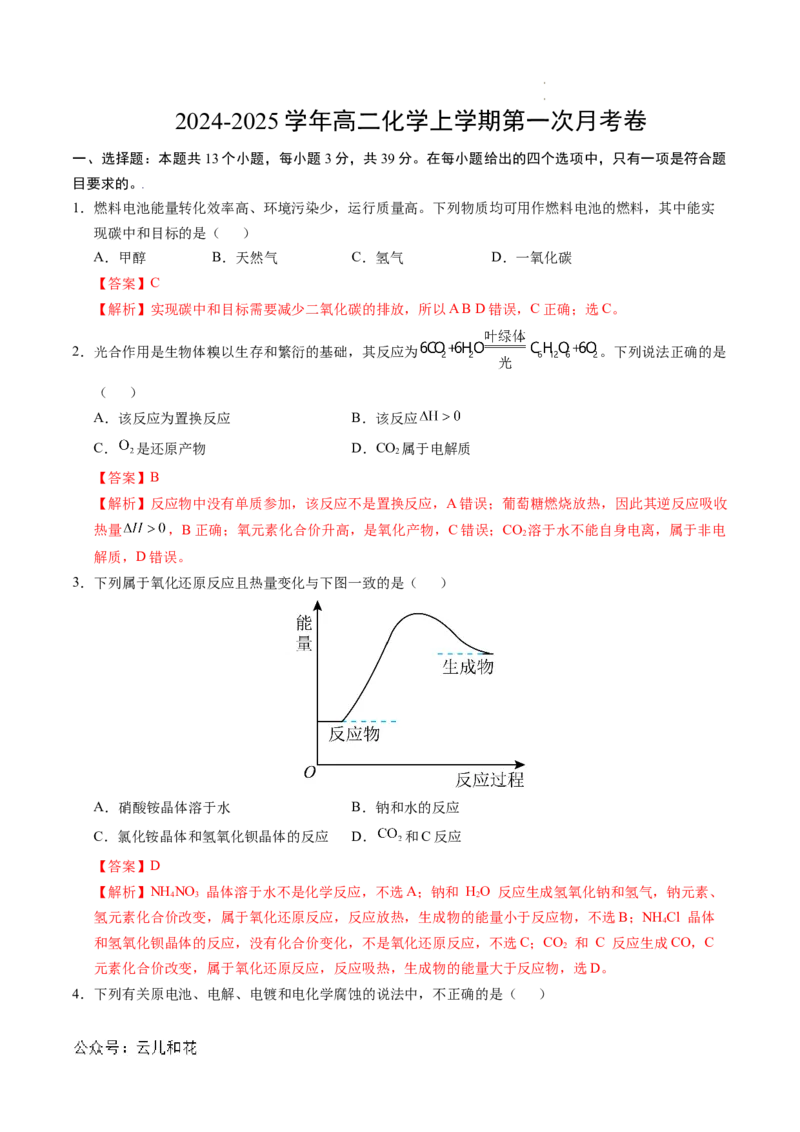
3.下列属于氧化还原反应且热量变化与下图一致的是( )
A.硝酸铵晶体溶于水 B.钠和水的反应
C.氯化铵晶体和氢氧化钡晶体的反应 D. 和C反应
【答案】D
【解析】NH NO 晶体溶于水不是化学反应,不选A;钠和 HO 反应生成氢氧化钠和氢气,钠元素、
4 3 2
氢元素化合价改变,属于氧化还原反应,反应放热,生成物的能量小于反应物,不选B;NH Cl 晶体
4
和氢氧化钡晶体的反应,没有化合价变化,不是氧化还原反应,不选C;CO 和 C 反应生成CO,C
2
元素化合价改变,属于氧化还原反应,反应吸热,生成物的能量大于反应物,选D。
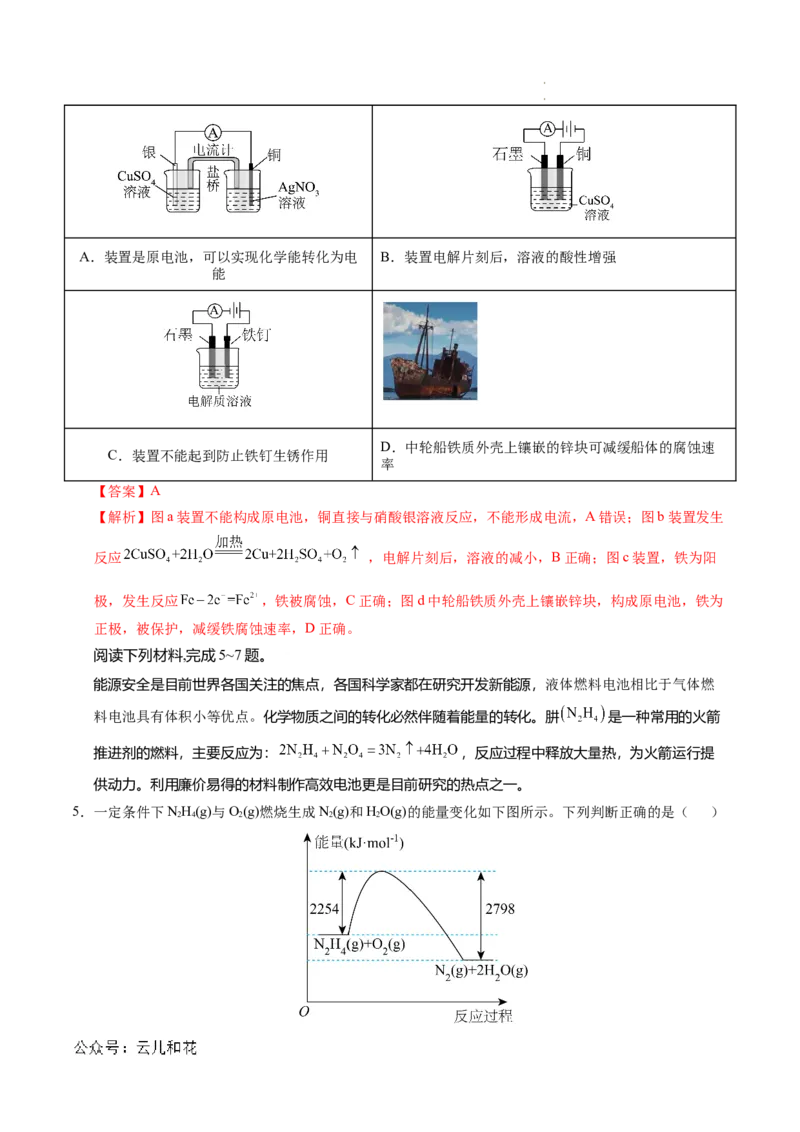
4.下列有关原电池、电解、电镀和电化学腐蚀的说法中,不正确的是( )
学科网(北京)股份有限公司 学科网(北京)股份有限公司A.装置是原电池,可以实现化学能转化为电 B.装置电解片刻后,溶液的酸性增强
能
D.中轮船铁质外壳上镶嵌的锌块可减缓船体的腐蚀速
C.装置不能起到防止铁钉生锈作用
率
【答案】A
【解析】图a装置不能构成原电池,铜直接与硝酸银溶液反应,不能形成电流,A错误;图b装置发生
反应 ,电解片刻后,溶液的减小,B正确;图c装置,铁为阳
极,发生反应 ,铁被腐蚀,C正确;图d中轮船铁质外壳上镶嵌锌块,构成原电池,铁为
正极,被保护,减缓铁腐蚀速率,D正确。
阅读下列材料,完成5~7题。
能源安全是目前世界各国关注的焦点,各国科学家都在研究开发新能源,液体燃料电池相比于气体燃
料电池具有体积小等优点。化学物质之间的转化必然伴随着能量的转化。肼 是一种常用的火箭
推进剂的燃料,主要反应为: ,反应过程中释放大量热,为火箭运行提
供动力。利用廉价易得的材料制作高效电池更是目前研究的热点之一。
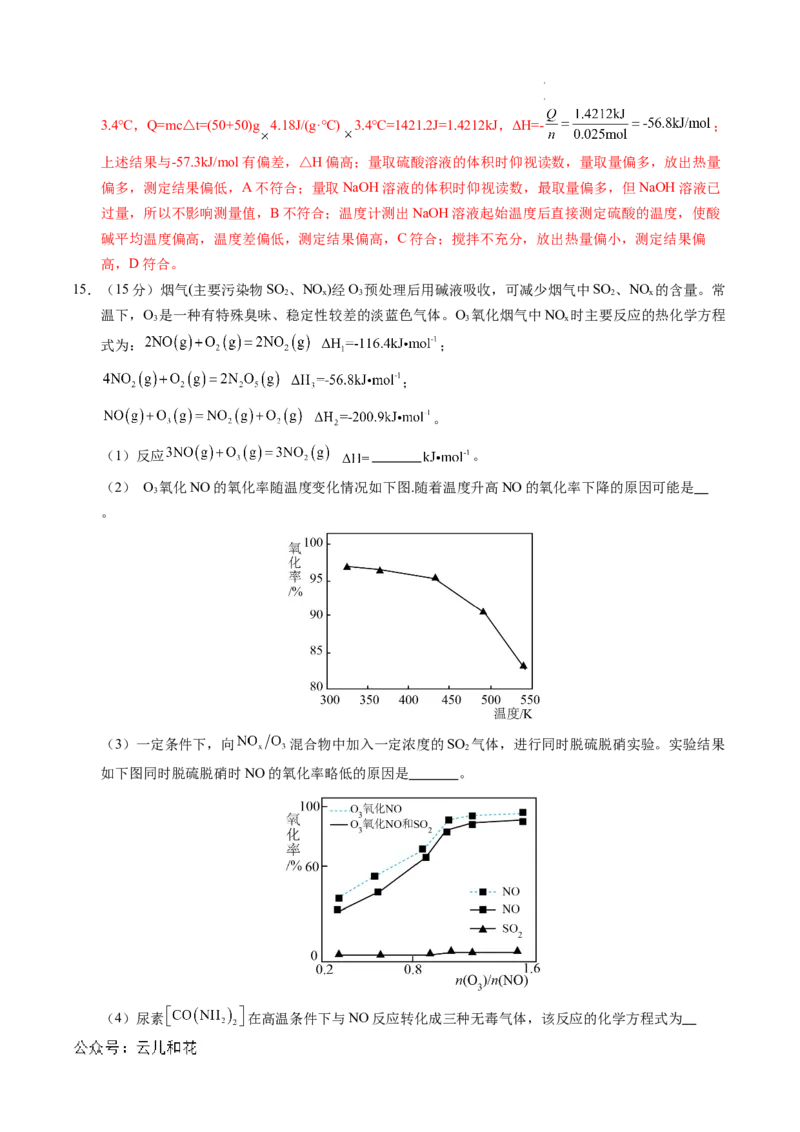
5.一定条件下NH(g)与O(g)燃烧生成N(g)和HO(g)的能量变化如下图所示。下列判断正确的是( )
2 4 2 2 2
学科网(北京)股份有限公司 学科网(北京)股份有限公司A.选择高效催化剂能有效降低该反应的焓变
B.由图可知断开1molN H(g)和1molO (g)中的化学键共需放出2254 kJ的热量
2 4 2
C.如果该反应使用等量的液态NH,则释放的热量更多
2 4
D.上述过程可表示为:NH(g)+O(g)=N(g)+2HO(g) =-544 kJ·mol-1
2 4 2 2 2
【答案】D
【解析】高效的催化剂能降低反应的活化能,加快反应速率,但是不改变反应的焓变,A错误;断开需
吸收热量而不是放出热量,B错误;液态NH 的能量比等量的气态NH 低,如果使用等量的液态
2 4 2 4
NH,则释放的热量更少,C错误;由图可知,该反应的ΔH=2254 kJ·mol-1-2798 kJ·mol-1=-544
2 4
kJ·mol-1,热化学方程式可以写成NH(g)+O(g)=N(g)+2HO(g) ΔH=-544 kJ·mol-1,D正确。
2 4 2 2 2
6.下列有关叙述正确的是( )
A.煤是一种化石燃料,其主要成分是碳的单质
B.燃料电池的能量转化率可达100%,属于环境友好电池
C.肼 具有还原性,可作为火箭推进剂的燃料
D.乙醇汽油是一种清洁能源,作为汽车燃料不会产生任何污染
【答案】C
【解析】煤是由有机物和少量无机物组成的复杂混合物,故其主要成分不是单质碳,A错误;燃料电池
是将化学能转变为电能的装置,还会伴有热能等能量的释放,能量转化率不会达100%,B错误;肼
具有还原性,能与氧化剂反应产生大量热量,可作为火箭推进剂的燃料,C正确;乙醇汽油是
一种清洁能源,燃烧过程中可能会产生CO等污染气体,D错误。
7.一种以液态肼(N H)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为
2 4
电解质溶液。下列关于该电池的叙述正确的是( )
A.NH 的结构式为:
2 4
B.a极的反应式:
C.b极发生氧化反应
D.放电时,电流从a极经过负载流向b极
【答案】B
【解析】该燃料电池中,负极上燃料失电子发生氧化反应,电极反应式为:NH+4OH--4e-
2 4
学科网(北京)股份有限公司 学科网(北京)股份有限公司=N ↑+4H O,正极上电池总反应为:NH+O =N ↑+2H O,结合离子的移动方向。根据N原子的成键特
2 2 2 4 2 2 2
点,NH 的结构式为: ,A错误;由分析可知a为负极,电极反应式为
2 4
,B正确;b为正极,发生还原反应,C错误;放电时,电流由正极流
向负极,即从b极经过负载流向a极,D错误。
8.在熔融盐体系中,B电极为石墨,A电极上利用 和 获得电池材料硅钛合金( ),装置如
题图所示。下列说法正确的是( )
A.电极B和电源负极相连,发生氧化反应
B.电极A的电极反应式:
C.电解时, 向B电极迁移
D.理论上每转移 电子,B电极上产生
【答案】C
【解析】在熔融盐体系中,B电极为石墨,石墨上O2-失去电子被氧化为氧气,则B为电解池阳极,A
为电解池阴极。根据分析,B为电解池阳极,与电源正极相连,发生氧化反应,A错误;在熔融盐体系
中,不能有水参与反应: ,B错误;电解过程中,阴离子向着阳极移
动,则O2-向B电极迁移,C正确;B电极上发生 ,理论上每转移1mol电子,产生
0.25mol氧气,但未指明是否为标准状况,则氧气体积不一定为5.6L ,D错误。
9.已知反应: ; ;
;则反应 的 为( )
A. B.
C. D.
【答案】D
学科网(北京)股份有限公司 学科网(北京)股份有限公司【解析】已知反应:① ;② ;③
,根据盖斯定律,将①×3+②×2-③×2,整理可得
,则△H=3△H+2△H -2△H,D正确,选D。
1 2 3
10.已知CH 的燃烧热为890.3 kJ·mol-1,下列化学反应表示正确的是( )
4
A.铅蓄电池的正极反应:Pb-2e-+ =PbSO
4
B.电解饱和NaCl溶液:2Na++2Cl- 2Na+Cl↑
2
C.CH 燃烧:CH(g)+2O(g)=CO (g)+2HO(g) ∆H=-890.3 kJ·mol-1
4 4 2 2 2
D.一定条件下NO 与NH 的反应:6NO +8NH 7N+12HO
2 3 2 3 2 2
【答案】D
【解析】铅蓄电池放电时PbO 在正极得到电子生成PbSO ,电极方程式为:PbO +2e-+4H++
2 4 2
=PbSO+2H O,A错误;电解饱和NaCl溶液的反应的离子方程式为2Cl-+2H O 2OH-+H ↑+Cl↑,
4 2 2 2 2
B错误;甲烷的燃烧热是1mol甲烷燃烧生成二氧化碳和液态水放出的能量,正确的热化学方程式为:
CH(g)+2O(g)=CO (g)+2HO(l) ∆H=-890.3 kJ·mol-1,C错误;一定条件下NO 与NH 反应生成氮
4 2 2 2 2 3
气和水,反应的化学方程式为:6NO +8NH 7N+12HO,D正确。
2 3 2 2
11.FeCl 溶液吸收HS气体后的再生过程可降解酸性污水中的硝酸盐,其电解工作原理如下图所示,下列
3 2
说法正确的是( )
A.a为电解池的阴极
B.电极b上的反应为2NO +10e-+6H O=N↑+12OH-
2 2
C.随着电解进行电解池中的H+向a极移动
D.反应池中发生的离子反应为:2Fe3++H S =2Fe2++S↓+2H+
2
学科网(北京)股份有限公司 学科网(北京)股份有限公司【答案】D
【解析】FeCl 具有强氧化性,反应池中 FeCl 溶液氧化 HS 生成 S 单质,发生的反应为
3 3 2
2FeCl +H S=2FeCl +2HCl+S↓,反应池中溶液M转移到电解池左池,由图可知,电解池左池产
3 2 2
生Fe3+,右池中NO转化为氮气,即左池中Fe2+失电子生成Fe3+,右池中NO发生得电子的还
原反应,则左池 a极为阳极、右池 b极为阴极,阳极反应式为 Fe2+-e-=Fe3+,阴极反应式为
2NO+10e-+12H+=6H O+N↑。由装置b电极上反应可知,NO发生得电子的还原反应,则电极b
2 2
为阴极,电极 a 为阳极, A 项错误;电极 b 为阴极,电极反应式为 2NO+10e-
+12H+=6H O+N↑,B项错误;电解池中阳离子向阴极移动,则 H+向b极移动,C项错误;由
2 2
分 析 可 知 , 反 应 池 中 FeCl 溶 液 氧 化 HS 生 成 S 单 质 , 发 生 的 反 应 为
3 2
2FeCl +H S=2FeCl +2HCl+S↓,离子方程式为:2Fe3++H S =2Fe2++S↓+2H+,D项正确。
3 2 2 2
12.通过以下反应可获得新型能源二甲醚(CHOCH )。下列说法不正确的是( )
3 3
①C(s)+ H O(g)=CO(g)+H (g) △H=a kJ/mol
2 2 1
②CO(g)+H O(g)=CO(g)+H(g) △H=b kJ/mol
2 2 2 2
③CO (g)+3H(g)=CH OH(g)+H O(g) △H=c kJ/mol
2 2 3 2 3
④2CH OH(g)=CH OCH (g)+HO(g) △H=d kJ/mol
3 3 3 2 4
A.反应①②为反应③提供原料气
B.反应③也是CO 资源化利用的方法之一
2
C.反应CHOH(g)= CHOCH (g)+ HO(l) △H= kJ/mol
3 3 3 2
D.反应2CO(g)+4H(g)=CH OCH (g)+ H O(g)的△H=(2b+2c+d) kJ/mol
2 3 3 2
【答案】C
【解析】反应①②可以生成CO 和H,为③提供原料气,A正确;反应③消耗二氧化碳生成燃料甲
2 2
醇,也是CO 资源化利用的方法之一,B正确;反应CHOH(g)= CHOCH (g)+ HO(g) 可由反应
2 3 3 3 2
④× 得到,故△H= kJ/mol,但是若水为液态,则会放出更多热量,C错误;反应2CO(g)
+4H (g)=CH OCH (g)+ H O(g)可由②×2+③×2+④,故其焓变△H=(2b+2c+d) kJ/mol,D正确。
2 3 3 2
13.工业上电解硝酸镍溶液,可以获取高纯镍和硝酸,其工作原理如图所示。
学科网(北京)股份有限公司 学科网(北京)股份有限公司下列说法正确的是( )
A.a为直流电源的正极,镍棒上发生的反应:Ni2+ + 2e−= Ni
B.A膜为阴离子交换膜,B膜为阳离子交换膜
C.电解一段时间后,乙池和丙池中的NO 的浓度均会增加
D.电解过程中,若有2 mol电子转移,理论上可获得11.2 L O
2
【答案】C
【解析】由已知条件知,工业上电解硝酸镍溶液,可以获取高纯镍和硝酸,故镍棒为阴极,发生反应
Ni2+ + 2e−= Ni,石墨为阳极,发生反应 。镍棒为阴极,则a为直流电源的负极,
A错误;甲池发生反应Ni2+ + 2e−= Ni,丙池发生反应 ,该装置还可以获取硝酸,
故A膜为阳离子交换膜,氢离子从丙池进入乙池,B膜为阴离子交换膜,硝酸根离子从甲池进入乙
池,获得硝酸,B错误;由B项知,电解一段时间后,乙池NO 的浓度会增加,丙池中的NO 物质
的量不变,但水被消耗,故NO 的浓度也会增加,C正确;没有标明标准状况,无法计算氧气的体
积,D错误。
二、非选择题:本题共4小题,共61分。
14.(17分)化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于放热反应的是_____(填字母)。
A.碳与水蒸气反应
B.铝和氧化铁反应
C.CaCO 受热分解
3
D.氢气还原三氧化钨制取钨E.锌与盐酸反应
(2)获取能量变化的途径
①已知:
化学键 Si-O Si-Cl H-H H-Cl Si-Si Si-C
键能(kJ·mol-1) a b c d e f
则:SiCl (g)+2H(g)= Si(s)+4HCl(g)的反应热 (已知1molSi中含有2molSi-Si)
4 2
②已知在常温常压下:
i、2CHOH(l)+3O (g)=2CO (g)+4HO(g)
3 2 2 2
ii、HO(l)=HO(g)
2 2
写出表示甲醇燃烧热的热化学方程式 。
③利用实验装置测量利用下图图装置测定中和热的实验步骤如下:
学科网(北京)股份有限公司 学科网(北京)股份有限公司①用量筒量取0.25mol/L的硫酸50mL倒入小烧杯中,测出硫酸溶液温度;
②用另一量筒量取50mL0.55mol/LNaOH溶液,并用同一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液的最高温度。
回答下列问题:
I.仪器a的名称为
Ⅱ.做了四次实验,并将实验数据记录如下:
起始温度t℃
1
终止温度t/℃
2
温度实验次数
HSO NaOH 平均值
2 4
1 26.2 26.0 26.1 29.5
2 27.0 27.4 27.2 32.3
3 25.9 25.9 25.9 29.2
4 26.4 26.2 26.3 29.8
近似认为0.55mol/LNaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容
c=4.18J/(g·℃),通过以上数据计算中和热ΔH= (结果保留小数点后一位)。上述结果与-57.3kJ/mol
有偏差的原因可能是 。
A.量取硫酸溶液的体积时仰视读数
B.量取NaOH溶液的体积时仰视读数
C.温度计测出NaOH溶液起始温度后直接测定硫酸的温度
D.搅拌不充分
【答案】(1)BE(3分)
(2) ①236 (3分) ② CHOH(l)+ O(g)=CO (g)+2HO(l) (3分)
3 2 2 2
③环形玻璃搅拌棒 (2分) -56.8kJ/mol (3分) CD(3分)
【解析】(1)碳与水蒸气反应是吸热反应,A不符合;铝和氧化铁反应是放热反应,B符合;CaCO
3
受热分解是吸热反应,C不符合;氢气还原三氧化钨制取钨是吸热反应,D不符合;锌与盐酸反应是
放热反应,E符合。(2)①1molSi中含有2molSi-Si键,结合表中键能及反应可知,SiCl (g)+2H(g)=
4 2
Si(g)+ 4HCl(g)的△H= (360kJ/mol) 4+(436kJ/mol) 2- (176kJ/mol) 2-(431kJ/ mol) 4=+236kJ/mol。。
②根据盖斯定律,由i- ii得反应2CHOH(l)+3O (g)=2CO (g)+4HO(l)
3 2 2 2
;故表示甲醇燃烧热的热化学方程式为CHOH(l)+ O(g)=CO (g)
3 2 2
+2H O(l) 。③I.仪器a的名称为环形玻璃搅拌棒;根据表中数据可知,四次实
2
验的温度差分别为3.4℃、5.1℃、3.3℃、3.5℃,第二次实验数据误差太大,舍去,则平均温度差为
学科网(北京)股份有限公司 学科网(北京)股份有限公司3.4℃,Q=mc△t=(50+50)g 4.18J/(g·℃) 3.4℃=1421.2J=1.4212kJ,ΔH=- ;
上述结果与-57.3kJ/mol有偏差,△H偏高;量取硫酸溶液的体积时仰视读数,量取量偏多,放出热量
偏多,测定结果偏低,A不符合;量取NaOH溶液的体积时仰视读数,最取量偏多,但NaOH溶液已
过量,所以不影响测量值,B不符合;温度计测出NaOH溶液起始温度后直接测定硫酸的温度,使酸
碱平均温度偏高,温度差偏低,测定结果偏高,C符合;搅拌不充分,放出热量偏小,测定结果偏
高,D符合。
15.(15分)烟气(主要污染物SO 、NO )经O 预处理后用碱液吸收,可减少烟气中SO 、NO 的含量。常
2 x 3 2 x
温下,O 是一种有特殊臭味、稳定性较差的淡蓝色气体。O 氧化烟气中NO 时主要反应的热化学方程
3 3 x
式为: ;
;
。
(1)反应 。
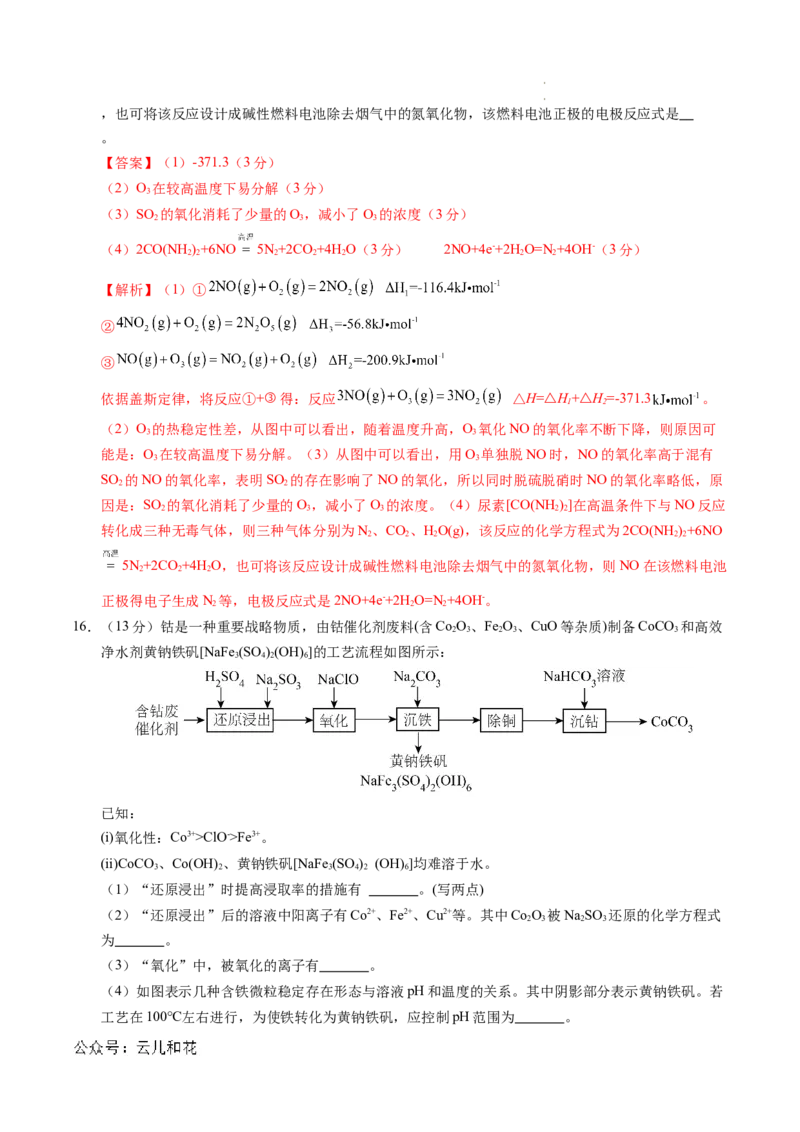
(2) O 氧化NO的氧化率随温度变化情况如下图.随着温度升高NO的氧化率下降的原因可能是
3
。
(3)一定条件下,向 混合物中加入一定浓度的SO 气体,进行同时脱硫脱硝实验。实验结果
2
如下图同时脱硫脱硝时NO的氧化率略低的原因是 。
(4)尿素 在高温条件下与NO反应转化成三种无毒气体,该反应的化学方程式为
学科网(北京)股份有限公司 学科网(北京)股份有限公司,也可将该反应设计成碱性燃料电池除去烟气中的氮氧化物,该燃料电池正极的电极反应式是
。
【答案】(1)-371.3(3分)
(2)O 在较高温度下易分解(3分)
3
(3)SO 的氧化消耗了少量的O,减小了O 的浓度(3分)
2 3 3
(4)2CO(NH)+6NO 5N+2CO +4H O(3分) 2NO+4e-+2H O=N+4OH-(3分)
2 2 2 2 2 2 2
【解析】(1)①
②
③
依据盖斯定律,将反应①+③得:反应 △H=△H+△H=-371.3 。
1 2
(2)O 的热稳定性差,从图中可以看出,随着温度升高,O 氧化NO的氧化率不断下降,则原因可
3 3
能是:O 在较高温度下易分解。(3)从图中可以看出,用O 单独脱NO时,NO的氧化率高于混有
3 3
SO 的NO的氧化率,表明SO 的存在影响了NO的氧化,所以同时脱硫脱硝时NO的氧化率略低,原
2 2
因是:SO 的氧化消耗了少量的O,减小了O 的浓度。(4)尿素[CO(NH)]在高温条件下与NO反应
2 3 3 2 2
转化成三种无毒气体,则三种气体分别为N、CO、HO(g),该反应的化学方程式为2CO(NH)+6NO
2 2 2 2 2
5N+2CO +4H O,也可将该反应设计成碱性燃料电池除去烟气中的氮氧化物,则NO在该燃料电池
2 2 2
正极得电子生成N 等,电极反应式是2NO+4e-+2H O=N+4OH-。
2 2 2
16.(13分)钴是一种重要战略物质,由钴催化剂废料(含Co O、Fe O、CuO等杂质)制备CoCO 和高效
2 3 2 3 3
净水剂黄钠铁矾[NaFe (SO )(OH) ]的工艺流程如图所示:
3 4 2 6
已知:
(i)氧化性:Co3+>ClO->Fe3+。
(ii)CoCO 、Co(OH) 、黄钠铁矾[NaFe (SO ) (OH) ]均难溶于水。
3 2 3 4 2 6
(1)“还原浸出”时提高浸取率的措施有 。(写两点)
(2)“还原浸出”后的溶液中阳离子有Co2+、Fe2+、Cu2+等。其中Co O 被NaSO 还原的化学方程式
2 3 2 3
为 。
(3)“氧化”中,被氧化的离子有 。
(4)如图表示几种含铁微粒稳定存在形态与溶液pH和温度的关系。其中阴影部分表示黄钠铁矾。若
工艺在100℃左右进行,为使铁转化为黄钠铁矾,应控制pH范围为 。
学科网(北京)股份有限公司 学科网(北京)股份有限公司(5) 可制备锂离子电池的电极材料钴酸锂 。一种锂离子电池装置如图所示,充放电
过程中,存在 与 之间的转化。放电时, 从A电极向B电极迁移,写出该电池放
电时的正极反应: ,若用该电池电解食盐水,当1molLi+通过隔膜时,电解池阴极收集到的气
体体积在标准状况下为 L。
【答案】(1)搅拌、升高温度、粉碎含钴废催化剂、增大HSO 、NaSO 溶液浓度(2分)
2 4 2 3
(2)Co O+ Na SO + 2H SO =2CoSO+ Na SO + 2H O(2分)
2 3 2 3 2 4 4 2 4 2
(3)Fe2+(2分)
(4)0.7~2.2(2分)
(5) +xe-+xLi+= (2分) 11.2(3分)
【解析】含钴废渣加入硫酸和还原剂亚硫酸钠,得到含Co2+、Fe2+、Cu2+的盐溶液,加入氧化剂次氯酸
钠将亚铁离子氧化为铁离子,加入碳酸钠将铁离子转化为黄钠铁矾沉淀,滤液除去铜后加入碳酸氢钠
得到CoCO 沉淀。(1)根据影响反应速率的因素,搅拌、升高温度、粉碎含钴废催化剂、增大
3
HSO 、NaSO 溶液浓度等都能加快“还原浸出”速率。(2)亚硫酸钠具有还原性,酸性条件下将三
2 4 2 3
价钴还原为二价钴,亚硫酸钠中硫化合价由+4变为+6,结合电子守恒,反应为Co O+ Na SO +
2 3 2 3
2HSO =2CoSO+ Na SO + 2H O。(3)“氧化”中,加入氧化剂次氯酸钠将亚铁离子氧化为铁离子,
2 4 4 2 4 2
Co2+不能被氧化,故为亚铁离子。(4)由图可知,工艺在100℃左右进行,为使铁转化为黄钠铁矾,
应控制pH范围为0.7~2.2。(5)放电时, 从A电极向B电极迁移,则A为负极、B为正极,该电
池放电时的正极反应为 得到电子发生还原反应转化为 : +xe-+xLi+=
;若用该电池电解食盐水,当1molLi+通过隔膜时,则电路中转移电子1mol,电解池阴极反应为
学科网(北京)股份有限公司 学科网(北京)股份有限公司,则收集到的0.5mol氢气,气体体积在标准状况下为11.2L。
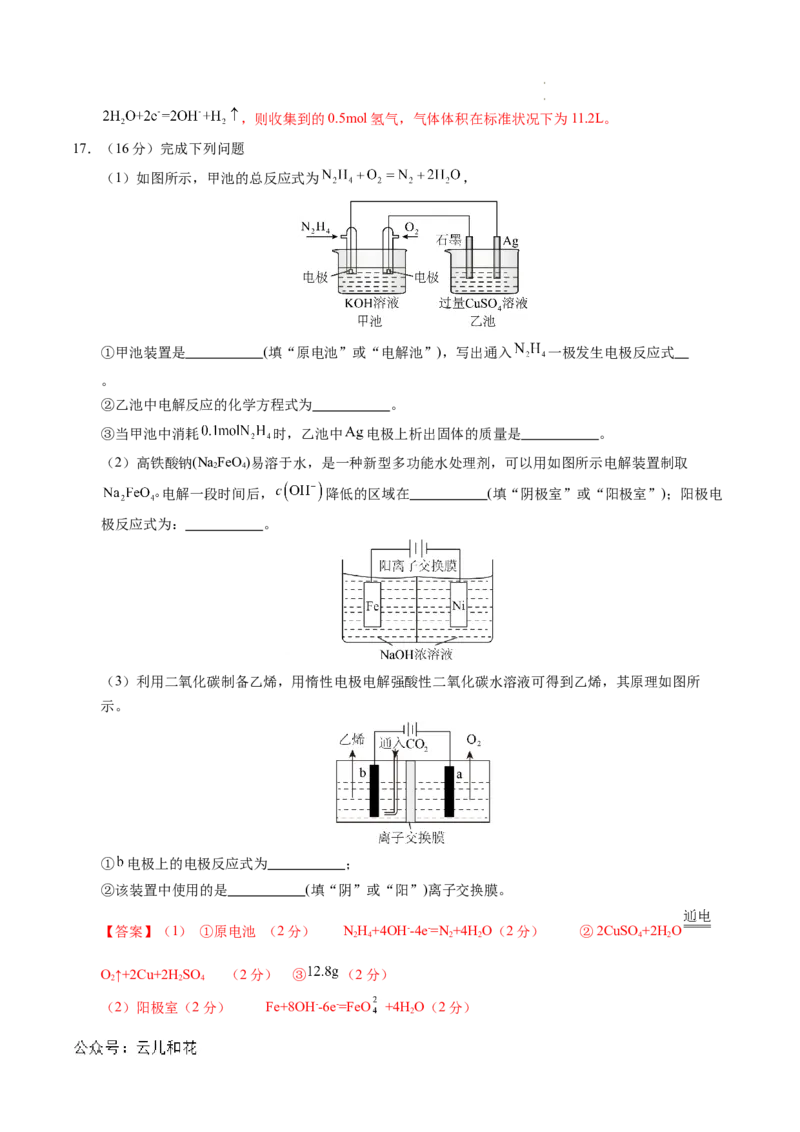
17.(16分)完成下列问题
(1)如图所示,甲池的总反应式为 ,
①甲池装置是 (填“原电池”或“电解池”),写出通入 一极发生电极反应式
。
②乙池中电解反应的化学方程式为 。
③当甲池中消耗 时,乙池中 电极上析出固体的质量是 。
(2)高铁酸钠(Na FeO)易溶于水,是一种新型多功能水处理剂,可以用如图所示电解装置制取
2 4
电解一段时间后, 降低的区域在 (填“阴极室”或“阳极室”);阳极电
极反应式为: 。
(3)利用二氧化碳制备乙烯,用惰性电极电解强酸性二氧化碳水溶液可得到乙烯,其原理如图所
示。
① 电极上的电极反应式为 ;
②该装置中使用的是 (填“阴”或“阳”)离子交换膜。
【答案】(1) ①原电池 (2分) NH+4OH--4e-=N +4H O(2分) ②2CuSO +2H O
2 4 2 2 4 2
O↑+2Cu+2H SO (2分) ③ (2分)
2 2 4
(2)阳极室(2分) Fe+8OH--6e-=FeO +4H O(2分)
2
学科网(北京)股份有限公司 学科网(北京)股份有限公司(3) ① (2分) ②阳(2分)
【解析】(1)①甲池的总反应式为NH+O=N +2HO,可以将化学能转化为电能,故甲池为原电
2 4 2 2 2
池;通入NH 的电极为负极,其电极方程式为NH+4OH--4e-=N +4H O;②乙池中,与负极相连的Fe
2 4 2 4 2 2
电极为阴极,与通入O 的正极相连的石墨电极为阳极,电解质为硫酸铜溶液,则阴极生成Cu,阳极
2
生成O,电解反应的化学方程式为:2CuSO +2H O O↑+2Cu+2H SO ;③甲池中每消耗0.1 mol
2 4 2 2 2 4
NH,转移电子0.4mol,乙池电极上会析出Cu0.2mol,质量为0.2mol×64g/mol=12.8g。(2)阳极是活
2 4
泼电极Fe,Fe失去电子生成FeO 的电极方程式为Fe+8OH--6e-=FeO +4H O,同时消耗OH-使
2
c(OH-)降低,即c(OH-)降低的区域在阳极室。(3)① b电极与电源的负极相连,作阴极,溶液中的
CO 得到电子被还原转化为乙烯,溶液显酸性,因此阴极上的电极反应式为2CO+12e-
2 2
+12H+=C H+4H O;②为了防止OH-与阴极区的CO 反应,因此该装置中使用的是阳离子交换膜。
2 4 2 2
学科网(北京)股份有限公司 学科网(北京)股份有限公司