2024-2025 学年度第一学期第四次阶段性检测高二化学
注意事项:
1.本试卷满分100分,考试时间75分钟。
2.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
3.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。回答非选择题时,
将答案直接写在答题卡上。
4.考试结束后将答题卡收回。
第 I 卷(选择题)
一.选择题(共16小题,每小题3分,共48分)
1.已知反应:① ,②稀溶液中,
下列结论正确的是( )
A.碳的燃烧热
B.碳的燃烧热
C. 稀溶液与足量浓 溶液反应的反应热小于
D. 的稀溶液与含 的稀溶液反应放出的热量为
2.已知:CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) H1=-akJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(g) H2=-bkJ·mol△-1
CH4(g)+2O2(g)=CO2(g)+2H2O(1) △H3=-ckJ·mol-1
则下列叙述正确的是( ) △
A.由上述热化学方程式可知 H2< H3
B.甲烷的燃烧热为bkJ·mol-l△ △
C. 2CH3OH(g)=2CH4(g)+O2(g) H=2(b-a)kJ/mol-1
D.当甲醇和甲烷物质的量之比为△1:2时,其完全燃烧生成CO2 和H2O(l)时,放出的热量为QkJ,则该混
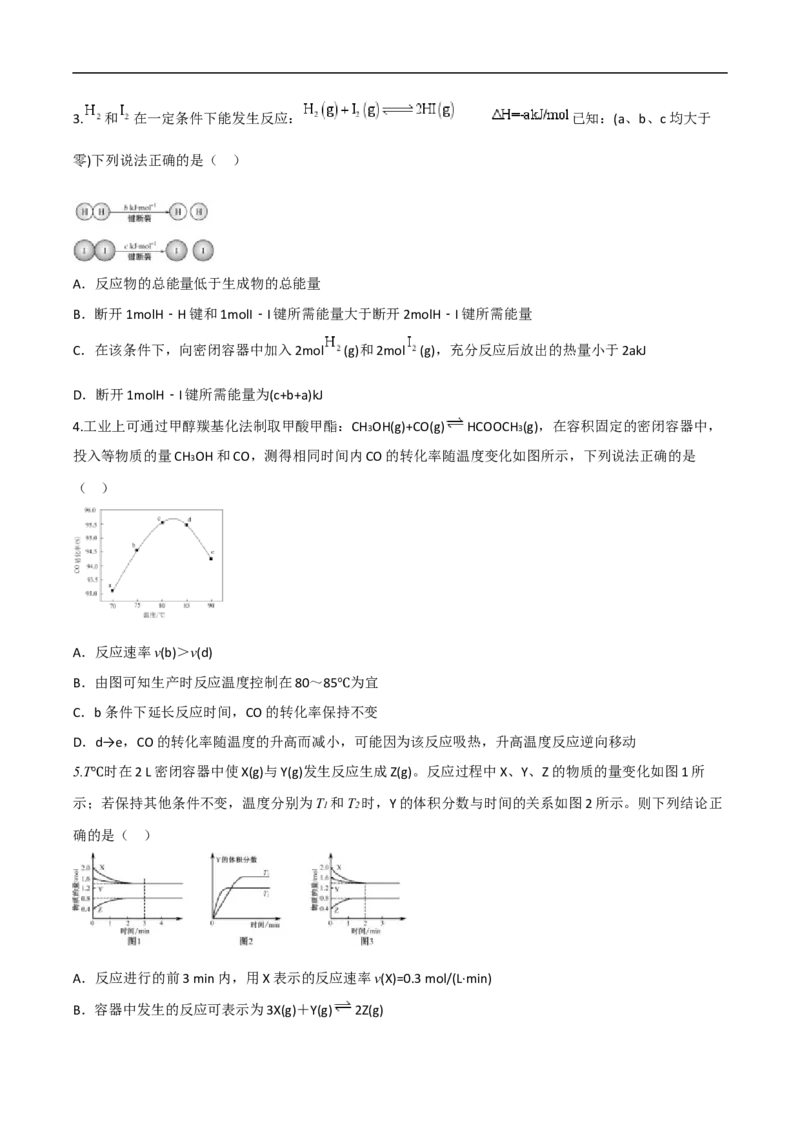
合物中甲醇的物质的量为Q/(a+2b)mol3. 和 在一定条件下能发生反应: 已知:(a、b、c均大于
零)下列说法正确的是( )
A.反应物的总能量低于生成物的总能量
B.断开1molH﹣H键和1molI﹣I键所需能量大于断开2molH﹣I键所需能量
C.在该条件下,向密闭容器中加入2mol (g)和2mol (g),充分反应后放出的热量小于2akJ
D.断开1molH﹣I键所需能量为(c+b+a)kJ
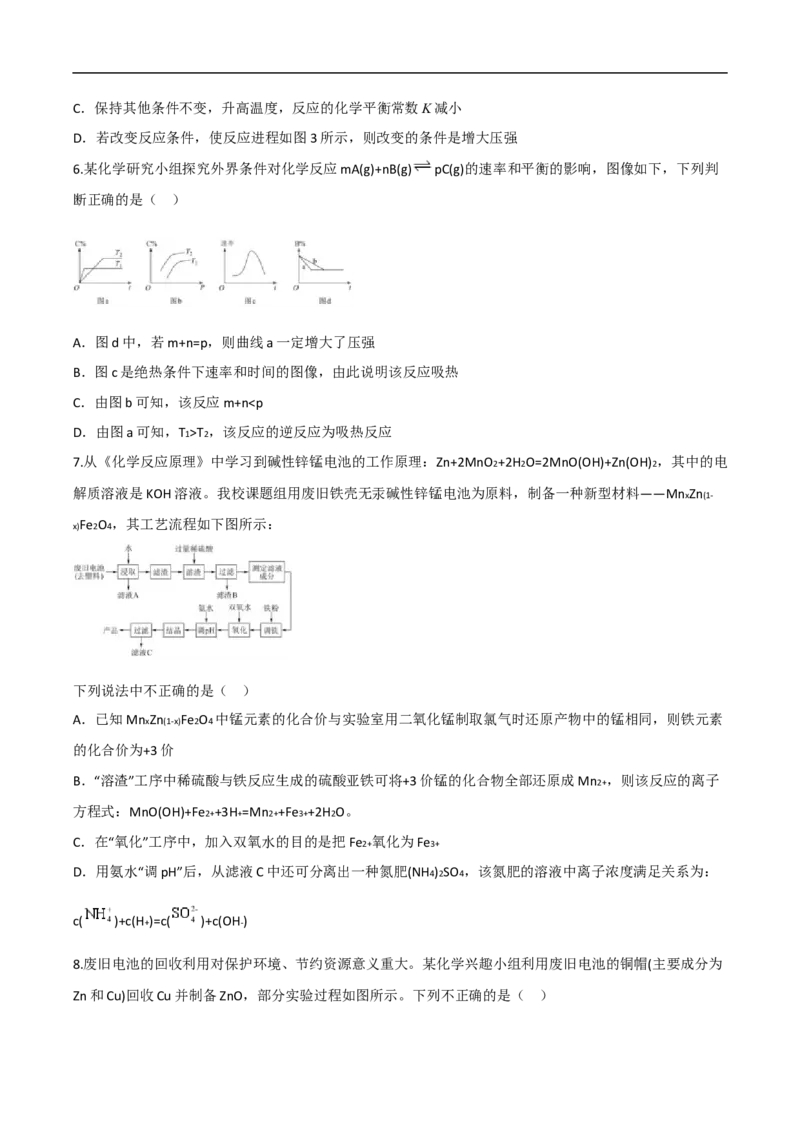
4.工业上可通过甲醇羰基化法制取甲酸甲酯:CH3OH(g)+CO(g) HCOOCH3(g),在容积固定的密闭容器中,
投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图所示,下列说法正确的是
( )
A.反应速率v(b)>v(d)
B.由图可知生产时反应温度控制在80~85 为宜
C.b条件下延长反应时间,CO的转化率保持℃不变
D.d→e,CO的转化率随温度的升高而减小,可能因为该反应吸热,升高温度反应逆向移动
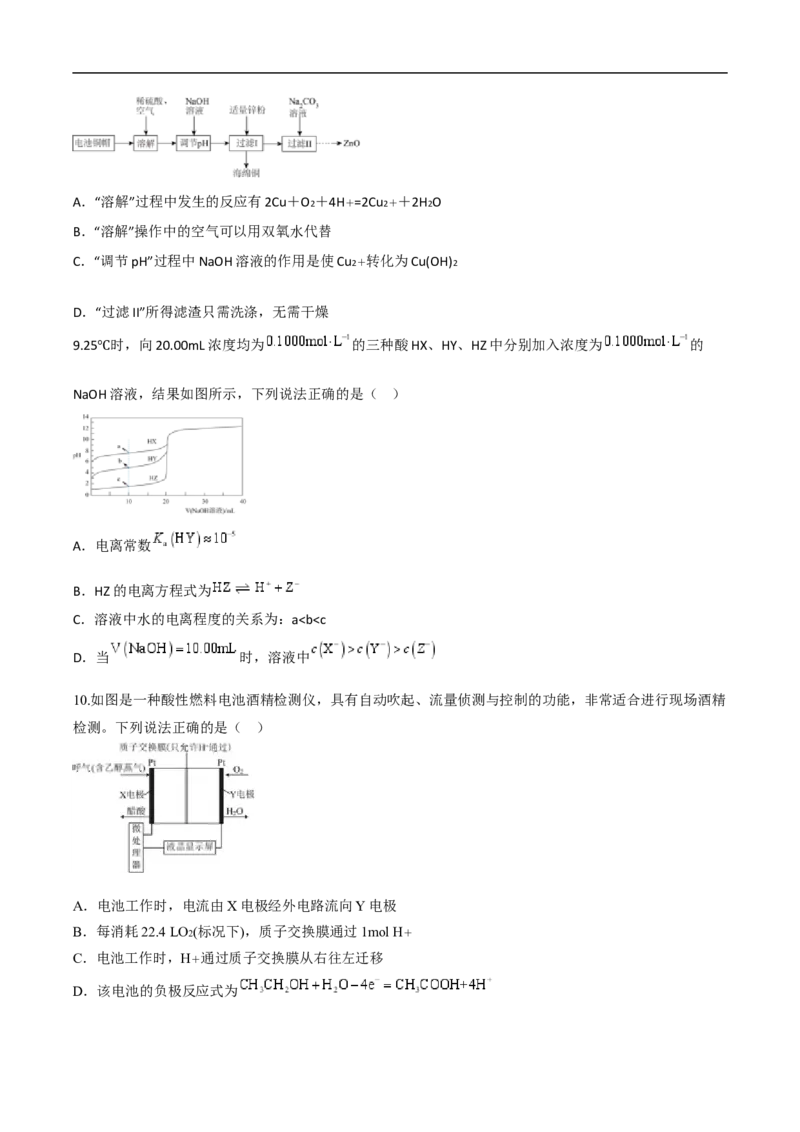
5.T 时在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图1所
示;℃若保持其他条件不变,温度分别为T1 和T2 时,Y的体积分数与时间的关系如图2所示。则下列结论正
确的是( )
A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol/(L·min)
B.容器中发生的反应可表示为3X(g)+Y(g) 2Z(g)C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
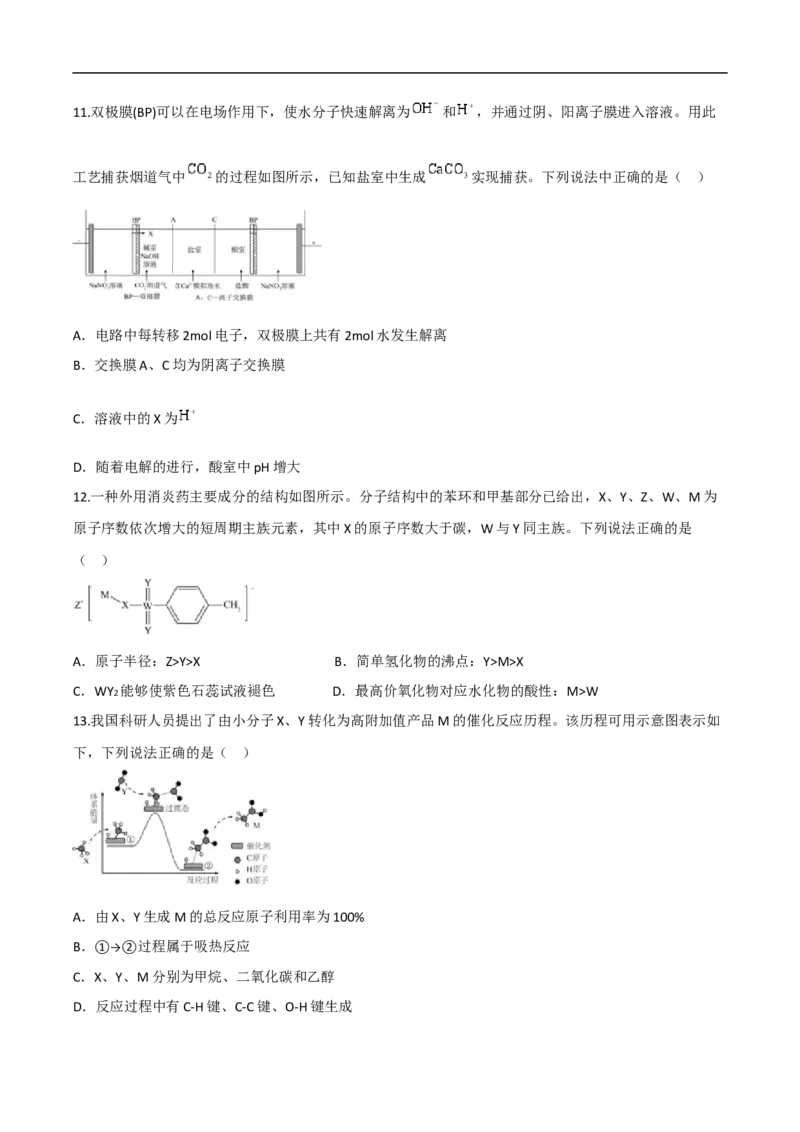
6.某化学研究小组探究外界条件对化学反应mA(g)+nB(g) pC(g)的速率和平衡的影响,图像如下,下列判
断正确的是( )
A.图d中,若m+n=p,则曲线a一定增大了压强
B.图c是绝热条件下速率和时间的图像,由此说明该反应吸热
C.由图b可知,该反应m+n
T2 ,该反应的逆反应为吸热反应
7.从《化学反应原理》中学习到碱性锌锰电池的工作原理:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2 ,其中的电
解质溶液是KOH溶液。我校课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料——MnxZn(1-
x)Fe2O4 ,其工艺流程如下图所示:
下列说法中不正确的是( )
A.已知MnxZn(1-x)Fe2O4 中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中的锰相同,则铁元素
的化合价为+3价
B.“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+ ,则该反应的离子
方程式:MnO(OH)+Fe2++3H+=Mn2++Fe3++2H2O。
C.在“氧化”工序中,加入双氧水的目的是把Fe2+ 氧化为Fe3+
D.用氨水“调pH”后,从滤液C中还可分离出一种氮肥(NH4)2SO4 ,该氮肥的溶液中离子浓度满足关系为:
c( )+c(H+)=c( )+c(OH-)
8.废旧电池的回收利用对保护环境、节约资源意义重大。某化学兴趣小组利用废旧电池的铜帽(主要成分为
Zn和Cu)回收Cu并制备ZnO,部分实验过程如图所示。下列不正确的是( )A.“溶解”过程中发生的反应有2Cu+O2 +4H+=2Cu2+ +2H2O
B.“溶解”操作中的空气可以用双氧水代替
C.“调节pH”过程中NaOH溶液的作用是使Cu2+ 转化为Cu(OH)2
D.“过滤II”所得滤渣只需洗涤,无需干燥
9.25 时,向20.00mL浓度均为 的三种酸HX、HY、HZ中分别加入浓度为 的
℃
NaOH溶液,结果如图所示,下列说法正确的是( )
A.电离常数
B.HZ的电离方程式为
C.溶液中水的电离程度的关系为:aY>X B.简单氢化物的沸点:Y>M>X
C.WY2 能够使紫色石蕊试液褪色 D.最高价氧化物对应水化物的酸性:M>W
13.我国科研人员提出了由小分子X、Y转化为高附加值产品M的催化反应历程。该历程可用示意图表示如
下,下列说法正确的是( )
A.由X、Y生成M的总反应原子利用率为100%
B.①→②过程属于吸热反应
C.X、Y、M分别为甲烷、二氧化碳和乙醇
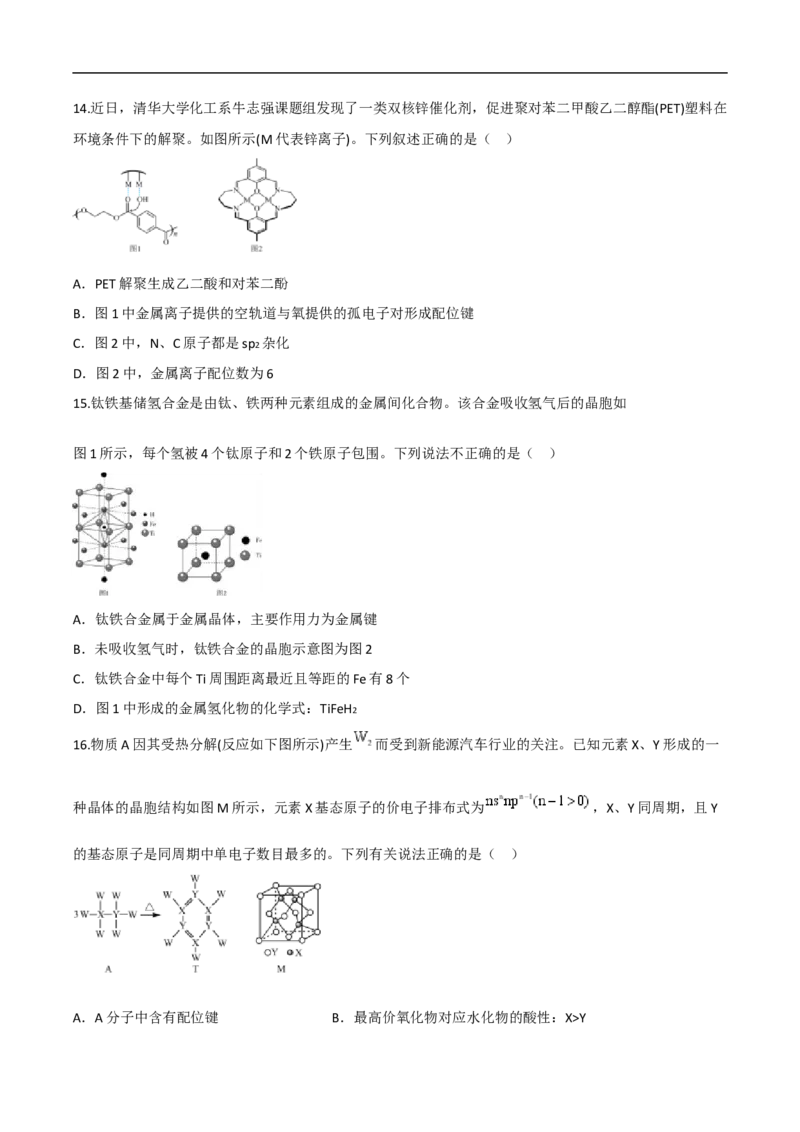
D.反应过程中有C-H键、C-C键、O-H键生成14.近日,清华大学化工系牛志强课题组发现了一类双核锌催化剂,促进聚对苯二甲酸乙二醇酯(PET)塑料在
环境条件下的解聚。如图所示(M代表锌离子)。下列叙述正确的是( )
A.PET解聚生成乙二酸和对苯二酚
B.图1中金属离子提供的空轨道与氧提供的孤电子对形成配位键
C.图2中,N、C原子都是sp2 杂化
D.图2中,金属离子配位数为6
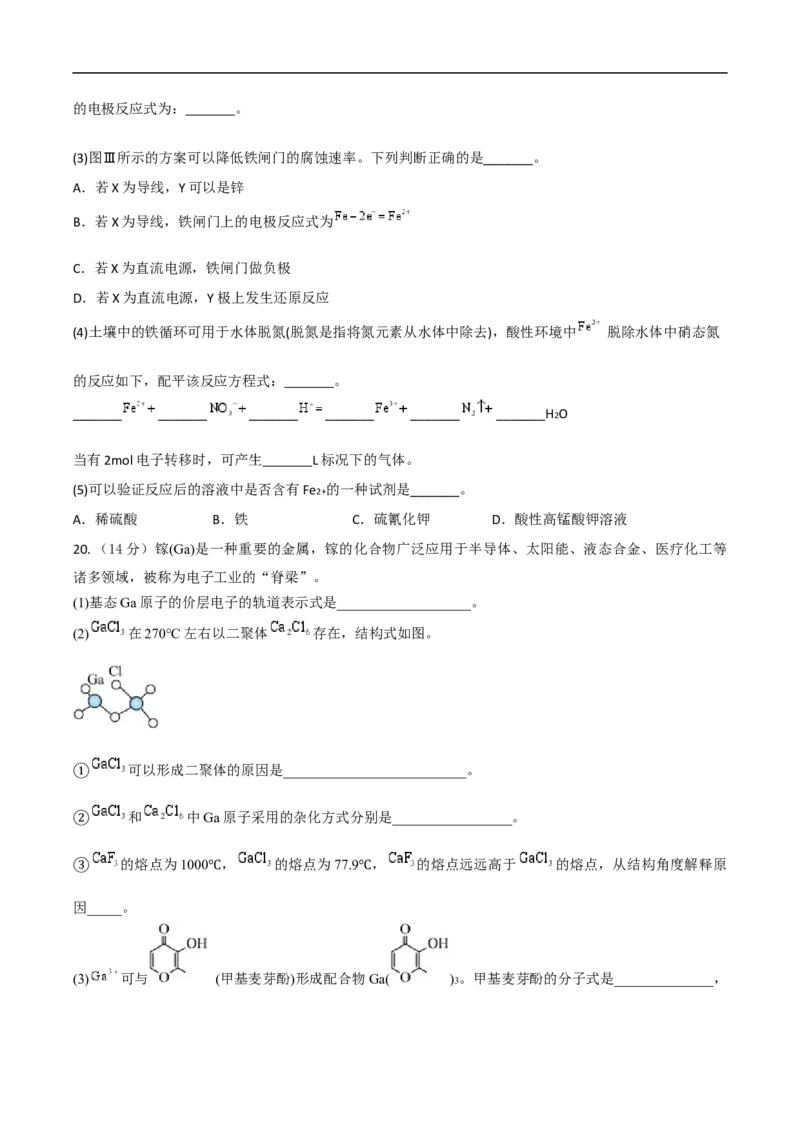
15.钛铁基储氢合金是由钛、铁两种元素组成的金属间化合物。该合金吸收氢气后的晶胞如
图1所示,每个氢被4个钛原子和2个铁原子包围。下列说法不正确的是( )
A.钛铁合金属于金属晶体,主要作用力为金属键
B.未吸收氢气时,钛铁合金的晶胞示意图为图2
C.钛铁合金中每个Ti周围距离最近且等距的Fe有8个
D.图1中形成的金属氢化物的化学式:TiFeH2
16.物质A因其受热分解(反应如下图所示)产生 而受到新能源汽车行业的关注。已知元素X、Y形成的一
种晶体的晶胞结构如图M所示,元素X基态原子的价电子排布式为 ,X、Y同周期,且Y
的基态原子是同周期中单电子数目最多的。下列有关说法正确的是( )
A.A分子中含有配位键 B.最高价氧化物对应水化物的酸性:X>YC.T分子不可能所有原子共平面 D.晶体M中,X的配位数为12
第 II 卷(非选择题)
二、非选择题(共52分)
17.(12分)在T 时,向1L固定体积的密闭容器M中加入2molX和1molY,发生如下反应:
℃
;该反应达到平衡后,放出的热量为 ,物质X
的转化率为 ;若平衡后再升高温度,混合气体的平均相对分子质量减小。
请回答下列问题:
(1)化学计量数 的值为 。
(2)下列能说明该反应达到了化学平衡状态的是 。
a.容器内压强一定 b.容器内气体的密度一定
c.容器内Z的分子数一定 d.容器内气体的质量一定
(3)维持T 温度不变,若起始时向容器M中加入2molX、1molY和1molAr(稀有气体不参与反应),则反应达
到平衡后℃放出的热量是 。
(4)维持T 温度不变,若在一个和原容器体积相等的恒压容器N中加入2molX和1molY,发生题给反应并
达到平衡℃,则 (填“M”或“N”)容器中的反应先达到平衡状态,容器中X的质量分数M
N(填“>”、“<”或“=”)。
(5)已知:该反应的平衡常数随温度的变化情况如表所示:
温度/ 200 250 300 350
℃
平衡常数K 9.94 5.2 1 0.5
若在某温度下,2molX和1molY在容器M中反应并达到平衡,X的平衡转化率为50%,则该温度为
。
℃(6)维持T 温度不变,若起始时向容器M中加入4molX和6molY,反应达到平衡时容器内的分子数目减少
10%,则反℃应中放出的热量为 kJ。
18.(12分)Ⅰ.常温下,如果取0.2 mol/LCH3COOH溶液与0.2 mol/L NaOH溶液等体积混合(忽略混合后溶液
体积的变化),测得混合溶液的pH=9,试回答以下问题:
(1)混合溶液的pH=9的原因是:(用离子方程式表示) 。
(2)该混合溶液中由水电离出的c(H+)和pH=9的NaOH溶液中由水电离出c(H+)的比值为 。
(3)求该混合溶液中下列算式的计算结果:c(Na+)-c(CH3COO-)= mol/L(代入数据,列出算式即可)
c(OH-)-c(CH3COOH)= moL/L。
Ⅱ.(4)25 下,向20 mL 0.1 mol•L-1 Na2CO3 溶液中逐滴加入0.1 mol•L-1 HCl溶液40 mL,溶液中含碳元素的各
种微粒(C℃O2 因逸出未画出)物质的量分数(纵轴),随溶液pH变化的部分情况
如图所示。回答下列问题:
①在同一溶液中,H2CO3 、HCO 、CO (填“能”或“不能”)大量共存;
②当pH=7时,溶液中Na+ 、Cl- 、HCO 三种离子的浓度大小关系为 ;
③已知在25 时,CO 的第一步水解常数Kh1=2.0×10-4 ,当溶液中c(HCO ) c(CO )=2 1时,溶液的pH=
℃ ∶ ∶
。
(5)下列固体物质溶于水,再将其溶液加热,蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是
(填字母序号)。
①胆矾 ②氯化铝 ③硫酸铝 ④Na2CO3 ⑤NaHCO3 ⑥高锰酸钾
A.③④ B.①③④ C.①②③④⑤ D.全部
19.(14分)海水资源可以有效利用,有时也会给生产、生活带来困扰,读图,回答问题:
(1)氯碱工业能耗大,通过如图I改进的设计,可大幅度降低能耗,不正确的是_______。
A.电极A接电源正极,发生氧化反应
B.电极B的电极反应式为: =
C.应选用阳离子交换膜,在右室获得浓度较高的NaOH溶液
D.改进设计中通过提高电极B上反应物的氧化性来降低电解电压,减少能耗
(2)图Ⅱ中铁棒浸入一段时间之后发现,越靠近烧杯底部发生电化学腐蚀就越轻微,则发生该腐蚀时,正极的电极反应式为: 。
(3)图Ⅲ所示的方案可以降低铁闸门的腐蚀速率。下列判断正确的是_______。
A.若X为导线,Y可以是锌
B.若X为导线,铁闸门上的电极反应式为
C.若X为直流电源,铁闸门做负极
D.若X为直流电源,Y极上发生还原反应
(4)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),酸性环境中 脱除水体中硝态氮
的反应如下,配平该反应方程式: 。
_______ _______ _______ _______ _______ _______H2O
当有2mol电子转移时,可产生 L标况下的气体。
(5)可以验证反应后的溶液中是否含有Fe2+ 的一种试剂是_______。
A.稀硫酸 B.铁 C.硫氰化钾 D.酸性高锰酸钾溶液
20.(14分)镓(Ga)是一种重要的金属,镓的化合物广泛应用于半导体、太阳能、液态合金、医疗化工等
诸多领域,被称为电子工业的“脊梁”。
(1)基态Ga原子的价层电子的轨道表示式是___________________。
(2) 在270°C左右以二聚体 存在,结构式如图。
可以形成二聚体的原因是__________________________。
①
和 中Ga原子采用的杂化方式分别是_________________。
②
的熔点为1000 , 的熔点为77.9 , 的熔点远远高于 的熔点,从结构角度解释原
③ ℃ ℃
因_____。
(3) 可与 (甲基麦芽酚)形成配合物Ga( )3 。甲基麦芽酚的分子式是______________,甲基麦芽酚中,与 形成配位键的原子是________。高二化学参考答案
1-5CCCBB 6-10CDCAC 11-16BDABDC
17.【答案】
(1)1 (2)ac (3)
(4)N > (5)350 (6)0.5
18.【答案】
(1) CH3COO-+H2O CH3COOH+OH- (2)104 :1 (3)10-5-10-9 10-9
(4)不能 c(Na ⇌ +)>c(Cl-)>c(HCO ) 10 (5)A
19.【答案】
(1)B (2)O2 +4e- +2H2O=4OH- (3)A
(4)10Fe2+ + 2NO + 12H+=10Fe3++1N2↑+6H2O 4.48L (5)D
20.【答案】
(1)
(2) 镓可以提供空轨道、而氯可以提供孤电子对,两者能形成配位键 sp2 杂化、sp3 杂化 为
离子晶体, 为分子晶体
(3) C6H6O3 O