文档内容
2024级高二学年上学期9月考试
化学试题(致远)
时长:75分钟 分值:100分
一、选择题(每题3分,共45分) A.该反应为吸热反应
1.向绝热恒容密闭容器中通入 和 ,在一定条件下发生反应 B.压强的大小关系:
,正反应速率随时间变化的示意图如下图,下列结论中正确 C. 、 、 三点的化学平衡常数:
的个数为
D. 若向该容器中充入 和 发生上述反应, 点的
3.某温度下,在恒容密闭容器中充入一定量的X(g)。发生下列反应:反应I:
△H<0;反应Ⅱ: △H<0测得各气体浓度与反应时间的关系如图所示。下列
1 2
说法不正确的是
①反应在c点到达平衡
② 浓度:a点大于c点
③反应物的总能量高于生成物的总能量
④逆反应速率图像在此时间段内和上图趋势相同
⑤混合物颜色不再变化,说明反应达到平衡
⑥达到平衡后,改变容器体积增大压强,逆反应速率可能先增大后减小
A.2个 B.3个 C.4个 D.5个 A.活化能:
B. X(g)的起始浓度为
2.某课题组为探究汽车尾气转化为氮气的最佳反应条件,向体积为 的刚性容器中按 C.升高温度,反应I、Ⅱ的速率均增大,X的平衡转化率降低
D.其他条件不变,在该体系平衡时再投入一定量的X(g),则达到新平衡后Z的体积分数大于原平
衡
充入 和 ,发生反应: 。已知正、逆反应速率可以表
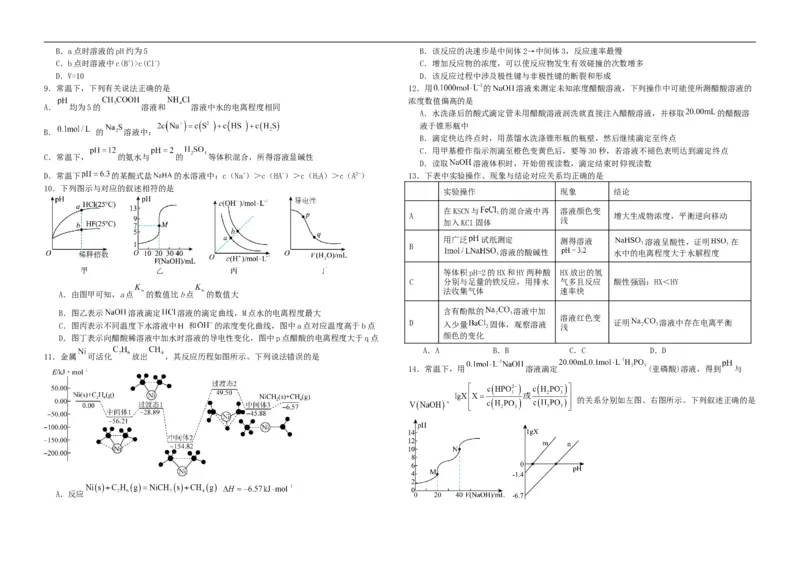
4.下列有关图像分析和说法正确的是
达为 , ( , 表示速率常数),测得 的平
衡转化率与温度、压强的关系如图所示。下列说法正确的是C.正反应速率:
D.800℃条件下,混合气体的起始压强与平衡压强之比为90:91
6.下列有关化学反应方向的描述中正确的是
A.某吸热反应能自发进行,因此该反应是熵增反应
B.知道了某过程有自发性之后,可预测反应过程发生的快慢
C.CaCO(s) CaO(s)+CO(g) △H>0,该反应能否自发进行与温度无关
3 2
D.冰融化为水的过程中:△H<0,△S>0
A.图甲表示合成氨反应在恒温恒容下进行的速率—时间图,Ⅰ、Ⅱ两过程到达平衡时,平衡常 7.剧毒物氰化钠(NaCN)固体遇水或酸生成剧毒易燃的 HCN 气体,同时 HCN 又能与水互溶,造成
数:K <K 水污染。已知部分弱酸的电离平衡常数如下表:
Ⅰ Ⅱ
弱酸 HCOOH HCN HCO
B.图乙表示 ,在恒温恒容条件下,按 投 2 3
K =4.3×10-7
a1
入 和 的混合气体建立平衡的过程,当 与 的转化率为 时,说明反应已达到平衡
K=
a
电离平衡常数(25℃) 1.77×10-4 K a =5.0×10-10 K a2 =5.6×10-11
C.图丙表示 在不同温度下平衡时的 体积分数—压强图,则气体密度:
下列选项错误的是
A点 点 A.相同浓度的 HCOOH和NaCN 的溶液中,水的电离程度前者小
B.中和等体积、等pH 的 HCOOH 溶液和 HCN 溶液消耗 NaOH 的物质的量前者小于后者
D.图丁表示不同温度下水溶液中 与 的关系,a点和d点 ,溶液都呈中性
C.等体积、等物质的量浓度的 HCOONa 和 NaCN 溶液中所含离子总数前者大于后者
5.丙烯在催化剂上选择性还原NO的反应为 。 D.向NaCN溶液中通入少量CO 发生的离子反应为2CN-+HO+CO=2HCN+
2 2 2
8.常温时,用0.1000 mol·L-1的HCl溶液滴定V mL 0.1000 mol·L-1的BOH弱碱溶液。溶液的
在三个2 L的恒容密闭容器中分别加入0.5 mol 和4.5 mol NO发生上述反应,实验测得三
个容器中n(NO)随时间(t)的变化如图所示。下列说法错误的是 pH、分布系数δ(B+)[B+的分布系数= ]随滴加HCl溶液体积V(HCl)的变化关系如下
图所示。
A.500℃条件下,曲线a所在的容器中使用了合适的催化剂
B.500℃条件下,20 min时达到平衡,则该容器中0~20min内用 表示的平均反应速率为
下列有关说法错误的是
A.BOH的电离平衡常数K 约为1.0×10-5
bB.a点时溶液的pH约为5 B.该反应的决速步是中间体2→中间体3,反应速率最慢
C.b点时溶液中c(B+)>c(Cl-) C.增加反应物的浓度,可以使反应物发生有效碰撞的次数增多
D.V=10 D.该反应过程中涉及极性键与非极性键的断裂和形成
9.常温下,下列有关说法正确的是 12.用 的 溶液来测定未知浓度醋酸溶液,下列操作中可能使所测醋酸溶液的
浓度数值偏高的是
A. 均为5的 溶液和 溶液中水的电离程度相同
A.水洗涤后的酸式滴定管未用醋酸溶液润洗就直接注入醋酸溶液,并移取 的醋酸溶
液于锥形瓶中
B. 的 溶液中:
B.滴定快达终点时,用蒸馏水洗涤锥形瓶的瓶壁,然后继续滴定至终点
C.用甲基橙作指示剂滴至橙色变黄色后,要等30秒,若溶液不褪色表明达到滴定终点
C.常温下, 的氨水与 的 等体积混合,所得溶液显碱性
D.读取 溶液体积时,开始俯视读数,滴定结束时仰视读数
D.常温下 的某酸式盐 的水溶液中:c(Na+)>c(HA-)>c(HA)>c(A2-) 13.下表中实验操作、现象与结论对应关系均正确的是
2
10.下列图示与对应的叙述相符的是
实验操作 现象 结论
在KSCN与 的混合液中再 溶液颜色变
A 增大生成物浓度,平衡逆向移动
加入KCl固体 浅
用广泛 试纸测定 测得溶液 溶液呈酸性,证明 在
B
溶液的酸碱性 水中的电离程度大于水解程度
等体积pH=2的HX和HY两种酸 HX放出的氢
C 分别与足量的铁反应,用排水 气多且反应 酸性强弱:HX<HY
法收集气体 速率快
A.由图甲可知,a点 的数值比b点 的数值大
B.图乙表示 溶液滴定 溶液的滴定曲线,M点水的电离程度最大 含有酚酞的 溶液中加
溶液红色变
C.图丙表示不同温度下水溶液中 和 的浓度变化曲线,图中a点对应温度高于b点 D 入少量 固体,观察溶液 浅 证明 溶液中存在电离平衡
D.图丁表示向醋酸稀溶液中加水时溶液的导电性变化,图中p点醋酸的电离程度大于q点 颜色的变化
A.A B.B C.C D.D
11.金属 可活化 放出 ,其反应历程如图所示。下列说法错误的是
14.常温下,用 溶液滴定 (亚磷酸)溶液,得到 与
、 的关系分别如左图、右图所示。下列叙述正确的是
A.反应A. 点对应的溶液中:
B.曲线 表示 与 的变化关系
C. 时,
D. 的平衡常数 已知:①“酸浸”后,钛主要以 形式存在, 在热水中易水解。
15.为研究反应 ,向一固定体积的容器中加入足量1molX和2molY发生反应。
②饱和 溶液在低于 时,析出 ;在 时,析出 ;在高
一定条件下,在甲、乙两种催化剂作用下,反应相同时间,测得Y的转化率与温度的关系如下图
所示。下列说法错误的是 于 时,析出 。
③ 不溶于水和稀酸。
回答下列问题:
(1) 中钛的化合价为 ,“一定条件”是 。
(2) ,为了得到较纯净的副产品 ,在“浓缩结晶”之前要进行的操作是
。
(3)“滤渣”的主要成分为 (填化学式)。
A.反应达到平衡后,恒温时,再加入少量Z,达到新平衡时Y的体积分数减小
(4)写出“沉淀 钛白粉”的化学方程式: 。
B.在相同温度下,与催化剂甲相比,乙使反应活化能更低
C.M点可能是该反应的平衡点
(5)用氧化还原滴定法测定 的质量分数:一定条件下,将 溶解并还原为 ,再以
D.反应达到平衡后,恒温时,再加入少量Y,Z的体积分数减小
二、填空题(共55分)
溶液作指示剂,用新配制的 标准溶液滴定 至全部生成 。滴定分析时,称
16.钛白粉(纳米级)可作为白色无机颜料,广泛应用于功能陶瓷、催化剂、化妆品和光敏材料等
行业。一种由硫酸制取白色颜料钛白粉 的生产工艺如下。【原料钛铁矿 中往往含 取 (摩尔质量为 )样品 , 消耗 标准溶液 :
有 、 、 、 、 等杂质】 ①写出用 标准溶液滴定 至全部生成 时发生反应的离子方程式: 。
②达到滴定终点的现象为 。
③ 的质量分数为 (用含M、w、c、V的代数式表示)。
17.近年来,我国大力加强温室气体 氢化合成甲醇技术的工业化量产研究,实现可持续发展。
在合适的催化剂作用下,二氧化碳可催化加氢制甲醇。(1)已知:①
②
则反应③ 。
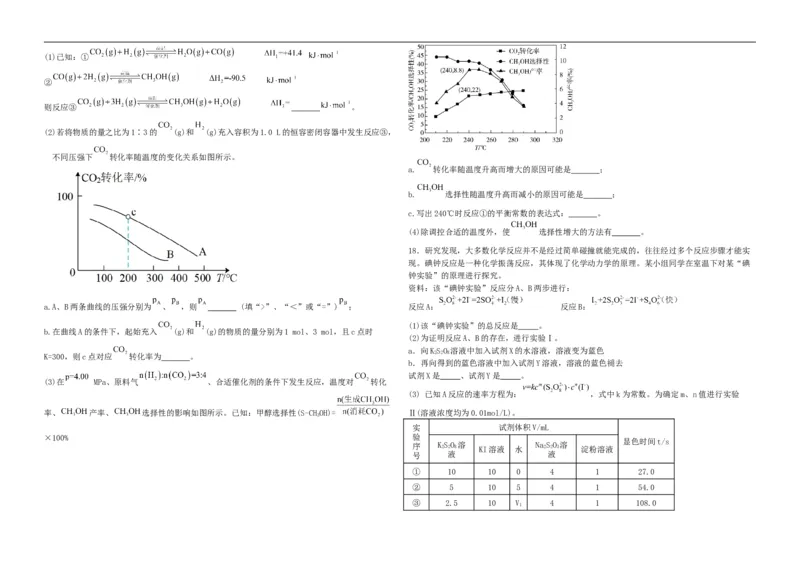
(2)若将物质的量之比为1∶3的 (g)和 (g)充入容积为1.0 L的恒容密闭容器中发生反应③,
不同压强下 转化率随温度的变化关系如图所示。
a. 转化率随温度升高而增大的原因可能是 ;
b. 选择性随温度升高而减小的原因可能是 ;
c.写出240℃时反应①的平衡常数的表达式: 。
(4)除调控合适的温度外,使 选择性增大的方法有 。
18.研究发现,大多数化学反应并不是经过简单碰撞就能完成的,往往经过多个反应步骤才能实
现。碘钟反应是一种化学振荡反应,其体现了化学动力学的原理。某小组同学在室温下对某“碘
钟实验”的原理进行探究。
资料:该“碘钟实验”反应分A、B两步进行:
a.A、B两条曲线的压强分别为 、 ,则 (填“>”、“<”或“=”) ; 反应A: 反应B:
(1)该“碘钟实验”的总反应是 。
b.在曲线A的条件下,起始充入 (g)和 (g)的物质的量分别为1 mol、3 mol,且c点时
(2)为证明反应A、B的存在,进行实验Ⅰ。
a.向KSO 溶液中加入试剂X的水溶液,溶液变为蓝色
2 2 8
K=300,则c点对应 转化率为 。
b.再向得到的蓝色溶液中加入试剂Y溶液,溶液的蓝色褪去
试剂X是 、试剂Y是 。
(3)在 MPa、原料气 、合适催化剂的条件下发生反应,温度对 转化
(3) 已知A反应的速率方程为: ,式中k为常数。为确定m、n值进行实验
率、 产率、 选择性的影响如图所示。已知:甲醇选择性(S-CHOH)= Ⅱ(溶液浓度均为0.01mol/L)。
3
实 试剂体积V/mL
×100% 验
显色时间t/s
序 K 2 S 2 O 8 溶 KI溶液 水 Na 2 S 2 O 3 溶 淀粉溶液
号 液 液
① 10 10 0 4 1 27.0
② 5 10 5 4 1 54.0
③ 2.5 10 V 4 1 108.0
1④ 10 5 5 4 1 54.0
①表中V= 。
1
②通过数据计算得知:m= ,n= 。
(4)为探究其他因素对该“碘钟实验”的影响,进行实验Ⅲ(溶液浓度均为0.01mol/L)。
试剂体积V/mL
KSO 溶 NaSO 溶
2 2 8 KI溶液 水 2 2 3 淀粉溶液
液 液
5 5 3 11 1
实验过程中,溶液颜色始终无明显变化。试结合该“碘钟实验”总反应方程式及反应A与反应B
速率的相对快慢关系,解释实验Ⅲ未产生颜色变化的原因: 。
19.西南油气田甲烷产量高,甲烷的综合利用产氢是一项重要的课题。
甲烷水蒸气重整过程涉及的反应如下:
和 随水碳比的变化曲线分别是 、 (填序号)。
反应I:
(3)一定条件下,向 恒容密闭容器中通入 发生反应I、II,达到平衡时,
反应II:
容器中 为 为 ,反应Ⅰ的化学平衡常数为 (用含a、b、V的代数式
反应III:
表示)。
过程中自由能( ,设 和 不随温度变化)随温度变化趋势如图所示: (4)甲烷二氧化碳重整产氢的技术理论: 条件下,气体分子吸附至催化剂表面后发生反应,
此过程机理模型如图所示(*表示吸附在催化剂表面的活性物种)。
①根据图示写出该化学反应方程式 。
(1)判断反应I、II反应焓变的符号: 0, 0(填“>”或“<”),在
②在催化剂中添加少量多孔 能提高 转化率,其原因是 。
时,发生的反应有: (选用“I、II、III”作答)。
(2)在 、 条件下,甲烷水蒸气重整反应达到平衡时体系中各组分摩尔分数(物质ⅰ的摩
尔分数 )与投料水碳比[ ]的关系如图所示。