文档内容
2022年湖南省永州市中考化学试卷
一、选择题(本题共10个小题,每小题只有一个正确答案。请将正确选项填涂到答题卡上
相应的位置。每小题2分,共20分)
1.空气中含量最多的物质是( )
A.N B.O C.HO D.CO
2 2 2 2
2.生活中下列物质加入适量水不能形成溶液的是( )
A.食醋 B.食用油 C.白砂糖 D.食盐
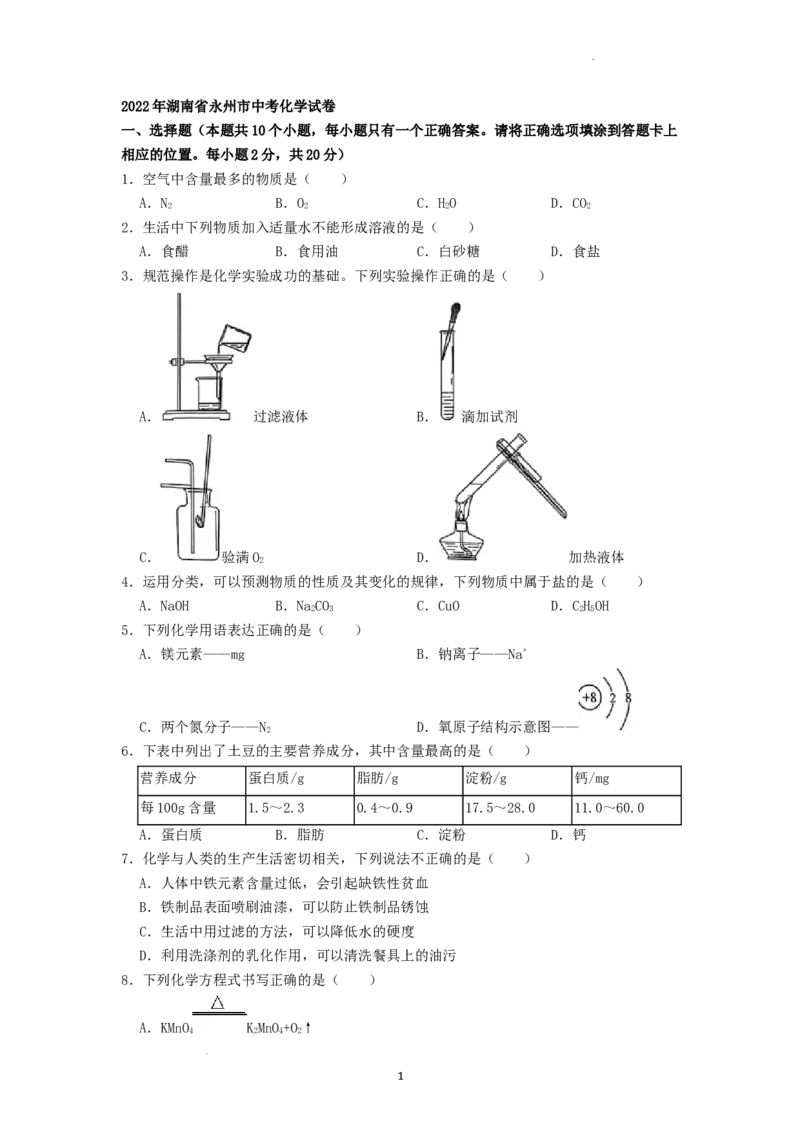
3.规范操作是化学实验成功的基础。下列实验操作正确的是( )
A. 过滤液体 B. 滴加试剂
C. 验满O D. 加热液体
2
4.运用分类,可以预测物质的性质及其变化的规律,下列物质中属于盐的是( )
A.NaOH B.NaCO C.CuO D.CHOH
2 3 2 5
5.下列化学用语表达正确的是( )
A.镁元素——mg B.钠离子——Na+
C.两个氮分子——N D.氧原子结构示意图——
2
6.下表中列出了土豆的主要营养成分,其中含量最高的是( )
营养成分 蛋白质/g 脂肪/g 淀粉/g 钙/mg
每100g含量 1.5~2.3 0.4~0.9 17.5~28.0 11.0~60.0
A.蛋白质 B.脂肪 C.淀粉 D.钙
7.化学与人类的生产生活密切相关,下列说法不正确的是( )
A.人体中铁元素含量过低,会引起缺铁性贫血
B.铁制品表面喷刷油漆,可以防止铁制品锈蚀
C.生活中用过滤的方法,可以降低水的硬度
D.利用洗涤剂的乳化作用,可以清洗餐具上的油污
8.下列化学方程式书写正确的是( )
A.KMnO KMnO+O↑
4 2 4 2
1
学科网(北京)股份有限公司B.FeO+2CO 2Fe+2CO
2 3 2
C.Al+CuSO═AlSO+Cu
4 4
D.NaCO+BaCl═BaCO↓+2NaCl
2 3 2 3
9.我国科学家屠呦呦从传统中药中成功分离提取出抗疟疾的有效成分青蒿素,获得诺贝尔
生理学或医学奖。青蒿素的化学式为C H O,下列说法不正确的是( )
15 22 5
A.青蒿素分子中含有11个氢分子
B.青蒿素的相对分子质量为282
C.青蒿素中碳、氢元素的质量比为90:11
D.青蒿素中氧元素的质量分数约为28.4%
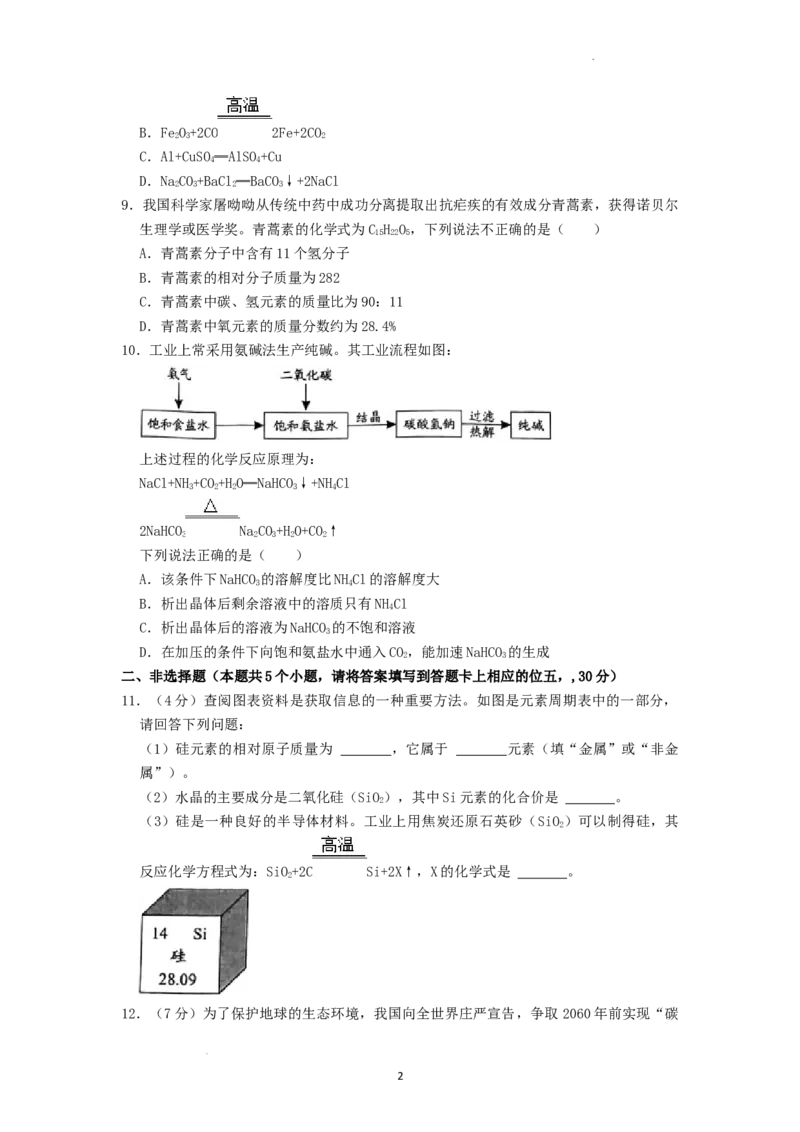
10.工业上常采用氨碱法生产纯碱。其工业流程如图:
上述过程的化学反应原理为:
NaCl+NH+CO+HO═NaHCO↓+NHCl
3 2 2 3 4
2NaHCO NaCO+HO+CO↑
3 2 3 2 2
下列说法正确的是( )
A.该条件下NaHCO 的溶解度比NHCl的溶解度大
3 4
B.析出晶体后剩余溶液中的溶质只有NHCl
4
C.析出晶体后的溶液为NaHCO 的不饱和溶液
3
D.在加压的条件下向饱和氨盐水中通入CO,能加速NaHCO 的生成
2 3
二、非选择题(本题共5个小题,请将答案填写到答题卡上相应的位五,,30分)
11.(4分)查阅图表资料是获取信息的一种重要方法。如图是元素周期表中的一部分,
请回答下列问题:
(1)硅元素的相对原子质量为 ,它属于 元素(填“金属”或“非金
属”)。
(2)水晶的主要成分是二氧化硅(SiO),其中Si元素的化合价是 。
2
(3)硅是一种良好的半导体材料。工业上用焦炭还原石英砂(SiO )可以制得硅,其
2
反应化学方程式为:SiO+2C Si+2X↑,X的化学式是 。
2
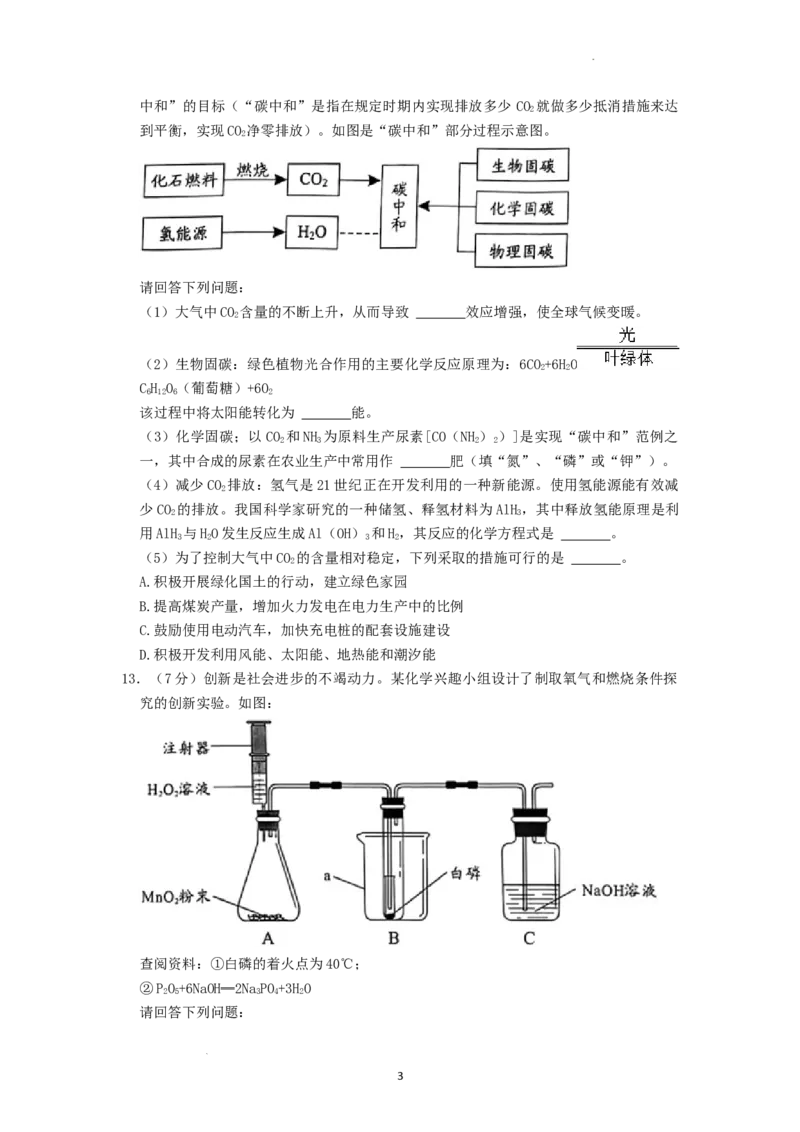
12.(7分)为了保护地球的生态环境,我国向全世界庄严宣告,争取2060年前实现“碳
2
学科网(北京)股份有限公司中和”的目标(“碳中和”是指在规定时期内实现排放多少 CO 就做多少抵消措施来达
2
到平衡,实现CO 净零排放)。如图是“碳中和”部分过程示意图。
2
请回答下列问题:
(1)大气中CO 含量的不断上升,从而导致 效应增强,使全球气候变暖。
2
(2)生物固碳:绿色植物光合作用的主要化学反应原理为:6CO+6HO
2 2
CH O(葡萄糖)+6O
6 12 6 2
该过程中将太阳能转化为 能。
(3)化学固碳;以CO 和NH 为原料生产尿素[CO(NH ) )]是实现“碳中和”范例之
2 3 2 2
一,其中合成的尿素在农业生产中常用作 肥(填“氮”、“磷”或“钾”)。
(4)减少CO 排放:氢气是21世纪正在开发利用的一种新能源。使用氢能源能有效减
2
少CO 的排放。我国科学家研究的一种储氢、释氢材料为AlH ,其中释放氢能原理是利
2 3
用AlH 与HO发生反应生成Al(OH) 和H,其反应的化学方程式是 。
3 2 3 2
(5)为了控制大气中CO 的含量相对稳定,下列采取的措施可行的是 。
2
A.积极开展绿化国土的行动,建立绿色家园
B.提高煤炭产量,增加火力发电在电力生产中的比例
C.鼓励使用电动汽车,加快充电桩的配套设施建设
D.积极开发利用风能、太阳能、地热能和潮汐能
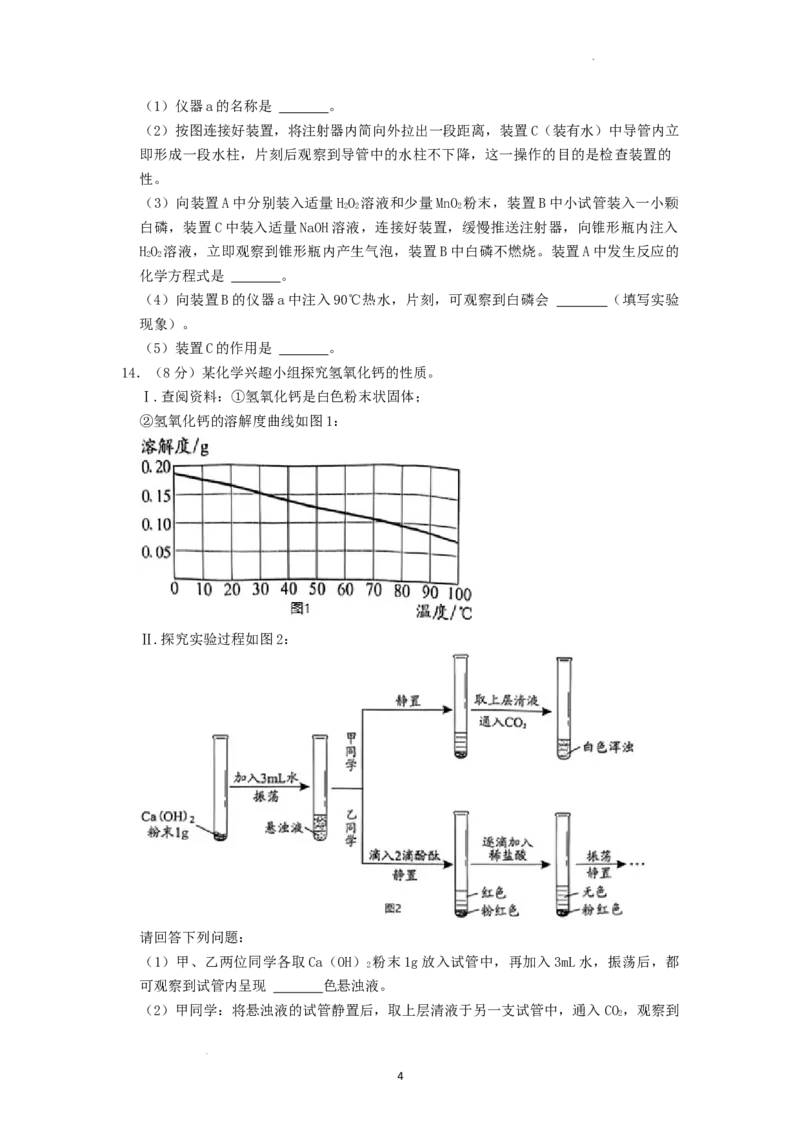
13.(7分)创新是社会进步的不竭动力。某化学兴趣小组设计了制取氧气和燃烧条件探
究的创新实验。如图:
查阅资料:①白磷的着火点为40℃;
②PO+6NaOH═2NaPO+3HO
2 5 3 4 2
请回答下列问题:
3
学科网(北京)股份有限公司(1)仪器a的名称是 。
(2)按图连接好装置,将注射器内简向外拉出一段距离,装置C(装有水)中导管内立
即形成一段水柱,片刻后观察到导管中的水柱不下降,这一操作的目的是检查装置的
性。
(3)向装置A中分别装入适量HO 溶液和少量MnO 粉末,装置B中小试管装入一小颗
2 2 2
白磷,装置C中装入适量NaOH溶液,连接好装置,缓慢推送注射器,向锥形瓶内注入
HO 溶液,立即观察到锥形瓶内产生气泡,装置B中白磷不燃烧。装置A中发生反应的
2 2
化学方程式是 。
(4)向装置B的仪器a中注入90℃热水,片刻,可观察到白磷会 (填写实验
现象)。
(5)装置C的作用是 。
14.(8分)某化学兴趣小组探究氢氧化钙的性质。
Ⅰ.查阅资料:①氢氧化钙是白色粉末状固体;
②氢氧化钙的溶解度曲线如图1:
Ⅱ.探究实验过程如图2:
请回答下列问题:
(1)甲、乙两位同学各取Ca(OH) 粉末1g放入试管中,再加入3mL水,振荡后,都
2
可观察到试管内呈现 色悬浊液。
(2)甲同学:将悬浊液的试管静置后,取上层清液于另一支试管中,通入CO ,观察到
2
4
学科网(北京)股份有限公司溶液变白色浑浊,该白色浑浊是 (填化学式)。
(3)乙同学:①向悬浊液的试管中滴入2滴酚酞,振荡、静置后,观察到上层溶液呈
红色,下层悬浊物呈粉红色;然后向试管中逐滴加入稀盐酸,观察到上层红色溶液逐渐
变为无色,其反应的化学方程式是 。
②再将试管振荡、静置后,观察到试管上层清液又呈现 色,其原因是 。
15.(4分)为了分析铁粉和铜粉混合物样品的组成,某同学称取 12.0g样品,加入到足
量的稀HSO 溶液中,充分反应完全后,过滤、洗涤、干燥,称量剩余固体的质量为
2 4
3.6g。
(1)样品中铁粉的质量为 g。
(2)若在上述反应条件时H 的密度为0.09g/L,试计算产生H 的体积(写出详细的计
2 2
算过程,保留小数点后一位)。
5
学科网(北京)股份有限公司6
学科网(北京)股份有限公司