文档内容
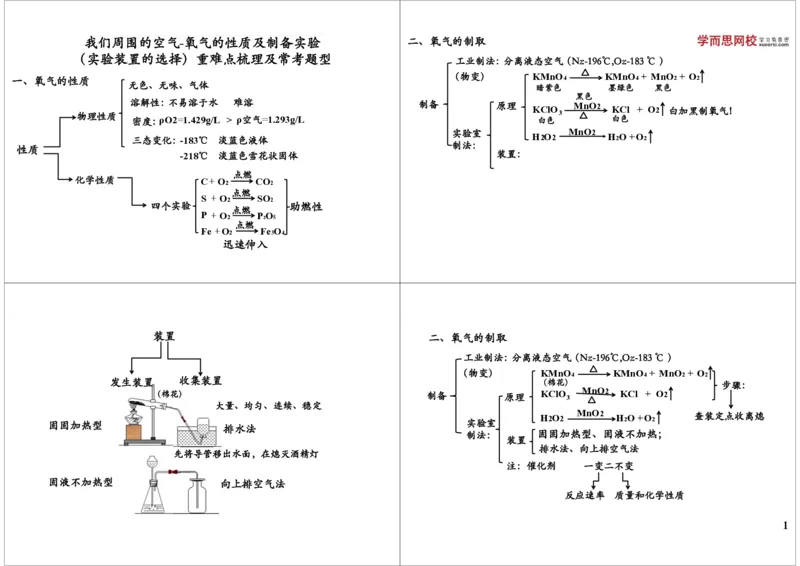
我们周围的空气-氧气的性质及制备实验 二、氧气的制取
(实验装置的选择)重难点梳理及常考题型
工业制法:分离液态空气(N2:-196℃,O2:-183℃ )
一、氧气的性质 (物变) KMnO 4 KMnO 4 + MnO 2 + O 2
无色、无味、气体
暗紫色 墨绿色 黑色
黑色
物理性质
溶
密
解
度
性
:ρ
:
O
不
2=
易
1
溶
.42
于
9g
水
/L >
难
ρ空
溶
气=1.293g/L
制备 原理
K 白 C 色 lO 3
MnO2
白 KC 色 l + O2 白加黑制氧气!
实验室 MnO2
三态变化:-183℃ 淡蓝色液体 H2O2 H 2 O +O 2
制法:
性质
-218℃ 淡蓝色雪花状固体 装置:
点燃
化学性质 C+ O CO
2 2
点燃
S + O SO
2 2
四个实验 助燃性
点燃
P + O PO
2 2 5
点燃
Fe+O FeO
2 3 4
迅速伸入
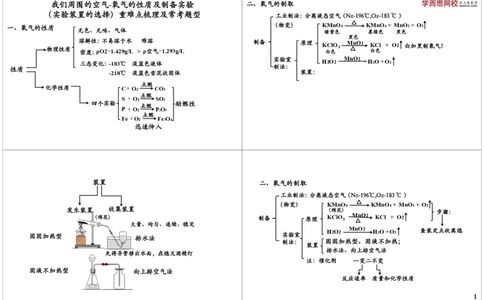
装置 二、氧气的制取
工业制法:分离液态空气(N2:-196℃,O2:-183℃ )
(物变) KMnO 4 KMnO 4 + MnO 2 + O 2
发生装置 收集装置 (棉花) 步骤:
(棉花) 制备 原理 KClO 3
MnO2
KCl + O2
大量、均匀、连续、稳定
固固加热型 实验室
H2O2
MnO2
H
2
O +O
2
查装定点收离熄
排水法
制法: 固固加热型、固液不加热;
装置
排水法、向上排空气法
先将导管移出水面,在熄灭酒精灯
注:催化剂 一变二不变
固液不加热型 向上排空气法
反应速率 质量和化学性质
1催化剂的反应 二、氧气的制取
KClO
3
+ MnO2 KMnO
4
+ Cl
2
+ O
2
工业制法:分离液态空气(N2:-196℃,O2:-183℃ )
KMnO K MnO + MnO +O
4 2 4 2 2 (物变) KMnO 4 KMnO 4 + MnO 2 + O 2
K 2 MnO 4 + Cl 2 MnO 2 + KCl+ O 2 制备
原理
(
K
棉
Cl
花
O
)
3
MnO2
KCl + O2
步骤:
KClO 3 MnO2 KCl + O 2 H2O2 MnO2 H
2
O +O
2
查装定点收离熄
实验室
固固加热型、固液不加热;
制法:
装置
检验:中
排水法、向上排空气法
验满:口
注:催化剂 一变二不变
反应速率 质量和化学性质
三、两大基本反应及物质的分类 【例1】小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液——“双氧水”,他联
想到在化学课上曾用过氧化氢溶液制取氧气,他高兴的将家中的“双氧水”拿到学
化合反应:(多变一) 校的实验室,在老师的指导下和同学们一起做了如下实验。
【第一组实验】小明欲证明该双氧水是否失效。
分解反应:(一变多) 白磷自然
实验过程:
由缓慢氧化所引起
①在试管中加入5ml“双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
氧化反应:物质与氧发生的反应
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条
仍未复燃;
剧烈氧化:既发光又放热的氧化反应(燃烧)
③如右下图装置进行操作,带火星的木条燃烧,水槽中冰水所起的作用是
缓慢氧化:只放热不发光的氧化反应 (呼吸,变质,生锈) _____________________________________________________。
(空气、溶液、合金)
混合物:有两种或两种以上物质混合而成
物质
纯净物:由一种物质所组成(O 2、N 2、H 2、CO 2、H
2
O)
(相对纯净) 24K千足金 2【第二组实验】小明欲证明二氧化锰在双氧水的分解反应中起催化作用,该物 【例2】小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种叫做过氧化
质在反应前后质量是否发生变化。 钙的淡黄色固体,用来增加鱼池中的含氧量。小明刚学完氧气的实验室制法,
(1)实验原理 于是他想可否用过氧化钙制取氧气。
写出化学反应的文字表达式_______________________________。 [提出问题]过氧化钙可否用于制取氧气?
(2)实验步骤 [查阅资料]部分内容如下:过氧化钙(CaO
2
)室温下稳定,在300℃时分解
生成氧气,可做增氧剂、杀菌剂等。
①______________________________________;
[猜想与验证]
②将二氧化锰装入大试管中并加入5ml“双氧水”;
(1)小明依据_______________________________,提出猜想I加热过氧化钙
③待反应结束后,将大试管里的固体物质进行过滤、洗涤、烘干、称量;
可制取氧气。
④________________________________________________。
(3)做完此实验后,小方认为要证明二氧化锰是一种催化剂,还需要再补充
一个
探究实验:探究___________________________________________。
【实验反思】依据所做的实验,影响化学反应速率的因素可能是
___________________________等。
(2)小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想II:过氧化
实验装置 实验主要过程
钙与水反应可制取氧气。
实验装置 实验主要过程
①检验装置气密性。操作如下:先将导管伸
①检验装置气密性。
入液面下,用手紧握试管,观察到
②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导
________________,松开手后,有液体进入
管口几乎收集不到气体。该装置放置到第二天,集气瓶中
导管。
只收集到极少量气体,振荡试管后仍有少量细小气泡缓慢
②加入过氧化钙,加热,导管口有大量气泡
冒出。 放出。
③收集满一瓶气体。
④停止加热。熄灭酒精灯前,应
实验结论:不能用过氧化钙与水反应制取氧气。
_________________。
⑤检验气体。方法是__________________
[分析与反思]
____________________________________。 ①虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙
做增氧剂的主要原因是______________________________________________。
②小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?
你的合理建议:___________________________________________。 3