文档内容
江苏省泰州市2018年中考化学真题试题
(考试时间:化学、物理共150分钟题号范围:化学1~20;物理21~50)
(化学满分:60分)
请注意:1.本试卷分选择题和非选择题两个部分
2.答题卡正面为化学学科的答题范围,反面为物理学科的答题范围。所有试题的答案均填写在答
题卡上,答案写在试卷上无效。
可能用到的相对原子质量:H-1 C-12 N—14 O-16 F-19 Mg-24 Cl-35.5
第一部分 选择题(共20分)
第1~10题,每小题只有一个选项符合题意。每小题1分,共10分。
1.习近平总书记提出“绿水青山就是金山银山”的理念,下列做法符合这一理念的有
A.发展清洁能源 B.随意焚烧秸秆 C.乱丢废旧电池 D.提倡毁林造田
2.下列变化属于化学变化的是
A.玻璃破碎 B.石蜡熔化 C.食物腐败 D.汽油挥发
3.下列物质由离子构成的是
A.二氧化碳 B.水 C.金刚石 D.氯化钠
4.下列物质可用作钾肥的是
A.KCl B.NHHCO C.(NH)PO D.NaSO
4 3 4 3 4 2 4
5.下列厨房用品中,易溶于水形成溶液的是
A.花生油 B.面粉 C.白糖 D.辣椒粉
6.下列物质的用途中,主要利用其物理性质的是
A.用生石灰做干燥剂 B.用氢气制造燃料电池
C.用铜丝制作导线 D.用稀盐酸除去水垢
7.下列实验操作正确的是
毛玻璃片的
粗糙面向下
A.塞紧胶塞 B.贮存氧气 C.过滤 D.吹灭酒精灯
8.下列化学用语表示正确的是
A.钙离子:Ca+2 B.2个氢原子:H
2- 2
C.氧化钠中氧元素化合价:NaO D.3个氯分子:3Cl
2 2
9.芯片是内含集成电路的硅片,下图是硅元素在元素周期表中的相关信息,下列说法正确的是
A.硅元素属于金属元素
B.硅元素的原子序数为14
14 Si
C.硅元素的相对原子质量为28.09g
硅
D.硅元素是地壳中含量最高的元素 28.09
10.下列做法正确的是
A.用肥皂水区分硬水和软水
B.用活性炭净化水就可以得到纯水
C.用酚酞试液区分二氧化碳气体和氯化氢气体
D.用pH试纸测定溶液pH时,应先用蒸馏水将试纸润湿Ⅰ Ⅱ Ⅰ Ⅱ Ⅰ Ⅱ
第11-15题,每小题有一个或两个选项符合题意。若正确答案包括两个选项,只选一个且正确得1分;错选
得0分。每小题2分,共10分。
11.化学概念在逻辑上存在如下关系
并列关系 交叉关系 包含关系
下列对概念间相互关系的说法正确的是
A.混合物与纯净物属于交叉关系 B.糖类与淀粉属于并列关系
C.中和反应与复分解反应属于并列关系 D.合成材料与塑料属于包含关系12.C H FNO 为抗癌新药
22 19 4 2
西达苯胺的化学式。下列关于西达苯胺的说法正确的是
A.西达苯胺是一种有机物
B.西达苯胺由碳、氢、氧、氮四种元素组成
C西达苯胺中碳元素和氮元素的质量比为11:2
D.西达苯胺各元素的质量分数中氧元素的质量分数最小
13.下列对实验意外事故的处理方法错误的是
A.若不慎将稀硫酸溅入眼睛,要先用手揉眼睛,再立即用水冲洗
B.若不慎将烧碱溶液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液
C.若不慎将燃着的酒精灯碰倒,洒出的酒精在桌面上燃烧,应立刻用湿抹布扑盖
D.若不慎将少量浓硫酸沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
14.下列有关物质的鉴别、除杂、分离所用的试剂或方法正确的是
选项 实验目的 所用试剂或方法
A 鉴别氯化钾溶液和硫酸钾溶液 AgNO 溶液
3
B 鉴别氢氧化钠固体和硝酸铵固体 水
C 除去氯化钠溶液中的硝酸钾 降温结晶
D 分离氯化钾固体与二氧化锰 溶解、过滤
15.下图是某汽车尾气净化装置中发生反应的微观示意图。下列说法正确的是
一氢原子(核电荷数为1)
催化剂
一氧原子(核电荷数为8)
X Y Z
一氮原子(核电荷数为7)
W
A.该反应中,Z是由Y分解生成的
B一个Y和W分子中均有10个电子
C.参加反应的X与生成的Z的质量比为9:7
D.化学反应前后,催化剂的质量和性质一定不变
第二部分 非选择题(共40分)
16.(8分)化学是人类进步的阶梯。
(1)航天服是保障航天员的生命活动和工作能力的个人密闭装备。航天服保暖层通常含有合成纤维、羊毛等
材料,羊毛的主要成分是__________,燃烧羊毛时有________________气味。
(2)造船业已成为泰州市的一项支柱产业。造船需要大量钢铁,未经处理的钢铁易锈蚀,锈蚀的主要原因是
__________________,请写出防止钢铁锈蚀的一种方法:__________________。甲
(3)制作“蔬菜面条”时,常常在面粉中加入一定量的蔬菜汁,“蔬菜面条”比普通面条多提供的营养物质
主要是________和矿物质。取一根普通面条,在面条上滴1滴碘水,可以观察到面条表面呈______色。
(4)大量使用煤、石油、________等化石燃料会产生SO 等污染物,这些污染物溶于雨水后会形成________,
2
因此,使用时应该进行脱硫处理。
17.(9分)请回答下列实验问题:
(1)现提供下列装置
A B C D E F
①上图C装置中,甲仪器的名称是__________。
②实验室将双氧水加入二氧化锰粉末制取氧气,发生装置是____(填序号),反应的化学方程式为
____________________,若用E装置收集氧气,当有______________时,开始收集气体。
③实验室可以按照“B→F→F→真空气囊”的装置顺序制取纯净的CO 气体,B装置中发生反应的化学方程
2
式为________________________________,第一个F装置盛放试剂的作用是__
______________,第二个F装置盛放的试剂为______________。
(2)实验室用氯化钠固体配制50g15%的氯化钠溶液的步骤有:计算、称取氯化钠、量取水、溶解、转移。
①在溶解过程中,玻璃棒的作用是____________________________。
②下列操作中,可能导致配制氯化钠溶液的溶质质量分数偏大的是_______(填序号)。
a.称取时,将氯化钠置于托盘天平的右盘
b.量取水时俯视读数
c.用已有少量水的烧杯溶解氯化钠
d.转移时,有少量溶液溅出
18.(8分)A~I是初中化学常见物质。A与B在高温条件下反应生成C和D,该反应在工业上口可用于冶炼金
属,A和C是组成元素相同的两种气体,D在气体E中燃烧生成黑色固体B.
(1)固态C的俗名是_________,实验室区分气体A和C的液体试剂为_______________。
(2)E、F的化学式分别为_________、_________。
高温
(3)A+B—→ C+D的化学方程式为____________________,D+F→G+H的反应类型是__________。
(4)向F的溶液中加入一定量的D,充分反应后,过滤,向滤渣中滴加I的稀溶液,有气泡产生,同时生成G,
则滤渣的成分是____________,I的化学式为_________。
19.(9分)为探究CO 与NaOH溶液发生的反应,某兴趣小组尝试用不同的方式进行实验。
2
【查阅资料】
Ⅰ.20℃时,几种物质在水中的溶解度见下表:
物质 NaCO NaHCO Ca(OH) Ba(OH)
2 3 3 2 2
溶解度/g 21.5 9.6 0.165 3.89
Ⅱ.本实验条件下,NaCO 溶液和NaHCO 溶液的pH分别约为11.0和8.5。
2 3 3
【实验探究】
(1)实验一:小雨取一充满CO 的矿泉水瓶,加入一定量的水,立即拧紧瓶盖,振荡,发现瓶子变瘪,小雨另取
2
一相同的充满CO 的矿泉水瓶,向其中加入与水等体积的NaOH溶液,立即拧紧瓶盖,振荡,得到溶液X,此时
2
观察到的现象是_________________________________,实验中,小雨采用两只矿泉水瓶做对比实验的目的
是_________________________________。(2)实验二:为检验CO 与NaOH溶液反应的产物,小亮取实验一所得溶液X少许,向其中滴加BaCl 溶液,有
2 2
白色沉淀产生,该反应的化学方程式为_____________________________,实验中不宜将BaCl 溶液换成
2
CaCl 溶液的原因是_____________________________________。
2
(3)实验三:小华取实验一所得溶液X少许,向其中加入过量的BaCl 溶液,振荡,静置,取上层清液,滴入1
2
滴酚酞试液,发现溶液呈____色,证明溶液X中有NaOH剩余。实验中,小华没有直接向少量溶液X中滴入酚
酞试液,理由是___________________________________。
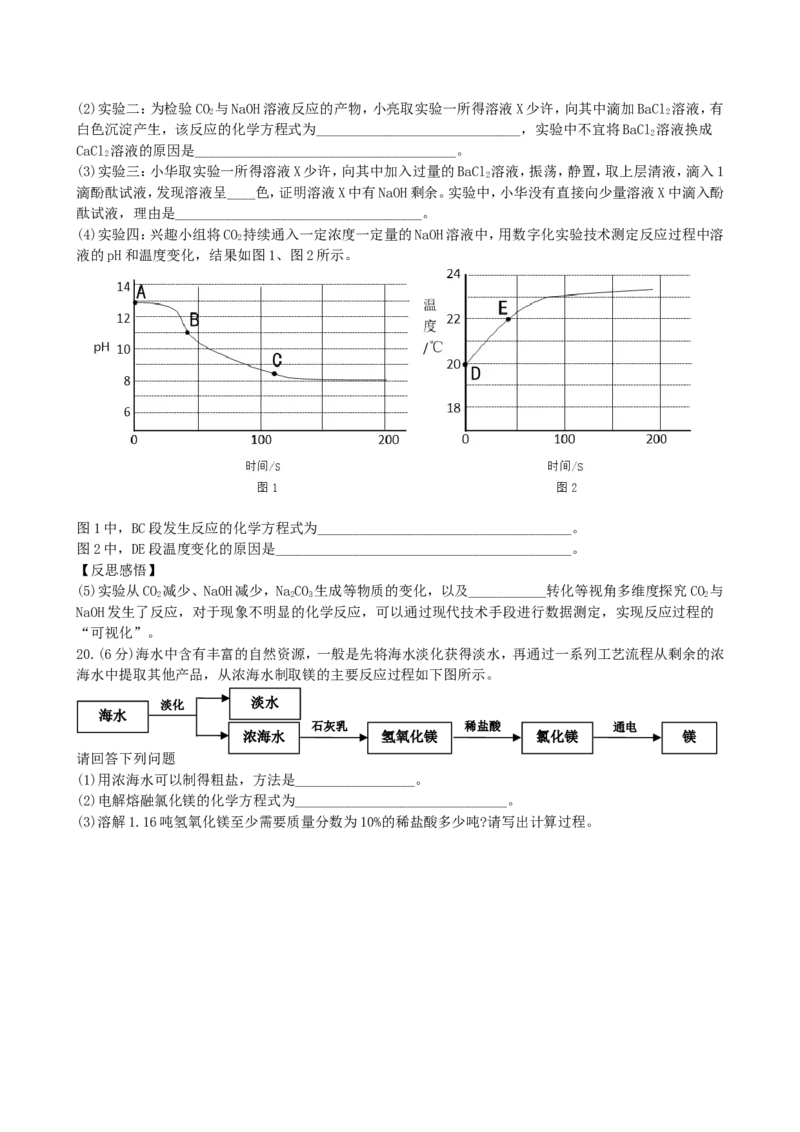
(4)实验四:兴趣小组将CO 持续通入一定浓度一定量的NaOH溶液中,用数字化实验技术测定反应过程中溶
2
液的pH和温度变化,结果如图1、图2所示。
图1中,BC段发生反应的化学方程式为____________________________________。
图2中,DE段温度变化的原因是__________________________________________。
【反思感悟】
(5)实验从CO 减少、NaOH减少,NaCO 生成等物质的变化,以及___________转化等视角多维度探究CO 与
2 2 3 2
NaOH发生了反应,对于现象不明显的化学反应,可以通过现代技术手段进行数据测定,实现反应过程的
“可视化”。
20.(6分)海水中含有丰富的自然资源,一般是先将海水淡化获得淡水,再通过一系列工艺流程从剩余的浓
海水中提取其他产品,从浓海水制取镁的主要反应过程如下图所示。
淡化 淡水
海水
石灰乳 稀盐酸 通电
浓海水 氢氧化镁 氯化镁 镁
请回答下列问题
(1)用浓海水可以制得粗盐,方法是_________________。
(2)电解熔融氯化镁的化学方程式为______________________________。
(3)溶解1.16吨氢氧化镁至少需要质量分数为10%的稀盐酸多少吨?请写出计算过程。