文档内容
班级 姓名 学号 分数
第二章 分子结构与性质(A卷·知识通关练)
核心知识1 共价键的特征与类型
1. 下列不属于共价键成键因素的是
A.共用电子在两原子核之间高概率出现
B.成键原子的原子轨道在空间重叠
C.成键后体系能量降低,趋于稳定
D.两原子核体积大小要适中
2. 下列说法正确的是 ( )
A.气体单质中,一定有σ键,可能有π键
B.基态C原子有两个未成对电子,所以最多只能形成2个共价键
C.1个N原子最多只能与3个H原子结合形成NH3分子,是由共价键的饱和性所决定的
D.所有的原子轨道都具有一定的伸展方向,因此所有的共价键都具有方向性
3. 下列关于σ键和π键的说法中错误的是
A.双原子单质分子中只存在σ键,无π键
B.共价双键中有1个σ键和1个π键
C.σ键是原子轨道“头碰头”重叠,π键则为“肩并肩”重叠
D.乙烯分子中σ键比π键稳定,不易断裂
4. 为阿伏加德罗常数的值.下列说法不正确的是
A. 甲苯中 键总数为
B.标准状况下, 中含有的原子总数为
C. 正丁烷和 异丁烷的混合物中含共价键数目为
D. 的乙醇溶液中,含 键的数目为
5. 回答下列问题
(1)下列分子中,只含有 键的是___________(填序号,下同),既含有 键又含有 键的是___________。① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
(2)在①乙烷( 、②乙烯( )、③乙炔( )分子中碳碳键键长大小顺序是
___________(用序号表示)。
核心知识2 共价键的键参数
6. 下列有关共价键和键参数的说法不正确的是
A.1个乙烯( )分子中含有5个 键和1个 键
B.C—H键比Si—H键的键长更短,故 比 更稳定
C. 、 、 三种分子的键角依次增大
D.碳碳双键比碳碳单键的键能更大,故碳碳双键更稳定
7. 从实验测得不同物质中氧氧之间的键长和键能的数据:
O O O 2 O
键长(10-12m) 149 128 121 112
键能(kJ·mol-1) x y z=494 w=628
其中x、y的键能数据尚未测定,但可根据规律推导键能的大小顺序为w>z>y>x;该规律是A.成键的电子
数越多,键能越大 B.键长越长,键能越小
C.成键所用的电子数越少,键能越小 D.成键时电子对越偏移,键能越大
8. 分析下表数据,有关说法错误的是
化学键 O-O O=O N-N N=N N≡N
键能
142 497.3 193 418 948
化学键 C-C C=C C≡C C-H H-H
键能
347.7 615 812 413.4 436A. 不能发生加成反应是因为其中的π键比σ键更稳定
B.
C.O存在 ,N存在 ;同样,C可能存在
D.键长: ;同样的:
9. 化学键的键能是指气态原子间形成1mol化学键时释放的能量,如:H(g)+I(g)→H—I(g)+297kJ,即H
—I的键能为297kJ·mol-1,也可以理解为破坏1molH—I需要吸收297kJ的热量。化学反应的发生可以看成
旧化学键的破坏和新化学键的形成,下表是一些键能数据(单位:kJ·mol-1):
键能 键能 键能
H-
H-H 436 Cl-Cl 243 432
Cl
S=S 255 H-S 339 C-F 427
C-Cl 330 C-I 218 H-F 565
C-O 347 H-O 464
阅读上述信息,下列说法不正确的是A.键能越大,物质的热稳定性越强
B.每生成2molHCl气体,则释放出185kJ能量
C.H—O的键能大于H—S的键能,所以HO的溶沸点高于HS的溶沸点
2 2
D.C—Br的键能应在218~330kJ·mol-1之间
10. (1)完全燃烧一定质量的无水乙醇,放出的热量为QkJ,为完全吸收生成的CO,并使之生成正盐,消
2
耗0.8mol/L NaOH溶液50mL,则燃烧1mol酒精放出的热量是_________________。
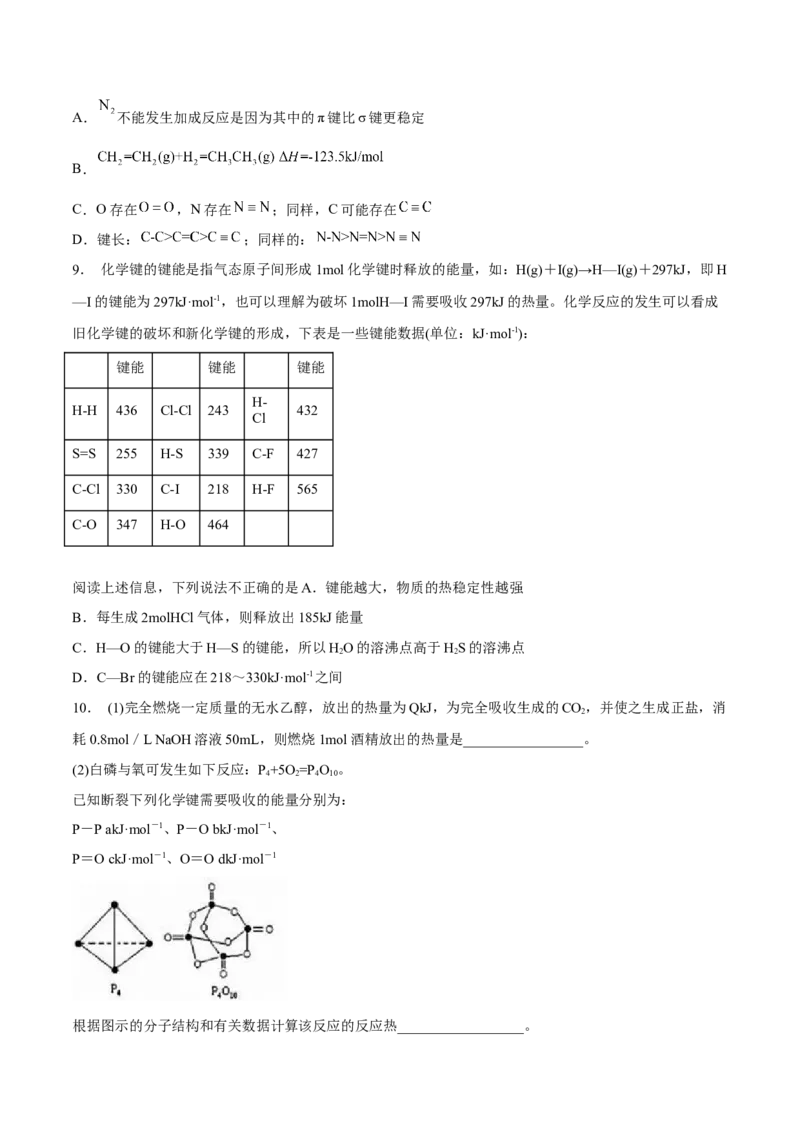
(2)白磷与氧可发生如下反应:P+5O =P O 。
4 2 4 10
已知断裂下列化学键需要吸收的能量分别为:
P-P akJ·mol-1、P-O bkJ·mol-1、
P=O ckJ·mol-1、O=O dkJ·mol-1
根据图示的分子结构和有关数据计算该反应的反应热__________________。(3)现根据下列3个热化学反应方程式:
Fe O(s)+3CO(g)=2Fe(s)+3CO (g) △H=-24.8kJ/mol
2 3 2
3Fe O(s)+ CO(g)=2Fe O(s)+ CO (g) △H=-47.2kJ/mol
2 3 3 4 2
Fe O(s)+CO(g)=3FeO(s)+CO (g) △H=-19.4kJ/mol
3 4 2
写出CO气体还原FeO固体得到Fe固体和CO 气体的热化学反应方程式:_______________。
2
核心知识3 价层电子对互斥模型及其应用
11. 关于价层电子对互斥理论说法错误的是
A.价层电子对包括σ键电子对和中心原子上的孤电子对
B.分子中键角越大,价层电子对相互排斥力越小,分子越稳定
C.用该理论预测HS和BF 的空间结构为V形和平面三角形
2 3
D.该理论一定能预测出多中心原子的分子、离子或原子团的空间构型
12. 根据杂化轨道理论和价层电子对互斥模型,判断下列分子或者离子的空间构型正确的是
选
分子式 中心原子杂化方式 VSEPR模型名称 空间结构
项
A sp V形 V形
B sp2 平面三角形 三角锥形
C sp2 四面体形 平面三角形
D sp3 正四面体形 正四面体形
A.A B.B C.C D.D
13. 用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,
下列判断正确的是
A.SO 、CS、HI都是直线形的分子
2 2
B.BF 键角为120°,SiCl 键角大于120°
3 4
C.COCl 、BF、SO 都是平面三角形的分子
2 3 3
D.PCl 、NH 、PCl 都是三角锥形的分子
3 3 5
14. 根据价层电子对互斥理论填空:
(1)OF 分子中,中心原子上的σ键电子对数为___,孤电子对数为___,价层电子对数为___,中心原子
2
的杂化方式为___杂化,VSEPR构型为____________,分子的立体构型为___________。(2)BF 分子中,中心原子上的σ键电子对数为___,孤电子对数为___,价层电子对数为___,中心原子
3
的杂化方式为___杂化,VSEPR构型为____________,分子的立体构型为___________。
(3)SO 2-分子中,中心原子上的σ键电子对数为___,孤电子对数为___,价层电子对数为___,中心原子
4
的杂化方式为___杂化,VSEPR构型为____________,分子的立体构型为___________。
15. 已知:①CS ②PCl ③HS ④CH O ⑤HO+ ⑥ ⑦BF ⑧SO 。请回答下列问题:
2 3 2 2 3 3 2
(1)中心原子没有孤电子对的是______(填序号,下同)。
(2)空间结构为直线形的分子或离子有______;空间结构为平面三角形的分子或离子有______。
(3)空间结构为V形的分子或离子有______。
(4)空间结构为三角锥形的分子或离子有______;空间结构为正四面体形的分子或离子有______。
核心知识4 原子轨道的杂化与杂化轨道类型
16. 下列有关杂化轨道的说法不正确的是
A.四面体形、三角锥形、V形分子的结构可以用 杂化轨道解释
B. 、 、sp杂化轨道的夹角分别为109°28'、120°、180°
C.杂化轨道全部参加形成化学键
D.杂化前后的轨道数不变,但轨道的形状发生了改变
17. 下列图形表示 杂化轨道的电子云轮廓图的是
A. B. C. D.
18. 在乙烯分子中有5个 键、1个 键,它们分别是
A. 杂化轨道形成的 键、未杂化的 轨道形成的 键
B. 杂化轨道形成的 键、未杂化的 轨道形成的 键
C. 、 之间是 形成的 键, 、 之间是未参加杂化的 轨道形成的 键D. 、 之间是 形成的 键, 、 之间是未参加杂化的 轨道形成的 键
19. 从微粒结构角度分析,下列说法错误的是
A. 的空间结构为直线形,中心原子的杂化方式为sp
B.HCO 中C原子的杂化方式为sp2
2 3
C.三氧化硫有单分子气体和三聚分子固体( )两种存在形式,两种形式中S原子的杂化
轨道类型相同
D. ( 相当于 中一个氧被硫替代)中心原子S的杂化方式为sp3
20. 根据杂化轨道理论和价层电子对互斥模型,对下列分子或者离子的判断完全正确的是
选项 化学式 中心原子杂化方式 价层电子对互斥模型 分子或离子的立体构型
A sp2 正四面体形 三角锥形
B HO sp2 四面体形 V形
2
C NH sp3 三角锥形 平面三角形
3
D CH sp3 正四面体形 正四面体形
4
A.A B.B C.C D.D
核心知识5 杂化轨道类型与分子空间结构的关系
21. 鲍林提出杂化轨道理论能解释分子的空间结构,下列关于粒子的描述正确的是
选项 粒子 空间结构 解释
A SO V形 S原子采取sp2杂化
2
B CO 直线形 C原子采取sp2杂化
2
C C H 平面形 C原子采取sp3杂化
2 4
D 四面体形 Cl原子采取sp3杂化A.A B.B C.C D.D
22. 有几种阴离子的信息如下:
阴离子 M
中心元素化合价
中心原子杂化类型
下列推断不正确的是
A. 和 的价电子总数相同 B.M的化学式为
C. 、 中氯原子的杂化类型都为 D.M的空间结构为V形
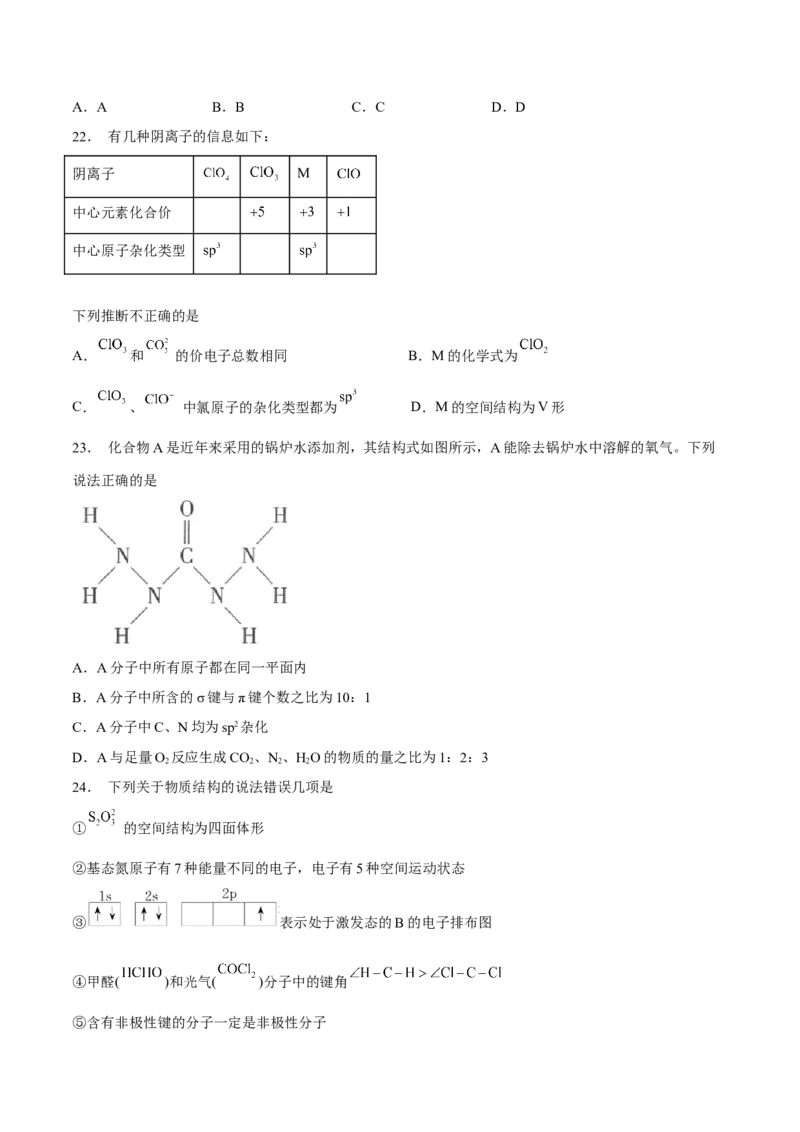
23. 化合物A是近年来采用的锅炉水添加剂,其结构式如图所示,A能除去锅炉水中溶解的氧气。下列
说法正确的是
A.A分子中所有原子都在同一平面内
B.A分子中所含的σ键与π键个数之比为10:1
C.A分子中C、N均为sp2杂化
D.A与足量O 反应生成CO、N、HO的物质的量之比为1:2:3
2 2 2 2
24. 下列关于物质结构的说法错误几项是
① 的空间结构为四面体形
②基态氮原子有7种能量不同的电子,电子有5种空间运动状态
③ 表示处于激发态的B的电子排布图
④甲醛( )和光气( )分子中的键角
⑤含有非极性键的分子一定是非极性分子⑥氢键的存在一定能使物质的熔、沸点升高
⑦ 、 、 均易溶于水的原因之一是与 均能形成氢键
⑧ 的沸点高于
⑨只要分子的空间结构为平面三角形,中心原子均为 杂化
⑩ 分子中 的键角
A.三项 B.四项 C.五项 D.六项
25. 氮元素可以形成多种化合物。回答以下问题:
(1)基态氮原子的价电子排布式是_________________。
(2)肼(N H)分子可视为NH 分子中的一个氢原子被-NH (氨基)取代形成的另一种氮的氢化物。
2 4 3 2
①NH 的结构式为_____。
2 4
②肼可用作火箭燃料,燃烧时发生的反应是:NO(l)+2NH(l)===3N (g)+4HO(g)
2 4 2 4 2 2
若该反应中有4mol N-H键断裂,则形成的π键有______mol。
③肼能与硫酸反应生成NHSO 。NHSO 与硫酸铵晶体类型相同,则NHSO 的晶体内不存在____。
2 6 4 2 6 4 2 6 4
A.离子键 B.共价键 C.配位键 D.范德华力
(3)FeCl 溶液与KSCN溶液混合,得到含多种配合物的红色溶液,其中配位数为5的配合物的化学式是
3
__________。KSCN中的阴离子与CO 互为等电子体,该阴离子的电子式是______________。
2
(4)美国科学家合成了结构呈“V”形对称的N+,已知该离子中各原子均达到8电子稳定结构。则有关该
5
离子的下列说法中正确的是_______________________。
A.每个N+中含有35个质子和36个电子
5
B.该离子中有非极性键和配位键
C.该离子中含有2个π键
D.与PCl +互为等电子体
4
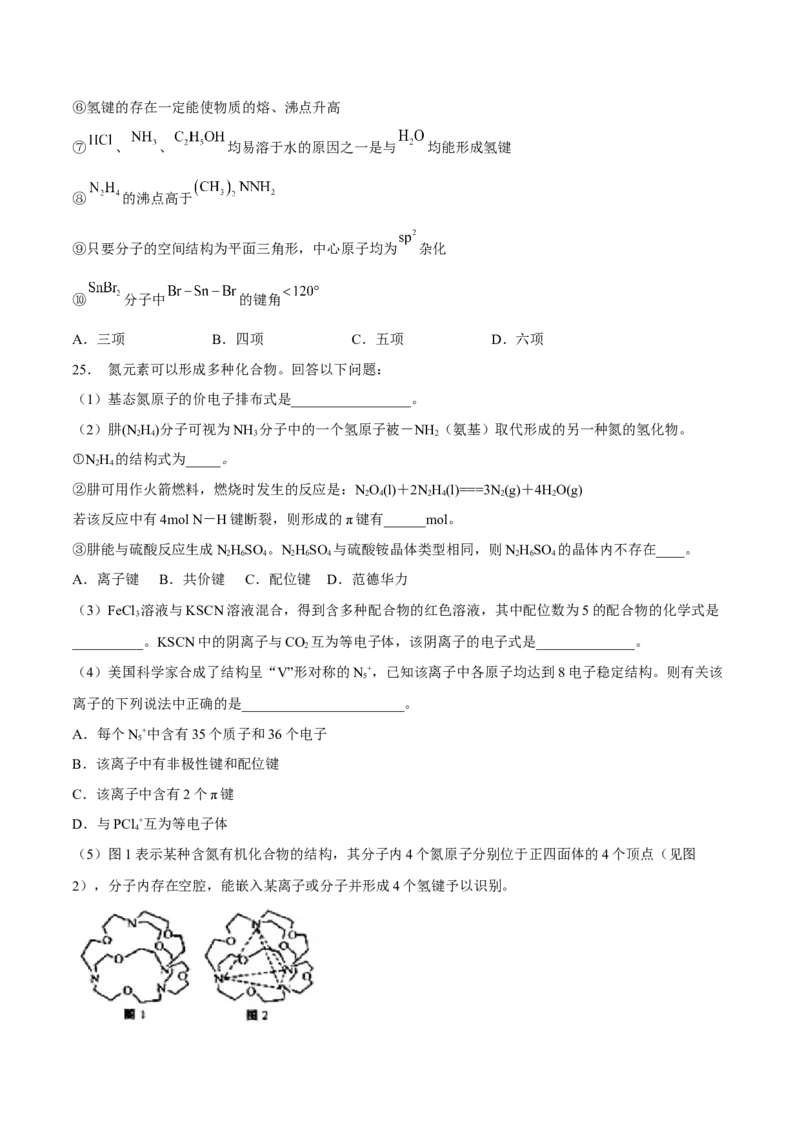
(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图
2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是_________(填标号)。
a.CF b.CH c.NH + d.HO
4 4 4 2
(6)N的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子
的构型为________形,阳离子中氮的杂化方式为_________。
核心知识6 键的极性、分子的极性及其判断
26. 下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是
A.2NaO+2H O=4NaOH+O
2 2 2 2
B.MgN+6H O=3Mg(OH)↓+2NH↑
3 2 2 2 3
C.2KOH+H SO =K SO +2H O
2 4 2 4 2
D.NH Cl+NaOH=NaCl+NH ↑+H O
4 3 2
27. 下列叙述中正确的是
A.以非极性键结合起来的双原子分子一定是非极性分子
B.以极性键结合起来的分子一定是极性分子
C.非极性分子只能是双原子单质分子
D.金属银晶体为面心立方最密堆积,其配位数为8
28. 下列各组物质中,都是由极性键构成的极性分子的是
A. 和 B. 和 C. 和 D. 和
29. 数据是科学推理中的重要证据,出下表中的数据,所得推论正确的是
羧酸
4.88
丙酸
4.76
乙酸
甲酸 3.75
2.86
氯乙酸
1.29
二氯乙酸
0.65
三氯乙酸
0.23
三氟乙酸A.相同浓度下,乙酸的酸性一定强于氯乙酸
B.烃基是吸电子基团,烃基越长,吸电子效应越大,使羧基中的羟基的极性越小,羧酸的酸性越弱
C.卤素原子是推电子基团,卤素原子使得羧基中羟基的极性变小,导致二氯乙酸的酸性强于一氯乙酸
D.氟原子的电负性大于氯原子,使 —的极性大于 —的极性,使三氟乙酸羧基中羟基的极性增大,
导致三氟乙酸容易电离出氢离子
30. 已知N、P同属于元素周期表的第VA族元素,N在第2周期,P在第3周期。NH 分子呈三角锥形,
3
氮原子位于锥顶,三个氢原子位于锥底,N—H键间的夹角是107°。
(1)PH 分子与NH 分子的构型关系是________(填“相同”或“相似”或“不相似”),P—H______极
3 3
性(填“有”或“无”),PH 分子________极性(填“有”或“无”)。
3
(2)NH 与PH 相比,热稳定性________更强(填化学式)。
3 3
(3)NH 、PH 在常温、常压下都是气体,但NH 比PH 易液化,其主要原因是________.
3 3 3 3
A.键的极性N—H比P—H强
B.分子的极性NH 比PH 强
3 3
C.相对分子质量PH 比NH 大
3 3
D.NH 分子之间存在特殊的分子间作用力
3
(4)笑气(NO)是一种麻醉剂,有关理论认为NO与CO 分子具有相似的结构(包括电子式)。已知
2 2 2
NO分子中氮原子只与氧原子相连,NO的电子式为____,其空间构型是____,由此可知它是____(填
2 2
“极性”或“非极性”)分子。
核心知识7 分子间作用力 分子的手性
31. 下列说法正确的是( )
A.范德华力是一种分子间作用力,也是一种特殊的化学键
B.非极性分子中,各原子间都以非极性键结合
C.常温常压下,卤素单质从F→I 由气态、液态到固态的原因是范德华力逐渐增大
2 2
D.HO是一种非常稳定的化合物,这是由于水分子间存在氢键
2
32. 物质的下列性质或数据与氢键无关的是A.水的沸点高于硫化氢
B.邻羟基苯甲酸( )的熔点为1.59°C,对羟基苯甲酸( )的熔
点为213°C
C.乙醇可与水以任意比混溶
D.HF的热稳定性大于HCl
33. 2001年诺贝尔化学奖授予在“手性碳原子的催化氢化、氧化反应”研究领域做出贡献的美、日三位
科学家。在有机物分子中,当碳原子连有四个不同的原子或基团时,这种碳原子称为“手性碳原子”,凡
具有一个手性碳原子的化合物一定具有光学活性。下列分子中含有“手性碳原子”的是
A.CBr F B.CHCHOH
2 2 3 2
C.CHCHCH D.CHCH(OH)COOH
3 2 3 3
34. 完成下列问题。
(1)3-氯-2-丁氨酸的结构简式为 ,1个该有机物分子中含有_______个手性
碳原子,其中-NH 中N原子的杂化轨道类型是_______。
2
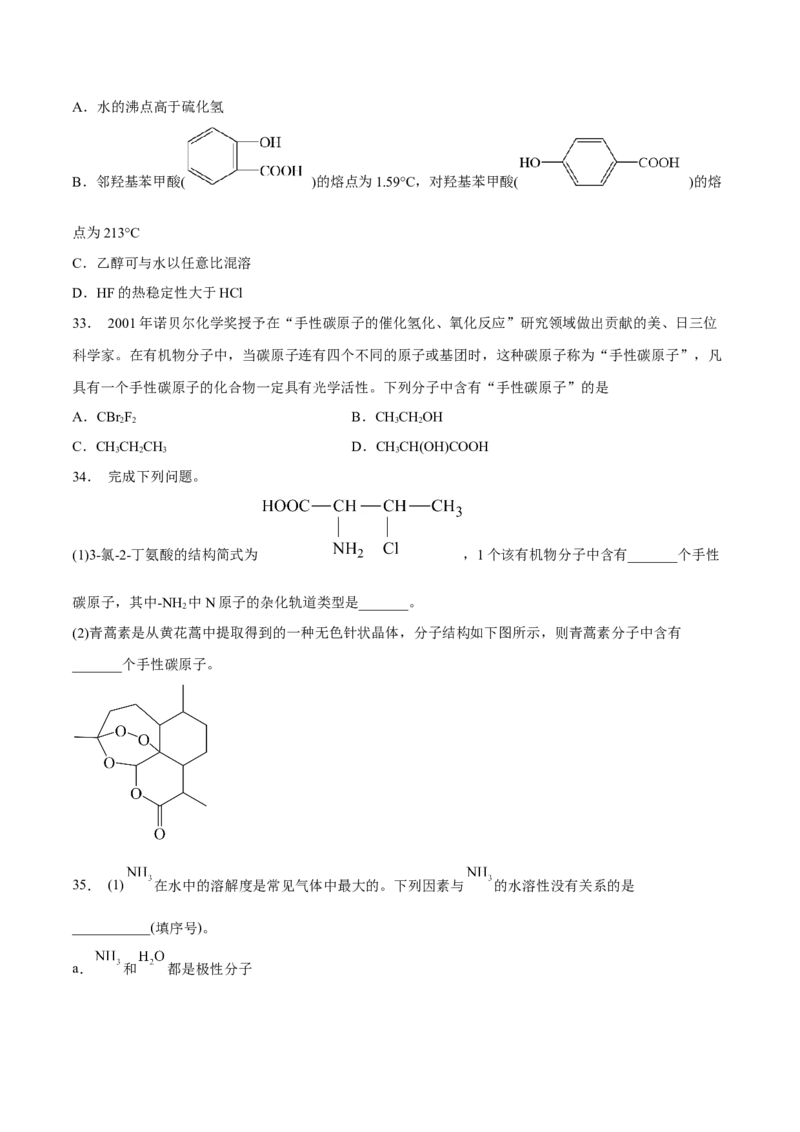
(2)青蒿素是从黄花蒿中提取得到的一种无色针状晶体,分子结构如下图所示,则青蒿素分子中含有
_______个手性碳原子。
35. (1) 在水中的溶解度是常见气体中最大的。下列因素与 的水溶性没有关系的是
___________(填序号)。
a. 和 都是极性分子b. 在水中易形成氢键
c. 溶于水建立了如下平衡:
d. 是一种易液化的气体
(2) 常温下为深红色液体,能与 、 等互溶,据此可判断 是___________(填“极性”
或“非极性”)分子。
(3)在①苯、② 、③HCHO、④ 、⑤ 五种有机溶剂中,碳原子采取 杂化的分子有
___________(填序号), 分子的空间结构是___________。 与 相比,___________的熔点较高。
(4)甲醛、甲醇和甲酸等碳原子个数较少的醛、醇和羧酸均易溶于水的原因是___________。