文档内容
高中化学人教版(2019)选择性必修1 第二章第一节 化学反应速率
一、单选题
1.决定化学反应速率的主要因素是( )
A. 反应物的性质 B. 反应温度
C. 使用催化剂 D. 反应物的
浓度
2.已知 4NH +5O = 4NO+6HO(g),若反应速率分别用 v(NH )、v(O )、v(NO)、v(H O)表示,则正确的关系是
3 2 2 3 2 2
( )
【来源:21·世纪·教育·网】
A. v(O )= v(NH) B. v(H O)= v(O ) C. v(H O)= v(NH) D. v(NO)= v(O )
2 3 2 2 2 3 2
3.“活化分子”是衡量化学反应速率快慢的重要依据,下列说法中不正确的是( )
A. 活化分子之间的碰撞一定是有效碰撞
B. 增大反应物的浓度,可使单位体积内的活化分子增多,反应速率加快
C. 对于有气体参加的反应,通过压缩容器增大压强,可使单位体积内的活化分子增多,反应速率加快
D. 催化剂能降低反应的活化能,使单位体积内的活化分子百分数增加
4.相同温度下,下列各组的反应中,前者速率一定大于后者的是( )
A. 10 mL 4 mol·L-1的NaHCO 溶液+10 mL 2 mol·L-1盐酸+20 mL水与20 mL 3 mol·L-1的NaHCO 溶
3 3
液+10 mL 2 mol·L-1盐酸+10 mL水
B. 同品质等质量的两份Al(OH) 分别与2 mol·L-1硫酸、2 mol ·L-1盐酸反应
3
C. 表面积完全相同的两块钠分别与200 mL、100 mL水反应
D. 0.5 mol·L-1的NaHCO 溶液分别与1 mol·L-1盐酸和0.5 mol·L-1硫酸混合
3
5.在标准状况下,将5.6 g铁粉投入100 mL 2 mol·L-1稀硫酸中,2 min时铁粉恰好完全溶解。关于该反应的
速率,四位同学提出了四种表示方法:
甲 v(Fe)=2.8 g·min-1; 乙 v(H SO )=1 mol·L-1·min-1;
2 4
丙 v(FeSO )=0.5 mol·L-1·min-1;
4
丁 v(H )=1.12 L·min-1。
2
下列说法正确的是( )
A. 甲错误,因为固体物质不能用来表示反应速率 B. 丁错误,因为速率的单位错误
C. 只有乙错误
D. 只有丙正确
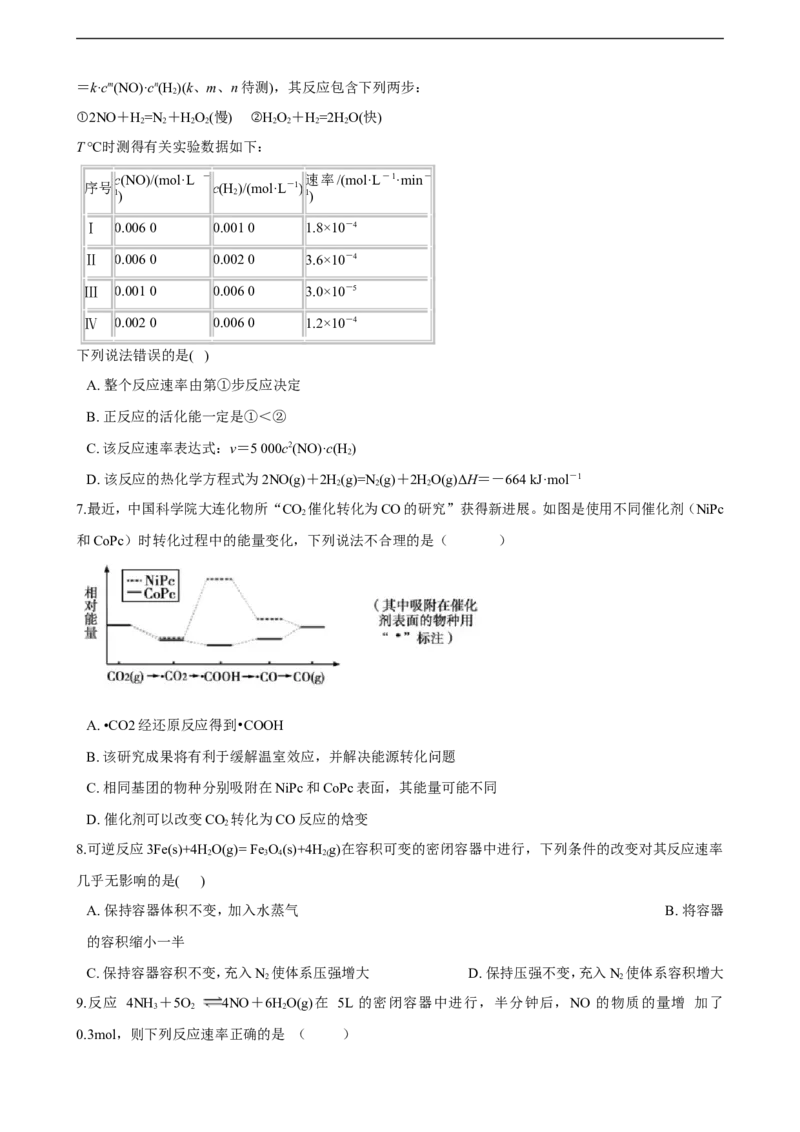
6.反应2NO(g)+2H(g)=N(g)+2HO(g)中,每生成7 g N , 放出166 kJ的热量,该反应的速率表达式为v
2 2 2 2=k·cm(NO)·cn(H )(k、m、n待测),其反应包含下列两步:
2
①2NO+H=N +HO(慢) ②HO+H=2H O(快)
2 2 2 2 2 2 2 2
T ℃时测得有关实验数据如下:
c(NO)/(mol·L - 速率/(mol·L-1·min-
序号 c(H )/(mol·L-1)
1) 2 1)
Ⅰ 0.006 0 0.001 0 1.8×10-4
Ⅱ 0.006 0 0.002 0 3.6×10-4
Ⅲ 0.001 0 0.006 0 3.0×10-5
Ⅳ 0.002 0 0.006 0 1.2×10-4
下列说法错误的是( )
A. 整个反应速率由第①步反应决定
B. 正反应的活化能一定是①<②
C. 该反应速率表达式:v=5 000c2(NO)·c(H )
2
D. 该反应的热化学方程式为2NO(g)+2H(g)=N(g)+2HO(g)ΔH=-664 kJ·mol-1
2 2 2
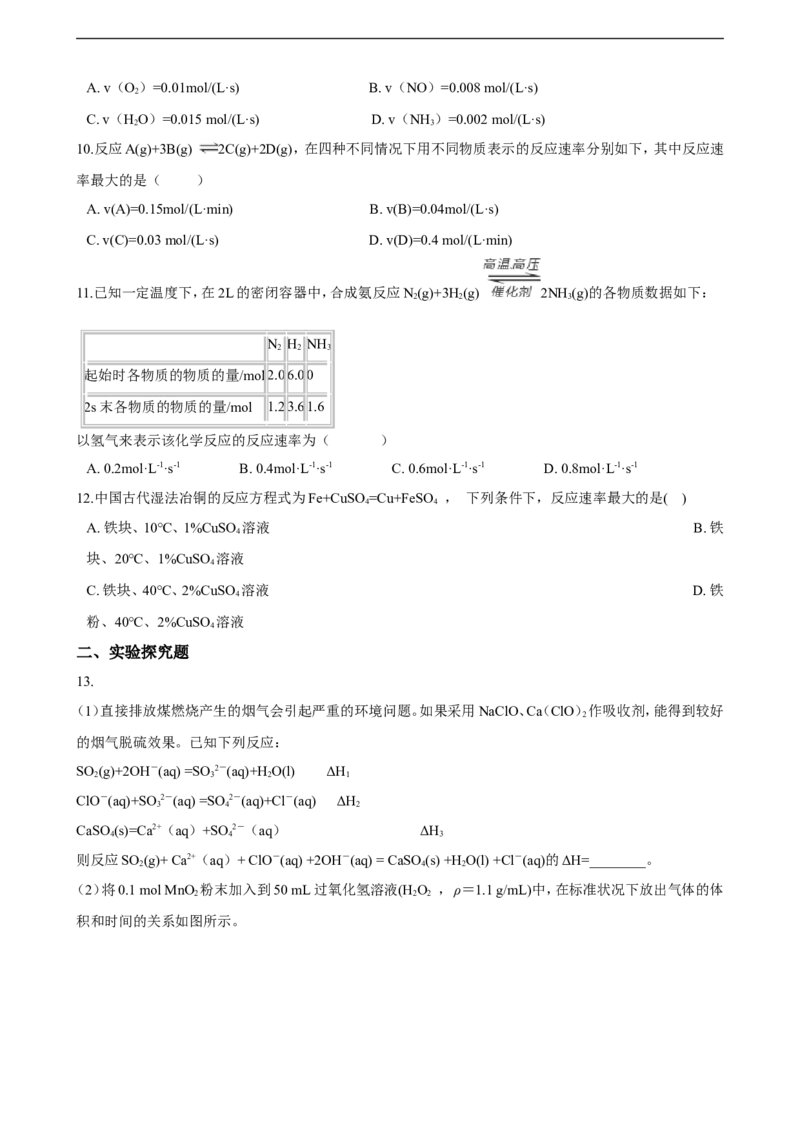
7.最近,中国科学院大连化物所“CO 催化转化为CO的研究”获得新进展。如图是使用不同催化剂(NiPc
2
和CoPc)时转化过程中的能量变化,下列说法不合理的是( )
www.21-cn-jy.com
A. •CO2经还原反应得到•COOH
B. 该研究成果将有利于缓解温室效应,并解决能源转化问题
C. 相同基团的物种分别吸附在NiPc和CoPc表面,其能量可能不同
D. 催化剂可以改变CO 转化为CO反应的焓变
2 2·1·c·n·j·y
8.可逆反应3Fe(s)+4H O(g)= Fe O(s)+4H g)在容积可变的密闭容器中进行,下列条件的改变对其反应速率
2 3 4 2(
几乎无影响的是( )
www-2-1-cnjy-com
A. 保持容器体积不变,加入水蒸气 B. 将容器
的容积缩小一半
C. 保持容器容积不变,充入N 使体系压强增大 D. 保持压强不变,充入N 使体系容积增大
2 2
9.反应 4NH +5O 4NO+6HO(g)在 5L 的密闭容器中进行,半分钟后,NO 的物质的量增 加了
3 2 2
0.3mol,则下列反应速率正确的是 ( )
2-1-c-n-j-yA. v(O)=0.01mol/(L·s) B. v(NO)=0.008 mol/(L·s)
2
C. v(HO)=0.015 mol/(L·s) D. v(NH )=0.002 mol/(L·s)
2 3
10.反应A(g)+3B(g) 2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速
率最大的是( )
A. v(A)=0.15mol/(L·min) B. v(B)=0.04mol/(L·s)
C. v(C)=0.03 mol/(L·s) D. v(D)=0.4 mol/(L·min)
11.已知一定温度下,在2L的密闭容器中,合成氨反应N(g)+3H(g) 2NH (g)的各物质数据如下:
2 2 3
N H NH
2 2 3
起始时各物质的物质的量/mol2.06.00
2s末各物质的物质的量/mol 1.23.61.6
以氢气来表示该化学反应的反应速率为( )
A. 0.2mol·L-1·s-1 B. 0.4mol·L-1·s-1 C. 0.6mol·L-1·s-1 D. 0.8mol·L-1·s-1
12.中国古代湿法冶铜的反应方程式为Fe+CuSO =Cu+FeSO , 下列条件下,反应速率最大的是( )
4 4
A. 铁块、10℃、1%CuSO 溶液 B. 铁
4
块、20℃、1%CuSO 溶液
4
C. 铁块、40℃、2%CuSO 溶液 D. 铁
4
粉、40℃、2%CuSO 溶液
4 21世纪教育网版权所有
二、实验探究题
13.
(1)直接排放煤燃烧产生的烟气会引起严重的环境问题。如果采用NaClO、Ca(ClO)作吸收剂,能得到较好
2
的烟气脱硫效果。已知下列反应:
21教育网
SO (g)+2OH-(aq) =SO 2-(aq)+H O(l) ΔH
2 3 2 1
ClO-(aq)+SO2-(aq) =SO 2-(aq)+Cl-(aq) ΔH
3 4 2
CaSO(s)=Ca2+(aq)+SO2-(aq) ΔH
4 4 3
则反应SO (g)+ Ca2+(aq)+ ClO-(aq) +2OH-(aq) = CaSO (s) +H O(l) +Cl-(aq)的ΔH=________。
2 4 2
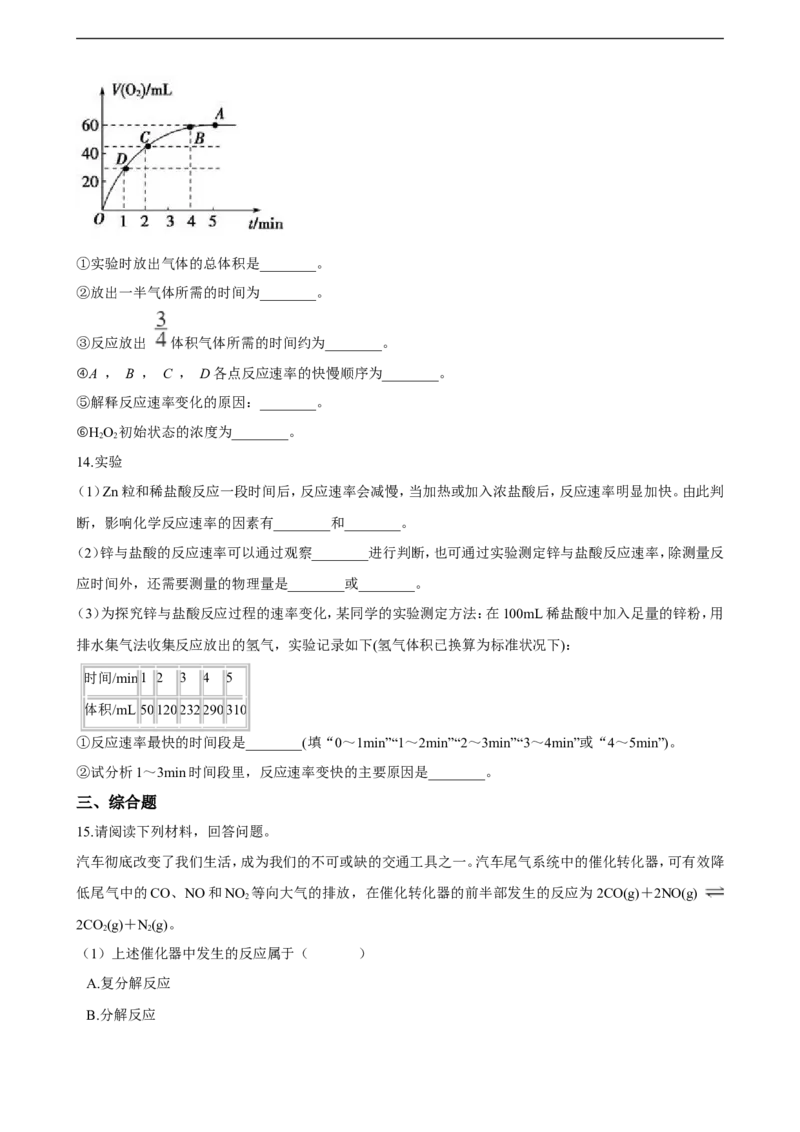
(2)将0.1 mol MnO 粉末加入到50 mL过氧化氢溶液(H O , ρ=1.1 g/mL)中,在标准状况下放出气体的体
2 2 2
积和时间的关系如图所示。
21*cnjy*com①实验时放出气体的总体积是________。
②放出一半气体所需的时间为________。
③反应放出 体积气体所需的时间约为________。
④A , B , C , D各点反应速率的快慢顺序为________。
⑤解释反应速率变化的原因:________。
⑥H O 初始状态的浓度为________。
2 2
14.实验
(1)Zn粒和稀盐酸反应一段时间后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快。由此判
断,影响化学反应速率的因素有________和________。
21教育名师原创作品
(2)锌与盐酸的反应速率可以通过观察________进行判断,也可通过实验测定锌与盐酸反应速率,除测量反
应时间外,还需要测量的物理量是________或________。
21*cnjy*com
(3)为探究锌与盐酸反应过程的速率变化,某同学的实验测定方法:在100mL稀盐酸中加入足量的锌粉,用
排水集气法收集反应放出的氢气,实验记录如下(氢气体积已换算为标准状况下):
时间/min1 2 3 4 5
体积/mL 50120232290310
①反应速率最快的时间段是________(填“0~1min”“1~2min”“2~3min”“3~4min”或“4~5min”)。
②试分析1~3min时间段里,反应速率变快的主要原因是________。
三、综合题
15.请阅读下列材料,回答问题。
汽车彻底改变了我们生活,成为我们的不可或缺的交通工具之一。汽车尾气系统中的催化转化器,可有效降
低尾气中的CO、NO和NO 等向大气的排放,在催化转化器的前半部发生的反应为2CO(g)+2NO(g)
2
2CO(g)+N(g)。
2 2
(1)上述催化器中发生的反应属于( )
A.复分解反应
B.分解反应C.置换反应
D.不属于四种基本反应
(2)关于反应2CO(g)+2NO(g) 2CO(g)+N(g)中,下列说法正确的是( )
2 2
A.CO作氧化剂
B.CO发生氧化反应
C.NO被氧化
D.NO作还原剂
(3)已知汽车尾气处理反应能量过程如下图,下列说法正确的是( )
A.该反应为放热反应
B.该反应为吸热反应
C.形成N≡N化学键需要吸收热量
D.反应物的总能量小于生成物的总能量
【来源:21cnj*y.co*m】
(4)下列反应条件的改变对该反应速率的影响正确的是( )
A.升高温度能减慢反应速率
B.增大反应物浓度能减缓反应速率
C.达到平衡时,CO能100%转化为CO
2
D.使用催化剂可以加快该反应的速率
【出处:21教育名师】
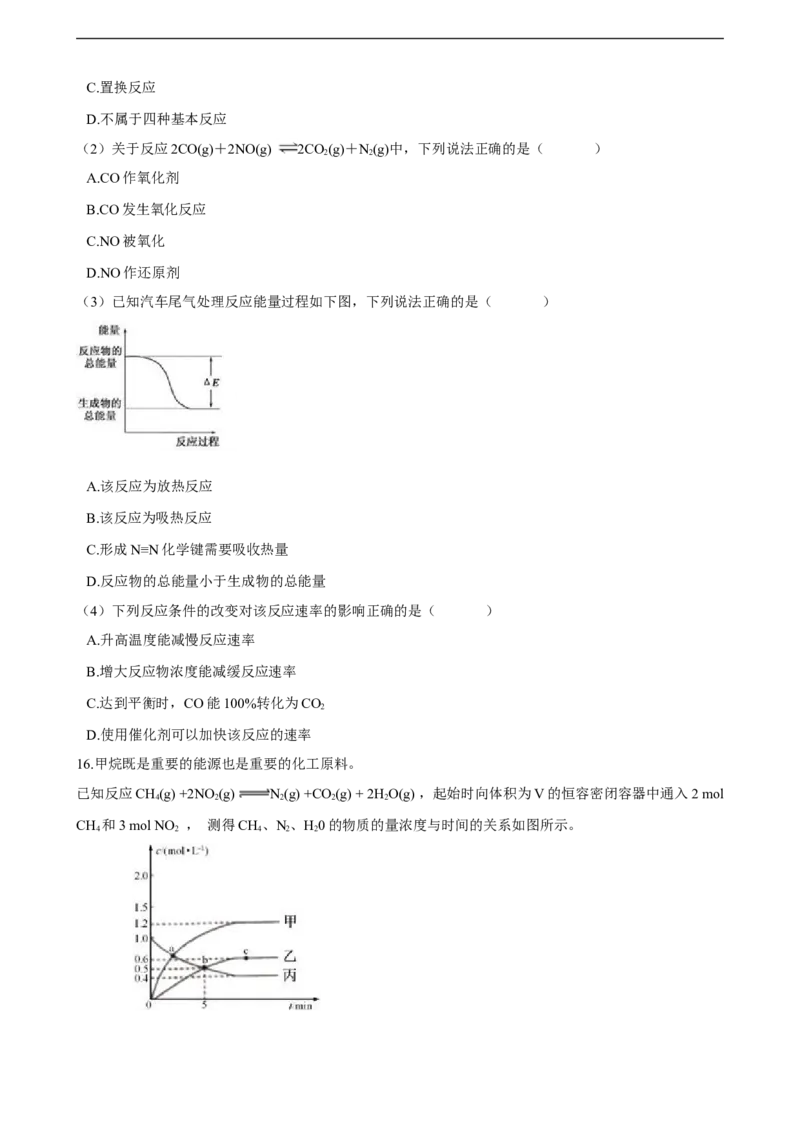
16.甲烷既是重要的能源也是重要的化工原料。
已知反应CH(g) +2NO (g) N(g) +CO (g) + 2HO(g) ,起始时向体积为V的恒容密闭容器中通入2 mol
4 2 2 2 2
CH 和3 mol NO , 测得CH、N、H0的物质的量浓度与时间的关系如图所示。
4 2 4 2 2(1)容器体积V=________L。
(2)图中表示HO的物质的量浓度与时间关系的是曲线________ (填“甲”“乙"或"丙")。
2
(3)0 ~5 min内,用N 表示的化学反应速率为________mol·L-1·min -1。
2
(4)a、b、c三点中达到平衡的点是________。 达到平衡时,NO 的转化率是________。
2
(物质平衡转化率=转化的物质的量/起始的物质的量 x100%)。
(5)a点时,n( CH ):n(NO ) =________。
4 2
答案解析部分
一、单选题
1. A
解析:决定化学反应速率的主要因素是反应物本身的性质,而浓度、温度、压强、催化剂是影响反应速率的
外界因素,
故答案为:A。
分析:化学反应速率受外因和本身的性质来决定。
2. A
解析:对于反应4NH
3
(g)+5O
2
(g)⇌4NO(g)+6H
2
O(g),
A.速率之比等于化学计量数之比,故v(NH ):v(O )=4:5,即v(O )= v(NH ),故A符合题意;
3 2 2 3
B.速率之比等于化学计量数之比,故v(O ):v(H O)=5:6,即v(H O)= v(O ),故B不符合题意;
2 2 2 2
C.速率之比等于化学计量数之比,故v(NH ):v(H O)=4:6,即v(H O)= v(NH ) ,故C不符合题意;
3 2 2 3
D.速率之比等于化学计量数之比,故v(O ):v(NO)=5:4,即v(NO)= v(O ) ,故D不符合题意;
2 2
故答案为A。
分析:同一化学反应中,不同物质表示的化学反应速率之比等于其化学计量数之比。
3. A
解析:A.活化分子的碰撞不一定能发生化学反应,而只有发生化学反应的碰撞才是有效碰撞,因此活化分子
之间的碰撞不一定是有效碰撞,选项错误,A符合题意;
B.增大反应物浓度,可增大单位体积内的活化分子数,使得反应速率加快,选项正确,B不符合题意;
C.对于有气体参与的反应,压缩体积,则单位时间内活化分子数增多,反应速率加快,选项正确,C不符合题
意;
D.催化剂可降低反应所需的活化能,使单位体积内的活化分子百分数增加,选项正确,D不符合题意;故答案为:A
分析:此题是对活化能的考查, 结合浓度、压强、催化剂对活化能的影响分析。
4. B
解析:A.前者的浓度小于后者,因此反应速率小于后者,A不符合题意;
B.2mol/L的硫酸溶液中c(H+)=4mol/L,2mol/L的盐酸溶液中c(H+)=2mol/L,前者c(H+)大,因此反应速率快,
B符合题意;
C.纯液体的浓度视为1,因此水的用量不影响反应速率,C不符合题意;
D.NaHCO 溶液的浓度相同,c(H+)也相同,因此二者的反应速率相同,D不符合题意;
3
故答案为:B
分析:此题是对反应速率影响因素的考查,解答此类题型时,应结合浓度、温度、压强、催化剂对反应速率
的影响进行分析。
5. C
解析:A.固体的浓度为常数,因此不用固体的浓度表示反应速率,但甲同学是用单位时间内固体减少的质量
表示反应速率,因此甲同学的说法正确,A不符合题意;
B.该反应过程中生成H 的物质的量为0.1mol,其在标准状态下的体积V=0.1mol×22.4L/mol=2.24L,因此单
2
位时间内产生H 的体积为1.12L,故可用v(H )=1.12L/min表示反应速率,丁同学的说法正确,B不符合题意;
2 2
C.该过程中 2min 内参与反应的 HSO 的物质的量为 0.1mol/L,因此用 HSO 表示的反应速率为
2 4 2 4
v(H SO )=0.05mol/(L·min),乙同学说法错误,C符合题意;
2 4
D.该过程中2min内生成FeSO 的物质的量为0.1mol/L,因此用FeSO 表示的反应速率为0.05mol/(L·min),
4 4
丙同学的说法错误,D不符合题意;
故答案为:C
分析:由单位确定该速率所表示的含义,从而确定该反应速率的表达是否正确。
6. B
解析:A.第①步反应为慢反应,反应速率为慢反应决定,因此整个反应速率由第①步反应决定,选项正确,A
不符合题意;
21·世纪*教育网
B.由于反应②的速率大于反应①,而反应速率越快,活化能越小,因此正反应的活化能①>②,选项错误,B
符合题意;
C.将实验Ⅰ、Ⅱ、Ⅲ数据代入反应速率的表达式v=k·cm(NO)·cn(H )中,可得k=5000、m=2、n=1,因此
2
k=5000c²(NO)·c(H ),选项正确,C不符合题意;
2
D.7gN 的 物 质 的 量 , 因 此 生 成 1molN 时 放 出 的 热 量 为
2 2
166kJ÷0.25mol=664kJ/mol,因此该反应的热化学方程式为 2NO(g)+2H(g)=N(g)+2HO(g)ΔH=-664
2 2 2
kJ·mol-1 , 选项正确,D不符合题意;故答案为:B
分析:A.反应速率的快慢主要由慢反应决定;
B.活化能越低,反应速率越快;
C.根据反应速率的表达式确定k、m、n的值,从而确定反应速率的表达式;
D.根据7gN 放出的热量计算反应热,从而得出反应的热化学方程式;
2
7. D
解析:A. •CO 转化为•COOH的过程中,碳元素的化合价降低,因此•CO 得到•COOH是还原反应,A符合
2 2
题意;
B. 该过程中,CO 转化为CO,可减少空气中的CO 的含量,缓解温室效应,同时反应生成CO具有可燃性,
2 2
可解决能源转化危机,B符合题意;
【版权所有:21教育】
C. 由图可知,•COOH吸附在NiPc中的能量高于吸附在CoPc上的能量,因此吸附在相同基团的物种分别吸
附在NiPc和CoPc表面,其能量不同,C符合题意;
D. 催化剂只影响反应速率,不改变反应焓变,D不符合题意;
故答案为:D。
分析:A. 根据物质的化合价变化分析;
B. 根据反应过程中物质转换分析;
C. 根据图示相对能量大小分析;
D. 催化剂只改变反应速率,不改变反应平衡和焓变;
8. C
解析:A.保持体积不变,充入水蒸气反应物浓度增大,反应速率增大,A不符合题意;
B.将容器的体积缩小一半,气体浓度增大,反应速率增大,B不符合题意;
C.保持体积不变,充入N , N 不参与反应,反应体系中的各物质的浓度不变,则反应速率不变,C符合题
2 2
意;
D.压强不变,充入N 使容器的体积增大,气体的浓度减小,反应速率减小,D不符合题意。
2
故答案为:C
分析:A.反应物浓度增大,正反应速率加快;
B.容器的体积缩小,气体浓度增大,反应速率加快;
C. 保持容器容积不变,充入无关气体对反应速率无影响;
D.反应物的浓度减小,反应速率变慢。
21cnjy.com
9. D
解析:A. 5L 的密闭容器中进行,半分钟后,NO 的物质的量增加了 0.3mol,则 v(NO)==0.002mol/(L·s)。V(O )= v(NO)=0.002mol/(L·s)× =0.0025mol/(L·s),A不符合题意;
2
B.由上述计算可知,v(NO)=0.002mol/(L·s),B不符合题意;
C.V(H O)= v(NO)=0.002mol/(L·s)× =0.003mol/(L.s),故不符合题意;
2
D.V(NH)=v(NO)=0.002mol/(L·s),D符合题意。
3
故答案为:D
分析:先计算NO的反应速率,然后根据化学反应速率和化学计量数成正比计算其他各物质的反应速率即
可;
21·cn·jy·com
10. C
解析:不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,对于反应:A(g)+3B(g)
2C(g)+2D(g);
A. =0.15 mol/(L•min);
B.v(B)=0.04mol/(L•s)=2.4 mol/(L•min),此时v(A)= =0.8mol/(L•min);
C.v(C)=0.03mol/(L•s)=1.8mol/(L•min),此时v(A)= =0.9 mol/(L•min);
D.v(D)=0.4mol/(L•min),此时v(A)= =0.2 mol/(L•min);故反应速率C>B>D>A。
故答案为:C
分析:根据化学反应速率和化学计量数成正比,当各物质的反应速率和其化学计量数的比值越大的,则反
应速率越快,越小的则越慢,据此进行解答,需要注意必须统一单位。
11. C
解析:由表格数据可知,△n(H )=6.0mol-3.6mol=2.4mol,则以氨气来表示该化学反应的反应速率为
2
=0.6 mol·L-1·s-1 , C符合题意。
故答案为:C分析:根据= 进行计算。
12. D
解析:综合考虑反应物接触面积、反应温度、反应物浓度三重因素,选择D项铁粉、40℃、2%CuSO 溶液有最
4
大的反应速率,D符合题意。
故答案为:D
分析:化学反应速率的影响因素:1.压强条件:对于有气体参与的化学反应,其他条件不变时(除体积),增大压
强,即体积减小,反应物浓度增大,单位体积内活化分子数增多,单位时间内有效碰撞次数增多,反应速率加快;
反之则减小。
2.温度条件:只要升高温度,反应物分子获得能量,使一部分原来能量较低分子变成活化分子,增加了活化分
子的百分数,使得有效碰撞次数增多,故反应速率加大(主要原因)。
3.催化剂:使用正催化剂能够降低反应所需的能量,使更多的反应物分子成为活化分子,大大提高了单位体
积内反应物分子的百分数,从而成千上万倍地增大了反应物速率.负催化剂则反之。
4.条件浓度:当其它条件一致下,增加反应物浓度就增加了单位体积的活化分子的数目,从而增加有效碰撞,
反应速率增加,但活化分子百分数是不变的。
5.其他因素:增大一定量固体的表面积(如粉碎),可增大反应速率,光照也可增大某些反应的速率;此外,超声
波、电磁波、溶剂等对反应速率也有影响。
二、实验探究题
13. (1)ΔH+ΔH-ΔH
1 2 3
(2)60 mL;1 min;2 min;D>C>B>A;随着反应的进行,HO 的浓度减小,反应速率减小;0.11 mol/L
2 2
解析:(1)根据盖斯定律可得,该反应的反应热ΔH=ΔH+ΔH -ΔH 。
1 2 3
(2)①由坐标图可知,反应进行至5min时完全反应,生成O 的体积为60mL;
2
②由坐标图可知,反应放出30mL气体所需的时间为1min;
③反应放出 体积O2(即45mL)时,所需时间为2min;
④曲线上A、B、C、D四点的斜率D>C>B>A,曲线的斜率越大,反应速率越快,因此反应速率D>C>B>A;
⑤反应过程中HO 的浓度逐渐减小,因此反应速率逐渐减慢;
2 2
⑥HO 完全反应时放出O 的物质的量 , 则参与反应的HO 的物质的
2 2 2 2 2
量为 , 则其物质的量浓度 。分析:(1)根据盖斯定律计算反应热;
(2)①5min后生成O 的体积最多;
2
②根据坐标图确定生成一半体积所需的时间;
③根据坐标图确定生成 体积所需的时间;
④根据曲线斜率确定反应速率;
⑤根据难度对反应速率的影响分析;
⑥根据反应生成O 的量,结合反应的化学方程式进行计算;
2
14. (1)反应温度;反应物浓度
(2)产生气泡的快慢;单位时间内产生气体的体积;单位时间内消耗锌的质量
(3)2~3min;该反应放热
解析:(1)温度越高,反应速率越快,适当提高反应物浓度,可以加快反应速率。Zn粒和稀盐酸反应一段时间
后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快。由此判断,影响化学反应速率的因素有
反应温度和反应物浓度;
(2)锌与盐酸的反应速率可以通过观察产生气泡的快慢进行判断,也可通过实验测定锌与盐酸反应速率,
除测量反应时间外,还需要测量的物理量是单位时间内产生气体的体积;
(3)①“0~1min”“1~2min”“2~3min”“3~4min”或“4~5min”对应时间段气体体积的变化量分别是:
70mL、112mL、58mL、20mL,反应速率最快的时间段是2~3min;
②1~3min时间段里,反应速率变快的主要原因是该反应放热,溶液温度升高,反应速率加快。
分析:(1)影响反应速率的因素包括: 浓度、温度、压强和催化剂,另外还有光、超声波、激光、搅拌、固体表
面积、形成原电池等 , 注意结合题意分析;
( 2)锌与盐酸的反应有H2产生,可以根据H2产生快慢,判断反应进行的快慢,而通过H2来计算反应速率,
需要检测其体积和对应的时间;
(3)①单位时间产生的气体体积大,则反应速率快;
②锌与盐酸的反应为放热反应。
三、综合题
15. (1)D
(2)B
(3)A
(4)D
解析:(1)A、上述反应为气体之间发生的反应,而复分解反应是指在溶液中发生的反应,因此上述反应不属于复分解反应,A不符合题意;
B、分解反应的特点是“一变多”,即反应物只有一种,生成物有多种,上述反应不属于分解反应,B不符合
题意;
C、置换反应是指单质与化合物反应生成新的单质和新的化合物,上述反应中反应物都是化合物,因此不属
于置换反应,C不符合题意;
D、上述反应不属于复分解反应、分解反应和置换反应,D符合题意;
故答案为:D
( 2)A、该反应中,CO中碳元素由+2价变为+4价, 化合价升高,发生氧化反应,为还原剂,A不符合题意;
B、该反应中,CO中碳元素由+2价变为+4价, 化合价升高,发生氧化反应,B符合题意;
C、该反应中,NO中氮元素由+2价变为0价,化合价降低,发生还原反应,被还原,C不符合题意;
D、该反应中,NO发生还原反应,为氧化剂,D不符合题意;
故答案为:B
(3)A、由图可知,反应物的总能量高于生成物的总能量,因此该反应为放热反应,A符合题意;
B、由A的分析可知,该反应为放热反应,B不符合题意;
C、反应过程中形成化学键需要释放能量,C不符合题意;
D、由图可知,该反应中反应物的总能量高于生成物的总能量,D不符合题意;
故答案为:A
(4)A、温度升高,反应速率加快,A不符合题意;
B、增大反应物浓度,反应速率加快,B不符合题意;
C、可逆反应达到平衡状态时,反应物仍有剩余,无法完全转化为生成物,C不符合题意;
D、催化剂可降低反应所需的活化能,因此使用催化剂可加快反应速率,D符合题意;
故答案为:D
分析:(1)根据发生的反应结合反应类型的特点进行分析;
(2)根据反应过程中元素化合价的变化和氧化还原反应的相关概念分析;
(3)根据图示能量变化确定反应的热效应,再结合选项分析;
(4)结合浓度、温度、压强、催化剂对反应速率的影响和可逆反应的特点分析;
16. (1)2
(2)甲
(3)0.1
(4)C;80% 或0.8
(5)4:5解析:(1)由分析可知,丙为CH , 充入CH 的物质的量为2mol,此时CH 的物质的量浓度为1.0mol/L,因
4 4 4
此可得,溶液的体积V=2L;
(2)由分析可知,图中表示HO的物质的量浓度与时间关系的是曲线甲;
2
( 3 ) 由 图 可 知 , 0~5min 内 , 反 应 生 成 c(N2)=0.5mol/L , 因 此 用 N2 表 示 的 反 应 速 率
;
( 4)反应达到平衡状态时,体系内各物质的物质的量浓度保持不变,因此a、b、c三点中表示反应达到平衡
状态的点是c;由图可知,当反应达到平衡状态时,参与反应的CH 的物质的量为(1.0mol/L-0.4mol/
4
L)×2L=1.2mol,因此参与反应的n(NO )=2×1.2mol=2.4mol,因此反应达到平衡状态时,NO 的转化率为:
2 2
;
( 5)由图可知,a点时体系内c(HO)=c(CH),令c(HO)=c(CH)=a mol/L,则由反应的化学方程式可知,参与
2 4 2 4
反应的c(CH)=(1-a)mol/L,反应生成的c(HO)=(2-2a)mol/L,因此可得2-2a=a,解得a= mol/L,则参与反应
4 2
的 c(CH)=(1- )= mol/L , 参 与 反 应 的 , 则 此 时 体 系 中 剩 余
4
因此a点时,n(CH):n(NO )=c(CH ):c(NO)= =4:5;
4 2 4 2
分析:由图可知,相同时间内,甲、乙两物质参与反应的物质的量浓度之比为2:1,因此甲为HO,以为N 或
2 2
CO;甲与丙的物质的量浓度之比为2:1,因此丙为CH;据此结合题干设问分析作答。
2 4