文档内容
第二章 第一节 第2课时 影响化学反应速率的因素 活化能 测试题
榆次一中 李金虎
一、选择题(本题共有15小题,每小题4分,共60分,每小题只有一个正确选项)
1. 下列说法正确的是( )
A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增多
B.有气体参加的化学反应,若增大压强(即缩小反应容器的容积),可增大活化分子的百分数,
从而使反应速率增大
C.升高温度能使化学反应速率增大的主要原因是减小了反应物分子中活化分子的百分数
D.催化剂能增大单位体积内活化分子的百分数,从而成千上万倍地增大反应速率
2. 过量锌粉跟100 mL 6 mol·L-1的HSO 反应,一定温度下,为减缓反应进行的速率,但又不影
2 4
响生成氢气的总量,可向反应物中加入适量的( )
A.碳酸钠固体 B.氯化钡固体
C.硫酸钾溶液 D.硫酸铜溶液
3. 对于有气体参加的反应,一定能使化学反应速率加快的因素是( )
①扩大容器的容积 ②使用催化剂 ③增加反应物的物质的量 ④升高温度
⑤缩小容积 ⑥增大容器内的压强
A.②③ B.②③④⑥
C.②④⑤ D.②④
4. 一定温度下,反应① C(s)+CO(g)===2CO(g) ΔH>0,反应② 2SO (g)+O(g)===2SO(g)
2 2 2 3
ΔH<0。下列有关以上两个反应的说法正确的是( )
A.降低温度反应①的速率减小,反应②的速率增大
B.增大压强反应①的速率不变,反应②的速率增大
C.增大压强反应①的速率增大,反应②的速率增大
D.升高温度反应①的速率增大,反应②的速率减小
5. 下列有关有效碰撞的说法不正确的是( )
A.能发生有效碰撞的分子一定是活化分子
B.有效碰撞是发生化学反应的充要条件
C.只要条件合适,普通分子之间的碰撞也可能是有效碰撞
D.活化分子间的碰撞不一定是有效碰撞
6. 下列说法正确的是( )
A.活化能接近零的反应,当反应物相互接触时,反应瞬间完成,而且温度对其反应速率几乎没有
影响
1
学科网(北京)股份有限公司B.升高温度和增大压强都是通过增大活化分子百分数来加快化学反应速率的
C.人们把能够发生有效碰撞的分子叫做活化分子,把活化分子具有的能量叫做活化能
D.活化能的大小不仅意味着一般分子成为活化分子的难易,也会对化学反应前后的能量变化产
生影响
7. 工业上利用可逆反应N(g)+3H(g) 2NH (g)合成氨,下列叙述正确的是( )
2 2 3
A.合成氨的适宜条件是高温、高压、催化剂,其中催化剂不改变该反应的逆反应速率
B.恒容通入氩气,使反应体系的压强增大,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
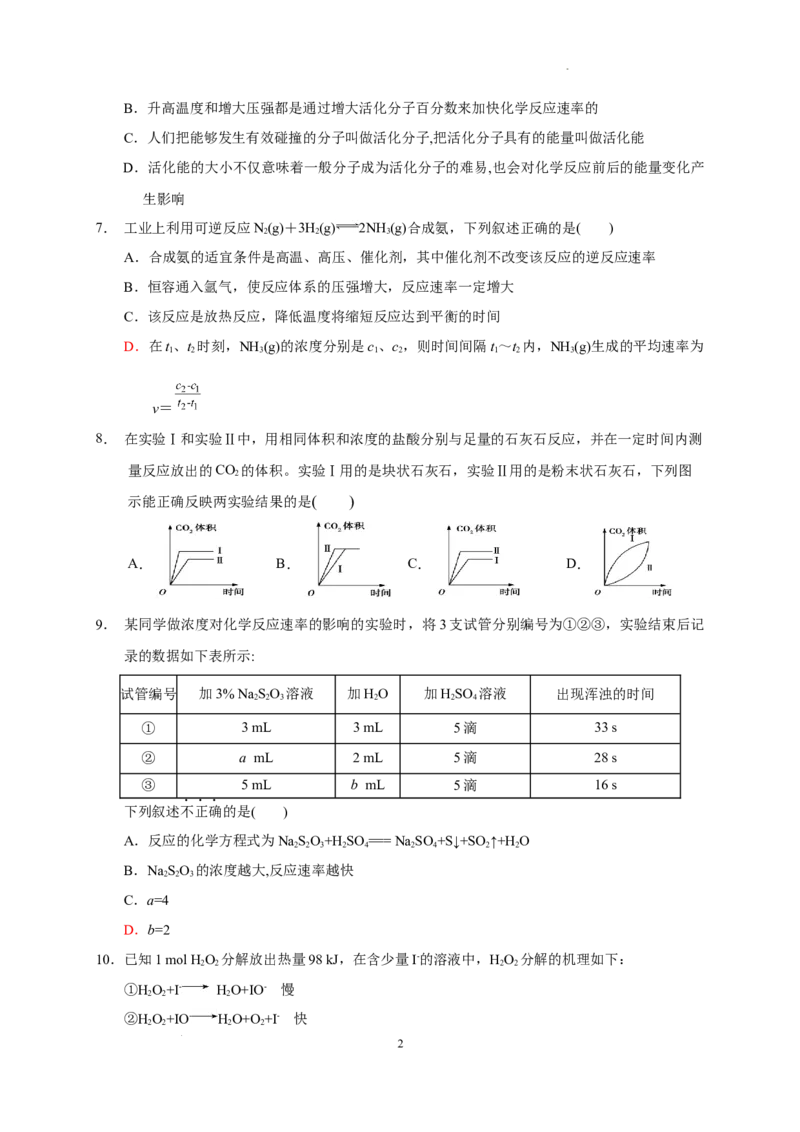
D.在t、t 时刻,NH (g)的浓度分别是c、c,则时间间隔t~t 内,NH (g)生成的平均速率为
1 2 3 1 2 1 2 3
v=
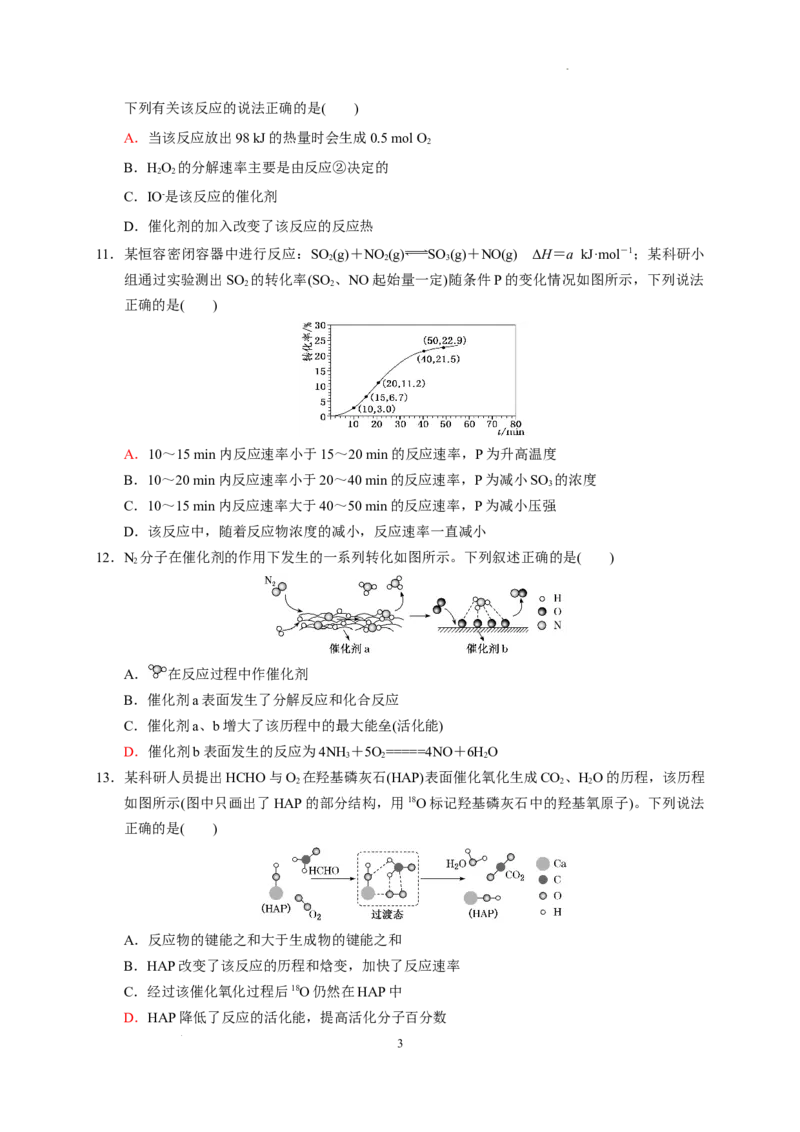
8. 在实验Ⅰ和实验Ⅱ中,用相同体积和浓度的盐酸分别与足量的石灰石反应,并在一定时间内测
量反应放出的CO 的体积。实验Ⅰ用的是块状石灰石,实验Ⅱ用的是粉末状石灰石,下列图
2
示能正确反映两实验结果的是( )
A. B. C. D.
9. 某同学做浓度对化学反应速率的影响的实验时,将3支试管分别编号为①②③,实验结束后记
录的数据如下表所示:
试管编号 加3% Na SO 溶液 加HO 加HSO 溶液 出现浑浊的时间
2 2 3 2 2 4
① 3 mL 3 mL 5滴 33 s
② a mL 2 mL 5滴 28 s
③ 5 mL b mL 5滴 16 s
下列叙述不正确的是( )
A.反应的化学方程式为NaSO+H SO === Na SO +S↓+SO ↑+H O
2 2 3 2 4 2 4 2 2
B.NaSO 的浓度越大,反应速率越快
2 2 3
C.a=4
D.b=2
10.已知1 mol H O 分解放出热量98 kJ,在含少量I-的溶液中,HO 分解的机理如下:
2 2 2 2
①HO+I- HO+IO- 慢
2 2 2
②HO+IO- HO+O+I- 快
2 2 2 2
2
学科网(北京)股份有限公司下列有关该反应的说法正确的是( )
A.当该反应放出98 kJ的热量时会生成0.5 mol O
2
B.HO 的分解速率主要是由反应②决定的
2 2
C.IO-是该反应的催化剂
D.催化剂的加入改变了该反应的反应热
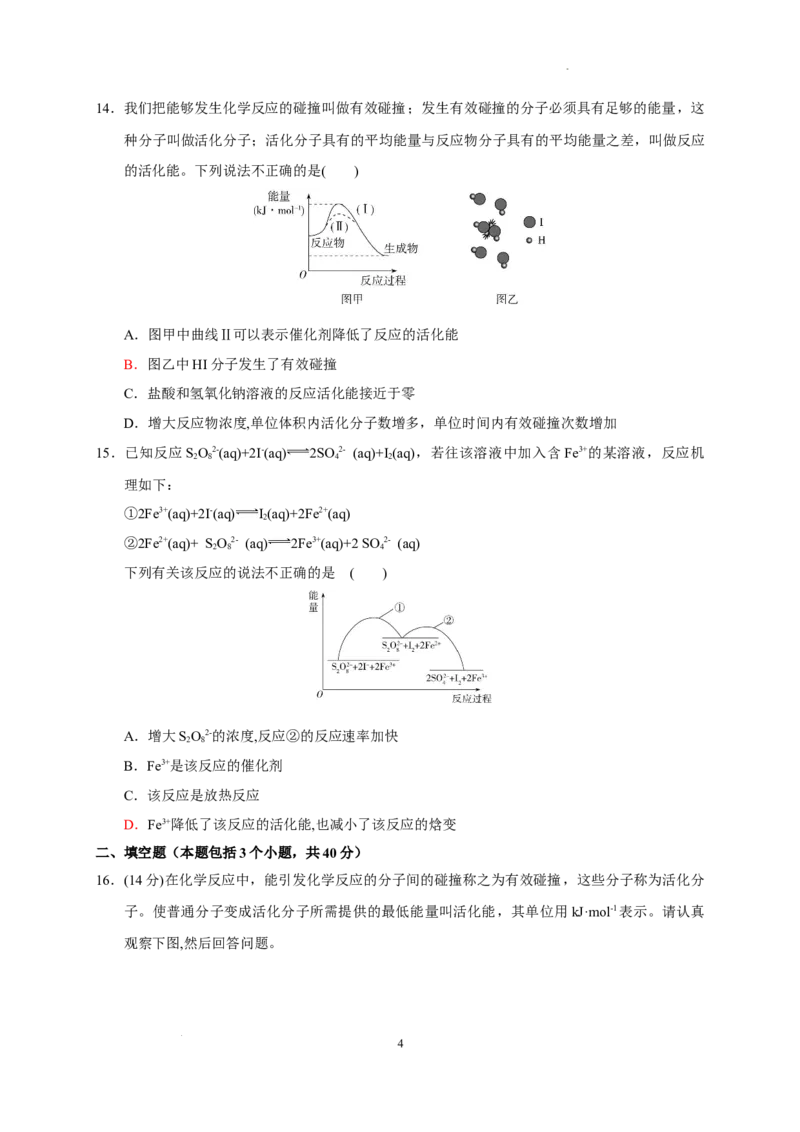
11.某恒容密闭容器中进行反应:SO (g)+NO (g) SO (g)+NO(g) ΔH=a kJ·mol-1;某科研小
2 2 3
组通过实验测出SO 的转化率(SO 、NO起始量一定)随条件P的变化情况如图所示,下列说法
2 2
正确的是( )
A.10~15 min内反应速率小于15~20 min的反应速率,P为升高温度
B.10~20 min内反应速率小于20~40 min的反应速率,P为减小SO 的浓度
3
C.10~15 min内反应速率大于40~50 min的反应速率,P为减小压强
D.该反应中,随着反应物浓度的减小,反应速率一直减小
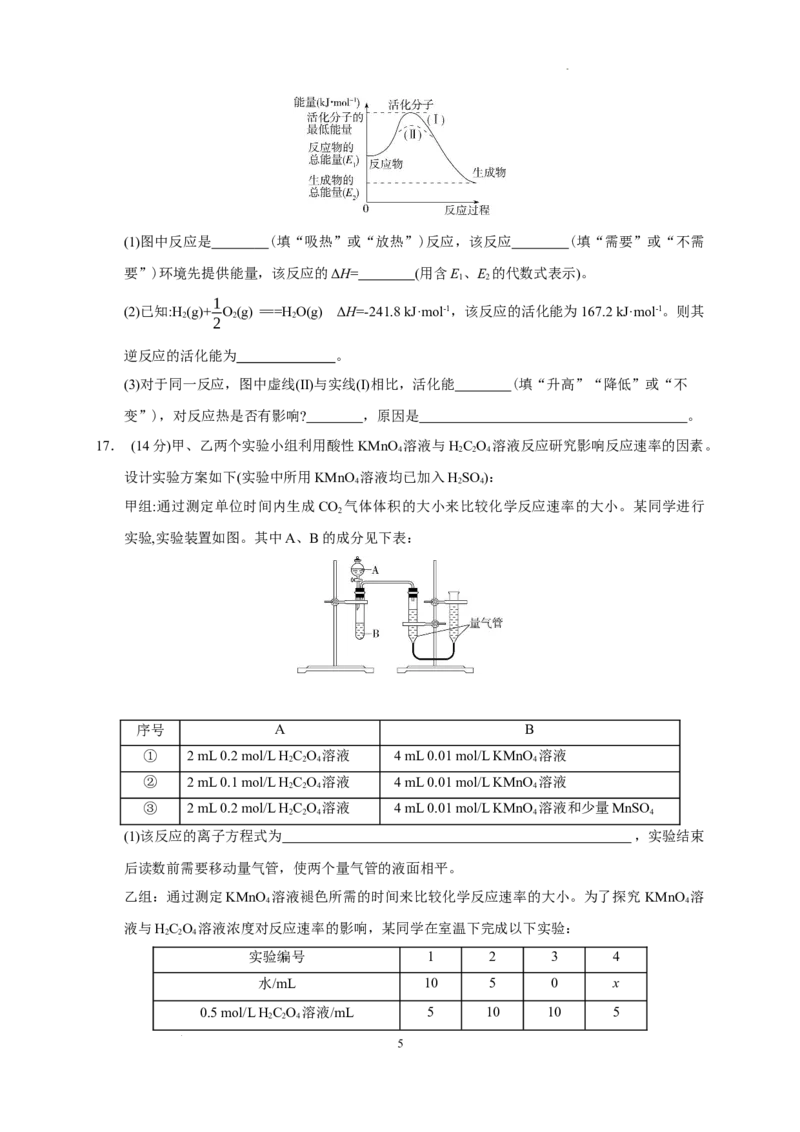
12.N 分子在催化剂的作用下发生的一系列转化如图所示。下列叙述正确的是( )
2
A. 在反应过程中作催化剂
B.催化剂a表面发生了分解反应和化合反应
C.催化剂a、b增大了该历程中的最大能垒(活化能)
D.催化剂b表面发生的反应为4NH +5O=====4NO+6HO
3 2 2
13.某科研人员提出HCHO与O 在羟基磷灰石(HAP)表面催化氧化生成CO 、HO的历程,该历程
2 2 2
如图所示(图中只画出了HAP的部分结构,用18O标记羟基磷灰石中的羟基氧原子)。下列说法
正确的是( )
A.反应物的键能之和大于生成物的键能之和
B.HAP改变了该反应的历程和焓变,加快了反应速率
C.经过该催化氧化过程后18O仍然在HAP中
D.HAP降低了反应的活化能,提高活化分子百分数
3
学科网(北京)股份有限公司14.我们把能够发生化学反应的碰撞叫做有效碰撞;发生有效碰撞的分子必须具有足够的能量,这
种分子叫做活化分子;活化分子具有的平均能量与反应物分子具有的平均能量之差,叫做反应
的活化能。下列说法不正确的是( )
A.图甲中曲线Ⅱ可以表示催化剂降低了反应的活化能
B.图乙中HI分子发生了有效碰撞
C.盐酸和氢氧化钠溶液的反应活化能接近于零
D.增大反应物浓度,单位体积内活化分子数增多,单位时间内有效碰撞次数增加
15.已知反应SO2-(aq)+2I-(aq) 2SO2- (aq)+I (aq),若往该溶液中加入含Fe3+的某溶液,反应机
2 8 4 2
理如下:
①2Fe3+(aq)+2I-(aq) I(aq)+2Fe2+(aq)
2
②2Fe2+(aq)+ SO2- (aq) 2Fe3+(aq)+2 SO2- (aq)
2 8 4
下列有关该反应的说法不正确的是 ( )
A.增大SO2-的浓度,反应②的反应速率加快
2 8
B.Fe3+是该反应的催化剂
C.该反应是放热反应
D.Fe3+降低了该反应的活化能,也减小了该反应的焓变
二、填空题(本题包括3个小题,共40分)
16.(14分)在化学反应中,能引发化学反应的分子间的碰撞称之为有效碰撞,这些分子称为活化分
子。使普通分子变成活化分子所需提供的最低能量叫活化能,其单位用kJ·mol-1表示。请认真
观察下图,然后回答问题。
4
学科网(北京)股份有限公司(1)图中反应是 (填“吸热”或“放热”)反应,该反应 (填“需要”或“不需
要”)环境先提供能量,该反应的ΔH= (用含E、E 的代数式表示)。
1 2
1
(2)已知:H (g)+ O(g) ===H O(g) ΔH=-241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1。则其
2 2 2
2
逆反应的活化能为 。
(3)对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能 (填“升高”“降低”或“不
变”),对反应热是否有影响? ,原因是 。
17. (14分)甲、乙两个实验小组利用酸性KMnO 溶液与HC O 溶液反应研究影响反应速率的因素。
4 2 2 4
设计实验方案如下(实验中所用KMnO 溶液均已加入HSO ):
4 2 4
甲组:通过测定单位时间内生成CO 气体体积的大小来比较化学反应速率的大小。某同学进行
2
实验,实验装置如图。其中A、B的成分见下表:
序号 A B
① 2 mL 0.2 mol/L H C O 溶液 4 mL 0.01 mol/L KMnO 溶液
2 2 4 4
② 2 mL 0.1 mol/L H C O 溶液 4 mL 0.01 mol/L KMnO 溶液
2 2 4 4
③ 2 mL 0.2 mol/L H C O 溶液 4 mL 0.01 mol/L KMnO 溶液和少量MnSO
2 2 4 4 4
(1)该反应的离子方程式为 ,实验结束
后读数前需要移动量气管,使两个量气管的液面相平。
乙组:通过测定KMnO 溶液褪色所需的时间来比较化学反应速率的大小。为了探究 KMnO 溶
4 4
液与HC O 溶液浓度对反应速率的影响,某同学在室温下完成以下实验:
2 2 4
实验编号 1 2 3 4
水/mL 10 5 0 x
0.5 mol/L H C O 溶液/mL 5 10 10 5
2 2 4
5
学科网(北京)股份有限公司0.2 mol/L KMnO 溶液/mL 5 5 10 10
4
时间/s 40 20 10 —
(2)x= ,4号实验中始终没有观察到溶液褪色,你认为可能的原因是 。
(3)2号实验中,用HC O 表示的反应速率为 (反应后溶液的总体积变化忽略不计)。
2 2 4
(4)在实验中发现酸性高锰酸钾溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色
不明显;但不久突然褪色,反应速率明显加快。某同学认为是反应放热导致溶液温度升高,再
次进行3号实验,测定反应过程中不同时间溶液的温度,结果如下表:
时间/s 0 5 10 15 20 25 30
温度/℃ 25 26 26 26 26.5 27 27
①结合实验目的与表中数据,你得出的结论是 。
②从影响化学反应速率的因素看,你认为还可能是 的影响。若用实验证明你的猜想,
除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是 。
a.硫酸钾 b.水 c.二氧化锰 d.硫酸锰
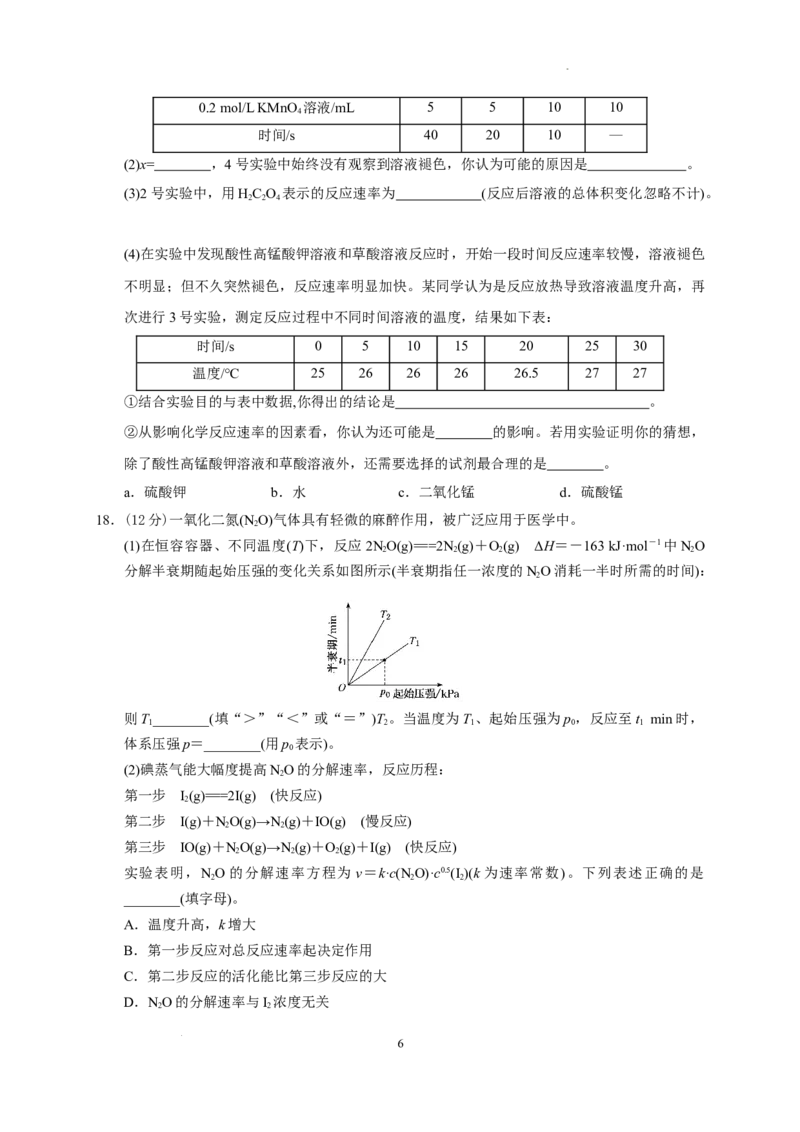
18.(12分)一氧化二氮(N O)气体具有轻微的麻醉作用,被广泛应用于医学中。
2
(1)在恒容容器、不同温度(T)下,反应2NO(g)===2N (g)+O(g) ΔH=-163 kJ·mol-1中NO
2 2 2 2
分解半衰期随起始压强的变化关系如图所示(半衰期指任一浓度的NO消耗一半时所需的时间):
2
则T________(填“>”“<”或“=”)T 。当温度为T 、起始压强为p ,反应至t min时,
1 2 1 0 1
体系压强p=________(用p 表示)。
0
(2)碘蒸气能大幅度提高NO的分解速率,反应历程:
2
第一步 I(g)===2I(g) (快反应)
2
第二步 I(g)+NO(g)→N (g)+IO(g) (慢反应)
2 2
第三步 IO(g)+NO(g)→N (g)+O(g)+I(g) (快反应)
2 2 2
实验表明,NO 的分解速率方程为 v=k·c(N O)·c0.5(I)(k 为速率常数)。下列表述正确的是
2 2 2
________(填字母)。
A.温度升高,k增大
B.第一步反应对总反应速率起决定作用
C.第二步反应的活化能比第三步反应的大
D.NO的分解速率与I 浓度无关
2 2
6
学科网(北京)股份有限公司1.答案:D
解析:浓度和压强的变化是改变单位体积内分子的总数,活化分子的百分数不变,而单位体积内活
化分子的数目与单位体积内分子总数成正比,也发生变化;温度、催化剂是改变活化分子的百分数,
单位体积内分子总数不变。
2.答案:C
解析:A项,NaCO 与HSO 反应生成CO 气体,H 量减少;B项,HSO +BaCl ===BaSO↓+
2 3 2 4 2 2 2 4 2 4
2HCl,c(H+)不变,速率不变;D项,形成铜锌原电池,速率加快。
3.答案:C
解析:对于有气体参加的反应,使用催化剂、升温、缩小体积,化学反应速率一定加快;而增加反
应物的物质的量,该反应物若是固体,速率不加快;增大容器内的压强,反应物浓度不一定增大,
反应速率不一定加快。
4.答案:C
解析:降低温度反应速率减小,升高温度反应速率增大,A、D错误;对于有气体参加的可逆反应,
增大压强反应速率增大,减小压强反应速率减小,B错误,C正确。
5.答案:C
解析:物质发生化学反应,分子间必须发生有效碰撞,普通分子间不能发生有效碰撞,A正确,C
错误;发生有效碰撞才能发生化学反应,发生化学反应必定发生了有效碰撞,B正确;活化分子间
的碰撞不一定是有效碰撞,D正确。
6.答案:A
解析:活化能接近零的反应,分子基本都是活化分子,只要接触就可迅速反应,温度对其反应速率
影响不大,A正确;增大压强是增加了单位体积内活化分子的数目,不改变活化分子百分数,B错
误;活化能指活化分子具有的平均能量与反应物分子具有的平均能量之差,C错误;活化能的大小
对化学反应前后的能量变化无影响,D错误。
7.答案:D
解析:催化剂在反应中同等程度地改变正、逆反应速率,A错;B项,通入氩气压强增大,但是各
物质的浓度不变,所以速率不变;C项,降温会减小反应速率,将延长达到平衡的时间,错误;D
项,由反应速率的表达式可知正确。
8.答案:B
7
学科网(北京)股份有限公司解析:相同体积和浓度的盐酸分别与足量CaCO 反应,产生CO 的量相同,但实验Ⅰ中用的CaCO
3 2 3
是块状的,实验Ⅱ中用的CaCO 是粉末状的,故实验Ⅱ中化学反应速率大,用时短,B项正确。
3
9.答案:B
解析:反应的化学方程式为NaSO+H SO ===Na SO +S↓+SO ↑+H O,A正确;在其他条件不变时,
2 2 3 2 4 2 4 2 2
反应物的浓度越大,反应速率越快,B正确;该实验是研究浓度对化学反应速率的影响,根据①可
知,3% Na SO 溶液与所加水的总体积为6 mL,则a=4,b=1,C正确,D错误。
2 2 3
10.答案:A
解析:当反应放出98 kJ的热量时消耗1 mol H O ,会生成0.5 mol O ,A正确;化学反应速率由慢
2 2 2
反应决定,HO 的分解速率主要由反应①决定,B错误;该反应的催化剂是I-,C错误;催化剂能
2 2
降低反应的活化能,从而加快化学反应速率,但不影响反应热,D错误。
11.答案:A
解析:在相同时间内,转化率变化值越大,表明反应中消耗的反应物越多,反应速率越大。由表中
数据知,10~15 min、15~20 min内,反应物转化率变化值分别为3.7%、4.5%,故后一个时间段内
反应速率较快,随着反应的进行,反应物浓度减小,又因容器容积不变,故改变的条件只能是升温,
A正确,C、D错误;10~20 min、20~40 min两个时间段内,转化率分别改变了8.2%、10.3%(注:
时间间隔不同),故10~20 min反应速率快,B错误。
12.答案:D
解析:由题图可知,在催化剂a表面氮气和氢气发生化合反应生成氨气,氨气做生成物,在催化剂
b表面氨气和氧气反应生成一氧化氮和水,氨气做反应物,则氨气在反应过程中做中间产物,A错
误;在催化剂a表面氮气和氢气发生化合反应生成氨气,没有发生分解反应,B错误;催化剂a、
b,降低了反应的活化能,从而提高反应速率,C错误;在催化剂b表面氨气和氧气反应生成一氧
化氮和水,反应的化学方程式为4NH +5O=====4NO+6HO,D正确。
3 2 2
13.答案:D
解析:根据甲醛的燃烧反应可知甲醛与氧气生成CO 和HO的反应为放热反应,则反应物的键能之
2 2
和小于生成物的键能之和,A项错误;催化剂能够改变反应的历程,但是不能改变反应的焓变,B
项错误;从题图可知,反应结束后18O在HO中,C项错误。
2
14.答案:B
解析:催化剂可降低反应的活化能,A正确;能够发生化学反应的碰撞才是有效碰撞,由图乙可知
碰撞后没有生成新物质,即没有发生化学反应,不是有效碰撞,B错误;盐酸和氢氧化钠溶液反应
的实质是氢离子与氢氧根离子反应生成水,在溶液中氢离子与氢氧根离子已经处于活跃状态,因此
盐酸和氢氧化钠溶液反应的活化能接近于零,C正确;增大反应物浓度,单位体积内活化分子数增
多,单位时间内有效碰撞次数增加,D正确。
15.答案:D
8
学科网(北京)股份有限公司解析:增大SO2-的浓度,反应②的反应速率加快,A正确;若往该溶液中加入含Fe3+的某溶液,
2 8
发生的总反应为SO2-(aq)+2I-(aq) 2SO2- (aq)+I (aq), Fe3+为该反应的催化剂,B正确;反应物
2 8 4 2
的总能量高于生成物的总能量,所以该反应是放热反应,C正确;催化剂不改变反应的焓变,D错
误。
16.答案:(1)放热 需要 E-E (2)409.0 kJ·mol-1
2 1
(3)降低 无影响 催化剂只能降低反应的活化能,不能改变反应物的总能量和生成物的
总能量之差,即反应热不改变
解析:(2)由图示可知ΔH=正反应活化能-逆反应活化能,故逆反应活化能=正反应活化能-ΔH=167.2
kJ·mol-1-(-241.8 kJ·mol-1)=409.0 kJ·mol-1。
17.答案: (1)2Mn +5H C O+6H+===2Mn2++10CO ↑+8H O
O- 2 2 4 2 2
4
(2)5 KMnO 溶液过量
4
(3)0.006 25 mol/(L·s)
(4)①温度不是反应速率突然加快的原因 ②催化剂 d
解析:(1)酸性KMnO 溶液与HC O 溶液反应生成二氧化碳、硫酸锰和水。(2)探究浓度对反应速率
4 2 2 4
的影响时,溶液的总体积都为20 mL,据此判断x的值;由于4号实验中高锰酸钾溶液过量,溶液最终没
有褪色。(3)根据n=cV计算出反应物的物质的量,计算可知高锰酸钾量不足,用高锰酸钾的物质的量来
Δc
计算反应消耗的草酸的物质的量,最后根据v= 计算出用HC O 表示的反应速率。(4)①根据题表
2 2 4
Δt
数据知,温度升高不明显,对反应速率影响不大,说明温度不是反应速率突然加快的原因。②酸性
KMnO 溶液与HC O 溶液反应生成了锰离子,锰离子有催化作用,所以还可能是催化剂的影响,要想
4 2 2 4
验证锰离子的催化作用,在做对照实验时同时加入硫酸锰观察反应速率是否有变化。
18.答案: 答案:(1)> 1.25p (2)AC
0
解析:(1)其他条件相同时,随着温度升高,化学反应速率增大,NO分解半衰期减小,故T >T 。
2 1 2
当温度为T 、起始压强为p 时,半衰期为t min,设起始时NO的物质的量为1 mol,则t min时
1 0 1 2 1
NO的物质的量为0.5 mol,用“三段式”法进行计算:
2
2NO(g)===2N (g)+O(g)
2 2 2
起始/mol 1 0 0
转化/mol 0.5 0.5 0.25
t min/mol 0.5 0.5 0.25
1
t min时总物质的量为(0.5+0.5+0.25)mol=1.25 mol,根据阿伏加德罗定律的推论可知,同温
1
同体积时,气体的压强之比等于其物质的量之比,则=,p=1.25p。
0
(2)温度升高,化学反应速率v=k·c(N O)·c0.5(I)增大,则k增大,A正确;化学反应速率由慢反
2 2
9
学科网(北京)股份有限公司应的反应速率决定,则第二步反应对总反应速率起决定作用,B错误;活化能小的反应更容易发生,
为快反应,故第二步反应的活化能比第三步反应的大,C正确;v=k·c(N O)·c0.5(I),所以NO分解
2 2 2
速率与I 浓度有关,D错误。
2
10
学科网(北京)股份有限公司11
学科网(北京)股份有限公司