文档内容
人教版(2019)必修第一册第二章第三节物质的量
课时训练十
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列溶液中溶质的物质的量浓度为1 的是
A.将250g胆矾( )溶于少量水,然后再将此溶液稀释至1L
B.将22.4LHCl气体溶于水配成1L溶液
C.将1L10 的浓盐酸与9L水混合
D.将40gNaOH溶解于1L水中
2.在0.2mol•L-1KAl(SO ) 溶液中,SO 的物质的量浓度为
4 2
A.0.1mol•L-1 B.0.2mol•L-1 C.0.4mol•L-1 D.0.8mol•L-1
3.下列有关物质的量浓度的叙述正确的是
A. 水中溶解了 后,所得溶液浓度为
B.配制 的 ,需用 胆矾
C.从 中取出 ,则这 的物质的量浓度是原溶液
的1/10
D. 的 中,
4.将 溶液加水稀释到300 mL,稀释后溶液中的NaOH的物质
的量浓度为
A. B.
C. D.
5.将100mL 0.5mol⋅L-1 NaCl溶液稀释到250mL,稀释后NaCl的物质的量浓度为
A.0.02mol⋅L-1 B.0.01mol⋅L-1 C.0.05mol⋅L-1 D.0.2mol⋅L-1
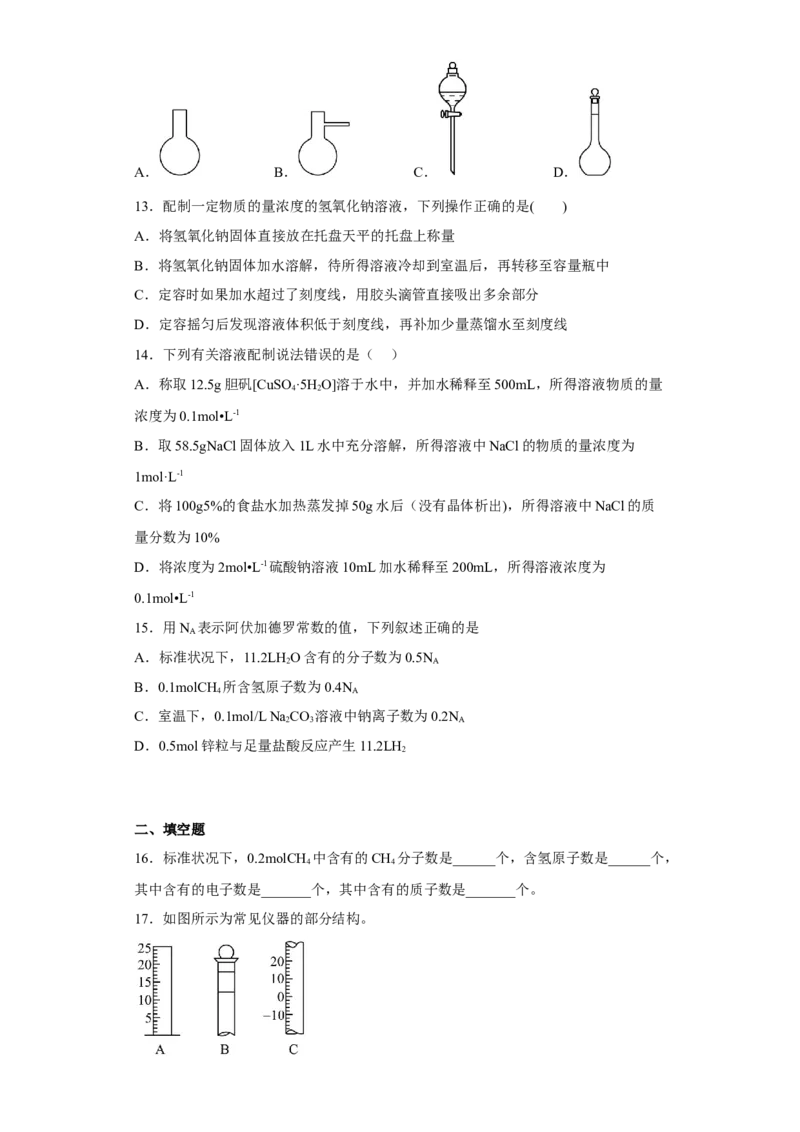
6.在 、 、 形成的混合溶液中, ,, ,则 为
A.0.01mol/L B.0.15mol/L C.0.20mol/L D.0.25mol/L
7.配制0.4 mol·L-1的NaCl溶液1 000 mL不需要用到的仪器是
A. B. C. D.
8.下列关于250 mL容量瓶的操作,正确的是
A. B. C. D.
9.欲配制100mL0.8mol·L-1的氯化钠溶液,下列说法错误的是
A.洗涤后,将洗涤液转移到100mL容量瓶中
B.在烧杯中用适量蒸馏水溶解NaCl固体
C.需称取4.68gNaCl固体
D.定容时,俯视容量瓶刻度线会导致所配溶液溶度偏大
10.下列操作使所配制的硫酸溶液浓度偏小的是
A.趁热将稀释的硫酸溶液转入容量瓶中并定容
B.定容时,仰视刻度线
C.洗好的容量瓶未经干燥直接进行实验
D.用蒸馏水清洗量取浓硫酸的量筒,并将洗涤液倒入烧杯中
11.蒸馏操作时,需要用到的仪器
A. B. C. D.
12.仪器名称为“容量瓶”的是
试卷第2页,共3页A. B. C. D.
13.配制一定物质的量浓度的氢氧化钠溶液,下列操作正确的是( )
A.将氢氧化钠固体直接放在托盘天平的托盘上称量
B.将氢氧化钠固体加水溶解,待所得溶液冷却到室温后,再转移至容量瓶中
C.定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分
D.定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
14.下列有关溶液配制说法错误的是( )
A.称取12.5g胆矾[CuSO ·5H O]溶于水中,并加水稀释至500mL,所得溶液物质的量
4 2
浓度为0.1mol•L-1
B.取58.5gNaCl固体放入1L水中充分溶解,所得溶液中NaCl的物质的量浓度为
1mol·L-1
C.将100g5%的食盐水加热蒸发掉50g水后(没有晶体析出),所得溶液中NaCl的质
量分数为10%
D.将浓度为2mol•L-1硫酸钠溶液10mL加水稀释至200mL,所得溶液浓度为
0.1mol•L-1
15.用N 表示阿伏加德罗常数的值,下列叙述正确的是
A
A.标准状况下,11.2LH O含有的分子数为0.5N
2 A
B.0.1molCH 所含氢原子数为0.4N
4 A
C.室温下,0.1mol/L NaCO 溶液中钠离子数为0.2N
2 3 A
D.0.5mol锌粒与足量盐酸反应产生11.2LH
2
二、填空题
16.标准状况下,0.2molCH 中含有的CH 分子数是______个,含氢原子数是______个,
4 4
其中含有的电子数是_______个,其中含有的质子数是_______个。
17.如图所示为常见仪器的部分结构。(1)请写出下列仪器的名称:A___________,B___________,C___________。
(2)仪器B上标记有___________(填序号)。
①质量②温度③刻度线④浓度⑤容积
(3)检验仪器B是否漏水的方法是___________。
18.用NaOH固体配制450mL0.2mol/L的NaOH溶液。请回答
(1)用托盘天平称量的NaOH的质量为___________
(2)定容时的操作:当液面接近容量瓶刻度线时,___________,再将容量瓶塞盖好,反
复上下颠倒摇匀。
(3)下列操作会使配制的NaOH溶液浓度偏低的是___________
A.定容时仰视容量瓶的刻度线
B.用已经部分变质了的固体试样进行配制
C.摇匀后发现液面低于容量瓶的刻度线,再滴加蒸馏水至刻度线
D.转移洗涤液时不小心将液体洒到容量瓶外,重新配制时继续使用该未清洗的容量
瓶
19.欲用NaCO 固体配制950mL 0.1mol•L-1的NaCO 溶液。请回答:
2 3 2 3
(1)Na CO 的相对分子质量是___________,摩尔质量是___________。
2 3
(2)配制该溶液应选用 ___________ mL容量瓶。
(3)用托盘天平称取 ___________ gNa CO 固体。
2 3
(4)将称好的固体放入___________中,用适量蒸馏水溶解。
(5)将恢复至室温的液体用___________引流注入容量瓶,并用少量蒸馏水洗涤溶解固体
的仪器2-3次,洗涤液也都注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀。
(6)向容量瓶中加入蒸馏水,直到液面在刻度线下1~2cm时,改用___________滴加蒸
馏水至___________的最低点与刻度线相切,盖好瓶塞,摇匀。
(7)配制好的溶液 ___________ (填“能”或“不能”)长期存放在容量瓶中。
(8)若实验中遇到下列情况,对溶液的物质的量浓度有何影响(填“偏大”、“偏小”或
“不变”)?
A.在烧杯中搅拌溶解溶质时,溅出少量溶液 ___________。
B.定容时,俯视容量瓶刻度线 ___________。
C.颠倒摇匀后,液面低于刻度线,再重新加水至刻度线 ___________。
20.如图为浓硫酸的标签。
试卷第4页,共3页配制200mL4.6mol/L的稀硫酸需取该硫酸的体积为_______。
三、实验题
21.实验室里需用480mL0.1mol·L-1的CuSO 溶液。
4
(1)①配制该溶液应选用___mL容量瓶。以下配制方法正确的是___(填字母)。
A.称取7.68gCuSO 加入500mL水
4
B.称取12.0g胆矾(CuSO ·5H O)加入500mL水
4 2
C.称取8.0gCuSO 加入500mL水
4
D.称取12.5g胆矾配成500mL溶液
②假如其他操作均准确无误,分析下列情况对配制溶液浓度的影响(填“偏高”、“偏
低”或“无影响”)
A.定容时俯视观察刻度线:___;
B.移液时,对用于溶解CuSO (或胆矾)的烧杯没有洗涤:___;
4
C.定容后,将容量瓶振荡摇匀,静置时发现液面低于刻度线,又补加水至刻度线:
___;
(2)用16mol·L-1的浓硫酸稀释成4mol·L-1的稀硫酸100mL,需要浓硫酸___mL。
22.已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体
积之比)后使用。请回答下列问题:(1)该“84消毒液”的物质的量浓度约___mol·L-1(小数点后保留一位)。
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中
c(Na+)=___mol·L-1。
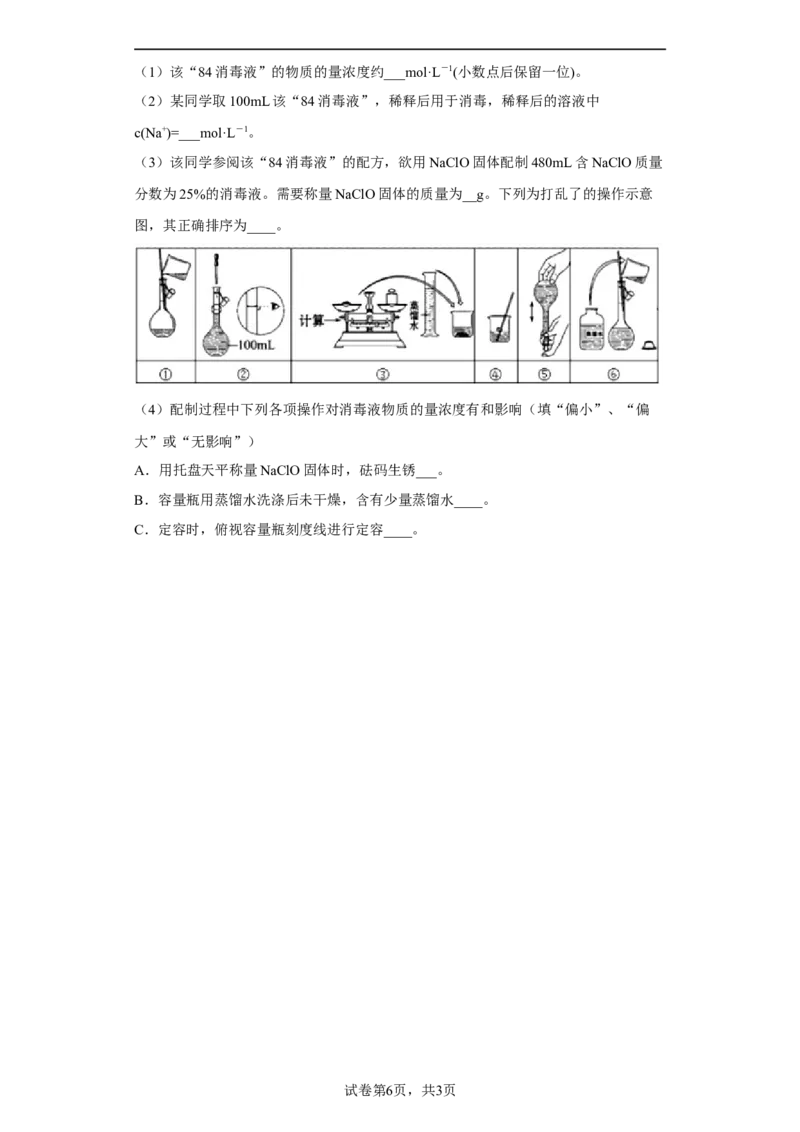
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量
分数为25%的消毒液。需要称量NaClO固体的质量为__g。下列为打乱了的操作示意
图,其正确排序为____。
(4)配制过程中下列各项操作对消毒液物质的量浓度有和影响(填“偏小”、“偏
大”或“无影响”)
A.用托盘天平称量NaClO固体时,砝码生锈___。
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水____。
C.定容时,俯视容量瓶刻度线进行定容____。
试卷第6页,共3页参考答案:
1.A
【分析】物质的量浓度表示单位体积的溶液里所含溶质的物质的量,溶液的体积与溶质或
溶剂的体积不能等效,据此分析解答。
【详解】A.250g胆矾( )的物质的量为 =1mol,将其溶于水形成硫
酸铜溶液,稀释至1L,则所得硫酸铜的物质的量浓度为 =1mol/L,A符合题意;
B.未给出是否是标准状况,无法利用给定条件计算溶质的物质的量浓度,B不符合题意;
C.浓盐酸与水混合后,溶液体积不是10L,C不符合题意;
D.将40gNaOH溶解于1L水中,得到的溶液体积大于1L,D不符合题意;
故选A。
2.C
【详解】由化学式可知,SO 的物质的量浓度为2×0.2mol•L-1=0.4mol•L-1;
故选C。
3.D
【详解】A. 加入水配成1L溶液,而不是在1L水中溶解,A错误;
B.配制 的 ,需要0.1mol硫酸铜,质量为16g,胆矾含有结晶水,
故需质量大于16g,B错误;
C.溶液是均一稳定的,前后浓度相等,C错误;
D.由化学式可知, 的 中, ,
D正确;
故选D。
4.C
【详解】氢氧化钠溶液稀释前后NaOH的物质的量不变,稀释后NaOH的物质的量浓度=
=0.05mol/L,故C正确,故选C。
5.D【详解】稀释100mL 0.5mol⋅L-1 NaCl溶液,溶液中NaCl物质的量不变,
,稀释到250mL后浓度为
;
故答案选D。
6.C
【详解】根据电荷守恒: ,得到 =0.20mol/L,C正
确;
故选C。
7.A
【详解】配制一定物质的量浓度溶液一般操作步骤为:计算、称量、溶解、冷却、移液、
洗涤、定容、摇匀等,用到的仪器依次为:托盘天平、药匙、烧杯、玻璃棒、容量瓶、胶
头滴管,所以配制0.4 mol·L-1的NaCl溶液1 000 mL,需1 000 mL容量瓶,溶解固体NaCl
需要用烧杯;定容时,当液面离刻度线1~2 cm时用胶头滴管加水,不需要圆底烧瓶,故
选A项。
8.C
【详解】A.容量瓶使用过程中,不能用手等触碰瓶口,以免污染试剂,A错误;
B.定容时,视线应与溶液凹液面和刻度线“三线相切”,不能仰视或俯视,B错误;
C.向容量瓶中转移液体,需用玻璃棒引流,玻璃棒下端位于刻度线以下,同时玻璃棒不
能接触容量瓶口,C正确;
D.定容完成后,盖上瓶塞,将容量瓶来回颠倒,将溶液摇匀,颠倒过程中,左手食指抵
住瓶塞,防止瓶塞脱落,右手扶住容量瓶底部,防止容量瓶从左手掉落,D错误;
答案选C。
9.C
【详解】A.为避免溶质损失,洗涤后,将洗涤液转移到100mL容量瓶中,A正确;
B.溶解在烧杯中进行,B正确;
C.氯化钠的质量m=100mL×0.8mol·L-1×58.5g/mol=4.68g,用托盘天平称取4.7g,C错误;
D.定容时,俯视容量瓶刻度线会导致溶液体积偏小,所配溶液溶度偏大,D正确;
答案选C。
答案第2页,共2页10.B
【详解】A.配制溶液进行转移操作前,应先将容易冷却至室温后在转移至容量瓶,趁热
将稀释的硫酸溶液转入容量瓶中并定容,导致所配溶液体积偏小,浓度偏大,故A不符合
题意;
B.定容时,仰视刻度线,导致所配溶液体积偏大,浓度偏小,故B符合题意;
C.洗好的容量瓶未经干燥直接进行实验,对所配溶液的浓度无影响,故C不符合题意;
D.用蒸馏水清洗量取浓硫酸的量筒,并将洗涤液倒入烧杯中,导致量取的溶质物质的量
偏大,所配溶液浓度偏大,故D不符合题意;
答案选B。
11.A
【详解】A.该仪器是直形冷凝管,用于蒸馏操作,A符合题意;
B.该仪器是蒸发皿,用于蒸发操作,B不符合题意;
C.该仪器是分液漏斗,用于分液和萃取操作,C不符合题意;
D.该仪器是容量瓶,用于配制一定物质的量浓度的溶液,D不符合题意;
故选A。
12.D
【详解】A.此仪器为圆底烧瓶,故A错误;
B.此仪器为蒸馏烧瓶,故B错误;
C.此仪器为分液漏斗,故C错误;
D.此仪器为容量瓶,故D正确;
故答案为D。
13.B
【详解】A.氢氧化钠固体易潮解、具有腐蚀性,不能直接放在托盘天平的托盘上称量,
应放在烧杯中称量,故A错误;
B.将氢氧化钠固体加水溶解,待所得溶液冷却到室温后再转移至容量瓶中,如不冷却会
使所配溶液的浓度偏高,故B正确;
C.定容时如果加水超过了刻度线,会使所配溶液的浓度偏低,应重新配制,故C错误;
D.定容后溶液的浓度已经确定了,定容摇匀后发现溶液体积低于刻度线,再补加少量蒸
馏水至刻度线,会使溶液的体积偏大,所配溶液的浓度偏低,故D错误;
答案选B。
14.B【详解】A.称取12.5g胆矾[CuSO ·5H O]的物质的量为 ,加水稀释至
4 2
500mL,所得溶液物质的量浓度为 ,故A正确;
B.由于水的体积为1L,则将58.5gNaCl固体放入1L水中时,溶液的体积大于1L,故溶液
的浓度小于1mol·L-1,故B错误;
C.100g5%的食盐水的质量为m=100g×5%=5g,加热蒸发掉50g水后,溶液的质量变为
50g,所得溶液中NaCl的质量分数为 ,故C正确;
D.将浓度2 mol·L-1硫酸钠溶液10mL加水稀释200mL,稀释后的浓度为
,故D正确;
故选B。
15.B
【详解】A.标况下水不是气体,不能用22.4L/mol进行计算,A错误;
B.0.1mol CH 含有0.4mol氢原子,即0.4N ,B正确;
4 A
C.溶液体积未知,无法计算溶液中微粒的数目,C错误;
D.未注明温度和压强,无法确定气体体积,D错误;
综上所述答案为B。
16. 0.2N 或1.204×1023 0.8N 或4.816×1023 2N 或1.204×1024 2N 或
A A A A
1.204×1024
【详解】标准状况下,0.2molCH 中含有的CH 分子数是0.2mol×N =0.2N 或1.204×1023个,
4 4 A A
一个分子中含有4个氢原子、10个电子、10个质子,则含氢原子数是0.2N ×4=0.8N 或
A A
4.816×1023、含有的电子数是0.2N ×10=2N 或1.204×1024个,含有的质子数是2N 或
A A A
1.204×1024。
17. 量筒 容量瓶 温度计 ②③⑤ 往容量瓶
中加入少量水,塞好瓶塞,用食指摁住瓶塞,母指在前,中指在后,无名指和小拇指自然
弯曲,另一只手托住瓶底,将容量瓶倒立,观察瓶塞周围是否有水漏出。如果不漏水,再
将容量瓶正立旋转瓶塞180°,重复上述操作
答案第4页,共2页【详解】(1)根据仪器结构可知,A为量筒,B为容量瓶,C为温度计;
(2)仪器B为容量瓶,容量瓶上标有温度、刻度线和容积,故答案选②③⑤;
(3)检验容量瓶是否漏水时,可往容量瓶中加入少量水,塞好瓶塞,用食指摁住瓶塞,母指
在前,中指在后,无名指和小拇指自然弯曲,另一只手托住瓶底,将容量瓶倒立,观察瓶
塞周围是否有水漏出。如果不漏水,再将容量瓶正立旋转瓶塞180°,重复上述操作。
18. 4.0g 改用胶头滴管,滴加蒸馏水至溶液的凹液面与刻度线相切
ABC
【详解】(1) 用NaOH固体配制450mL0.2mol/L的NaOH溶液应选用500mL的容量瓶,需
要NaOH的质量为500mL×10-3L×0.2mol/L×40g/mol=4.0g,故答案为:4.0;
(2) 定容时的操作:当液面接近容量瓶刻度线时, 改用胶头滴管,滴加蒸馏水至溶液的凹液
面与刻度线相切, 再将容量瓶塞盖好,反复上下颠倒摇匀,故答案为:改用胶头滴管,滴
加蒸馏水至溶液的凹液面与刻度线相切;
(3)A.定容时仰视容量瓶的刻度线,所配制溶液体积偏大,配制的NaOH溶液浓度偏低,
故A正确;
B.用已经部分变质了的固体试样进行配制,氢氧化钠质量变小,配制的NaOH溶液浓度
偏低,故B正确;
C.摇匀后发现液面低于容量瓶的刻度线,再滴加蒸馏水至刻度线,所配置溶液体积偏大,
配制的NaOH溶液浓度偏低,故C正确;
D.转移洗涤液时不小心将液体洒到容量瓶外,重新配制时继续使用该未清洗的容量瓶,
溶质质量增大,配制的NaOH溶液浓度偏高,故D错误;
故选ABC。
19. 106 106 g/mol 1000 10.6 烧杯 玻璃棒 胶头滴
管 液面 不能 偏小 偏大 偏小
【详解】(1)Na CO 的相对分子质量是106,摩尔质量是106g/mol;故答案为106;106g/
2 3
mol;
(2)容量瓶没有950mL的规格,配制溶液应选用大于等于该体积的容量瓶,所以配制该溶液
应选用1000mL容量瓶;故答案为1000;
(3)欲用NaCO 固体配制950mL 0.1mol•L﹣1的NaCO 溶液,需选择1000ml容量瓶,需要
2 3 2 3
NaCO 的质量m=0.1mol/L×1L×106g/mol=10.6g;故答案为10.6;
2 3
(4)将固体放入烧杯中溶解,故答案为烧杯;
(5)引流时用玻璃棒;故答案为玻璃棒;(6)定容时向容量瓶中加入蒸馏水,直到液面在刻度线下1~2cm时,改用胶头滴管滴加蒸
馏水至液面的最低点与刻度线相切,盖好瓶塞,摇匀;故答案为胶头滴管;液面;
(7)容量瓶只能作配置容器,不能作存放容器,所以配制好的溶液不能长期存放在容量瓶中,
故答案为不能;
(8)A、在烧杯中搅拌溶解溶质时,溅出少量溶液,导致溶质的物质的量偏小,溶液的浓度
偏小;B、定容时俯视刻度线,会导致溶液体积小于1L,溶液浓度偏大;C、定容之后,
溶液已经配制好,颠倒摇匀,部分溶液粘在刻度线以上,所以液面可能低于刻度线,此时
若再加水,会导致溶液浓度偏小。故答案为偏小;偏大;偏小。
【点睛】本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,要将配制溶
液的步骤熟记于心。易错点为:容量瓶的选择及误差分析。
20.50mL
【详解】根据 可计算出,图示浓硫酸的物质的量浓度为
;根据 ,
。
21. 500 D 偏高 偏低 偏低 25
【详解】(1)①480mL0.1mol·L-1的CuSO 溶液,由于没有480mL容量瓶,根据大而近的原
4
则,应选用500mL容量瓶;若使用CuSO 配制溶液,硫酸铜的质量为
4
0.1mol⋅L−1×0.5L×160g/mol=8.0g,若使用胆矾(CuSO ·5H O) 配制溶液,需要胆矾的质量为
4 2
0.1mol⋅L−1×0.5L×250g/mol=12.5g,所配溶液的体积为500mL,不能用500mL水的体积代
替溶液体积,综上分析,答案选D;
②A.定容时俯视观察刻度线,导致所配溶液的体积偏小,则配制溶液的浓度偏高;
B.移液时,对用于溶解CuSO (或胆矾)的烧杯没有洗涤,导致溶质未能完全转入容量瓶,
4
使所配溶液的溶质物质的量偏小,则配制溶液的浓度偏低;
C.定容后,将容量瓶振荡摇匀,静置时发现液面低于刻度线,又补加水至刻度线,导致
溶液体积偏大,则配制溶液的浓度偏低;
答案第6页,共2页(2)根据稀释定律,c V =c V ,则V = =25mL。
稀 稀 浓 浓 稀
22. 4.0 0.04 149 ③④①⑥②⑤ 偏大 无影响 偏大
【分析】(1)依据 计算该“84消毒液”的物质的量浓度;
(2)根据稀释前后溶质物质的量不变进行计算;
(3)配制480mL含NaClO的消毒液,应用500mL容量瓶,实际上配制的是500mLNaClO
溶液,再依据公式n=cV,m=nM计算NaClO的质量;依据配制一定物质的量浓度溶液的
一般步骤排序;
(4)依据配制一定物质的量浓度溶液的正确操作步骤判断,根据 分析操作对溶质的
物质的量或对溶液的体积的影响判断。
【详解】(1)该“84消毒液”的物质的量浓度约为
故答案为4.0;
(2)已知该“84消毒液”通常稀释100倍(体积之比)后使用,由(1)知该“84消毒液”
的浓度约为4.0mol/L,稀释前后钠离子物质的量不变,则c(Na+) V= c(Na+) ×100V,则稀
原 稀释
释后的溶液中c(Na+) =0.04mol·L-1;
稀释
故答案为0.04;
(3)配制480mL含NaClO质量分数为25%的消毒液,应用500mL容量瓶,实际上配制的
是500mLNaClO溶液,则NaClO的物质的量为n=cV=0.5L×4.0mol/L=2mol,质量
m=nM=2mol×74.5g/mol=149g;配制一定物质的量浓度溶液的一般步骤为:计算、称量、溶
解、转移、洗涤、定容、摇匀等,所以正确的操作排序为:③④①⑥②⑤;
故答案为149;③④①⑥②⑤;
(4)A.用托盘天平称量NaClO固体时,砝码生锈,称得的NaClO质量偏大,则溶液浓
度偏大;
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水,无影响;
C.定容时,俯视容量瓶刻度线进行定容,导致溶液体积偏小,配制溶液的浓度偏大;
故答案为偏大;无影响;偏大。
【点睛】容量瓶只有一条刻度线,只能配制与其规格相对应体积的溶液。容量瓶有以下规格:25mL、50mL、100mL、250mL、500mL、1000mL等,因此该题中配制480 mLNaClO
溶液,需要使用500mL容量瓶,在使用公式n(NaClO)=cV计算NaClO物质的量时,一定
注意代入的体积为0.5L,而不是0.48L,这是学生们的易错点。容量瓶的选用原则:如果
所配制溶液的体积正好与容量瓶的某一规格一致,直接选用该规格的容量瓶即可,如果不
一致,那么选择的容量瓶的规格跟实际配制溶液的体积相比较要大而近,比如该题配制
480ml溶液选用500ml容量瓶,再由实际配制的体积计算需要溶质的物质的量。
答案第8页,共2页