文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 02 物质的组成和结构
目 录
01 挑战中考题·查知识漏洞
命题点一 微粒的观点解释现象
命题点二 原子结构
命题点三 相对原子质量的概念及计算
命题点四 原子核外电子排布
命题点五 离子概念、形成和符号的书写与意义
命题点六 元素的概念及理解
命题点七 元素的分布
命题点八 元素符号书写及意义
命题点九 元素周期表
02 回顾教材·补知识漏洞
03 知识通关演练
命题点一 微粒的观点解释现象
1.(2023•广州)对下列宏观事实的微观解释,合理的是( )
A.空气湿度增大:单位体积空气中水分子数目增多
B.石墨一定条件下转变成金刚石:原子种类发生改变
C.CO 气体制成干冰:二氧化碳分子由运动变为静止
2
D.稀硫酸能使紫色石蕊溶液变红:溶液中含硫酸根离子
2.(2023•河北)在塑料袋中滴入几滴酒精,挤瘪后把口扎紧,放入热水中,塑料袋鼓起来,如图所示。
鼓起的过程中,塑料袋中酒精分子的( )
A.间隔增大 B.质量增大 C.种类增多 D.数目增多
命题点二 原子结构
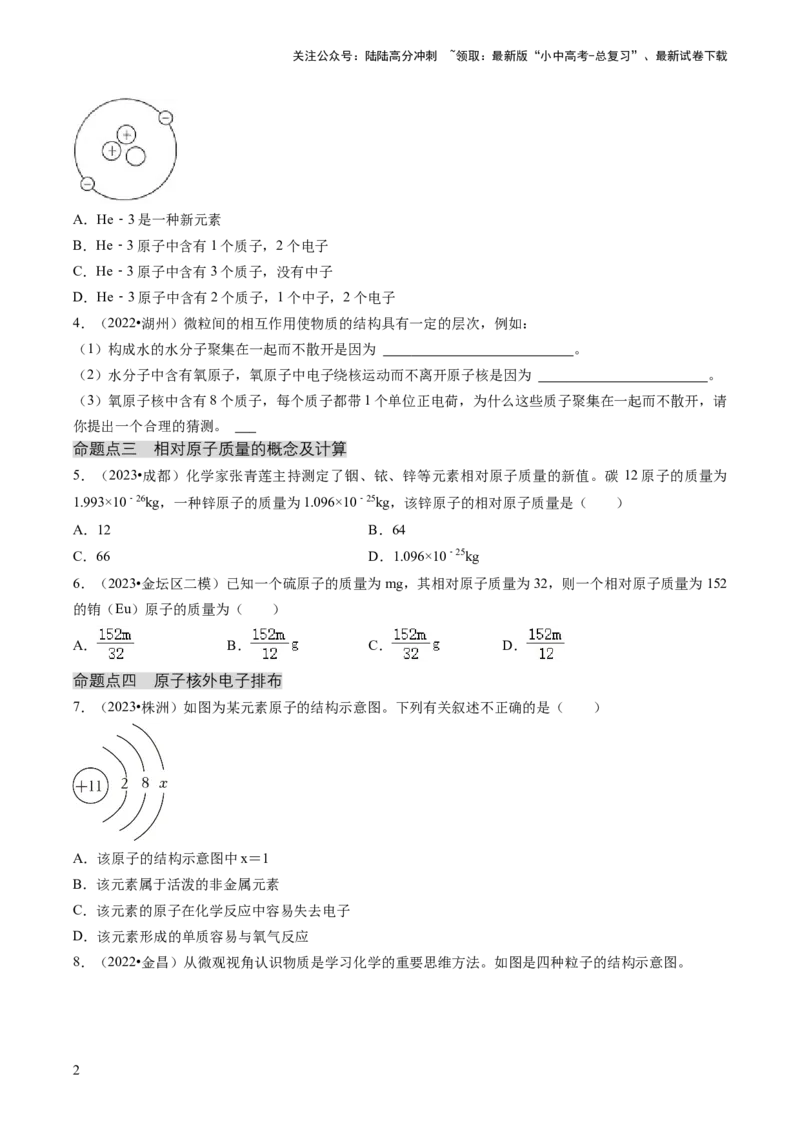
3.(2023•恩施州)嫦娥五号带回的月壤中含有大量安全无污染的核聚变原料 He﹣3(如图所示)。下列
关于He﹣3的说法正确的是( )
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.He﹣3是一种新元素
B.He﹣3原子中含有1个质子,2个电子
C.He﹣3原子中含有3个质子,没有中子
D.He﹣3原子中含有2个质子,1个中子,2个电子
4.(2022•湖州)微粒间的相互作用使物质的结构具有一定的层次,例如:
(1)构成水的水分子聚集在一起而不散开是因为 。
(2)水分子中含有氧原子,氧原子中电子绕核运动而不离开原子核是因为 。
(3)氧原子核中含有8个质子,每个质子都带1个单位正电荷,为什么这些质子聚集在一起而不散开,请
你提出一个合理的猜测。
命题点三 相对原子质量的概念及计算
5.(2023•成都)化学家张青莲主持测定了铟、铱、锌等元素相对原子质量的新值。碳 12原子的质量为
1.993×10﹣26kg,一种锌原子的质量为1.096×10﹣25kg,该锌原子的相对原子质量是( )
A.12 B.64
C.66 D.1.096×10﹣25kg
6.(2023•金坛区二模)已知一个硫原子的质量为mg,其相对原子质量为32,则一个相对原子质量为152
的铕(Eu)原子的质量为( )
A. B. C. D.
命题点四 原子核外电子排布
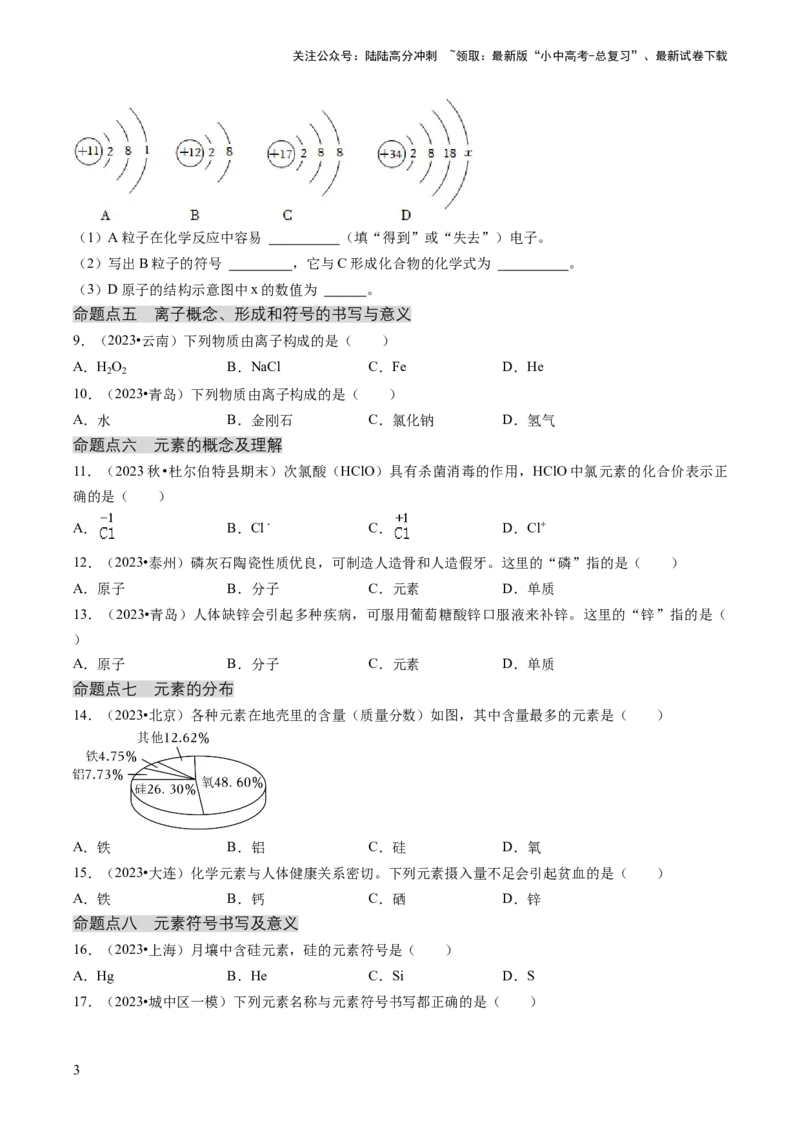
7.(2023•株洲)如图为某元素原子的结构示意图。下列有关叙述不正确的是( )
A.该原子的结构示意图中x=1
B.该元素属于活泼的非金属元素
C.该元素的原子在化学反应中容易失去电子
D.该元素形成的单质容易与氧气反应
8.(2022•金昌)从微观视角认识物质是学习化学的重要思维方法。如图是四种粒子的结构示意图。
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)A粒子在化学反应中容易 (填“得到”或“失去”)电子。
(2)写出B粒子的符号 ,它与C形成化合物的化学式为 。
(3)D原子的结构示意图中x的数值为 。
命题点五 离子概念、形成和符号的书写与意义
9.(2023•云南)下列物质由离子构成的是( )
A.H O B.NaCl C.Fe D.He
2 2
10.(2023•青岛)下列物质由离子构成的是( )
A.水 B.金刚石 C.氯化钠 D.氢气
命题点六 元素的概念及理解
11.(2023秋•杜尔伯特县期末)次氯酸(HClO)具有杀菌消毒的作用,HClO中氯元素的化合价表示正
确的是( )
A. B.Cl﹣ C. D.Cl+
12.(2023•泰州)磷灰石陶瓷性质优良,可制造人造骨和人造假牙。这里的“磷”指的是( )
A.原子 B.分子 C.元素 D.单质
13.(2023•青岛)人体缺锌会引起多种疾病,可服用葡萄糖酸锌口服液来补锌。这里的“锌”指的是(
)
A.原子 B.分子 C.元素 D.单质
命题点七 元素的分布
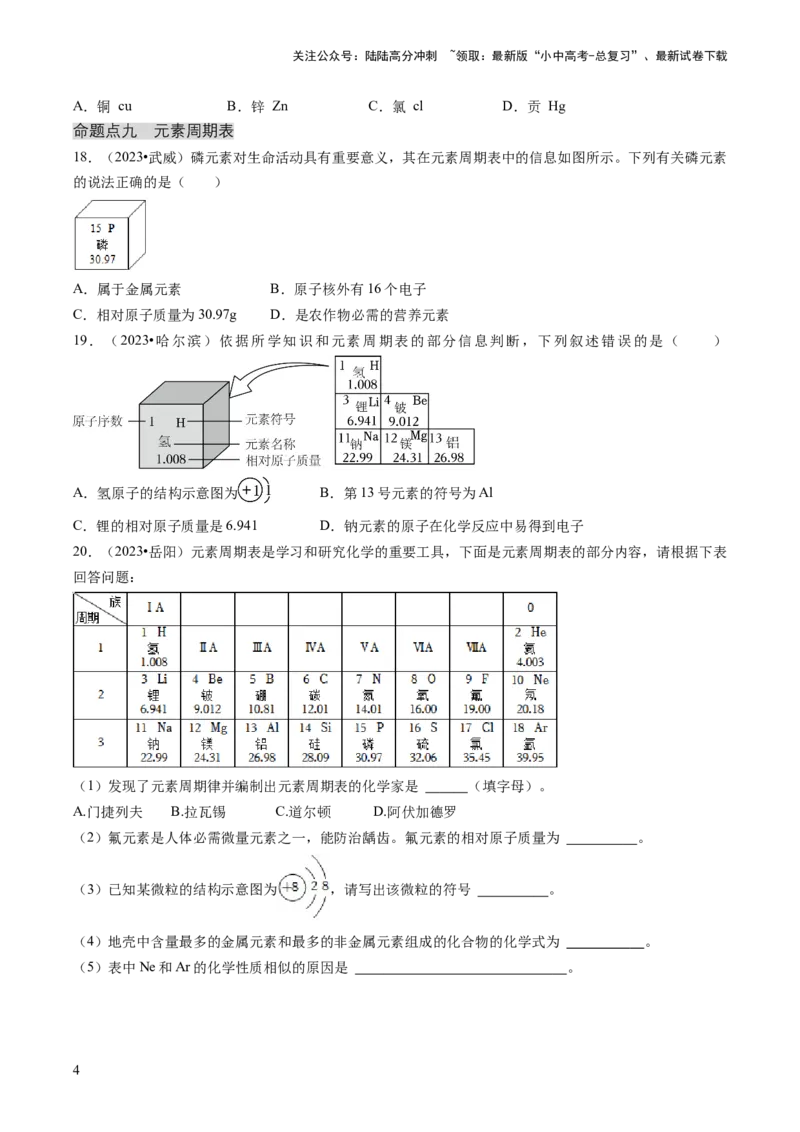
14.(2023•北京)各种元素在地壳里的含量(质量分数)如图,其中含量最多的元素是( )
A.铁 B.铝 C.硅 D.氧
15.(2023•大连)化学元素与人体健康关系密切。下列元素摄入量不足会引起贫血的是( )
A.铁 B.钙 C.硒 D.锌
命题点八 元素符号书写及意义
16.(2023•上海)月壤中含硅元素,硅的元素符号是( )
A.Hg B.He C.Si D.S
17.(2023•城中区一模)下列元素名称与元素符号书写都正确的是( )
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.铜 cu B.锌 Zn C.氯 cl D.贡 Hg
命题点九 元素周期表
18.(2023•武威)磷元素对生命活动具有重要意义,其在元素周期表中的信息如图所示。下列有关磷元素
的说法正确的是( )
A.属于金属元素 B.原子核外有16个电子
C.相对原子质量为30.97g D.是农作物必需的营养元素
19.(2023•哈尔滨)依据所学知识和元素周期表的部分信息判断,下列叙述错误的是( )
A.氢原子的结构示意图为 B.第13号元素的符号为Al
C.锂的相对原子质量是6.941 D.钠元素的原子在化学反应中易得到电子
20.(2023•岳阳)元素周期表是学习和研究化学的重要工具,下面是元素周期表的部分内容,请根据下表
回答问题:
(1)发现了元素周期律并编制出元素周期表的化学家是 (填字母)。
A.门捷列夫 B.拉瓦锡 C.道尔顿 D.阿伏加德罗
(2)氟元素是人体必需微量元素之一,能防治龋齿。氟元素的相对原子质量为 。
(3)已知某微粒的结构示意图为 ,请写出该微粒的符号 。
(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式为 。
(5)表中Ne和Ar的化学性质相似的原因是 。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
一、构成物质微粒
1、构成物质的粒子有分子、原子、离子,它们都可以直接构成物质。
2、由原子构成的物质
(1)金属单质,例如:金、铁。
(2)非金属固体单质,例如:碳、红磷、硫磺、硅。
(3)稀有气体单质,例如:氦气、氖气、氩气。
二、原子
1、原子结构
原子核(带正电) 质子(带正电)
(1)原子(不显电性) 中子(不带电)
核外电子(带负电)
(2)核电荷数:原子核所带电荷数。
(3)原子质量几乎全部集中在原子核上,但原子核体积很小,原子的体积由核外电子决定。
(4)在原子中,质子数=核外电子数=核电荷数。
2、原子或分子的基本性质
(1)质量和体积都很小。
(2)粒子之间都有间隔。
(3)粒子总在不断的运动。
(4)保持物质化学性质的微粒,决定于构成该物质的微粒是什么,如由分子构成的物质,保持其化学性
质的最小微粒就是分子,由原子构成的物质,保持其化学性质的最小微粒就是原子。保持水的化学性质的
粒子是水分子;保持铁的化学性质的粒子是铁原子。同种分子化学性质相同,不同种分子化学性质不同。
3、相对原子质量
(1)定义:一个原子质量与一个碳12原子的质量的1/12的比值就是相对原子质量。
(2)公式:相对原子质量=质子数+中子数
(3)理解:相对原子质量不是个质量是个比值;有单位,是“1”常省略不写;相对原子质量之比等于原
子实际质量之比;引入相对原子质量是为了书写、记忆和运算方便。
4、电子的排布
(1)在多电子的原子中,核外电子的能量不同,能量高的离核远,能量低的离核近。通常把电子在离核
远近不同的区域运动称为电子的分层排布。
(2)排布规律:(1)第1层最多2个电子;(2)第2层最多8个电子;(3)最外层最多8个。
(3)结构示意图含义:圆圈(原子核);圆圈内数字(核内质子数);弧线(电子层)。弧线上数字
(该电子层上电子数)
(4)原子分类(最外层电子数决定化学性质)
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
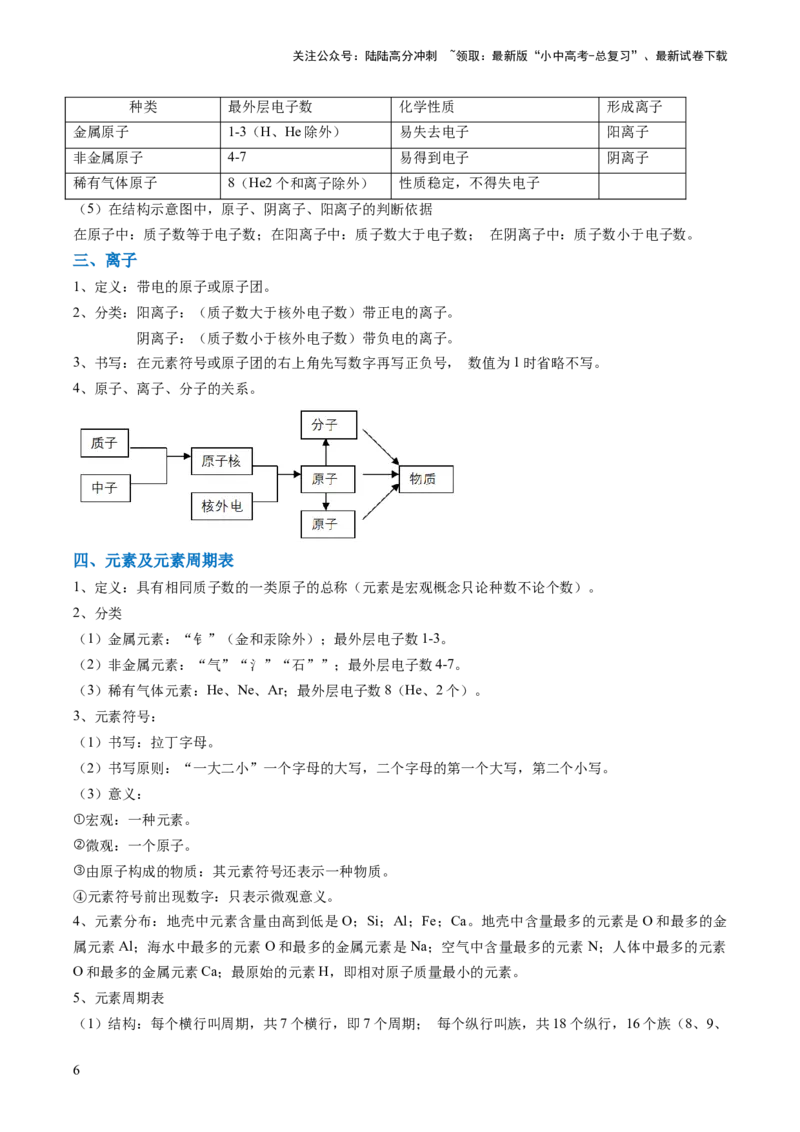
种类 最外层电子数 化学性质 形成离子
金属原子 1-3(H、He除外) 易失去电子 阳离子
非金属原子 4-7 易得到电子 阴离子
稀有气体原子 8(He2个和离子除外) 性质稳定,不得失电子
(5)在结构示意图中,原子、阴离子、阳离子的判断依据
在原子中:质子数等于电子数;在阳离子中:质子数大于电子数; 在阴离子中:质子数小于电子数。
三、离子
1、定义:带电的原子或原子团。
2、分类:阳离子:(质子数大于核外电子数)带正电的离子。
阴离子:(质子数小于核外电子数)带负电的离子。
3、书写:在元素符号或原子团的右上角先写数字再写正负号, 数值为1时省略不写。
4、原子、离子、分子的关系。
四、元素及元素周期表
1、定义:具有相同质子数的一类原子的总称(元素是宏观概念只论种数不论个数)。
2、分类
(1)金属元素:“钅”(金和汞除外);最外层电子数1-3。
(2)非金属元素:“气”“氵”“石””;最外层电子数4-7。
(3)稀有气体元素:He、Ne、Ar;最外层电子数8(He、2个)。
3、元素符号:
(1)书写:拉丁字母。
(2)书写原则:“一大二小”一个字母的大写,二个字母的第一个大写,第二个小写。
(3)意义:
宏观:一种元素。
微观:一个原子。
由原子构成的物质:其元素符号还表示一种物质。
④元素符号前出现数字:只表示微观意义。
4、元素分布:地壳中元素含量由高到低是O;Si;Al;Fe;Ca。地壳中含量最多的元素是O和最多的金
属元素Al;海水中最多的元素O和最多的金属元素是Na;空气中含量最多的元素N;人体中最多的元素
O和最多的金属元素Ca;最原始的元素H,即相对原子质量最小的元素。
5、元素周期表
(1)结构:每个横行叫周期,共7个横行,即7个周期; 每个纵行叫族,共18个纵行,16个族(8、9、
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
10三个纵行合成为1个族)。
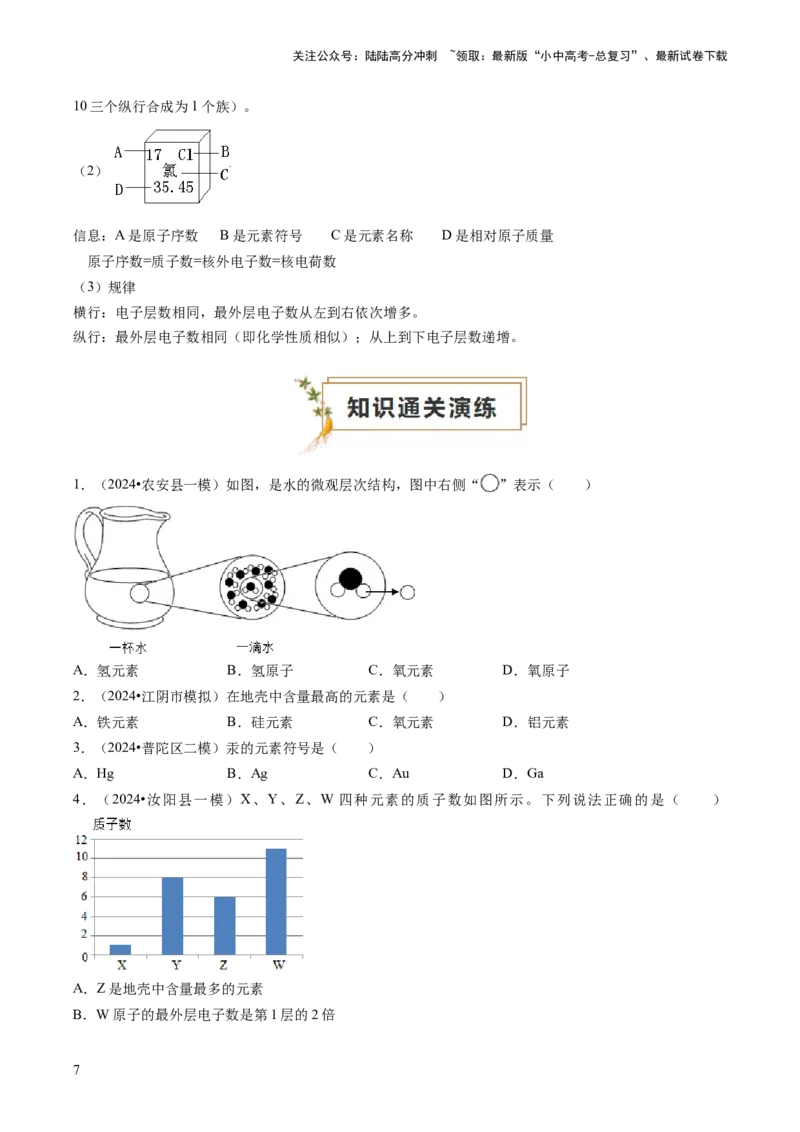
(2)
信息:A是原子序数 B是元素符号 C是元素名称 D是相对原子质量
原子序数=质子数=核外电子数=核电荷数
(3)规律
横行:电子层数相同,最外层电子数从左到右依次增多。
纵行:最外层电子数相同(即化学性质相似);从上到下电子层数递增。
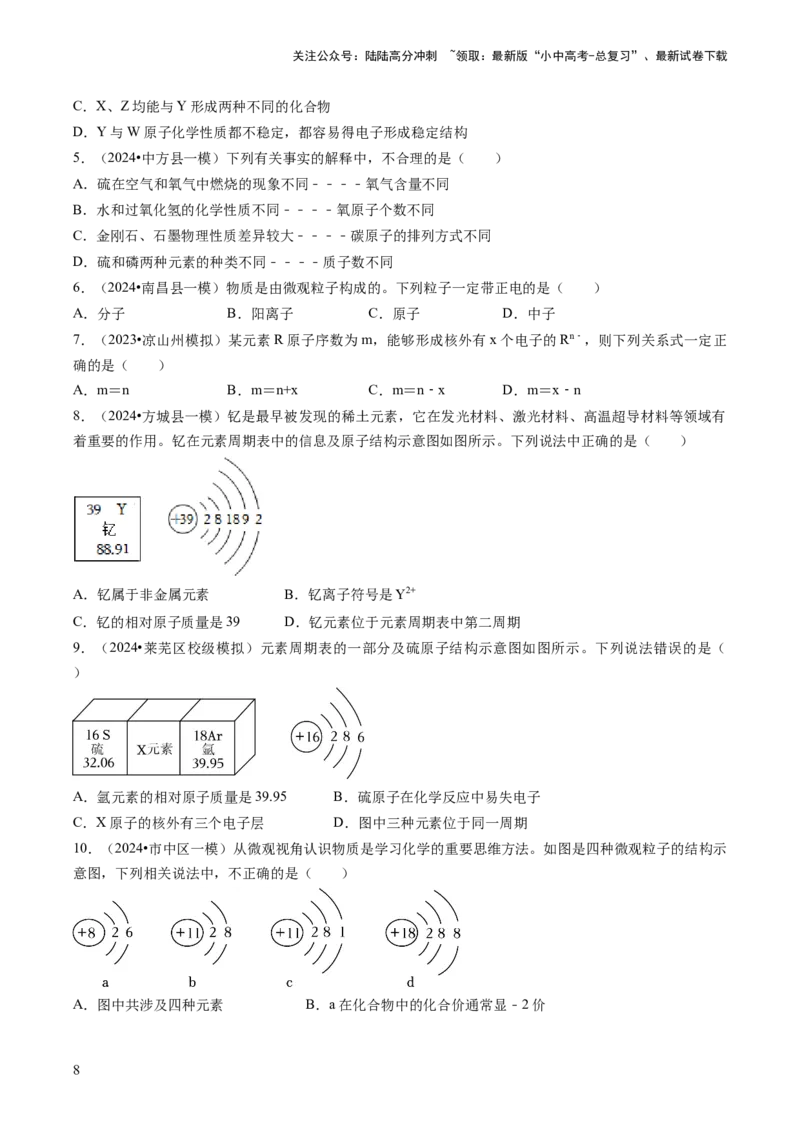
1.(2024•农安县一模)如图,是水的微观层次结构,图中右侧“ ”表示( )
A.氢元素 B.氢原子 C.氧元素 D.氧原子
2.(2024•江阴市模拟)在地壳中含量最高的元素是( )
A.铁元素 B.硅元素 C.氧元素 D.铝元素
3.(2024•普陀区二模)汞的元素符号是( )
A.Hg B.Ag C.Au D.Ga
4.(2024•汝阳县一模)X、Y、Z、W 四种元素的质子数如图所示。下列说法正确的是( )
A.Z是地壳中含量最多的元素
B.W原子的最外层电子数是第1层的2倍
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.X、Z均能与Y形成两种不同的化合物
D.Y与W原子化学性质都不稳定,都容易得电子形成稳定结构
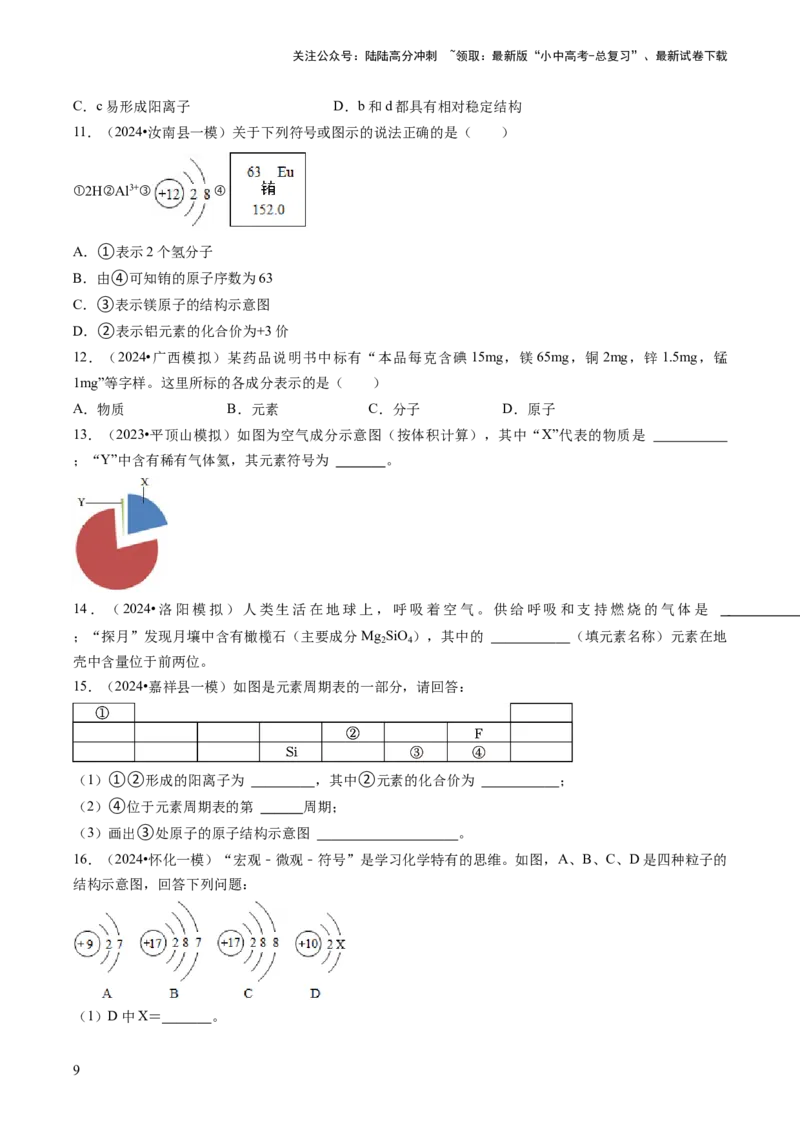
5.(2024•中方县一模)下列有关事实的解释中,不合理的是( )
A.硫在空气和氧气中燃烧的现象不同﹣﹣﹣﹣氧气含量不同
B.水和过氧化氢的化学性质不同﹣﹣﹣﹣氧原子个数不同
C.金刚石、石墨物理性质差异较大﹣﹣﹣﹣碳原子的排列方式不同
D.硫和磷两种元素的种类不同﹣﹣﹣﹣质子数不同
6.(2024•南昌县一模)物质是由微观粒子构成的。下列粒子一定带正电的是( )
A.分子 B.阳离子 C.原子 D.中子
7.(2023•凉山州模拟)某元素R原子序数为m,能够形成核外有x个电子的Rn﹣,则下列关系式一定正
确的是( )
A.m=n B.m=n+x C.m=n﹣x D.m=x﹣n
8.(2024•方城县一模)钇是最早被发现的稀土元素,它在发光材料、激光材料、高温超导材料等领域有
着重要的作用。钇在元素周期表中的信息及原子结构示意图如图所示。下列说法中正确的是( )
A.钇属于非金属元素 B.钇离子符号是Y2+
C.钇的相对原子质量是39 D.钇元素位于元素周期表中第二周期
9.(2024•莱芜区校级模拟)元素周期表的一部分及硫原子结构示意图如图所示。下列说法错误的是(
)
A.氩元素的相对原子质量是39.95 B.硫原子在化学反应中易失电子
C.X原子的核外有三个电子层 D.图中三种元素位于同一周期
10.(2024•市中区一模)从微观视角认识物质是学习化学的重要思维方法。如图是四种微观粒子的结构示
意图,下列相关说法中,不正确的是( )
A.图中共涉及四种元素 B.a在化合物中的化合价通常显﹣2价
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.c易形成阳离子 D.b和d都具有相对稳定结构
11.(2024•汝南县一模)关于下列符号或图示的说法正确的是( )
①2H②Al3+③ ④
A.①表示2个氢分子
B.由④可知铕的原子序数为63
C.③表示镁原子的结构示意图
D.②表示铝元素的化合价为+3价
12.(2024•广西模拟)某药品说明书中标有“本品每克含碘15mg,镁65mg,铜2mg,锌1.5mg,锰
1mg”等字样。这里所标的各成分表示的是( )
A.物质 B.元素 C.分子 D.原子
13.(2023•平顶山模拟)如图为空气成分示意图(按体积计算),其中“X”代表的物质是
;“Y”中含有稀有气体氦,其元素符号为 。
14.(2024•洛阳模拟)人类生活在地球上,呼吸着空气。供给呼吸和支持燃烧的气体是
;“探月”发现月壤中含有橄榄石(主要成分 Mg SiO ),其中的 (填元素名称)元素在地
2 4
壳中含量位于前两位。
15.(2024•嘉祥县一模)如图是元素周期表的一部分,请回答:
(1)①②形成的阳离子为 ,其中②元素的化合价为 ;
(2)④位于元素周期表的第 周期;
(3)画出③处原子的原子结构示意图 。
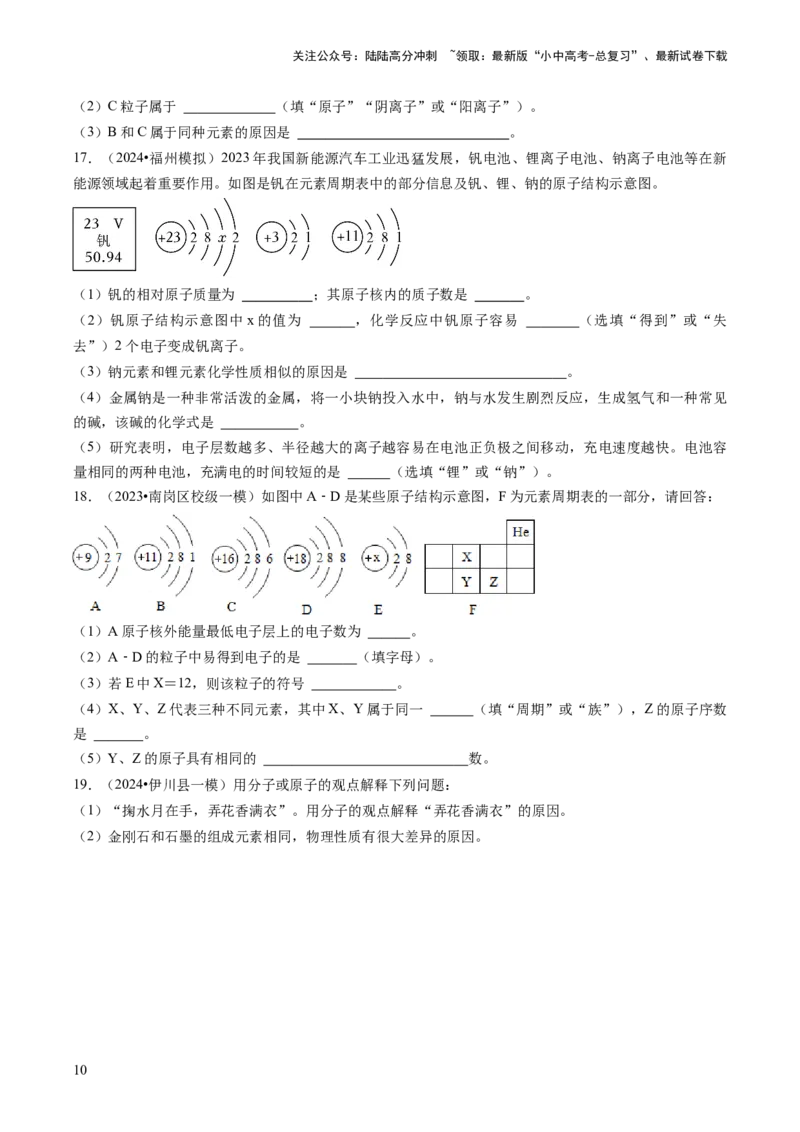
16.(2024•怀化一模)“宏观﹣微观﹣符号”是学习化学特有的思维。如图,A、B、C、D是四种粒子的
结构示意图,回答下列问题:
(1)D中X= 。
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)C粒子属于 (填“原子”“阴离子”或“阳离子”)。
(3)B和C属于同种元素的原因是 。
17.(2024•福州模拟)2023年我国新能源汽车工业迅猛发展,钒电池、锂离子电池、钠离子电池等在新
能源领域起着重要作用。如图是钒在元素周期表中的部分信息及钒、锂、钠的原子结构示意图。
(1)钒的相对原子质量为 ;其原子核内的质子数是 。
(2)钒原子结构示意图中x的值为 ,化学反应中钒原子容易 (选填“得到”或“失
去”)2个电子变成钒离子。
(3)钠元素和锂元素化学性质相似的原因是 。
(4)金属钠是一种非常活泼的金属,将一小块钠投入水中,钠与水发生剧烈反应,生成氢气和一种常见
的碱,该碱的化学式是 。
(5)研究表明,电子层数越多、半径越大的离子越容易在电池正负极之间移动,充电速度越快。电池容
量相同的两种电池,充满电的时间较短的是 (选填“锂”或“钠”)。
18.(2023•南岗区校级一模)如图中A﹣D是某些原子结构示意图,F为元素周期表的一部分,请回答:
(1)A原子核外能量最低电子层上的电子数为 。
(2)A﹣D的粒子中易得到电子的是 (填字母)。
(3)若E中X=12,则该粒子的符号 。
(4)X、Y、Z代表三种不同元素,其中X、Y属于同一 (填“周期”或“族”),Z的原子序数
是 。
(5)Y、Z的原子具有相同的 数。
19.(2024•伊川县一模)用分子或原子的观点解释下列问题:
(1)“掬水月在手,弄花香满衣”。用分子的观点解释“弄花香满衣”的原因。
(2)金刚石和石墨的组成元素相同,物理性质有很大差异的原因。
10