文档内容
2007 年海南高考化学真题及答案
注意事项:
1.本试卷第I卷(选择题)和第II卷(非选择题)两部分,答卷前,考生务必将自己的
姓名、准考证号填写在答题卡上。
2.回答第I卷时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其它答案标号。写在本试卷上无效。
3.回答第II卷时,将答案写在答题卡上。写在本试卷无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5
第I卷
一、选择题:本题共12小题,每小题3分,在每小题给出的四个选项中,只有一个选项符
合题目要求的。
1.下列物质中,不含有硅酸盐的是
A.水玻璃 B.硅芯片 C.黏土 D.普通水
泥
2.下列原子序数所对应的元素组中,两者可形成离子键的是
A.1和17 B.12和9 C.14和 6 D.
15和8
3.下列叙述正确的是
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2mol/L的盐酸,与等体积水混合后pH=1
D.pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7
4.下列叙述正确的是
A.一定温度、压强下,气体体积由其分子的大小决定
B.一定温度、压强下,气体体积由其物质的量的多少决定
C.气体摩尔体积是指1mol任何气体所占的体积为22.4L
D.不同的气体,若体积不等,则它们所含的分子数一定不等
5.下列烷烃在光照下与氯气反应,只生成一种一氯代烃的是
6.已知:(1)Zn(s)+1/2O(g)==ZnO(s),ΔH=-348.3kJ/mol
2
(2) 2Ag(s)+1/2 O(g)== AgO(s),ΔH=-31.0kJ/mol
2 2
则Zn(s)+ AgO(s)== ZnO(s)+ 2Ag(s)的ΔH等于
2
A . -317.3kJ/mol B . -379.3kJ/mol C . -332.8
kJ/mol D.317.3 kJ/mol7.下列实验现象的描述错误的是
A.氢气在氯气中燃烧生成绿色烟雾
B.红热的铁丝在氧气中燃烧,火星四射,生成黑色固体颗粒
C.点燃的硫在氧气中剧烈燃烧,发出蓝紫色火焰
D.钠在空气中燃烧,发出黄色的火焰,生成淡黄色固体
8.下列溶液能与镁反应生成氢气的是
A.氯化铵溶液 B.氢氧化钠溶液 C.碳酸钾溶液 D.饱和石灰水
9.由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③
加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是
A.②④⑤③① B.③②④①⑤ C.③④②⑤① D.②④③⑤①
10.能正确表示下列反应的离子方程式是
A.碳酸氢钙溶液和氢氧化钠溶液混合
HCO—+OH—==CO2—+HO
3 3 2
B.醋酸钠溶液和盐酸混合
CHCOONa+H+ == CHCOOH + Na+
3 3
C.少量金属钠放入冷水中
Na+ 2HO== Na++2OH—+H↑
2 2
D.硫酸铜溶液和氢氧化钡溶液混合
Cu2+ + SO2— +Ba2+ + 2OH—== Cu(OH)↓+ BaSO↓
4 2 4
11.在pH=1时,可大量共存且形成无色溶液的一组离子或分子是
A.Ca2+、CHCOOH、Br—、Na+ B.NO—、Fe3+、Mg2+、SO2—
3 3 4
C.HClO、Ba2+、Na+ 、Cl— D.K+、Cl—、Al3+、SO2—
3
12.有BaCl 和NaCl的混合溶液aL,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全
2
沉淀;另一份滴加 AgNO 溶液,使 Cl—离子完全沉淀。反应中消耗 xmol H SO 、ymol
3 2 4
AgNO。据此得知原混合溶液中的c(Na+)/ mol·L-1为
3
A.(y-2x)/a B.(y-x)/a C.(2y-2x)/a
D.(2y-4x)/a第II卷
本卷包括必考题和选考题两部分。第13题~第17题为必考题,每个试题考生都必须做答。
第18题~第29题为选考题,考生根据要求做答。
13.(10分)
下表为元素周期表的一部分,请回答有关问题:
IA IIA IIIA IVA VA VIA VIIA 0
2 ① ②
3 ③ ④ ⑤ ⑥ ⑦ ⑧
4 ⑨ ⑩
(1)⑤和⑧的元素符号是 和 ;
( 2 ) 表 中 最 活 泼 的 金 属 是 , 非 金 属 最 强 的 元 素
是 ;(填写元素符号)
(3)表中能形成两性氢氧化物的元素是 ,分别写出该元素的氢
氧化物与⑥、⑨最高价氧化物的水化物反应的化学方程式:
;
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:
。
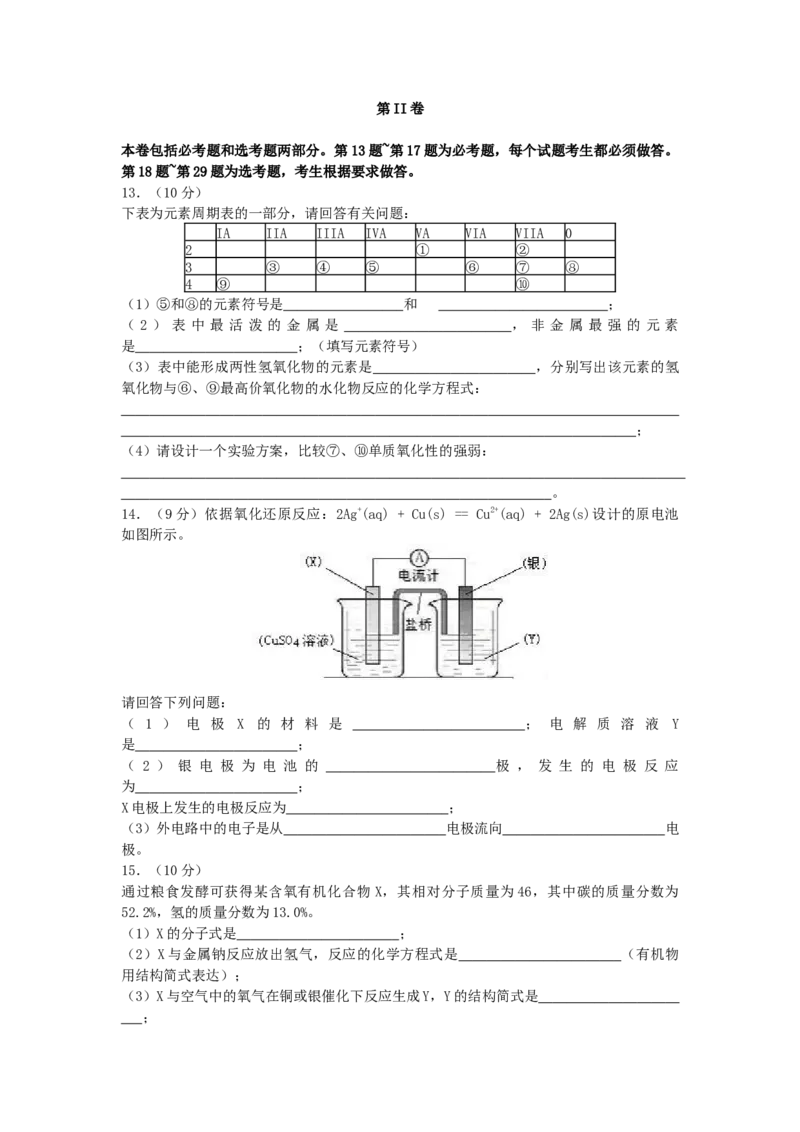
14.(9分)依据氧化还原反应:2Ag+(aq) + Cu(s) == Cu2+(aq) + 2Ag(s)设计的原电池
如图所示。
请回答下列问题:
( 1 ) 电 极 X 的 材 料 是 ; 电 解 质 溶 液 Y
是 ;
( 2 ) 银 电 极 为 电 池 的 极 , 发 生 的 电 极 反 应
为 ;
X电极上发生的电极反应为 ;
(3)外电路中的电子是从 电极流向 电
极。
15.(10分)
通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为
52.2%,氢的质量分数为13.0%。
(1)X的分子式是 ;
(2)X与金属钠反应放出氢气,反应的化学方程式是 (有机物
用结构简式表达);
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y的结构简式是
;(4)X与高锰酸钾酸性溶液反应可生成Z。在加热和浓硫酸作用下,X与Z反应可生成一种
有香味的物质W,若184gX和120gZ反应能生成106gW,计算该反应的产率。(要求写出计
算过程)
16.(6分)
PCl 的热分解反应如下:
5
PCl(g) PCl(g) + Cl(g)
5 3 2
(1) 写出反应的平衡常数表达式;
(2) 已知某温度下,在容积为10.0L的密闭容器中充入2.00mol PCl ,达到平衡后,测
5
得容器内PCl 的浓度为0.150mol/L。计算该温度下的平衡常数。
3
17.(9分)下表是稀硫酸与某金属反应的实验数据:
实验序金属 金属状态 C(HSO) V(HSO) 溶液温度/℃ 金属消失的
2 4 2 4
号 质量/g /mol·L-1 /mL 反应前 反应后 时间/s
1 0.10 丝 0.5 50 20 34 500
2 0.10 粉末 0.5 50 20 35 50
3 0.10 丝 0.7 50 20 36 250
4 0.10 丝 0.8 50 20 35 200
5 0.10 粉末 0.8 50 20 36 25
6 0.10 丝 1.0 50 20 35 125
7 0.10 丝 1.0 50 35 50 50
8 0.10 丝 1.1 50 20 34 100
9 0.10 丝 1.1 50 20 44 40
分析上述数据,回答下列问题:
(1)实验 4 和 5 表明, 对反应速率有影响,
反应速率越快,能表明同一规律的实验还
有 (填实验序号);
(2)仅表明反应物浓度对反应速率产生影响的实验有 =
(填实验序号);
(3)本实验中影响反应速率的其他因素还有 ,
其实验序号是 。
(4)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因:
。
以下是选考题,其中第18、19、20、21题为《有机化学基础》模块题,第22、23、24、
25题为《物质结构与性质》模块题,第26、27、28、29题为《化学与技术》模块题。考
生只能从三个模块中任选一个作答,不得跨模块答题,否则只能以所答的第一个模块计分。
《有机化学基础》模块
18-20为选择题,每小题只有一个正确选项,每小题3分
18.下列分子中,所有原子都处在同一平面的是
A.环已烯 B.丙炔 C.乙烷
D.苯
19.分子式为CH10的烯烃共有(要考虑顺反异构体)
5
A.5 种 B.6 种 C.7 种
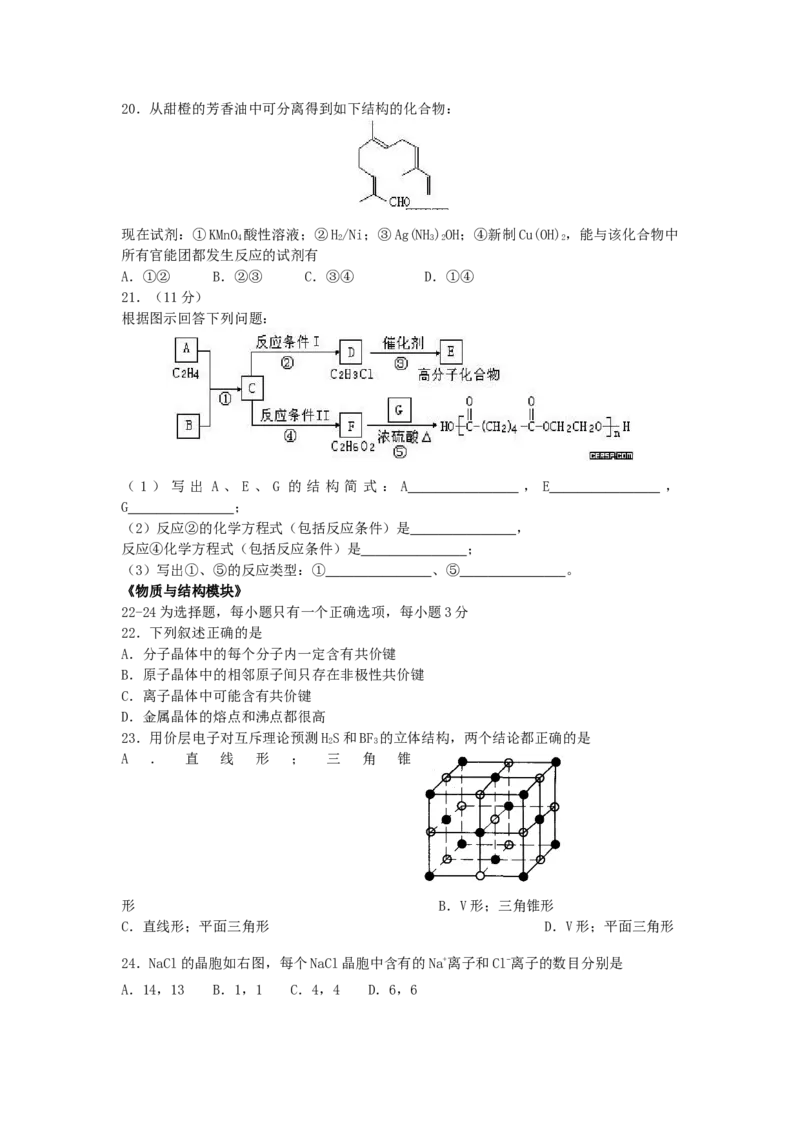
D.8种20.从甜橙的芳香油中可分离得到如下结构的化合物:
现在试剂:①KMnO 酸性溶液;②H/Ni;③Ag(NH)OH;④新制Cu(OH) ,能与该化合物中
4 2 3 2 2
所有官能团都发生反应的试剂有
A.①② B.②③ C.③④ D.①④
21.(11分)
根据图示回答下列问题:
( 1 ) 写 出 A 、 E 、 G 的 结 构 简 式 : A , E ,
G ;
(2)反应②的化学方程式(包括反应条件)是 ,
反应④化学方程式(包括反应条件)是 ;
(3)写出①、⑤的反应类型:① 、⑤ 。
《物质与结构模块》
22-24为选择题,每小题只有一个正确选项,每小题3分
22.下列叙述正确的是
A.分子晶体中的每个分子内一定含有共价键
B.原子晶体中的相邻原子间只存在非极性共价键
C.离子晶体中可能含有共价键
D.金属晶体的熔点和沸点都很高
23.用价层电子对互斥理论预测HS和BF 的立体结构,两个结论都正确的是
2 3
A . 直 线 形 ; 三 角 锥
形 B.V形;三角锥形
C.直线形;平面三角形 D.V形;平面三角形
24.NaCl的晶胞如右图,每个NaCl晶胞中含有的Na+离子和Cl-离子的数目分别是
A.14,13 B.1,1 C.4,4 D.6,625.(11分)
A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为
;
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号
为 ,C的元素符号为 ;
(3)D元素的正三价离子的3d亚层为半充满,D的元素符号为 ,其基态原子
的电子排布式为 。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符
号为 ,其基态原子的电子排布式为 。
《化学与技术》模块
26-28为选择题,每个小题只有一个正确选项,每小题3分
26.下列有关合成洗涤剂的叙述错误的是
A.在洗涤剂烷基苯磺酸钠中,烷基含碳原子的个数以12~18为宜
B.在洗涤剂烷基苯磺酸钠中,烷基应以带有支链的为宜
C.在合成洗涤剂中添加酶制剂可提高洗涤效果
D.在合成洗涤剂中应以无磷助剂代替含磷助剂
27.下列有关生铁炼钢的叙述错误的是
A.添加必要的元素,改善钢材的组织结构和性能
B.适当降低生铁中的含碳量,除去大部分硫、磷等杂质
C.加入硅、锰、铝等合金元素调整成分并脱去钢水中的氧
D.除去生铁中的非金属元素
28.目前下列工艺过程没有直接使用离子交换技术的是
A.硬水的软化 B.电解饱和食盐水制造
NaOH
C.电渗析淡化海水 D.海水中提取金属Mg
29.纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种
工艺。请按要求回答问题:
(1)“氨碱法”产生大量CaCl 废弃物,请写出该工艺中产生CaCl 的化学方程式:
2 2
;
(2)写出“联合制碱法”有关反应的化学方程式:
;
;
(3)CO 是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO 的来源有何不同?
2 2
;
(4)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应,列
出计算原子利用率的表达式:
原子利用率(%)=
。参考答案
第I卷
1、B 2、B 3、C 4、B 5、C 6、D 7、A 8、A 9、D 10、D 11、A 12、A
第II卷
13、(1)Si Ar
(2)K F
(3)铝(或Al)2Al(OH) + 3HSO==Al(SO) + 6HO
3 2 4 2 4 3 2
Al(OH) + KOH==KAlO +2HO
3 2 2
(4)在NaBr溶液中通入氯气(或加入氯水),溶液液变红棕色(或橙色)。
14、(1)Cu AgNO
3
(2)正极 Ag+ +e-=Ag↓ Cu-2e-=Cu2+
(3)X Ag
15、(1)CHO
2 6
(2)2CHOH + 2Na 2CHONa + H↑
2 5 2 5 2
(3)CHCHO
3
(4)Z为CHCOOH,与X反应的化学方程式为
3
浓硫酸
CHCOOH + CHOH CHCOOH + HO
3 2 5 3 2
△
已知n (CHCOOH)===2mol
3
n (C2H5OH)== > 2mol
所以乙醇过量,应以乙酸计算产率
2mol乙酸完全酯化可生成乙酸乙酯2mol×88g·mol-1=176g
所以该反应的产率为
×100%=60.2%
16、(1)K==
(2) PCl(g) PCl(g) + Cl(g)
5 3 2
c(起始)(mol/L) =0.200 0 0
c(变化)(mol/L) 0.150 0.150 0.150
c(平衡)(mol/L) 0.050 0.150 0.150
所以平衡常数K====0.45
17、(1)固体反应物的表面积 表面积越大 1和2
(2)3和4
(3)开始反应温度 6和7
(4)一定量的金属跟足量的硫酸反应放出的热量相同。
选考题
《有机化学基础》模块
18、D
19、B
20、A
21、(1)CH=CH HOOC(CH)COOH
2 2 2 4
(2)(3)加成 缩聚
《物质与结构模块》
22、C
23、D
24、C
25、(1)N
(2)Cl K
(3)Mn 1s22s22p63s23p63d54s2
(4) Cu 1s22s22p63s23p63d104s1
《化学与技术》模块
26、B
27、D
28、D
29、(1)2NHCl +(OH) △ C a Cl +2NH↑+2HO
4 2 2 3 2
(2)NH +HO +CO +NaCl=NaHCO↓+ NHCl
3 2 2 3 4
2NaHCO △ N a CO +CO↑+HO
3 2 3 2 2
(3)前者的CO 来自合成氨厂,后者的CO 来自煅烧石灰石。
2 2
(4)×100%=100%