文档内容
2008 年全国普通高等学校招生统一考试
上海化学试卷
考生注意:
1.本试卷满分l50分,考试时问120分钟·
2.本考试设试卷和答题纸两部分,试卷包括试题与答题要求;所有答题必须涂(选择
题)或写(非选择题)在答题纸上;做在试卷上一律不得分。
3.答题前,考生务必在答题纸上用钢笔或圆珠笔清楚填写姓名、准考证号,并将核对
后的条形码贴在指定位置上。
4.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
1.(08上海卷)食品检验是保证食品安全的重要措施,下列不属于食品安全检测指标的
是( )
A.淀粉的含量 B.二氧化硫的含量
C.亚硝酸盐的含量 D.甲醛的含量
2.(08上海卷)化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是(
)
3.(08上海卷)植物及其废弃物可以制取乙醇燃料,下列关于乙醇燃料的说法错误的是
( )
A.它是一种再生能源 B.乙醇易燃烧,污染小
C.乙醇只能在实验室内作燃料 D.粮食作物是制乙醇的重要原料
4.(08上海卷)下列化学式既能表示物质的组成,又能表示物质的一个分子的是( )
A.NaOH B.SiO C.Fe D.C H
2 3 8
5.(08上海卷)下列关于化学学习和研究的说法错误的是( )
A.化学模型有助于解释一些化学现象
B.质量守恒定律是大量实验事实的总结
C.化学家提出的假设都能被实验证实
D.化学基本原理的应用是有一定条件的
6.(08上海卷)下列物质中,只有氧化性、只有还原性,既有氧化性又有还原性的顺序
排列的一组是( )
A.F 、K、HCl B.Cl 、Al、H C.NO 、Na、Br D.O 、SO 、H O
2 2 2 2 2 2 2 2
7.(08上海卷)下列各化合物的命名中正确的是( )
8.(08上海卷)在一定的条件下,完全分解下列某化合物2g,产生氧气1.6g,此化合
物是( )9.(08上海卷)设N 为阿伏加德罗常数,下列说法正确的是( )
A
A.23gNa在氧气中完全燃烧失电子数为0.5N
A
B.1L2mol·L-1的MgCl 溶液中含Mg2+数为2N
2 A
C.标准状况下,11.2LSO 所含分子数为0.5N
3 A
D.室温下,8g甲烷含有共价键数为2N
A
10.(08上海卷)由图的装置中,干燥烧瓶内盛有某种气体,烧杯和滴定管内盛放某种
液体。挤压滴管的胶头,下列 与实验事实不相符的是( )
A.CO (NaHCO 溶液)/无色喷泉 B.NH (H O含酚酞)/红色喷泉
2 3 3 2
C.H S(CuSO 溶液)/黑色喷泉 D.HCl(AgNO 溶液)/白色喷泉
2 4 3
11.(08上海卷)常温下,某溶液中由水电离出来的c(H+)=1.0×10-13mol·L-1,该溶液
可能是( )
①二氧化硫 ②氯化铵水溶液 ③硝酸钠水溶液 ④氢氧化钠水溶液
A.①④ B.①② C.②③ D.③④
12.(08上海卷)取一张用饱和的NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通
直流电源,一段时间后,发现a电极与试纸接触处出现一个双色同心圆,内圈为白色,
外圈呈浅红色。则下列说法错误的是( )
A.b电极是阴极 B.a电极与电源的正极相连
C.电解过程中水是氧化剂 D.b电极附近溶液的pH变小
13.(08上海卷)已知在热的碱性溶液中,NaClO发生如下反应:3NaClO
2NaCl+NaClO 。在相同条件下NaClO 也能发生类似的反应,其最终产物是( )
3 2
A.NaCl、NaClO B.NaCl、NaClO C.NaClO、NaClO D.NaClO 、
3 3 3
NaClO
4
14.(08上海卷)某酸性溶液中只有Na+、CH COO-、H+、OH-四种离子。则下列描
3
述正确的是( )
A.该溶液由pH=3的CH COOH与pH=11的NaOH溶液等体积混合而成
3
B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH COOH溶液混合而成
3
C.加入适量的NaOH,溶液中离子浓度为c(CH COO-)>c(Na+)>c(OH-)>c(H+)
3
D.加入适量氨水,c(CH COO-)一定大于c(Na+)、c(NH +)之和
3 4
15.(08上海卷)已知气体的摩尔质量越小,扩散速度越快。右图所示为气体扩散速度
的实验,两种气体扩散相遇时形成白色烟环。下列关于甲、乙的判断正确的是( )
A.甲是浓氨水,乙是浓硫酸 B.甲是浓盐酸,乙是浓氨
水
C.甲是浓氨水,乙是浓盐酸 D.甲是浓硝酸,乙是浓氨
水
16.霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物。下列关于MMF的说法正
确的是( )
A.MMF能溶于水
B.MMF能发生取代反应和消去反应
C.1molMMF能与6mol氢气发生加成反应
D.1molMMF能与含3molNaOH溶液完全反应17.(08上海卷)已知:H (g)+F (g) 2HF(g)+270kJ,下列说法正确的是( )
2 2
A.2L氟化氢气体分解成1L的氢气和1L的氟气吸收270kJ热量
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ
18.(08上海卷)设计学生实验要注意安全、无污染、现象明显。根据启普发生器原理,
可用底部有小孔的试管制简 易的气体发生器(见右图)。若关闭K,不能使反应停止,可
将试管从烧杯中取出(会有部分气体逸散)。
下列气体的制取宜使用该装置的是( )
A.用二氧化锰(粉末)与双氧水制氧气
B.用锌粒与稀硫酸制氢气
C.用硫化亚铁(块状)与盐酸制硫化氢
D.用碳酸钙(块状)与稀硫酸制二氧化碳
19.(08上海卷)研究发现,空气中少量的NO 能参与硫酸型酸雨的形成,反应过程如
2
下:
①SO +N O SO +NO ②SO +H O H SO ③2NO+O 2NO
2 2 5 3 3 2 2 4 2 2
NO 在上述过程中的作用,与H SO 在下述变化中的作用相似的是( )
2 2 4
A.潮湿的氯气通过盛有浓H SO 的洗气瓶
2 4
B.硫化氢通入浓H SO
2 4
C.浓H SO 滴入萤石中,加热
2 4
D.加入少量的H SO 使乙酸乙酯水解
2 4
20.(08上海卷)下列离子方程式书写正确的是( )
A.AgNO 溶液滴入少量的Na S溶液 2Ag++S2- Ag S↓
3 2 2
B.过量的CO 通入Ca(ClO) 溶液中 ClO-+CO +H O HCO -+HClO
2 2 2 2 3
C.向Na CO 溶液中加入过量CH COOH溶液 CO 2-+2H+ CO ↑+H O
2 3 3 3 2 2
D.向Ba(OH) 溶液中加入少量的NaHSO 溶液 2HSO -+Ba2++2OH-
2 3 3
BaSO ↓+SO 2-+2H O
3 3 2
21.(08上海卷)等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时
间t产生气体体积V的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的实
验组别可能是( )
A.4-3-2-1 B.1-2-3-4 C.3-4-2-1 D.1-2-4-3
22.(08上海卷)在石灰窑中烧制生石灰,1molCaCO 完全分解所需要的能量,可燃烧
3
0.453mol碳来提供。设空气中O 体积分数为0.21,N 为0.79,则石灰窑产生的气
2 2
体中CO 的体积分数可能是( )
2
A.0.43 B.0.46 C.0.49 D.0.52
23.(08上海卷)(A)四种短周期元素的性质或结构信息如下表,请根据信息回答下列
问题:(1)B 元素在周期表中的位置是_________________________,写出 A 原子的电子排布式
__________________。
(2)写出C单质与水反应的化学方程式____________________________________________。A
与C形成的化合物溶于水后,溶液的pH__________7(填“大于”、“等于”或“小
于”)。
(3)D 元素最高价氧化物晶体的硬度________(填“大”、“小”),其理由是
____________________________。
(4)A、B两元素非金属性较强的是(写元素符号)__________。写出能证明这一结论的一
个实验事实__________
_____________________________________________。
。
24.(08上海卷)(B)元素A~D是元素周期表中短周期的四种元素,请根据表中的信
息回答下列问题。
(1)上表中与 A 属于同一周期的元素是_____________,写出 D 离子的电子排布式
______________________。
(2)D 和 C 形成的化合物属于_________晶体。写出 C 单质与水反应的化学方程式
_________________________。
(3)对元素B的单质或化合物描述正确的是_________。
a、B元素的最高正价为+6 b、常温、常压下单质难溶于水
c、单质分子中含有18个电子 d、在一定条件下镁条能与单质B反应
(4)A和D两元素金属性较强的是(写元素符号)_____。写出能证明该结论的一个实验事
实________________。
25.(08上海卷)某反应体系的物质有:NaOH、Au O 、Na S O 、Na S O 、Au O、
2 3 2 4 6 2 2 3 2
H O。
2
(1)请将Au O 之外谁反应物与生成物分别填入以下空格内。
2 3(2)反应中,被还原的元素是_______,还原剂是____________。
(3)将氧化剂与还原剂填入空格中,并标出电子转移的方向和数目。
(4)纺织工业中常用氯气作漂白剂,Na S O 可作为漂白后布匹“脱氯剂”,Na S O 和
2 2 3 2 2 3
Cl 反应的产物是 H SO 、NaCl 和 HCl,则还原剂与氧化剂物质的量之比为
2 2 4
__________。
26.(08上海卷)在2L密闭容器中,800℃时反应2NO(g)+O (g) 2NO (g)体系中,
2 2
n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=___________________。
已知:K(300℃)>K(350℃),该反应是________热反应。
(2)右图中表示NO 的变化的曲线是____________。
2
用O 表示从0~2s内该反应的平均速率v=___________。
2
(3)能说明该反应已经达到平衡状态的是___________。
a、v(NO )=2v(O ) b、容器内压强保持不变
2 2
c、v逆(NO)=2v正(O ) d、容器内的密度保持不变
2
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
a、及时分离出NO 气体 b、适当升高温度
2
c、增大O 的浓度 d、选择高效的催化剂
2
27.(08上海卷)(A)如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,
将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测
定)。试回答下列问题:
(1)实验 1 中,沉淀最终变为________色,写出沉淀变色的化学方程式
_______________________________。
(2)实验2甲针筒内的现象是:有___________生成,活塞________移动(填向外、向内、不)。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入
___________溶液中。
(3)实验3中,甲中的3mL气体是NO 和N O 的混合气体,那么甲中最后剩余的无色
2 2 4
气 体 是 _______ , 写 出 NO 与 H O 反 应 的 化 学 方 程 式 为
2 2
_______________________________。
(4)实验4中,已知:3Cl +2NH N +6HCl。甲针筒出活塞有移动,针筒内有
2 3 2
白烟产生外,气体的颜色变为____________。最后针筒内剩余气体的体积约为
________mL。
28.(08上海卷)(B)某实验小组用下列装置进行乙醇催化氧化的实验。
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式
________________________________________________________________________________。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反
应是______反应。
(2)甲和乙两个水浴作用不相同。甲的作用是_____________;乙的作用是
___________________。
(3)反应进行一段时间后,干燥管 a 中能收集到不同的物质,它们是
____________________________ 。 集 气 瓶 中 收 集 到 的 气 体 的 主 要 成 分 是
_____________________。
(4)若试管 a 中收集到的液体用紫色石蕊试纸,试纸显红色,说明液体中还有
____________。要除去该物质,可先在混合液中加入_________(填写字母)。
a、氯化钠溶液 b、苯 c、碳酸氢钠溶液 d、四氯化碳
然后再通过___________(填实验操作名称)即可除去。
29.(08上海卷)明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,
此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示:
根据上述图示,完成下列填空:
(1)明矾石焙烧后用稀氨水浸出。配制500mL稀氨水(每升含有39.20g氨)需要取浓
氨水(每升含有251.28g氨)__________mL,用规格为_______mL量筒量取。(2)氨水浸出后得到固体混合体系,过滤,滤液中除K+、SO 2-外,还有大量的NH +。
4 4
检验NH +的方法是_______________________________________________________。
4
(3)写出沉淀物中所有物质的化学式________________________________________。
(4)滤液I的成分是水和______________。
(5)为测定混合肥料K SO 、(NH ) SO 中钾的含量,请完善下列步骤:
2 4 4 2 4
①称取钾氮肥试样并溶于水,加入足量______溶液,产生白色沉淀。
②___________、__________、_________(依次填写实验操作名称)。
③冷却、称重。
(6)若试样为 mg,沉淀的物质的量为 nmol,则试样中 K SO 的物质的量为:
2 4
___________mol(用含有m、n的代数式表示)。
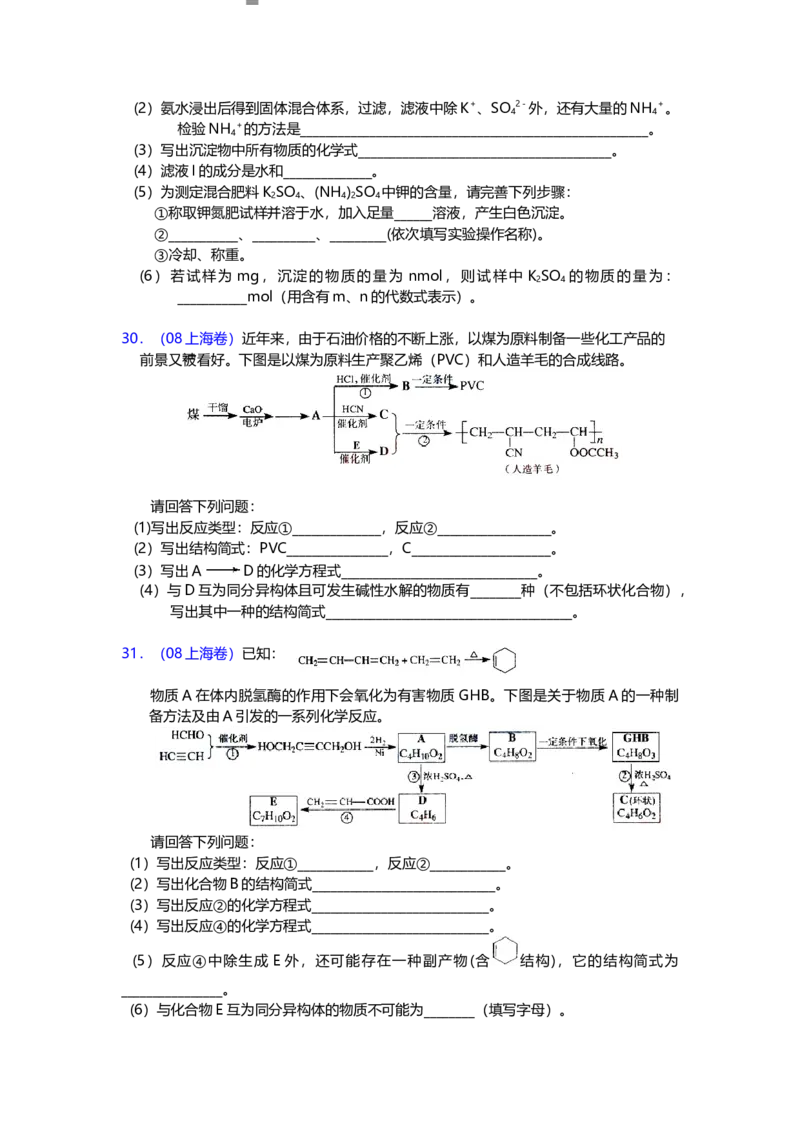
30.(08上海卷)近年来,由于石油价格的不断上涨,以煤为原料制备一些化工产品的
前景又被看好。下图是以煤为原料生产聚乙烯(PVC)和人造羊毛的合成线路。
请回答下列问题:
(1)写出反应类型:反应①______________,反应②__________________。
(2)写出结构简式:PVC________________,C______________________。
(3)写出A D的化学方程式_______________________________。
(4)与D互为同分异构体且可发生碱性水解的物质有________种(不包括环状化合物),
写出其中一种的结构简式_______________________________________。
31.(08上海卷)已知:
物质A在体内脱氢酶的作用下会氧化为有害物质 GHB。下图是关于物质A的一种制
备方法及由A引发的一系列化学反应。
请回答下列问题:
(1)写出反应类型:反应①____________,反应②____________。
(2)写出化合物B的结构简式_____________________________。
(3)写出反应②的化学方程式____________________________。
(4)写出反应④的化学方程式____________________________。
(5)反应④中除生成 E 外,还可能存在一种副产物(含 结构),它的结构简式为
________________。
(6)与化合物E互为同分异构体的物质不可能为________(填写字母)。a、醇 b、醛 c、羧酸 d、酚
32.(08上海卷)生态溶液涉及农家肥料的综合利用,某种肥料经发酵得到一种含有甲
烷、二氧化碳、氮气的混合气体。2.016L(标准状况)该气体通过盛有红色CuO粉末
△
的硬质玻璃管,发生的反应为:CH +4CuO CO +2H O+
4 2 2
4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过过
量的澄清石灰水,充分吸收,生成沉淀8.5g。
(1)原混合气体中甲烷的物质的量是____________。
(2)原混合气体中氮气的体积分数为多少?(写出计算过程)
33.(08上海卷)小苏打、胃舒、平达喜都是常用的中和胃酸的药物。
(1)小苏打片每片含0.5gNaHCO ,2片小苏打片和胃酸完全中和,被中和的 H+是
3
___________mol。
(2)胃舒平每片含0.245gAl(OH) 。中和胃酸时,6片小苏打片相当于胃舒平_____片。
3
(3)达喜的化学成分是铝和镁的碱式盐。
①取该碱式盐3.01g,加入2.0mol·L-1盐酸使其溶解,当加入盐酸42.5mL时,开始
产生CO ,加入盐酸至45.0mL时正好反应完全,计算该碱式盐样品中氢氧根
2
与碳酸根的物质的量之比。
②在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤,沉淀物进行干燥后
重1.74g,若该碱式盐中氢元素的质量分数为 0.040,试推测该碱式盐的化学
式。