文档内容
2015年安徽省高考理综化学试题
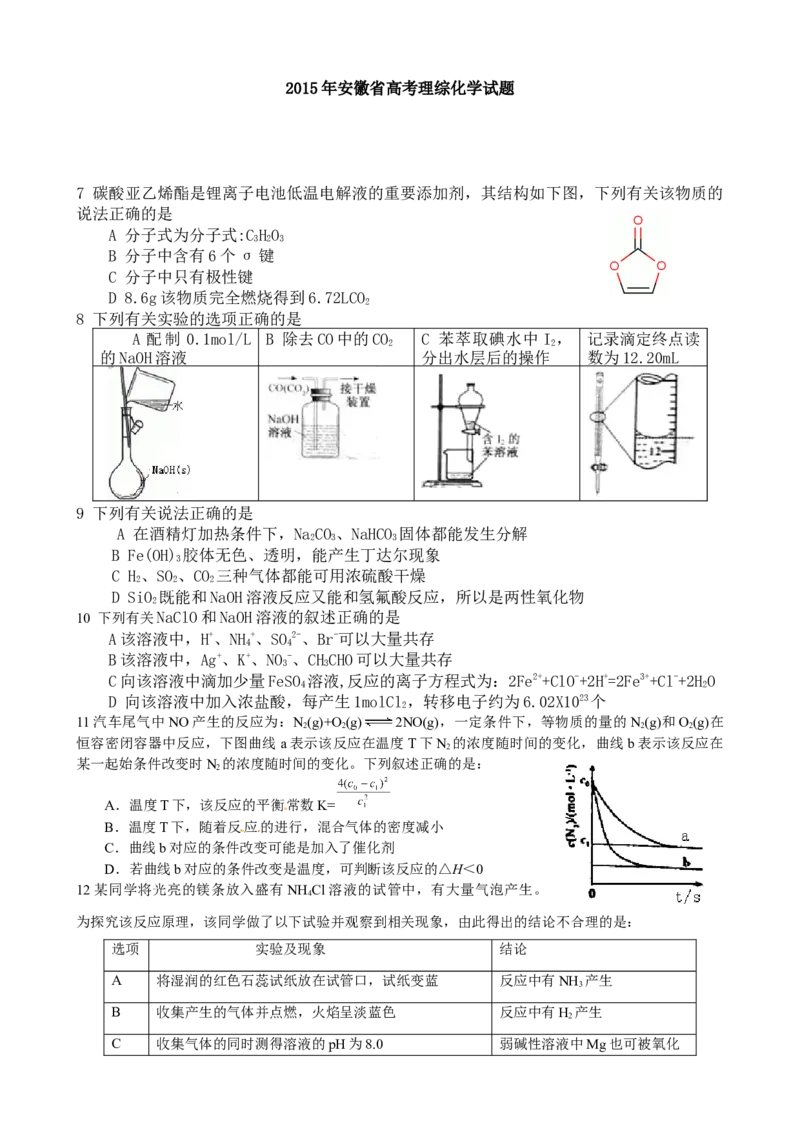
7 碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构如下图,下列有关该物质的
说法正确的是
A 分子式为分子式:C H O
3 2 3
B 分子中含有6个σ键
C 分子中只有极性键
D 8.6g该物质完全燃烧得到6.72LCO
2
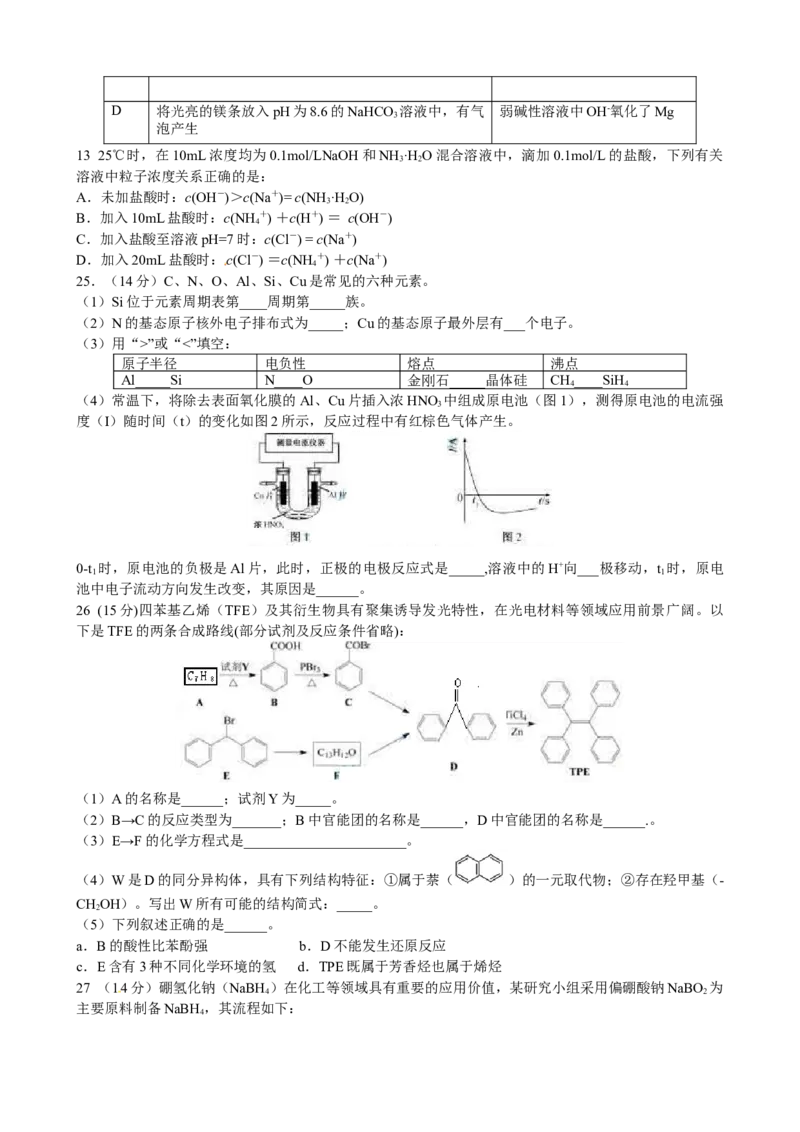
8 下列有关实验的选项正确的是
A 配制 0.1mol/L B 除去CO中的CO C 苯萃取碘水中 I , 记录滴定终点读
2 2
的NaOH溶液 分出水层后的操作 数为12.20mL
9 下列有关说法正确的是
A 在酒精灯加热条件下,Na CO 、NaHCO 固体都能发生分解
2 3 3
B Fe(OH) 胶体无色、透明,能产生丁达尔现象
3
C H 、SO 、CO 三种气体都能可用浓硫酸干燥
2 2 2
D SiO 既能和NaOH溶液反应又能和氢氟酸反应,所以是两性氧化物
2
10 下列有关NaClO和NaOH溶液的叙述正确的是
A该溶液中,H+、NH +、SO 2-、Br-可以大量共存
4 4
B该溶液中,Ag+、K+、NO -、CH CHO可以大量共存
3 3
C向该溶液中滴加少量FeSO 溶液,反应的离子方程式为:2Fe2++ClO-+2H+=2Fe3++Cl-+2H O
4 2
D 向该溶液中加入浓盐酸,每产生1molCl ,转移电子约为6.02X1023个
2
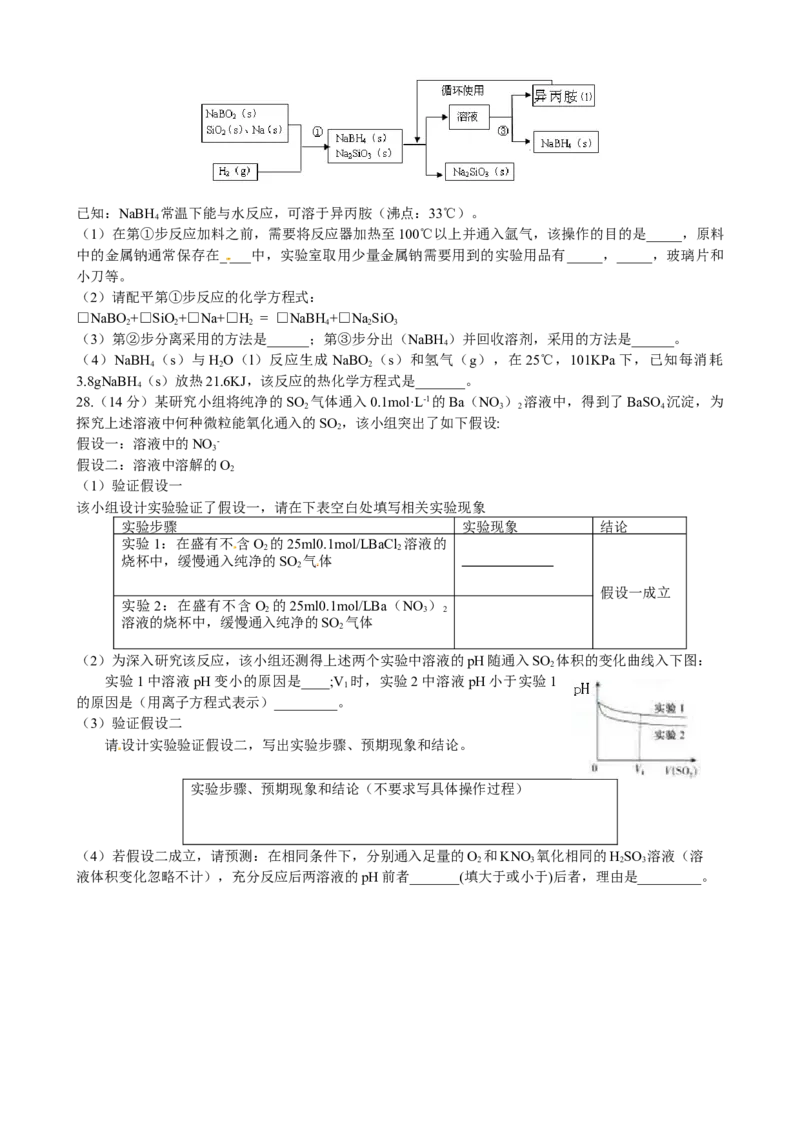
11汽车尾气中NO产生的反应为:N(g)+O(g) 2NO(g),一定条件下,等物质的量的N(g)和O(g)在
2 2 2 2
恒容密闭容器中反应,下图曲线 a表示该反应在温度T下N 的浓度随时间的变化,曲线b表示该反应在
2
某一起始条件改变时N 的浓度随时间的变化。下列叙述正确的是:
2
A.温度T下,该反应的平衡常数K=
B.温度T下,随着反应的进行,混合气体的密度减小
C.曲线b对应的条件改变可能是加入了催化剂
D.若曲线b对应的条件改变是温度,可判断该反应的△H<0
12某同学将光亮的镁条放入盛有NH Cl溶液的试管中,有大量气泡产生。
4
为探究该反应原理,该同学做了以下试验并观察到相关现象,由此得出的结论不合理的是:
选项 实验及现象 结论
A 将湿润的红色石蕊试纸放在试管口,试纸变蓝 反应中有NH 产生
3
B 收集产生的气体并点燃,火焰呈淡蓝色 反应中有H 产生
2
C 收集气体的同时测得溶液的pH为8.0 弱碱性溶液中Mg也可被氧化D 将光亮的镁条放入pH为8.6的NaHCO 溶液中,有气 弱碱性溶液中OH-氧化了Mg
3
泡产生
13 25℃时,在10mL浓度均为0.1mol/LNaOH和NH ·H O混合溶液中,滴加0.1mol/L的盐酸,下列有关
3 2
溶液中粒子浓度关系正确的是:
A.未加盐酸时:c(OH-)>c(Na+)= c(NH ·H O)
3 2
B.加入10mL盐酸时:c(NH +) +c(H+) = c(OH-)
4
C.加入盐酸至溶液pH=7时:c(Cl-) = c(Na+)
D.加入20mL盐酸时:c(Cl-) =c(NH +) +c(Na+)
4
25.(14分)C、N、O、Al、Si、Cu是常见的六种元素。
(1)Si位于元素周期表第____周期第_____族。
(2)N的基态原子核外电子排布式为_____;Cu的基态原子最外层有___个电子。
(3)用“>”或“<”填空:
原子半径 电负性 熔点 沸点
Al_____Si N____O 金刚石_____晶体硅 CH____SiH
4 4
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO 中组成原电池(图1),测得原电池的电流强
3
度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
0-t 时,原电池的负极是Al片,此时,正极的电极反应式是_____,溶液中的H+向___极移动,t 时,原电
1 1
池中电子流动方向发生改变,其原因是______。
26 (15分)四苯基乙烯(TFE)及其衍生物具有聚集诱导发光特性,在光电材料等领域应用前景广阔。以
下是TFE的两条合成路线(部分试剂及反应条件省略):
(1)A的名称是______;试剂Y为_____。
(2)B→C的反应类型为_______;B中官能团的名称是______,D中官能团的名称是______.。
(3)E→F的化学方程式是_______________________。
(4)W是D的同分异构体,具有下列结构特征:①属于萘( )的一元取代物;②存在羟甲基(-
CHOH)。写出W所有可能的结构简式:_____。
2
(5)下列叙述正确的是______。
a.B的酸性比苯酚强 b.D不能发生还原反应
c.E含有3种不同化学环境的氢 d.TPE既属于芳香烃也属于烯烃
27 (14分)硼氢化钠(NaBH )在化工等领域具有重要的应用价值,某研究小组采用偏硼酸钠NaBO 为
4 2
主要原料制备NaBH ,其流程如下:
4已知:NaBH 常温下能与水反应,可溶于异丙胺(沸点:33℃)。
4
(1)在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是_____,原料
中的金属钠通常保存在____中,实验室取用少量金属钠需要用到的实验用品有_____,_____,玻璃片和
小刀等。
(2)请配平第①步反应的化学方程式:
□NaBO +□SiO+□Na+□H = □NaBH +□NaSiO
2 2 2 4 2 3
(3)第②步分离采用的方法是______;第③步分出(NaBH )并回收溶剂,采用的方法是______。
4
(4)NaBH (s)与HO(l)反应生成NaBO (s)和氢气(g),在25℃,101KPa下,已知每消耗
4 2 2
3.8gNaBH (s)放热21.6KJ,该反应的热化学方程式是_______。
4
28.(14分)某研究小组将纯净的SO 气体通入0.1mol·L-1的Ba(NO ) 溶液中,得到了BaSO 沉淀,为
2 3 2 4
探究上述溶液中何种微粒能氧化通入的SO ,该小组突出了如下假设:
2
假设一:溶液中的NO -
3
假设二:溶液中溶解的O
2
(1)验证假设一
该小组设计实验验证了假设一,请在下表空白处填写相关实验现象
实验步骤 实验现象 结论
实验1:在盛有不含O 的25ml0.1mol/LBaCl 溶液的
2 2
烧杯中,缓慢通入纯净的SO 气体
2
假设一成立
实验2:在盛有不含O 的25ml0.1mol/LBa(NO )
2 3 2
溶液的烧杯中,缓慢通入纯净的SO 气体
2
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO 体积的变化曲线入下图:
2
实验1中溶液pH变小的原因是____;V 时,实验2中溶液pH小于实验1
1
的原因是(用离子方程式表示)_________。
(3)验证假设二
请设计实验验证假设二,写出实验步骤、预期现象和结论。
实验步骤、预期现象和结论(不要求写具体操作过程)
(4)若假设二成立,请预测:在相同条件下,分别通入足量的O 和KNO 氧化相同的HSO 溶液(溶
2 3 2 3
液体积变化忽略不计),充分反应后两溶液的pH前者_______(填大于或小于)后者,理由是_________。化学部分参考答案
7 A 8 B 9 C 10 D 11 A 12 D 13 B
25 (14分)(1)三 ⅣA, (2)1s22s22p3 1 (3) > < > <
(4)2H+ + NO -+e-=NO ↑+ HO 正 Al在浓HNO 中发生了钝化,氧化膜阻止了Al的进一步反
3 2 2 3
应
26(16分) (1)甲苯、酸性高锰酸钾溶液
(2)取代反应、羧基、羰基 (3)
(4)
(5)a d
27 (14分)(1)除去反应容器中的水蒸气和空气 煤油 镊子 滤纸
(2)NaBO +2SiO +4Na+2H = NaBH +2Na SiO
2 2 2 4 2 3
(3)过滤 蒸馏
(4)NaBH (s)+2HO(l) = NaBO (s)+4H (g) △H=-216 KJ/mol
4 2 2 2
28(14分)(1)无明显现象、有白色沉淀
(2)SO 溶于水生成HSO 3SO +2NO-+2H O=3SO 2-+ 4H++2NO
2 2 3 2 3 2 4
(或3HSO +2NO-= SO 2-+ 4H++2NO+2HO)
2 3 3 4 2
(3)
实验步骤、预期现象和结论(不要求写具体操作过程)
实验1作为参照实验
实验 3:将纯净的 SO 气体缓慢未经脱氧处理的的 25mL0.1mol/
2
LBaCl 溶液的烧杯中
2
若有白色沉淀,表明假设二成立,否则不成立。
(4)小于,反应的离子方程式表明,足量的O 和NO -分别氧化相同的HSO ,生成H+的物质的量前者
2 3 2 3
多于后者。(本题部分小题属于开放性试题,合理答案均给分)2015年高考安徽理综化学试题解析
7.碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构如下图。下列有关该物质的说法正确的是:
A.分子式为C HO B.分子中含6个σ键
3 2 3
C.分子中只有极性键 D.8.6g该物质完全燃烧得到6.72LCO
2
A
解析:考察有机分子结构和燃烧比例。分子式为 C HO ,有8个σ键, 含有C-C非
3 2 3
极性键,D项未指明标准状况。
8.下列有关实验的选项正确的是:
A.配制0.10mol·L-1 B.除去CO中的 C.苯萃取碘水中 D.记录滴定终点
NaOH溶液 CO I,分出水层后的 读数为12.20mL
2 2
操作
B
解析:考察实验基本操作。A、容量瓶不能用来做溶解容器,故A错误;B、正确;C、下层从下口
流出。上层液体从上口,倒出,故C错误;D、酸式滴定管的0刻度在上方,故读数为:11.80mL,
故D错误。选择B。
9.下列有关说法正确的是:
A.在酒精灯加热条件下,NaCO、NaHCO 固体都能发生分解
2 3 3
B.Fe(OH) 胶体无色、透明,能发生丁达尔现象
3
C.H、SO 、CO 三种气体都可用浓硫酸干燥
2 2 2
D.SiO 既能和氢氧化钠溶液反应又能和氢氟酸反应,所以是两性氧化物
2
C
解析:考察元素及其化合物知识。A、NaCO 固体受热不易分解,故A错误;B、Fe(OH) 胶体是红
2 3 3
褐色,故B错误;C、正确;D、SiO 和氢氟酸反应,没有生成盐和水,故D错误。选择C
2
10.下列有关NaClO和NaCl混合溶液的叙述正确的是:
A.该溶液中,H+、NH +、SO 2-、Br-可以大量共存
4 4
B.该溶液中,Ag+、K+、NO -、CHCHO可以大量共存
3 3
C.向该溶液中滴入少量FeSO 溶液,反应的离子方程式为:
4
2Fe2++ClO-+2H+=== Cl-+2Fe3++H O
2
D.向该溶液中加入浓盐酸,每产生1molCl ,转移电子约为6.02×1023个
2
D解析:考察离子反应。A、ClO-具有强氧化性,在酸性条件下,与Br-不能共存,故A 错误;
B、Ag+与Cl-不能共存,故B错误;C、该溶液中,应该是碱性条件下,故C错误;D、方程式为:
NaClO+2HCl=NaCl+H2O+Cl ↑,生成1molCl ,根据Cl ~e-,转移电子约为6.02×1023个,D正确。
2 2 2
选择D。
11.汽车尾气中,产生NO的反应为:N(g)+O(g) 2NO(g),一定条件下,等物质的量的 N(g)和
2 2 2
O(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N 的浓度随时间的变化,曲线b表
2 2
示该反应在某一起始条件改变时N 的浓度随时间的变化。下列叙述正确的是:
2
A.温度T下,该反应的平衡常数K=
B.温度T下,随着反应的进行,混合气体的密度减小
C.曲线b对应的条件改变可能是加入了催化剂 c a
0
D.若曲线b对应的条件改变是温度,可判断该反应的△H <
0
c a a
1
A
b
解析:考察化学平衡知识。根据平衡常数列式,A正确;温 度
0
t/s
T下,随着反应的进行,混合气体的密度不变;曲线b对应 的
b
条件改变不可能是加入了催化剂,因为改变了平衡状态;随着温度升高,C(N)减小,平衡正向移动,
2
正反应吸热。
12.某同学将光亮的镁条放入盛有NH Cl溶液的试管中,有大量气泡产生。为探究该反应原理,该同学
4
做了以下试验并观察到相关现象,由此得出的结论不合理的是:
选项 实验及现象 结论
A 将湿润的红色石蕊试纸放在试管口,试纸变蓝 反应中有NH 产生
3
B 收集产生的气体并点燃,火焰呈淡蓝色 反应中有H 产生
2
C 收集气体的同事测得溶液的pH为8.0 弱碱性溶液中Mg也可被氧化
D 将光亮的镁条放入 pH 为 8.6 的 NaHCO 溶液 弱碱性溶液中OH-氧化了Mg
3
中,有气泡产生
C
解析:考察实验方案设计。反应为Mg+2NH Cl===MgCl +2NH ↑+H↑;A、检验氨气的方法正确,
4 2 3 2
故A正确;B、火焰成淡蓝色,该气体为H,B正确;C、氯化铵溶
2
液呈酸性,使金属镁氧化,故C错误;D、NaHCO 溶液呈弱碱性,故D正确;选则C。
3
13.25℃时,在10mL浓度均为0.1mol/LNaOH和NH ·H O混合溶液中,滴加0.1mol/L的盐酸,下列有关
3 2
溶液中粒子浓度关系正确的是:
)1-L·lom(/)
N(c
2A.未加盐酸时:c(OH-)>c(Na+)= c(NH ·H O)
3 2
B.加入10mL盐酸时:c(NH +) +c(H+) = c(OH-)
4
C.加入盐酸至溶液pH=7时:c(Cl-) = c(Na+)
D.加入20mL盐酸时: c(Cl-) =c(NH +) +c(Na+)
4
B
解析:考察离子平衡。A、考虑水的电离与 NH ·H O 的电离,未加盐酸时:c(OH-)>c(Na+)>
3 2
c(NH ·H O);B,加入10mL盐酸时,NH ·H O没有反应,NaOH完全反应,质子守恒,c(NH +) +
3 2 3 2 4
c(H+) = c(OH-),正确;加入盐酸至溶液pH=7时,根据电荷守恒,c(Cl-) = c(Na+)+c(NH +);加入
4
20mL盐酸时,完全反应,溶液呈酸性,电荷守恒方程为:c(Cl-) +c(OH-)= c(Na+)+c(NH +)+c(H+)。
4
25.(14分)C、N、O、Al、Si、Cu是常见的六种元素。
(1)Si位于元素周期表第____周期第_____族。
(2)N的基态原子核外电子排布式为_____;Cu的基态原子最外层有___个电子。
(3)用“>”或“<”填空:
原子半径 电负性 熔点 沸点
Al_____Si N____O 金刚石_____晶体 CH____SiH
4 4
硅
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO 中组成原电池(图1),测得原电池的电流强
3
度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
0
t 1 t/s
b
图2
0-t1时,原电池的负极是Al片,此时,正极的电极反应式是_____,溶液中的H+向___极移动,t1
时,原电池中电子流动方向发生改变,其原因是______。
参考答案:
(1)三;ⅣA;
A/I(2)1s22s22p3;1个
(3)>,<,>,<
(4)2H+ + NO --e-=NO + HO,铜极,Al遇浓硝酸钝化。
3 2 2
解析:考察物质结构知识和原电池原理。Si位于元素周期表第三周期ⅢA族;N的基态原子核外电子排
布式为1s22s22p3;Cu的基态原子核外电子排布为:2、8、18、1故最外层有1个电子;同周期,半径
Al>Si,电负性NSi-Si,熔点:金刚石>Si;同主族,相对分子质量
CH