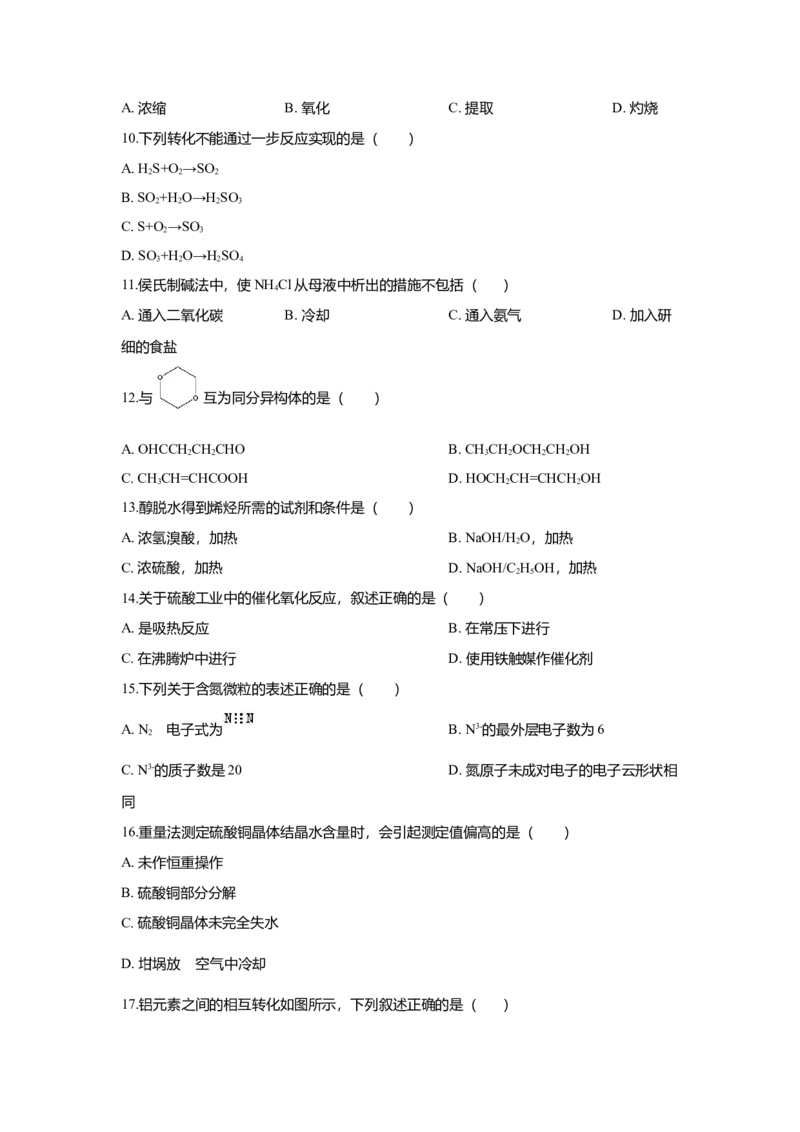文档内容
2018 年上海市普通高中学业水平等级性考试
化学试卷
相对原子质量:C-12 O-16
一、选择题(每题只有一个正确答案,每题2分,共计40分)
1.2018年3月《Nature》杂志上刊登了通过测量行星物质中48Ca/44Ca的比值,揭示了行星
演变的关系。48Ca和44Ca具有( )
A. 相同的质量数 B. 不同的质子数
C. 相同的中子数 D. 相同的电子数
2.我国自主研制的大型客机C919的机身大量使用铝锂合金材料。这是利用了铝锂合金性质
中的( )
.
A 高强度、低密度 B. 高强度、导热性
C. 低密度、导电性 D. 导电性、导热性
3.下列过程中,仅克服分子间作用力的是( )
A. 氯化钾熔融 B. 碳酸钠溶于水 C. 碘升华 D. 晶体硅
熔融
4.下列物质溶于水,溶液温度降低的是( )
A. 浓硫酸 B. NaOH C. NaCl D. NHCl
4
5.有机化学反应一般不具有的特点是( )
A. 反应比较复杂 B. 产率较高
C. 副产物较多 D. 反应速率较慢
6.下列固体中经充分加热分解,无固体残留的是( )
A. NHHCO B. NaHCO C. Al(OH) D. CaCO
4 3 3 3 3
7.下列有关二氧化碳的描述正确的是( )
A. 含有非极性键 B. 是直线形分子
C. 属于极性分子 D. 结构式为C=O=O
8.下列变化说明浓硫酸具有脱水性的是( )
A. 铁遇浓硫酸发生钝化 B. 蔗糖遇浓硫酸变黑
C. 加热时碳与浓硫酸反应 D. 加热时铜与浓硫酸反应
9.海水提溴的过程不包括( )A. 浓缩 B. 氧化 C. 提取 D. 灼烧
10.下列转化不能通过一步反应实现的是( )
A. H S+O→SO
2 2 2
B. SO +H O→H SO
2 2 2 3
C. S+O→SO
2 3
D. SO +H O→H SO
3 2 2 4
11.侯氏制碱法中,使NH Cl从母液中析出的措施不包括( )
4
A. 通入二氧化碳 B. 冷却 C. 通入氨气 D. 加入研
细的食盐
12.与 互为同分异构体的是( )
A. OHCCH CHCHO B. CHCHOCH CHOH
2 2 3 2 2 2
C. CHCH=CHCOOH D. HOCH CH=CHCH OH
3 2 2
13.醇脱水得到烯烃所需的试剂和条件是( )
A. 浓氢溴酸,加热 B. NaOH/H O,加热
2
C. 浓硫酸,加热 D. NaOH/C HOH,加热
2 5
14.关于硫酸工业中的催化氧化反应,叙述正确的是( )
A. 是吸热反应 B. 在常压下进行
C. 在沸腾炉中进行 D. 使用铁触媒作催化剂
15.下列关于含氮微粒的表述正确的是( )
的
A. N 电子式为 B. N3-的最外层电子数为6
2
C. N3-的质子数是20 D. 氮原子未成对电子的电子云形状相
同
16.重量法测定硫酸铜晶体结晶水含量时,会引起测定值偏高的是( )
A. 未作恒重操作
B. 硫酸铜部分分解
C. 硫酸铜晶体未完全失水
在
D. 坩埚放 空气中冷却
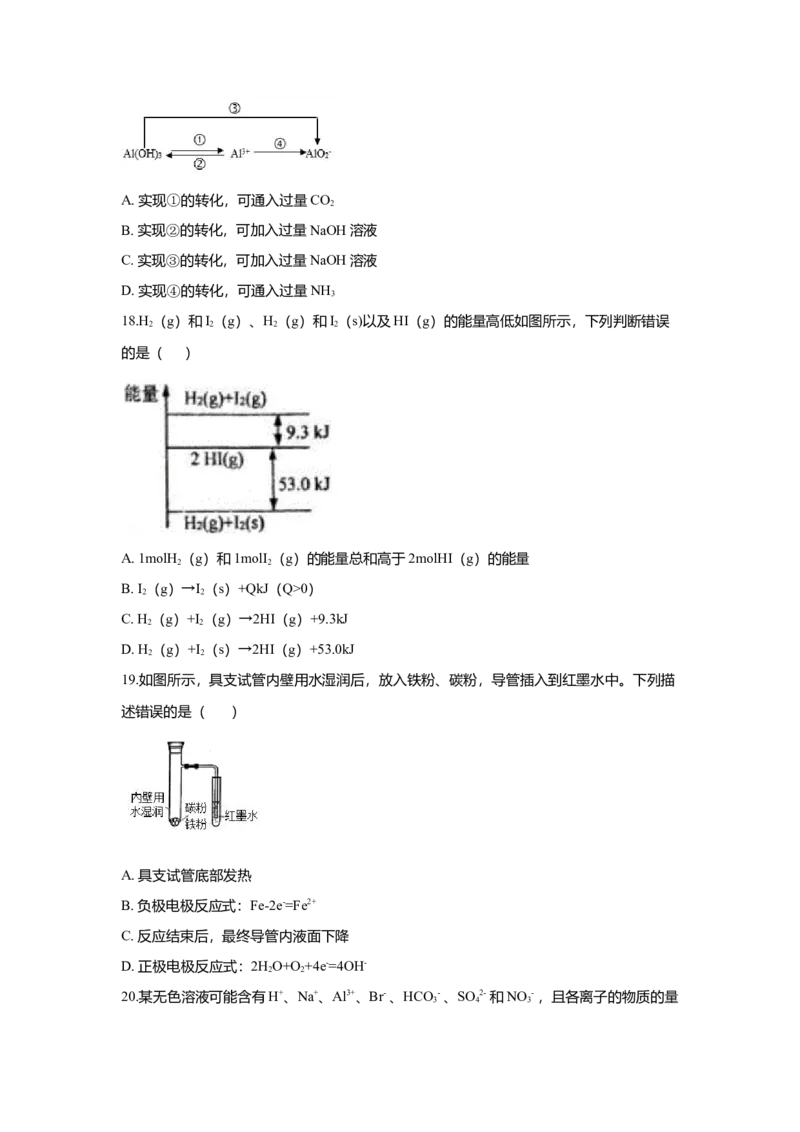
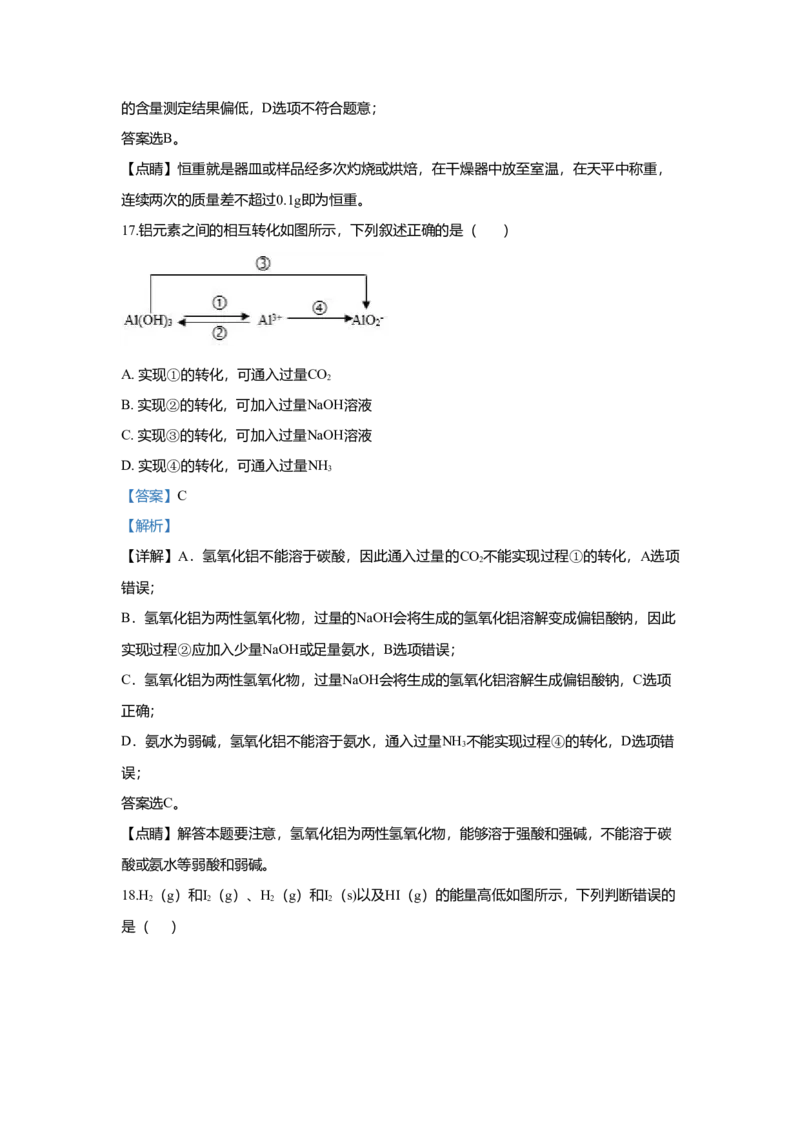
17.铝元素之间的相互转化如图所示,下列叙述正确的是( )A. 实现①的转化,可通入过量CO
2
B. 实现②的转化,可加入过量NaOH溶液
C. 实现③的转化,可加入过量NaOH溶液
D. 实现④的转化,可通入过量NH
3
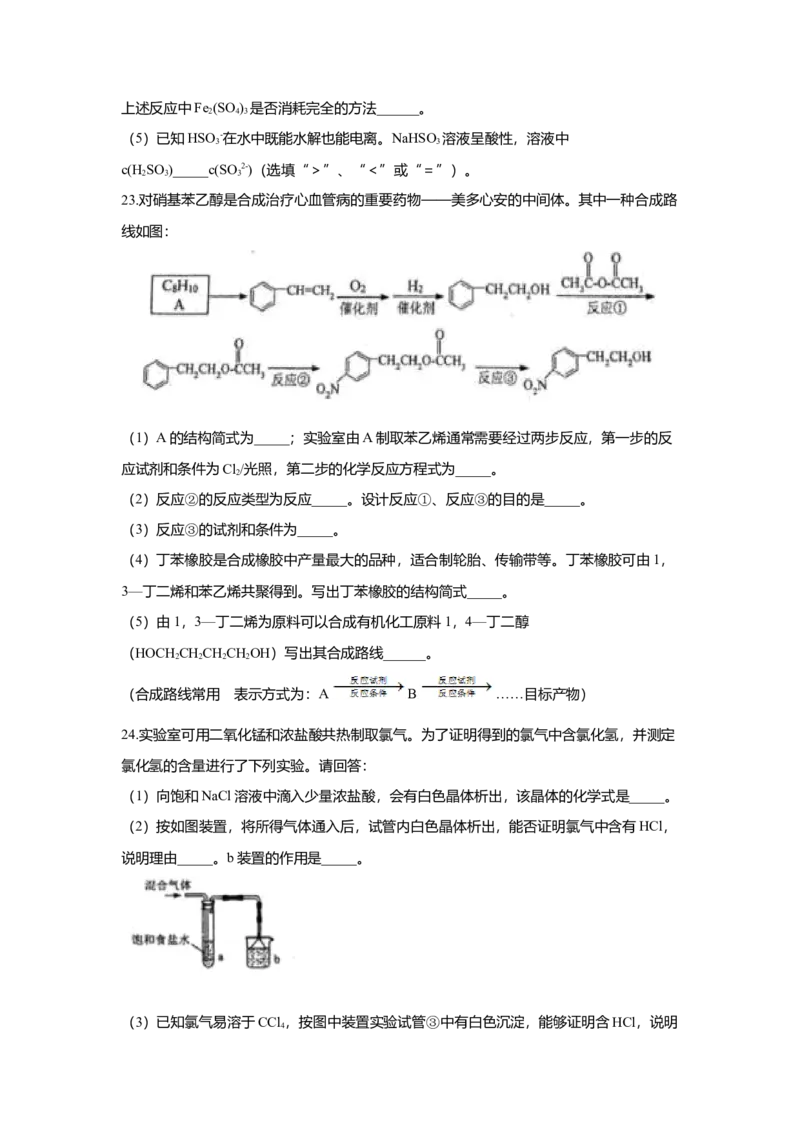
18.H (g)和I(g)、H(g)和I(s)以及HI(g)的能量高低如图所示,下列判断错误
2 2 2 2
的是( )
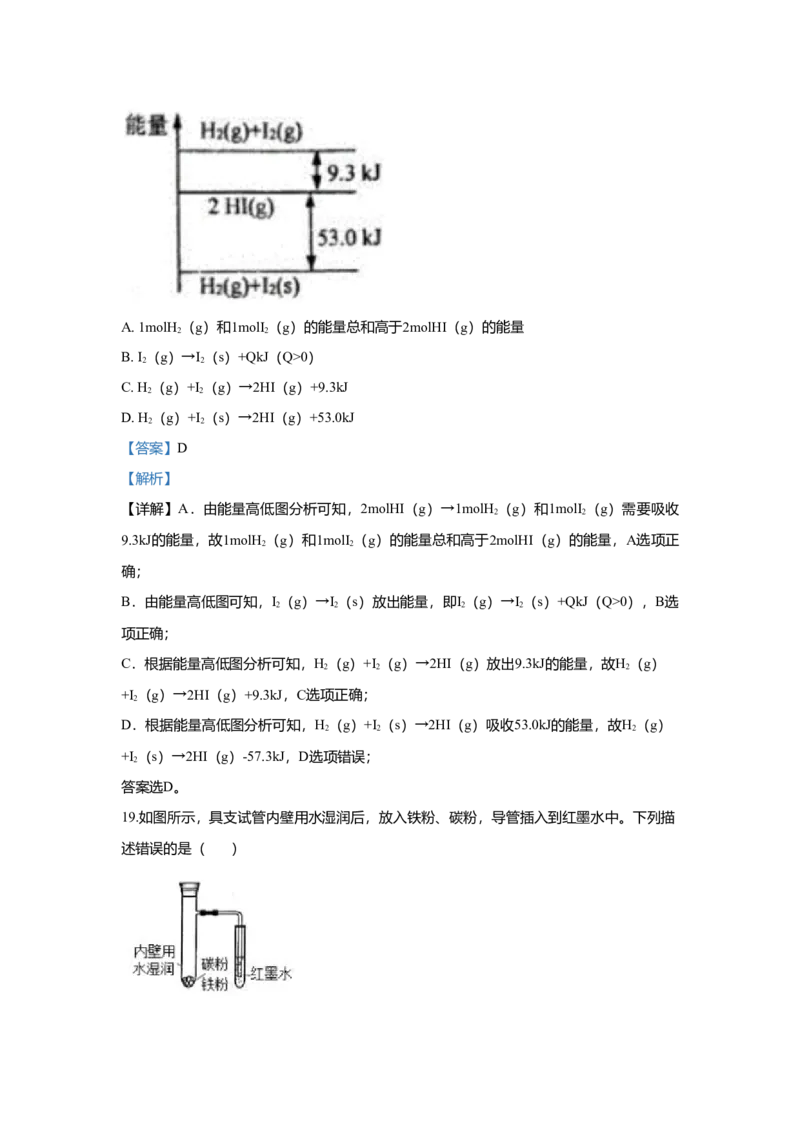
A. 1molH (g)和1molI (g)的能量总和高于2molHI(g)的能量
2 2
B. I (g)→I(s)+QkJ(Q>0)
2 2
C. H(g)+I (g)→2HI(g)+9.3kJ
2 2
D. H (g)+I (s)→2HI(g)+53.0kJ
2 2
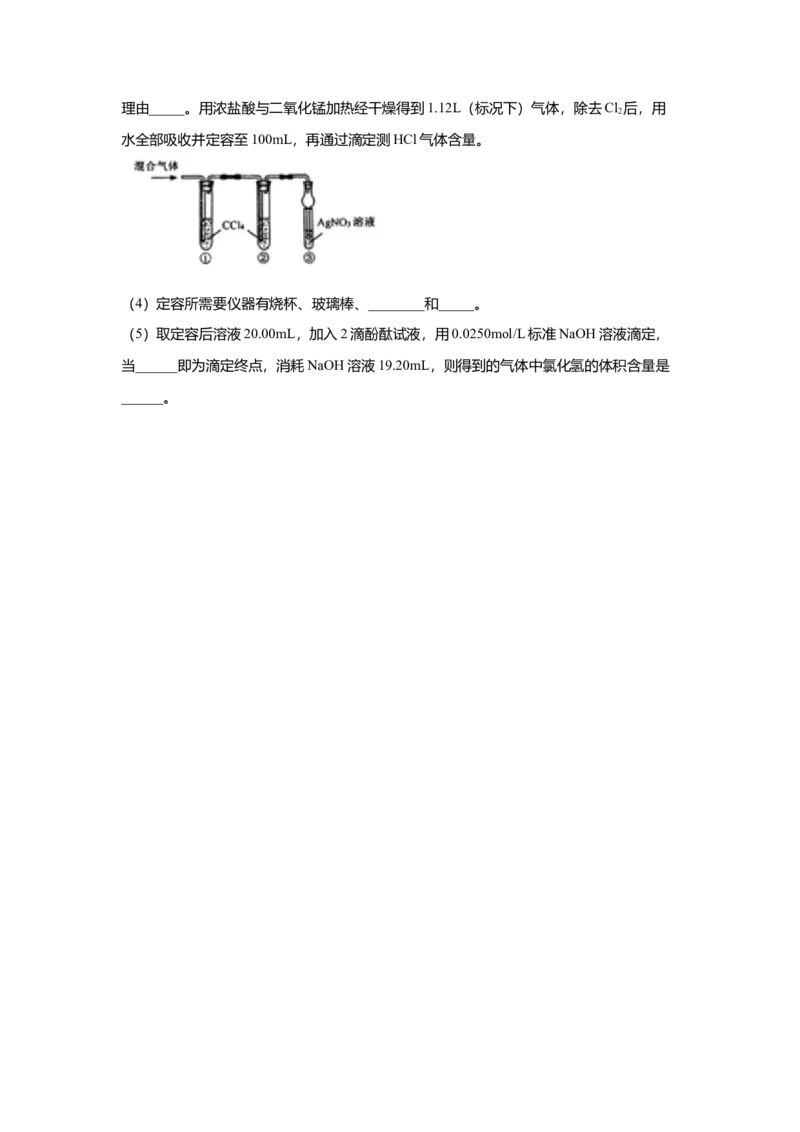
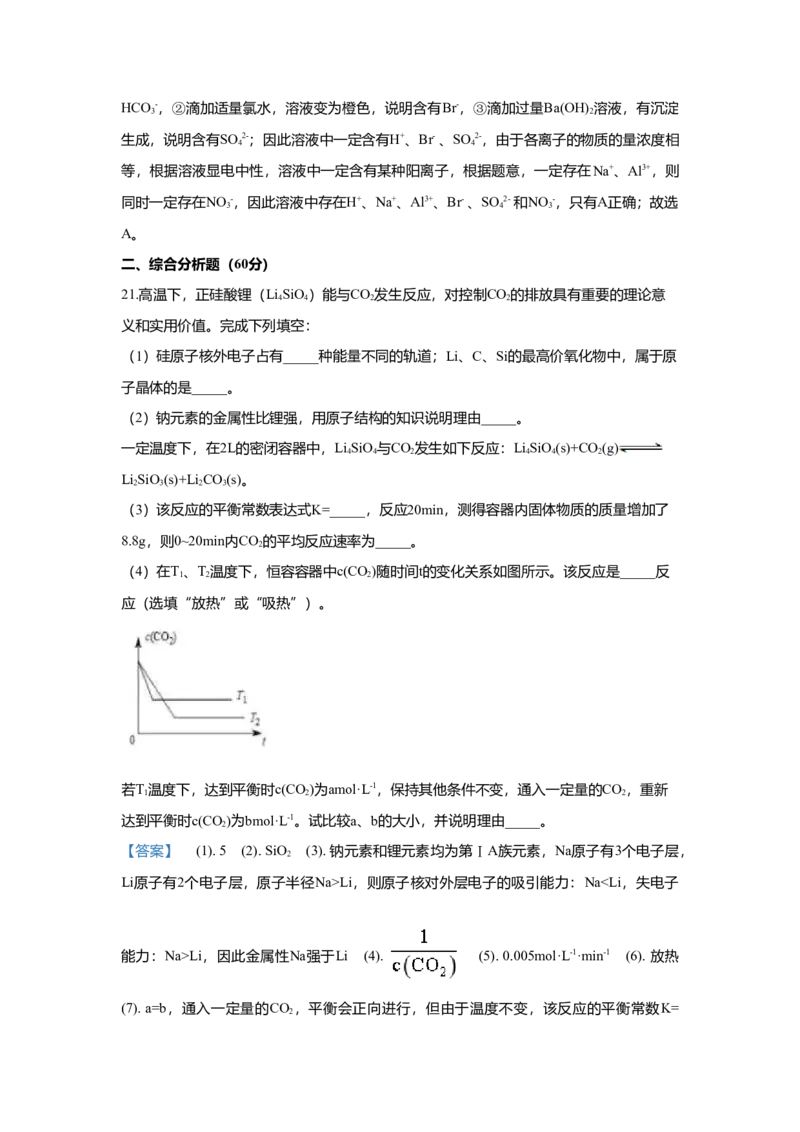
19.如图所示,具支试管内壁用水湿润后,放入铁粉、碳粉,导管插入到红墨水中。下列描
述错误的是( )
A. 具支试管底部发热
B. 负极电极反应式:Fe-2e-=Fe2+
C. 反应结束后,最终导管内液面下降
D. 正极电极反应式:2HO+O+4e-=4OH-
2 2
20.某无色溶液可能含有H+、Na+、Al3+、Br- 、HCO - 、SO 2- 和NO - ,且各离子的物质的量
3 4 3浓度相等。分别取样,①测得该溶液的pH=1;②滴加适量氯水,溶液变为橙色;③滴加过
量Ba(OH) 溶液,有沉淀生成。由此可知原溶液中
2
A. 一定含有NO - B. 可能含有Na+
3
C. 可能不含Al3+ D. 含有3种离子
二、综合分析题(60分)
21.高温下,正硅酸锂(LiSiO)能与CO 发生反应,对控制CO 的排放具有重要的理论意
4 4 2 2
义和实用价值。完成下列填空:
(1)硅原子核外电子占有_____种能量不同的轨道;Li、C、Si的最高价氧化物中,属于
原子晶体的是_____。
(2)钠元素的金属性比锂强,用原子结构的知识说明理由_____。
一定温度下,在2L的密闭容器中,LiSiO 与CO 发生如下反应:LiSiO(s)+CO(g)
4 4 2 4 4 2
LiSiO(s)+Li CO(s)。
2 3 2 3
(3)该反应的平衡常数表达式K=_____,反应20min,测得容器内固体物质的质量增加了
8.8g,则0~20min内CO 的平均反应速率为_____。
2
(4)在T、T 温度下,恒容容器中c(CO)随时间t的变化关系如图所示。该反应是_____
1 2 2
反应(选填“放热”或“吸热”)。
若T 温度下,达到平衡时c(CO)为amol·L-1,保持其他条件不变,通入一定量的CO,重
1 2 2
新达到平衡时c(CO)为bmol·L-1。试比较a、b的大小,并说明理由_____。
2
22.高铁酸盐具有极强的氧化性,可作水处理剂。低温下,在NaFeO 溶液中加入KOH浓
2 4
溶液可析出KFeO。完成下列填空:
2 4
(1)写出上述得到KFeO 的化学方程式_____。
2 4
(2)NaFeO 和稀HSO 发生如下反应:NaFeO+H SO →Fe (SO )+O ↑+Na SO +H O。配
2 4 2 4 2 4 2 4 2 4 3 2 2 4 2
平上述化学方程式_____。若反应中产生3.36L(标准状况)的氧气,则转移电子数为
_____。
(3)实验室配制Fe (SO ) 溶液时,需加入少量稀硫酸,结合离子方程式用化学平衡移动
2 4 3
原理解释其原因______ 。
(4)在Fe (SO ) 溶液中滴加NaHSO 溶液,n(SO 2-)增大,则还原产物是____。写出检验
2 4 3 3 4上述反应中Fe (SO ) 是否消耗完全的方法______。
2 4 3
(5)已知HSO -在水中既能水解也能电离。NaHSO 溶液呈酸性,溶液中
3 3
c(HSO )_____c(SO 2-)(选填“>”、“<”或“=”)。
2 3 3
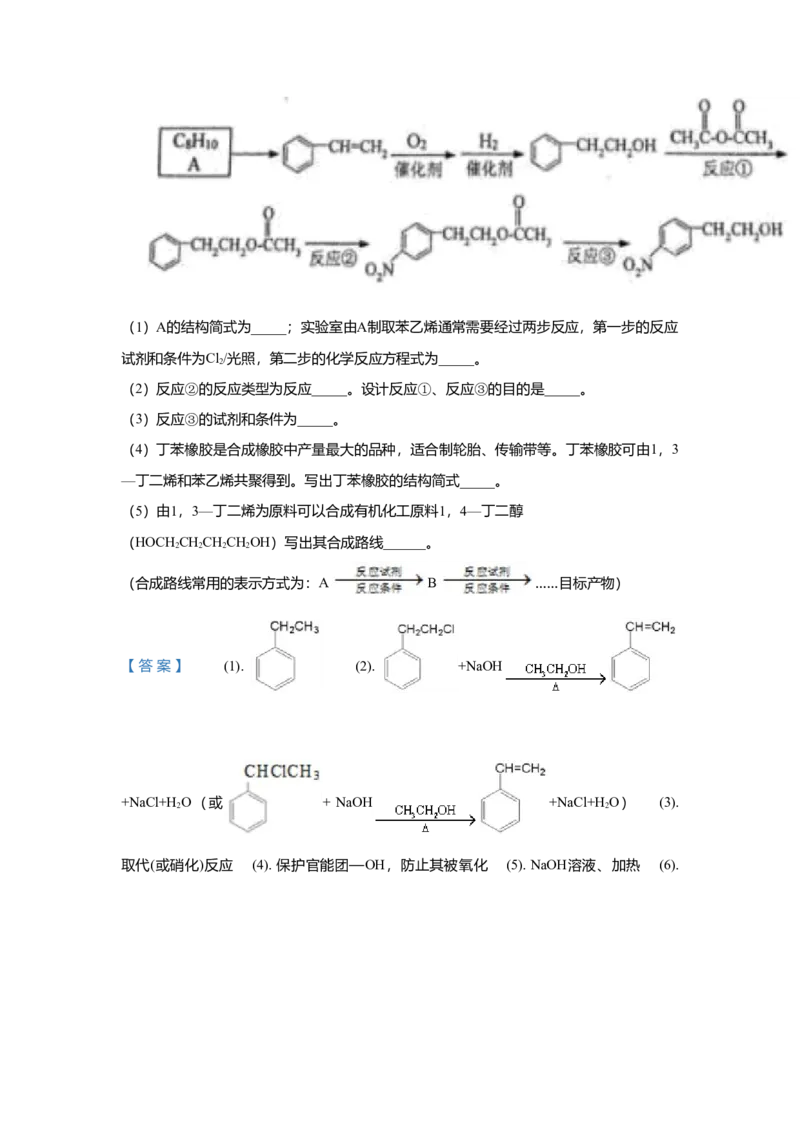
23.对硝基苯乙醇是合成治疗心血管病的重要药物——美多心安的中间体。其中一种合成路
线如图:
(1)A的结构简式为_____;实验室由A制取苯乙烯通常需要经过两步反应,第一步的反
应试剂和条件为Cl/光照,第二步的化学反应方程式为_____。
2
(2)反应②的反应类型为反应_____。设计反应①、反应③的目的是_____。
(3)反应③的试剂和条件为_____。
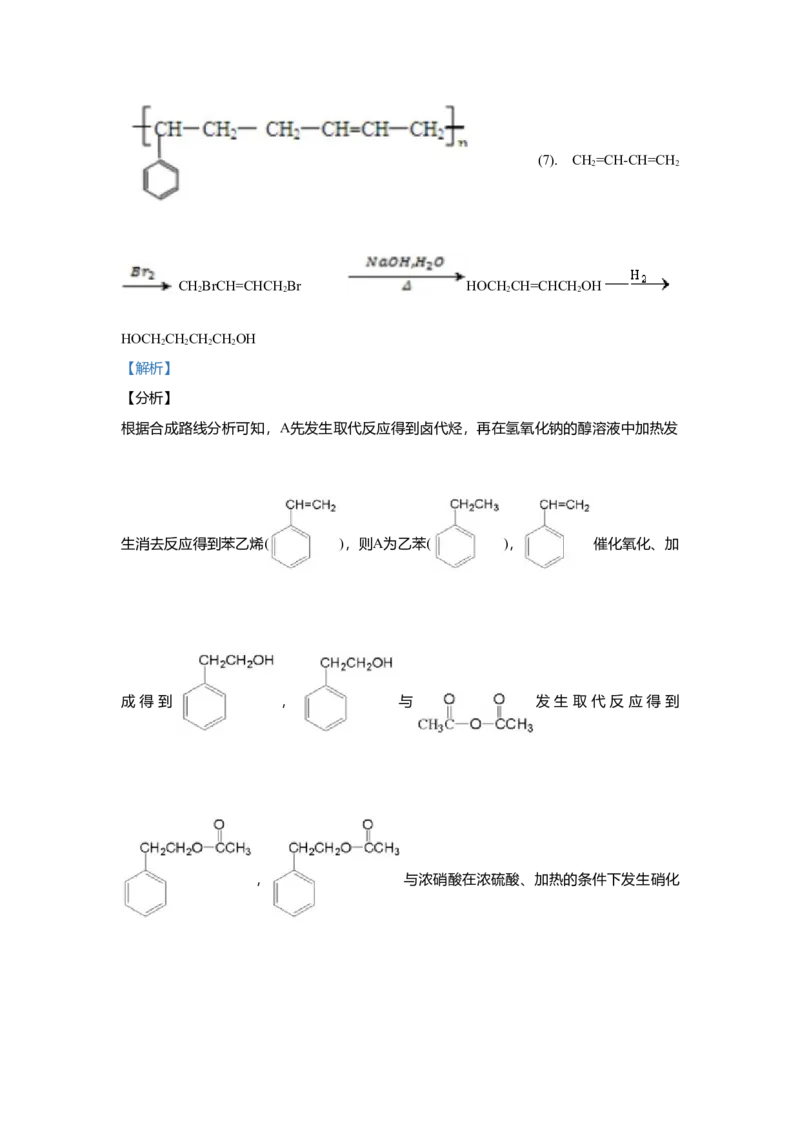
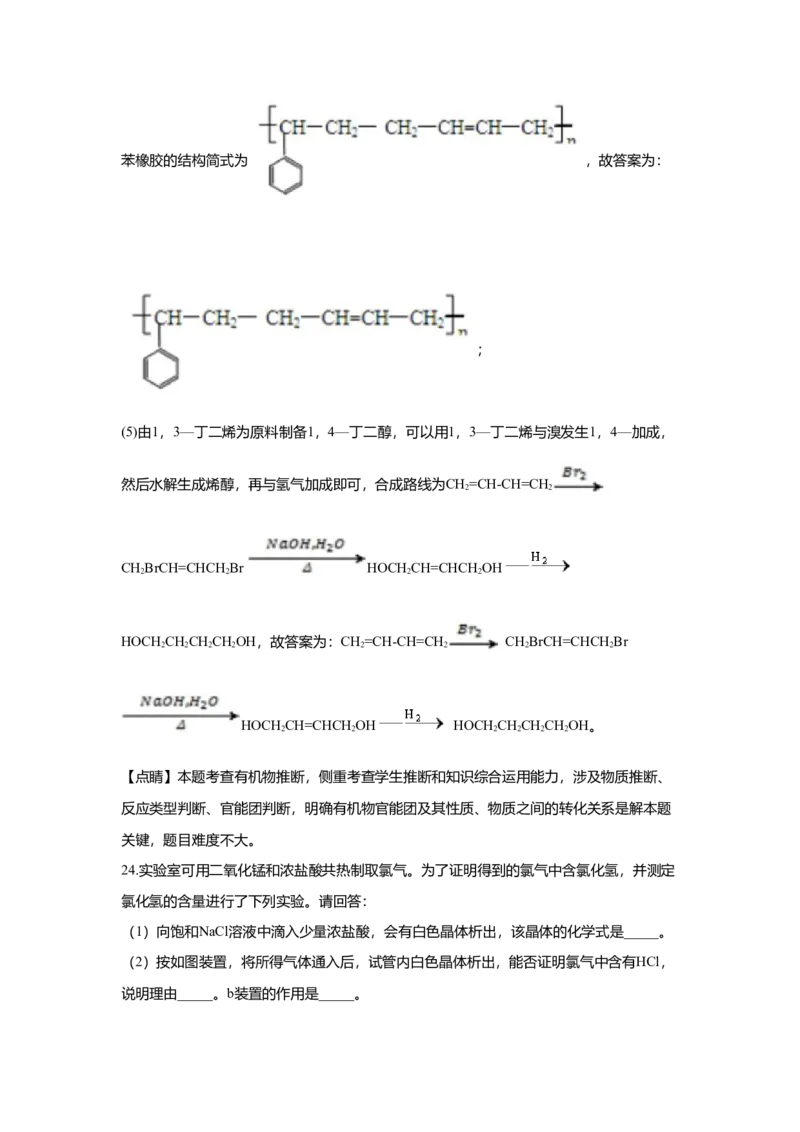
(4)丁苯橡胶是合成橡胶中产量最大的品种,适合制轮胎、传输带等。丁苯橡胶可由1,
3—丁二烯和苯乙烯共聚得到。写出丁苯橡胶的结构简式_____。
(5)由1,3—丁二烯为原料可以合成有机化工原料1,4—丁二醇
(HOCH CHCHCHOH)写出其合成路线______。
2 2 2 2
(合成路线常用 的 表示方式为:A B ……目标产物)
24.实验室可用二氧化锰和浓盐酸共热制取氯气。为了证明得到的氯气中含氯化氢,并测定
氯化氢的含量进行了下列实验。请回答:
(1)向饱和NaCl溶液中滴入少量浓盐酸,会有白色晶体析出,该晶体的化学式是_____。
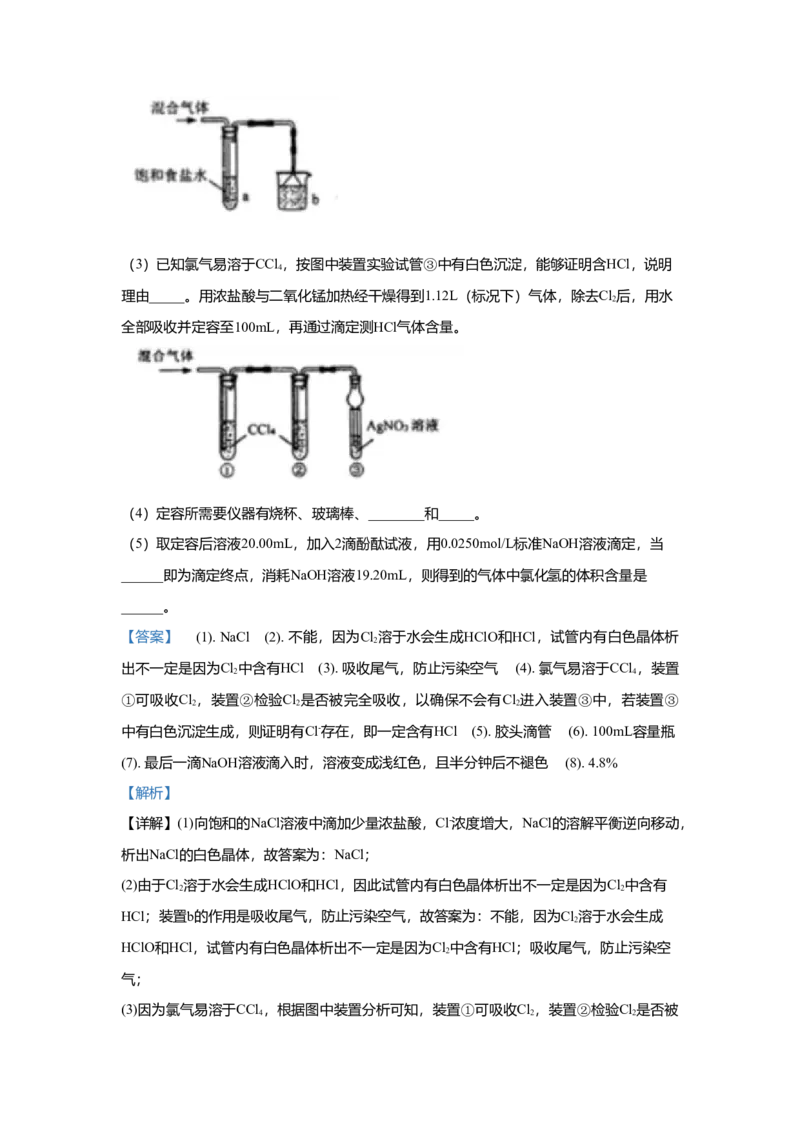
(2)按如图装置,将所得气体通入后,试管内白色晶体析出,能否证明氯气中含有HCl,
说明理由_____。b装置的作用是_____。
(3)已知氯气易溶于CCl ,按图中装置实验试管③中有白色沉淀,能够证明含HCl,说明
4理由_____。用浓盐酸与二氧化锰加热经干燥得到1.12L(标况下)气体,除去Cl 后,用
2
水全部吸收并定容至100mL,再通过滴定测HCl气体含量。
(4)定容所需要仪器有烧杯、玻璃棒、________和_____。
(5)取定容后溶液20.00mL,加入2滴酚酞试液,用0.0250mol/L标准NaOH溶液滴定,
当______即为滴定终点,消耗NaOH溶液19.20mL,则得到的气体中氯化氢的体积含量是
______。2018年上海市高中化学等级考试卷
答案解析版
相对原子质量:C-12 O-16
一、选择题(每题只有一个正确答案,每题2分,共计40分)
1.2018年3月《Nature》杂志上刊登了通过测量行星物质中48Ca/44Ca的比值,揭示了行星演
变的关系。48Ca和44Ca具有( )
A. 相同的质量数 B. 不同的质子数
C. 相同的中子数 D. 相同的电子数
【答案】D
【解析】
【分析】
原子符号的左上角数字是质量数,原子序数=质子数=核电荷数=原子核外电子数,质量数=
质子数+中子数,据此分析解答。
【详解】A.48Ca和44Ca的质量数分别为48、44,质量数不相同,A选项错误;
B.48Ca和44Ca为Ca 同位素,Ca是20号元素,故48Ca和44Ca质子数均为20,质子数相同,
B选项错误;
C.质量数=质子数+中子数,则48Ca和44Ca的中子数分别为28、24,中子数不同,C选项错
误;
D.原子核外电子数=质子数,故48Ca和44Ca的电子数均为20,电子数相同,D选项正确;
答案选D。
2.我国自主研制的大型客机C919的机身大量使用铝锂合金材料。这是利用了铝锂合金性质
中的( )
A. 高强度、低密度 B. 高强度、导热性
C. 低密度、导电性 D. 导电性、导热性
【答案】A
【解析】
【详解】铝锂合金的密度较小,强度较大,能够实现飞机减重的目标,因此使用铝锂合金
是利用铝锂合金的高强度、低密度的特点;答案选A。
3.下列过程中,仅克服分子间作用力的是( )
A. 氯化钾熔融 B. 碳酸钠溶于水 C. 碘升华 D. 晶体硅熔融
【答案】C
【解析】
【详解】A.KCl是离子化合物,KCl熔融时需要克服离子键的作用,A选项不满足题意;
B.碳酸钠是离子化合物,碳酸钠溶于水时需要克服离子键的作用,B选项不满足题意;
C.碘单质属于分子晶体,碘单质升华是物理变化,碘升华仅克服分子间的作用力,C选项
满足题意;
D.晶体硅属于原子晶体,晶体硅熔融破坏的是共价键,D选项不满足题意;
答案选C。
【点睛】本题考查化合物的类型和微粒间作用力的判断,题目难度不大,在解答时需要注
意物质发生变化时粒子间作用力的变化。
4.下列物质溶于水,溶液温度降低的是( )
A. 浓硫酸 B. NaOHC. NaCl D. NHCl
4
【答案】D
【解析】
【详解】A.浓硫酸溶于水中稀释放出大量的热,溶液温度升高,A选项不满足题意;
B.NaOH溶于水的过程是放热过程,溶液温度升高,B选项不满足题意;
C.NaCl溶于水溶液温度无明显变化,C选项不满足题意;
D.NH Cl溶于水,溶液温度降低,D选项满足题意;
4
答案选D。
5.有机化学反应一般不具有的特点是( )
A. 反应比较复杂 B. 产率较高
C. 副产物较多 D. 反应速率较慢
【答案】B
【解析】
【详解】有机物的化学反应比较复杂,一般较慢,且常伴有副反应的发生,导致产率不高
故B选项满足题意;
答案选B。
6.下列固体中经充分加热分解,无固体残留的是( )A. NHHCO B. NaHCO C. Al(OH) D. CaCO
4 3 3 3 3
【答案】A
【解析】
【详解】A.NH HCO 受热分解后生成氨气、水和二氧化碳,无固体残留,A选项符合题
4 3
意;
B.NaHCO 受热分解后生成碳酸钠、水和二氧化碳,有碳酸铵固体残留,B选项不符合题
3
意;
C.Al(OH) 受热分解后生成氧化铝和水,有氧化铝固体残留,C选项不符合题意;
3
D.CaCO 受热分解后生成氧化钙和二氧化碳,有氧化钙固体残留,D选项不符合题意;
3
答案选A。
7.下列有关二氧化碳的描述正确的是( )
A. 含有非极性键 B. 是直线形分子
C. 属于极性分子 D. 结构式为C=O=O
【答案】B
【解析】
【详解】A.二氧化碳分子中碳原子和氧原子形成极性共价键,不含有非极性共价键,A选
项错误;
B.二氧化碳分子中中心原子的价层电子对数为 ,不含有孤对电子,为sp
杂化,空间构型为直线形,是直线形分子,B选项正确;
C.二氧化碳为直线形分子,二氧化碳分子是对称结构,正负电中心重合,是非极性分子,
C选项错误;
D.二氧化碳分子的中心原子是C,故其结构简式应为O=C=O,D选项错误;
答案选B。
【点睛】C选项,根据分子中电荷是否分布均匀来判断分子的极性,若分子的电荷分布均
匀、正负电中心重合,则该分子是非极性分子,若分子的电荷分布不均匀、正负电中心不
重合,则该分子是极性分子。
8.下列变化说明浓硫酸具有脱水性的是( )
A. 铁遇浓硫酸发生钝化 B. 蔗糖遇浓硫酸变黑
C. 加热时碳与浓硫酸反应 D. 加热时铜与浓硫酸反应【答案】B
【解析】
【详解】A.铁遇浓硫酸发生钝化是因为浓硫酸具有强氧化性,A选项不符合题意;
B.蔗糖遇浓硫酸变黑是因为浓硫酸具有脱水性,将蔗糖中的H元素和O元素按照水分子的
比例(H:O=2:1)脱出来,剩下黑色的碳单质,B选项符合题意;
C.加热时碳与浓硫酸反应 因为浓硫酸具有强氧化性,可将碳单质氧化成二氧化碳,而
自身被还原为二氧化硫,C选项不符合题意;
D.加热时铜与浓硫酸反应是因为浓硫酸具有强氧化性,可将Cu单质氧化成Cu2+,而自身
被还原为二氧化硫,在此反应中硫酸还会表现酸性,D选项不符合题意;
答案选B。
9.海水提溴的过程不包括( )
A. 浓缩 B. 氧化 C. 提取 D. 灼烧
【答案】D
【解析】
【详解】海水中溴离子含量较低,应先浓缩,再将溴离子转化为溴需要加入氧化剂,通常
选择氯气氧化溴离子得到单质溴:2Br-+Cl=Br +2Cl-,再利用溴的挥发性,鼓入热空气或热
2 2
水蒸气将溴分离出来,二氧化硫与溴反应富集后,再利用氯气将HBr氧化成溴,最后蒸馏
(或萃取分液)提取获得Br ,过程中不包含灼烧,
2
答案选D。
10.下列转化不能通过一步反应实现的是( )
A. H S+O→SO
2 2 2
B. SO +H O→H SO
2 2 2 3
C. S+O→SO
2 3
D. SO +H O→H SO
3 2 2 4
【答案】C
【解析】
【详解】A.HS和O 发生氧化还原反应生成SO 和HO,能够一步反应实现转化,A选项不
2 2 2 2
满足题意;
B.常温下,SO 与HO直接反应生成HSO ,能够一步反应实现转化,B选项不满足题意;
2 2 2 3
C.S在氧气中燃烧生成SO ,SO 在催化剂存在的条件下进一步氧化生成SO ,所以不能通
2 2 3过一步反应实现转化,C选项满足题意;
D.SO 可与HO反应直接生成HSO ,能够一步反应实现转化,D选项不满足题意;
3 2 2 4
答案选C。
11.侯氏制碱法中,使NH Cl从母液中析出的措施不包括( )
4
A. 通入二氧化碳 B. 冷却 C. 通入氨气 D. 加入研细的食盐
【答案】A
【解析】
【分析】
母液中含氯化铵和饱和碳酸氢钠,要析出NH Cl,则溶液应该达到饱和,饱和NH Cl溶液中
4 4
存在溶解平衡:NH Cl(s) NH +(aq)+Cl-(aq),若要析出氯化铵,应该使平衡逆向移动。
4 4
【详解】A.通入二氧化⇌碳后,对铵根离子和氯离子没有影响,对母液中析出NH Cl无帮助,
4
A选项满足题意;
B.冷却母液,氯化铵的溶解度降低,有利于氯化铵的析出,B选项不满足题意;
C.通入氨气将碳酸氢钠转化为溶解度更大的碳酸钠,同时溶液中铵根离子浓度增大,平
衡逆向移动,有利于氯化铵的析出,C选项不满足题意;
D.加入食盐,溶液中氯离子浓度增大,平衡逆向移动,有利于氯化铵的析出,D选项不满
足题意;
答案选A。
12.与 互为同分异构体的是( )
A. OHCCH CHCHO B. CHCHOCH CHOH
2 2 3 2 2 2
C. CHCH=CHCOOH D. HOCH CH=CHCH OH
3 2 2
【答案】D
【解析】
【分析】
分子式相同,结构不同的化合物互为同分异构体, 的分子式为C HO,据此分析
4 8 2
解答问题。
【详解】A.OHCCH CHCHO的分子式为C HO,与 的分子式不同,A选项不符
2 2 4 6 2合题意;
B.CHCHOCH CHOH的分子式为C H O,与 的分子式不同,B选项不符合题
3 2 2 2 4 10 2
意;
C.CHCH=CHCOOH的分子式为C HO,与 的分子式不同,C选项不符合题意;
3 4 6 2
D.HOCH CH=CHCH OH的分子式为C HO,与 的分子式相同,且结构不同,
2 2 4 8 2
是 的同分异构体,D选项符合题意;
答案选D。
13.醇脱水得到烯烃所需的试剂和条件是( )
A. 浓氢溴酸,加热 B. NaOH/H O,加热
2
C. 浓硫酸,加热 D. NaOH/C HOH,加热
2 5
【答案】C
【解析】
【详解】A.醇与浓氢溴酸加热发生取代反应,生成溴代烃,A不选;
B.NaOH/H O,加热的条件下醇不发生脱水反应得到烯烃,B不选;
2
C.醇在浓硫酸作催化剂、加热的条件下,发生消去反应脱水得到烯烃,C选;
D.NaOH/C HOH,加热的条件下醇不能脱水得到烯烃,D不选;
2 5
答案选C。
14.关于硫酸工业中的催化氧化反应,叙述正确的是( )
A. 是吸热反应 B. 在常压下进行
C. 在沸腾炉中进行 D. 使用铁触媒作催化剂
【答案】B
【解析】
【详解】A.硫酸工业中的催化氧化反应是放热反应,A选项错误;
B.硫酸工业中的催化氧化反应选择在常压下进行,B选项正确;
C.硫酸工业中的催化氧化反应是在接触室中发生反应,C选项错误;D.硫酸工业中的催化氧化反应使用VO作催化剂,D选项错误;
2 5
答案选B。
15.下列关于含氮微粒的表述正确的是( )
A. N 的电子式为 B. N3-的最外层电子数为6
2
C. N3-的质子数是20 D. 氮原子未成对电子的电子云形状相同
【答案】D
【解析】
【详解】A.N分子中N原子之间形成三对共用电子对,每个氮原子还剩一对孤对电子,其
2
电子式为: ,A选项错误;
B.N原子得到3个电子形成N3-,其最外层电子数为8,B选项错误;
C.质子数=原子序数=核电荷数,N3-的质子数为7,C选项错误;
D.N原子中未成对电子处于2p轨道,p轨道 电子云形状都为哑铃形,D选项正确;
答案选D。
【点睛】本题考查含氮微粒的结构,注意掌握常见化学用语的概念及表示方法,掌握原子
和离子的相互转化、常见原子的质子数是解答本题的关键。
16.重量法测定硫酸铜晶体结晶水含量时,会引起测定值偏高的是( )
A. 未作恒重操作
B. 硫酸铜部分分解
C. 硫酸铜晶体未完全失水
D. 坩埚放在空气中冷却
【答案】B
【解析】
【详解】A.未作恒重操作可能会导致结晶水的含量偏低,A选项不符合题意;
B.硫酸铜部分分解,称量前后的质量差变大,导致结晶水的含量测定结果偏高,B选项符
合题意;
C.硫酸铜晶体未完全失水,将导致前后的质量差变小,结晶水的含量测定结果偏低,C选
项不符合题意;
D.在空气中冷却,硫酸铜又吸收空气中的水蒸气,导致加热前后的质量差变小,结晶水的含量测定结果偏低,D选项不符合题意;
答案选B。
【点睛】恒重就是器皿或样品经多次灼烧或烘焙,在干燥器中放至室温,在天平中称重,
连续两次的质量差不超过0.1g即为恒重。
17.铝元素之间的相互转化如图所示,下列叙述正确的是( )
A. 实现①的转化,可通入过量CO
2
B. 实现②的转化,可加入过量NaOH溶液
C. 实现③的转化,可加入过量NaOH溶液
D. 实现④的转化,可通入过量NH
3
【答案】C
【解析】
【详解】A.氢氧化铝不能溶于碳酸,因此通入过量的CO 不能实现过程①的转化,A选项
2
错误;
B.氢氧化铝为两性氢氧化物,过量的NaOH会将生成的氢氧化铝溶解变成偏铝酸钠,因此
实现过程②应加入少量NaOH或足量氨水,B选项错误;
C.氢氧化铝为两性氢氧化物,过量NaOH会将生成的氢氧化铝溶解生成偏铝酸钠,C选项
正确;
D.氨水为弱碱,氢氧化铝不能溶于氨水,通入过量NH 不能实现过程④的转化,D选项错
3
误;
答案选C。
【点睛】解答本题要注意,氢氧化铝为两性氢氧化物,能够溶于强酸和强碱,不能溶于碳
酸或氨水等弱酸和弱碱。
18.H (g)和I(g)、H(g)和I(s)以及HI(g)的能量高低如图所示,下列判断错误的
2 2 2 2
是( )A. 1molH (g)和1molI (g)的能量总和高于2molHI(g)的能量
2 2
B. I (g)→I(s)+QkJ(Q>0)
2 2
C. H(g)+I (g)→2HI(g)+9.3kJ
2 2
D. H (g)+I (s)→2HI(g)+53.0kJ
2 2
【答案】D
【解析】
【详解】A.由能量高低图分析可知,2molHI(g)→1molH (g)和1molI (g)需要吸收
2 2
9.3kJ的能量,故1molH (g)和1molI (g)的能量总和高于2molHI(g)的能量,A选项正
2 2
确;
B.由能量高低图可知,I(g)→I(s)放出能量,即I(g)→I(s)+QkJ(Q>0),B选
2 2 2 2
项正确;
C.根据能量高低图分析可知,H(g)+I (g)→2HI(g)放出9.3kJ的能量,故H(g)
2 2 2
+I (g)→2HI(g)+9.3kJ,C选项正确;
2
D.根据能量高低图分析可知,H(g)+I (s)→2HI(g)吸收53.0kJ的能量,故H(g)
2 2 2
+I (s)→2HI(g)-57.3kJ,D选项错误;
2
答案选D。
19.如图所示,具支试管内壁用水湿润后,放入铁粉、碳粉,导管插入到红墨水中。下列描
述错误的是( )A. 具支试管底部发热
B. 负极电极反应式:Fe-2e-=Fe2+
C. 反应结束后,最终导管内液面下降
D. 正极电极反应式:2HO+O+4e-=4OH-
2 2
【答案】C
【解析】
【分析】
由题干信息分析可知,该装置中Fe和C形成原电池发生吸氧腐蚀,Fe作负极失去电子,电
极反应式为:Fe-2e-=Fe2+,C作正极,O 在正极得到电子,电极反应式为2HO+O+4e-
2 2 2
=4OH-,据此分析解答问题。
【详解】A.Fe发生吸氧腐蚀,是放热反应,因此具支试管底部会发热,A选项正确;
B.由上述分析可知,Fe作负极失去电子,电极反应式为:Fe-2e-=Fe2+,B选项正确;
C.具支试管中氧气被消耗,压强减小,与外界压强形成气压差,则导管内液面会上升,C
选项错误;
D.根据上述分析,C作正极,O在正极得到电子,电极反应式为2HO+O+4e-=4OH-,D选
2 2 2
项正确;
答案选C。
20.某无色溶液可能含有H+、Na+、Al3+、Br- 、HCO - 、SO 2- 和NO - ,且各离子的物质的量
3 4 3
浓度相等。分别取样,①测得该溶液的pH=1;②滴加适量氯水,溶液变为橙色;③滴加过
量Ba(OH) 溶液,有沉淀生成。由此可知原溶液中
2
A. 一定含有NO - B. 可能含有Na+
3
C. 可能不含Al3+ D. 含有3种离子
【答案】A
【解析】
【分析】
某无色溶液可能含有H+、Na+、Al3+、Br- 、HCO - 、SO 2- 和NO - ,且各离子的物质的量浓
3 4 3
度相等。分别取样,①测得该溶液的pH=1,说明溶液显强酸性,溶液中一定含有H+,一定
不存在HCO -,②滴加适量氯水,溶液变为橙色,说明含有Br-,③滴加过量Ba(OH) 溶液,
3 2
有沉淀生成,说明含有SO 2-。结合各离子的物质的量浓度相等分析解答。
4
【详解】①测得该溶液的pH=1,说明溶液显强酸性,溶液中一定含有H+,一定不存在HCO -,②滴加适量氯水,溶液变为橙色,说明含有Br-,③滴加过量Ba(OH) 溶液,有沉淀
3 2
生成,说明含有SO 2-;因此溶液中一定含有H+、Br- 、SO 2-,由于各离子的物质的量浓度相
4 4
等,根据溶液显电中性,溶液中一定含有某种阳离子,根据题意,一定存在Na+、Al3+,则
同时一定存在NO -,因此溶液中存在H+、Na+、Al3+、Br- 、SO 2- 和NO -,只有A正确;故选
3 4 3
A。
二、综合分析题(60分)
21.高温下,正硅酸锂(LiSiO)能与CO发生反应,对控制CO的排放具有重要的理论意
4 4 2 2
义和实用价值。完成下列填空:
(1)硅原子核外电子占有_____种能量不同的轨道;Li、C、Si的最高价氧化物中,属于原
子晶体的是_____。
(2)钠元素的金属性比锂强,用原子结构的知识说明理由_____。
一定温度下,在2L的密闭容器中,LiSiO与CO发生如下反应:LiSiO(s)+CO(g)
4 4 2 4 4 2
LiSiO(s)+Li CO(s)。
2 3 2 3
(3)该反应的平衡常数表达式K=_____,反应20min,测得容器内固体物质的质量增加了
8.8g,则0~20min内CO的平均反应速率为_____。
2
(4)在T、T温度下,恒容容器中c(CO)随时间t的变化关系如图所示。该反应是_____反
1 2 2
应(选填“放热”或“吸热”)。
若T温度下,达到平衡时c(CO)为amol·L-1,保持其他条件不变,通入一定量的CO,重新
1 2 2
达到平衡时c(CO)为bmol·L-1。试比较a、b的大小,并说明理由_____。
2
【答案】 (1). 5 (2). SiO (3). 钠元素和锂元素均为第ⅠA族元素,Na原子有3个电子层,
2
Li原子有2个电子层,原子半径Na>Li,则原子核对外层电子的吸引能力:NaLi,因此金属性Na强于Li (4). (5). 0.005mol·L-1·min-1 (6). 放热
(7). a=b,通入一定量的CO ,平衡会正向进行,但由于温度不变,该反应的平衡常数K=
2不变,故达到新平衡时c(CO)不变,即a=b
2
【解析】
【详解】(1)硅是14号元素,基态硅原子的核外电子排布式为1s22s22p63s23p2,其核外电子共
占有5种能量不同的轨道;Li、C、Si的最高价氧化物分别为LiO、CO 、SiO ,LiO是离子
2 2 2 2
晶体、CO是分子晶体、SiO是原子晶体,故答案为:5;SiO;
2 2 2
(2) 钠元素的金属性比锂强,从原子结构解释:钠元素和锂元素均为第ⅠA族元素,Na原子
有3个电子层,Li原子有2个电子层,原子半径Na>Li,则原子核对外层电子的吸引能力:
NaLi,因此金属性Na强于Li,故答案为:钠元素和锂元素均为第
ⅠA族元素,Na原子有3个电子层,Li原子有2个电子层,原子半径Na>Li,则原子核对外层
电子的吸引能力:NaLi,因此金属性Na强于Li;
(3)平衡常数等于生成物的平衡浓度幂之积除以反应物的平衡浓度幂之积,根据化学反应方
程式LiSiO(s)+CO(g) LiSiO(s)+Li CO(s),反应物为气体的是二氧化碳,生成物均
4 4 2 2 3 2 3
为固体,则平衡常数 ;反应中固体增加的质量即为消耗的CO的质量,反
2
应20min消耗的CO的质量为8.8g,∆c(CO)=8.8g÷44g/mol÷2L=0.1mol·L-1,则0~20min内CO
2 2 2
的平均反应速率 ,
故答案为: ;0.005mol·L-1·min-1;
(4)由图像分析可知,T先达到平衡,则温度T>T,T到T的过程是升温,c(CO)增大,平
1 1 2 2 1 2
衡逆向移动,则该反应是放热反应;若T温度下,达到平衡时c(CO)为amol·L-1,保持其他
1 2
条件不变,通入一定量的CO,平衡会正向进行,但由于温度不变,该反应的平衡常数K=
2
不变,故达到新平衡时c(CO)不变,即a=b,故答案为:放热;a=b,通入一
2定量的CO,平衡会正向进行,但由于温度不变,该反应的平衡常数K= 不变,
2
故达到新平衡时c(CO)不变,即a=b。
2
【点睛】第(3)小问为本题的难点,需要学生正确理解平衡常数的表达方式,同时理解反应
中固体增加的质量即为消耗的CO的质量为本题的解答关键,第(4)题的第二问a、b的大小
2
比较为易错点,注意巧用化学平衡常数作答。
22.高铁酸盐具有极强的氧化性,可作水处理剂。低温下,在NaFeO溶液中加入KOH浓溶
2 4
液可析出KFeO。完成下列填空:
2 4
(1)写出上述得到KFeO 化学方程式_____。
2 4
(2)NaFeO和稀HSO 发生如下反应:NaFeO+H SO →Fe (SO )+O ↑+Na SO +H O。配
2 4 2 4 2 4 2 4 2 4 3 2 2 4 2
平上述化学方程式_____。若反应中产生3.36L(标准状况)的氧气,则转移电子数为_____。
(3)实验室配制Fe (SO )溶液时,需加入少量稀硫酸,结合离子方程式用化学平衡移动原
2 4 3
理解释其原因______。
(4)在Fe (SO )溶液中滴加NaHSO溶液,n(SO 2-)增大,则还原产物是____。写出检验上
2 4 3 3 4
述反应中Fe (SO )是否消耗完全的方法______。
2 4 3
(5)已知HSO -在水中既能水解也能电离。NaHSO溶液呈酸性,溶液中
3 3
c(HSO )_____c(SO 2-)(选填“>”、“<”或“=”)。
2 3 3
【 答 案 】 (1). Na FeO+2KOH=K FeO+2NaOH (2).
2 4 2 4
4NaFeO+10H SO =2Fe (SO )+3O ↑+4Na SO +10H O (3). 0.6N (4). Fe3+易水解:Fe3+
2 4 2 4 2 4 3 2 2 4 2 A
+3H O Fe(OH) +3H+,加入少量稀硫酸可使水解平衡逆向移动,抑制其水解,减少损
2 3
耗 (5). FeSO (6). 取少量溶液于试管中,向试管中加入KSCN溶液,若溶液不变红,则
4
证明Fe (SO )消耗完全,若溶液变成红色,Fe (SO )未消耗完全 (7). <
2 4 3 2 4 3
【解析】
【分析】
(1)根据题干信息写出化学反应方程式;
(2)根据氧化还原反应规律,得失电子守恒进行方程式的配平和相关计算;
(3)Fe3+易水解,加入少量稀硫酸可抑制其水解,从此角度进行分析解答;
(4)结合氧化还原反应分析问题,检验Fe3+用KSCN溶液;
(5)根据溶液的酸碱性判断HSO -的电离程度和水解程度相对大小,从而判断粒子浓度大小
3关系。
【详解】(1)由题干信息可知,低温下,在NaFeO溶液中加入KOH浓溶液可析出KFeO,
2 4 2 4
化学反应方程式为NaFeO+2KOH=K FeO+2NaOH,故答案为:
2 4 2 4
NaFeO+2KOH=K FeO+2NaOH;
2 4 2 4
(2)Na FeO和稀HSO 发生如下反应:NaFeO+H SO →Fe (SO )+O ↑+Na SO +H O,反应中
2 4 2 4 2 4 2 4 2 4 3 2 2 4 2
NaFeO的Fe元素的化合价由+6价降低至+3价,反应中O元素的化合价由-2价升高至0价,
2 4
根据氧化还原反应得失电子守恒配平可得反应方程式为
4NaFeO+10H SO =2Fe (SO )+3O ↑+4Na SO +10H O,反应中每生成1molO 转移4mol电子,
2 4 2 4 2 4 3 2 2 4 2 2
标况下3.36LO 的物质的量为0.15mol,则转移的电子为0.15mol×4=0.6mol,数目为0.6N ,
2 A
故答案为:4NaFeO+10H SO =2Fe (SO )+3O ↑+4Na SO +10H O;0.6N ;
2 4 2 4 2 4 3 2 2 4 2 A
(3)Fe (SO )溶液中Fe3+易水解:Fe3++3H O Fe(OH) +3H+,加入少量稀硫酸可使水解平
2 4 3 2 3
衡逆向移动,抑制其水解,减少损耗,故答案为:Fe3+易水解:Fe3++3H O
2
Fe(OH) +3H+,加入少量稀硫酸可使水解平衡逆向移动,抑制其水解,减少损耗;
3
(4)在Fe (SO )溶液中滴加NaHSO溶液,n(SO 2-)增大,发生反应:2Fe3++HSO -+H O=SO 2-
2 4 3 3 4 3 2 4
+2Fe2++3H+,Fe3+被还原成Fe2+,故还原产物为FeSO ,检验上述反应中Fe (SO )是否消耗完
4 2 4 3
全即检验溶液中是否还存在着Fe3+,可用KSCN溶液进行检验,具体方法为:取少量溶液于
试管中,向试管中加入KSCN溶液,若溶液不变红,则证明Fe (SO )消耗完全,若溶液变成
2 4 3
红色,Fe (SO )未消耗完全,故答案为:FeSO ;取少量溶液于试管中,向试管中加入
2 4 3 4
KSCN溶液,若溶液不变红,则证明Fe (SO )消耗完全,若溶液变成红色,Fe (SO )未消耗
2 4 3 2 4 3
完全;
(5)NaHSO溶液呈酸性,则HSO -的电离程度大于水解程度,则水解产生的HSO 的浓度小
3 3 2 3
于电离生成的SO 2-的浓度,故答案为:<。
3
23.对硝基苯乙醇是合成治疗心血管病的重要药物——美多心安的中间体。其中一种合成路
线如图:(1)A的结构简式为_____;实验室由A制取苯乙烯通常需要经过两步反应,第一步的反应
试剂和条件为Cl/光照,第二步的化学反应方程式为_____。
2
(2)反应②的反应类型为反应_____。设计反应①、反应③的目的是_____。
(3)反应③的试剂和条件为_____。
(4)丁苯橡胶是合成橡胶中产量最大的品种,适合制轮胎、传输带等。丁苯橡胶可由1,3
—丁二烯和苯乙烯共聚得到。写出丁苯橡胶的结构简式_____。
(5)由1,3—丁二烯为原料可以合成有机化工原料1,4—丁二醇
(HOCH CHCHCHOH)写出其合成路线______。
2 2 2 2
(合成路线常用的表示方式为:A B ……目标产物)
【答案】 (1). (2). +NaOH
+NaCl+HO(或 + NaOH +NaCl+HO) (3).
2 2
取代(或硝化)反应 (4). 保护官能团—OH,防止其被氧化 (5). NaOH溶液、加热 (6).(7). CH =CH-CH=CH
2 2
CHBrCH=CHCH Br HOCH CH=CHCH OH
2 2 2 2
HOCH CHCHCHOH
2 2 2 2
【解析】
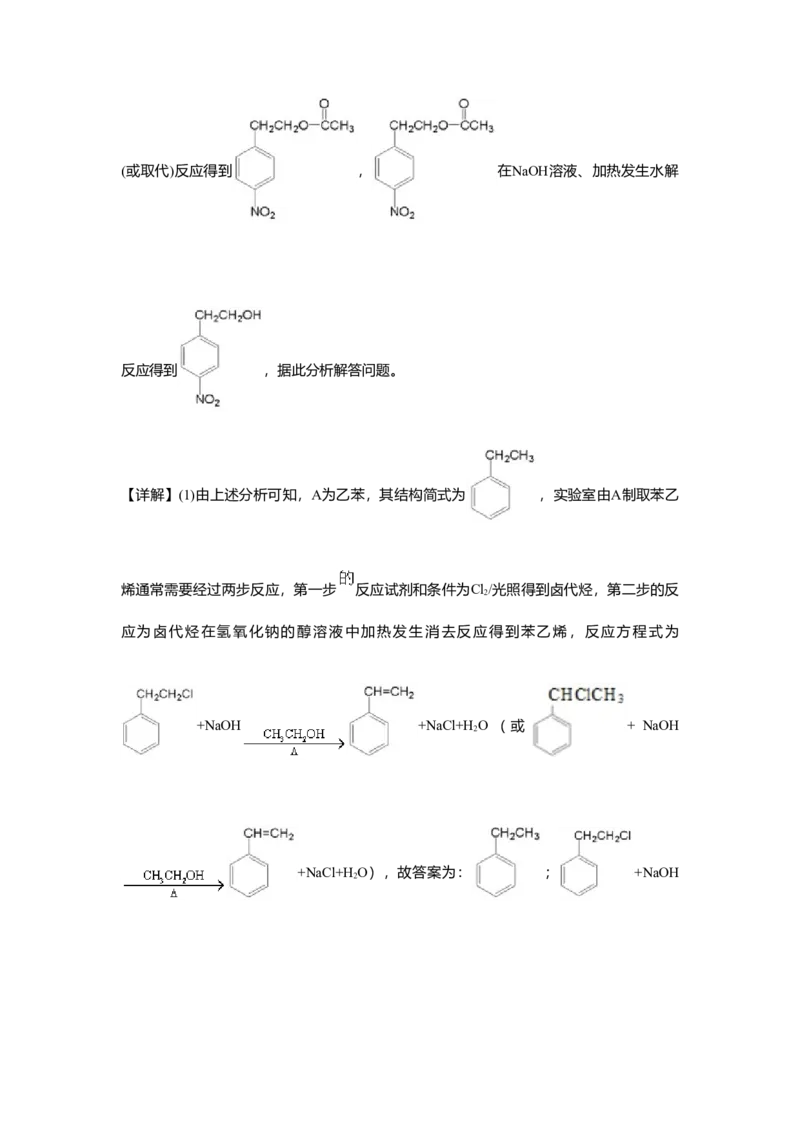
【分析】
根据合成路线分析可知,A先发生取代反应得到卤代烃,再在氢氧化钠的醇溶液中加热发
生消去反应得到苯乙烯( ),则A为乙苯( ), 催化氧化、加
成 得 到 , 与 发 生 取 代 反 应 得 到
, 与浓硝酸在浓硫酸、加热的条件下发生硝化(或取代)反应得到 , 在NaOH溶液、加热发生水解
反应得到 ,据此分析解答问题。
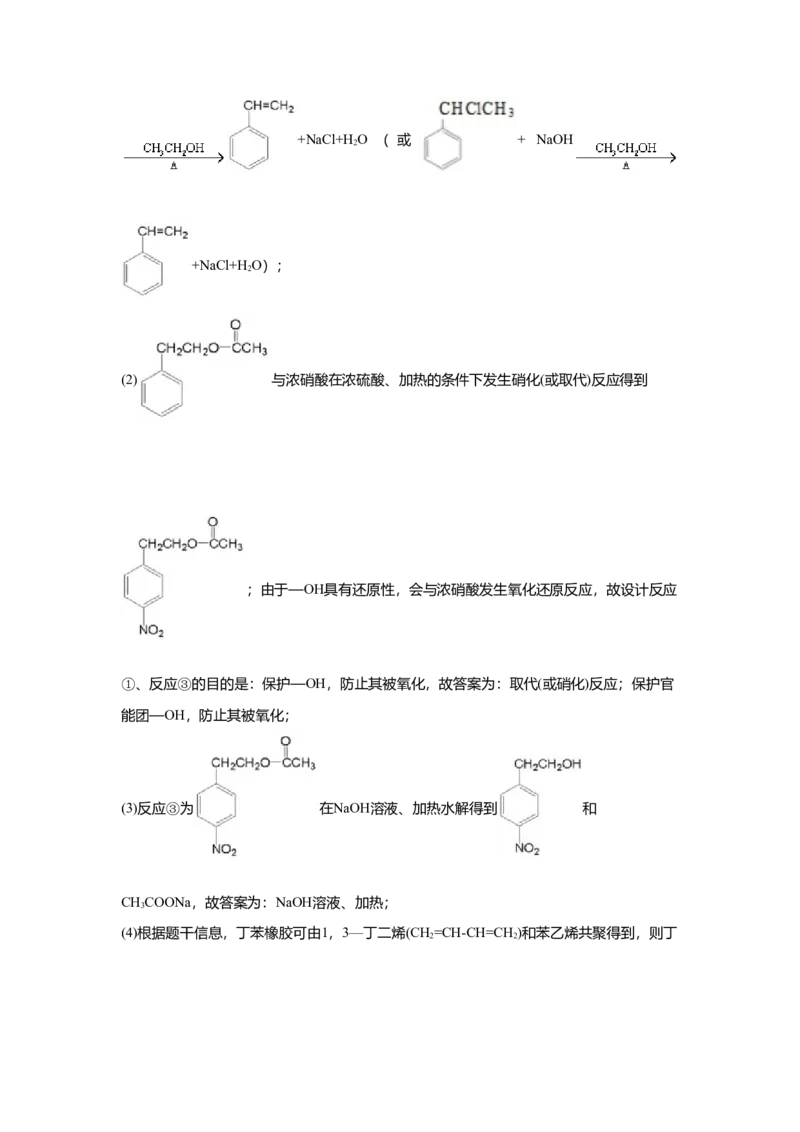
【详解】(1)由上述分析可知,A为乙苯,其结构简式为 ,实验室由A制取苯乙
烯通常需要经过两步反应,第一步 反应试剂和条件为Cl/光照得到卤代烃,第二步的反
2
应为卤代烃在氢氧化钠的醇溶液中加热发生消去反应得到苯乙烯,反应方程式为
+NaOH +NaCl+HO(或 + NaOH
2
+NaCl+HO),故答案为: ; +NaOH
2+NaCl+HO ( 或 + NaOH
2
+NaCl+HO);
2
(2) 与浓硝酸在浓硫酸、加热的条件下发生硝化(或取代)反应得到
;由于—OH具有还原性,会与浓硝酸发生氧化还原反应,故设计反应
①、反应③的目的是:保护—OH,防止其被氧化,故答案为:取代(或硝化)反应;保护官
能团—OH,防止其被氧化;
(3)反应③为 在NaOH溶液、加热水解得到 和
CHCOONa,故答案为:NaOH溶液、加热;
3
(4)根据题干信息,丁苯橡胶可由1,3—丁二烯(CH=CH-CH=CH )和苯乙烯共聚得到,则丁
2 2苯橡胶的结构简式为 ,故答案为:
;
(5)由1,3—丁二烯为原料制备1,4—丁二醇,可以用1,3—丁二烯与溴发生1,4—加成,
然后水解生成烯醇,再与氢气加成即可,合成路线为CH=CH-CH=CH
2 2
CHBrCH=CHCH Br HOCH CH=CHCH OH
2 2 2 2
HOCH CHCHCHOH,故答案为:CH=CH-CH=CH CHBrCH=CHCH Br
2 2 2 2 2 2 2 2
HOCH CH=CHCH OH HOCH CHCHCHOH。
2 2 2 2 2 2
【点睛】本题考查有机物推断,侧重考查学生推断和知识综合运用能力,涉及物质推断、
反应类型判断、官能团判断,明确有机物官能团及其性质、物质之间的转化关系是解本题
关键,题目难度不大。
24.实验室可用二氧化锰和浓盐酸共热制取氯气。为了证明得到的氯气中含氯化氢,并测定
氯化氢的含量进行了下列实验。请回答:
(1)向饱和NaCl溶液中滴入少量浓盐酸,会有白色晶体析出,该晶体的化学式是_____。
(2)按如图装置,将所得气体通入后,试管内白色晶体析出,能否证明氯气中含有HCl,
说明理由_____。b装置的作用是_____。(3)已知氯气易溶于CCl ,按图中装置实验试管③中有白色沉淀,能够证明含HCl,说明
4
理由_____。用浓盐酸与二氧化锰加热经干燥得到1.12L(标况下)气体,除去Cl后,用水
2
全部吸收并定容至100mL,再通过滴定测HCl气体含量。
(4)定容所需要仪器有烧杯、玻璃棒、________和_____。
(5)取定容后溶液20.00mL,加入2滴酚酞试液,用0.0250mol/L标准NaOH溶液滴定,当
______即为滴定终点,消耗NaOH溶液19.20mL,则得到的气体中氯化氢的体积含量是
______。
【答案】 (1). NaCl (2). 不能,因为Cl 溶于水会生成HClO和HCl,试管内有白色晶体析
2
出不一定是因为Cl 中含有HCl (3). 吸收尾气,防止污染空气 (4). 氯气易溶于CCl ,装置
2 4
①可吸收Cl ,装置②检验Cl 是否被完全吸收,以确保不会有Cl 进入装置③中,若装置③
2 2 2
中有白色沉淀生成,则证明有Cl-存在,即一定含有HCl (5). 胶头滴管 (6). 100mL容量瓶
(7). 最后一滴NaOH溶液滴入时,溶液变成浅红色,且半分钟后不褪色 (8). 4.8%
【解析】
【详解】(1)向饱和的NaCl溶液中滴加少量浓盐酸,Cl-浓度增大,NaCl的溶解平衡逆向移动,
析出NaCl的白色晶体,故答案为:NaCl;
(2)由于Cl溶于水会生成HClO和HCl,因此试管内有白色晶体析出不一定是因为Cl中含有
2 2
HCl;装置b的作用是吸收尾气,防止污染空气,故答案为:不能,因为Cl溶于水会生成
2
HClO和HCl,试管内有白色晶体析出不一定是因为Cl中含有HCl;吸收尾气,防止污染空
2
气;
(3)因为氯气易溶于CCl ,根据图中装置分析可知,装置①可吸收Cl,装置②检验Cl是否被
4 2 2完全吸收,以确保不会有Cl进入装置③中,若装置③中有白色沉淀生成,则证明有Cl-存在,
2
即一定含有HCl,故答案为:氯气易溶于CCl ,装置①可吸收Cl,装置②检验Cl是否被完
4 2 2
全吸收,以确保不会有Cl进入装置③中,若装置③中有白色沉淀生成,则证明有Cl-存在,
2
即一定含有HCl;
(4)配制一定物质的量浓度的溶液时,定容操作需要的仪器有烧杯、玻璃棒、胶头滴管和
100mL的容量瓶,故答案为:胶头滴管;100mL容量瓶;
(5)酚酞溶液作指示剂,用0.0250mol/L标准NaOH溶液滴定,当最后一滴NaOH溶液滴入时,
溶液变成浅红色,且半分钟后不褪色,则达到滴定终点,若消耗NaOH溶液19.20mL,则
20mLHCl溶液中
则100mLHCl溶液中n(HCl)=0.024mol·L-1×0.1L=0.0024mol,因此得到的气体中氯化氢的体积
含量为 ,故答案为:最后一滴NaOH溶液滴入时,溶液
变成浅红色,且半分钟后不褪色;4.8%。