文档内容
性重铬酸钾溶液变色,B叙述不正确;
2020 年全国统一高考化学试卷(新课标Ⅰ)
C.该有机物的分子中有酯基,故其能够发生水解反应,C叙述正确;
一、选择题:本题共 13个小题,每小题 6分。共 78分,在每小题给出的四个选项中,只有一项 D.该有机物分子中与羟基相连的碳原子的邻位碳原子上有氢原子,故其可以在一定的条件下发生消去反应生成
是符合题目要求的。 碳碳双键,D叙述正确。
1.国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、含氯消毒剂、过氧乙酸(CH COOOH)、 综上所述,故选B。
3
氯仿等均可有效灭活病毒。对于上述化学药品,下列说法错误的是 3.下列气体去除杂质的方法中,不能实现目的的是
A. CH CH OH能与水互溶
3 2 气体(杂质) 方法
B. NaClO通过氧化灭活病毒
A SO (H S) 通过酸性高锰酸钾溶液
2 2
C. 过氧乙酸相对分子质量为76
D. 氯仿的化学名称是四氯化碳 B Cl 2 (HCl) 通过饱和的食盐水
【答案】D
C N (O ) 通过灼热的铜丝网
2 2
【解析】
D NO(NO ) 通过氢氧化钠溶液
2
【详解】A.乙醇分子中有羟基,其与水分子间可以形成氢键,因此乙醇能与水互溶,A说法正确;
B.次氯酸钠具有强氧化性,其能使蛋白质变性,故其能通过氧化灭活病毒,B说法正确;
A. A B. B C. C D. D
C.过氧乙酸的分子式为C H O ,故其相对分子质量为76,C说法正确;
2 4 3
【答案】A
D.氯仿的化学名称为三氯甲烷,D说法不正确。
【解析】
综上所述,故选D。
【详解】A.SO 和H S都具有较强的还原性,都可以被酸性高锰酸钾溶液氧化;因此在用酸性高锰酸钾溶液除
2 2
2.紫花前胡醇 可从中药材当归和白芷中提取得到,能提高人体免疫力。有关该化合
杂质H S时,SO 也会被吸收,故A项不能实现除杂目的;
2 2
B.氯气中混有少量的氯化氢气体,可以用饱和食盐水除去;饱和食盐水在吸收氯化氢气体的同时,也会抑制氯
物,下列叙述错误的是
气在水中的溶解,故B项能实现除杂目的;
A. 分子式为C H O
14 14 4
B. 不能使酸性重铬酸钾溶液变色 C.氮气中混有少量氧气,在通过灼热的铜丝网时,氧气可以与之发生反应:2CuO ==2CuO ,而铜与氮
2
C. 能够发生水解反应 气无法反应,因此可以采取这种方式除去杂质氧气,故C项能实现除杂目的;
D. 能够发生消去反应生成双键
D.NO 可以与NaOH发生反应:2NO 2NaOH=NaNO NaNO H O,NO与NaOH溶液不能发生反
2 2 3 2 2
【答案】B
应;尽管NO可以与NO 一同跟NaOH发生反应:NONO 2NaOH=2NaNO H O,但由于杂质的含量
【解析】 2 2 2 2
一般较少,所以也不会对NO的量产生较大的影响,故D项能实现除杂的目的;
【详解】A.根据该有机物的分子结构可以确定其分子式为C H O ,A叙述正确;
14 14 4
答案选A。
B.该有机物的分子在有羟基,且与羟基相连的碳原子上有氢原子,故其可以被酸性重铬酸钾溶液氧化,能使酸
【点睛】除杂操作原则可概括为“不多不少,简单最好”:首先,避免引入新的杂质;其次,尽量避免产品的损失;最后,方法越简单越好。 D.通过分析可知,反应中间体CH COI与水作用生成的HI可以使甲醇转化为CH I,方程式可写成:
3 3
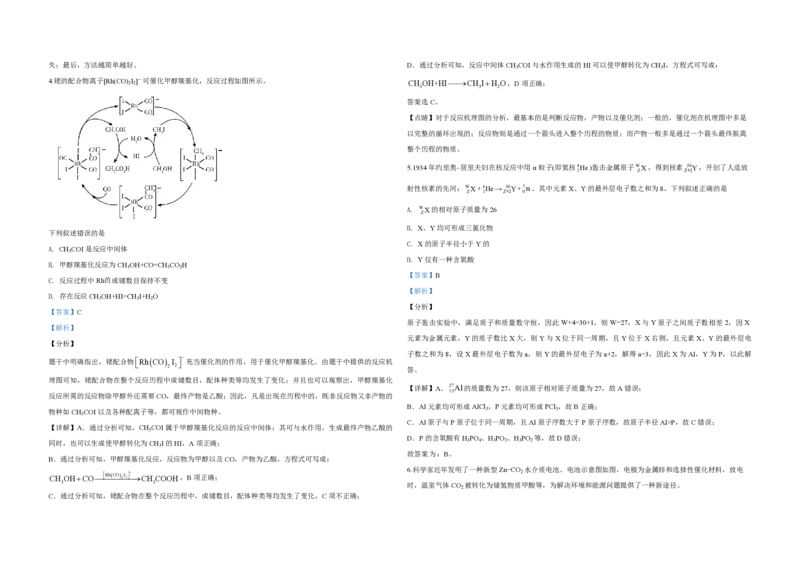
4.铑的配合物离子[Rh(CO) 2 I 2 ]-可催化甲醇羰基化,反应过程如图所示。 CH OH+HICH IH O,D项正确;
3 3 2
答案选C。
【点睛】对于反应机理图的分析,最基本的是判断反应物,产物以及催化剂;一般的,催化剂在机理图中多是
以完整的循环出现的;反应物则是通过一个箭头进入整个历程的物质;而产物一般多是通过一个箭头最终脱离
整个历程的物质。
5.1934年约里奥–居里夫妇在核反应中用α粒子(即氦核4He)轰击金属原子WX,得到核素 30Y,开创了人造放
2 Z Z+2
射性核素的先河:WX+4He→ 30Y+1n。其中元素X、Y的最外层电子数之和为8。下列叙述正确的是
Z 2 Z+2 0
A. WX的相对原子质量为26
Z
B. X、Y均可形成三氯化物
下列叙述错误的是
C. X的原子半径小于Y的
A. CH COI是反应中间体
3
D. Y仅有一种含氧酸
B. 甲醇羰基化反应为CH OH+CO=CH CO H
3 3 2
【答案】B
C. 反应过程中Rh的成键数目保持不变
【解析】
D. 存在反应CH OH+HI=CH I+H O
3 3 2
【分析】
【答案】C
原子轰击实验中,满足质子和质量数守恒,因此W+4=30+1,则W=27,X与Y原子之间质子数相差2,因X
【解析】
元素为金属元素,Y的质子数比X大,则Y与X位于同一周期,且Y位于X右侧,且元素X、Y的最外层电
【分析】
子数之和为8,设X最外层电子数为a,则Y的最外层电子为a+2,解得a=3,因此X为Al,Y为P,以此解
题干中明确指出,铑配合物RhCO I 充当催化剂的作用,用于催化甲醇羰基化。由题干中提供的反应机
2
2
答。
理图可知,铑配合物在整个反应历程中成键数目,配体种类等均发生了变化;并且也可以观察出,甲醇羰基化
【详解】A.27Al的质量数为27,则该原子相对原子质量为27,故A错误;
13
反应所需的反应物除甲醇外还需要CO,最终产物是乙酸;因此,凡是出现在历程中的,既非反应物又非产物的
B.Al元素均可形成AlCl ,P元素均可形成PCl ,故B正确;
物种如CH COI以及各种配离子等,都可视作中间物种。 3 3
3
C.Al原子与P原子位于同一周期,且Al原子序数大于P原子序数,故原子半径Al>P,故C错误;
【详解】A.通过分析可知,CH COI属于甲醇羰基化反应的反应中间体;其可与水作用,生成最终产物乙酸的
3
D.P的含氧酸有H PO 、H PO 、H PO 等,故D错误;
同时,也可以生成使甲醇转化为CH I的HI,A项正确; 3 4 3 3 3 2
3
故答案为:B。
B.通过分析可知,甲醇羰基化反应,反应物为甲醇以及CO,产物为乙酸,方程式可写成:
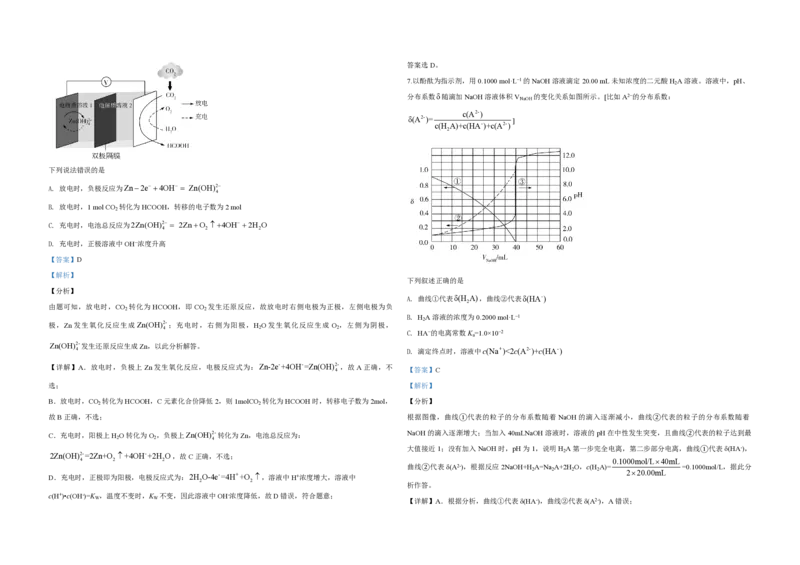
6.科学家近年发明了一种新型Zn−CO 水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电
CH OHCO Rh CO 2 I 2 CH COOH,B项正确; 2
3 3 时,温室气体CO 被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
2
C.通过分析可知,铑配合物在整个反应历程中,成键数目,配体种类等均发生了变化,C项不正确;答案选D。
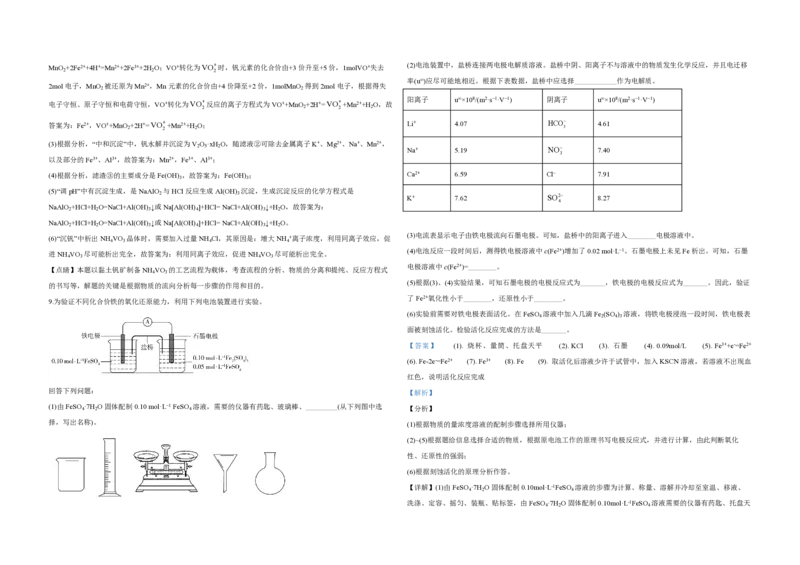
7.以酚酞为指示剂,用0.1000 mol·L−1的NaOH溶液滴定20.00 mL未知浓度的二元酸H A溶液。溶液中,pH、
2
分布系数δ随滴加NaOH溶液体积V 的变化关系如图所示。[比如A2−的分布系数:
NaOH
c(A2-)
δ(A2-)=
]
c(H A)+c(HA-)+c(A2-)
2
下列说法错误的是
A. 放电时,负极反应为Zn2e 4OH Zn(OH)2
4
B. 放电时,1 mol CO 转化为HCOOH,转移的电子数为2 mol
2
C. 充电时,电池总反应为2Zn(OH)2 2ZnO 4OH 2H O
4 2 2
D. 充电时,正极溶液中OH−浓度升高
【答案】D
【解析】
下列叙述正确的是
【分析】
A. 曲线①代表δ(H A),曲线②代表δ(HA-)
2
由题可知,放电时,CO 转化为 HCOOH,即 CO 发生还原反应,故放电时右侧电极为正极,左侧电极为负
2 2
B. H A溶液的浓度为0.2000 mol·L−1
2
极,Zn发生氧化反应生成Zn(OH)2-;充电时,右侧为阳极,H O发生氧化反应生成 O ,左侧为阴极,
4 2 2
C. HA−的电离常数K =1.0×10−2
a
Zn(OH)2-发生还原反应生成Zn,以此分析解答。
4 D. 滴定终点时,溶液中c(Na+)<2c(A2-)+c(HA-)
【详解】A.放电时,负极上 Zn发生氧化反应,电极反应式为:Zn-2e-+4OH-=Zn(OH)2-,故 A正确,不
4 【答案】C
选; 【解析】
B.放电时,CO 转化为HCOOH,C元素化合价降低2,则1molCO 转化为HCOOH时,转移电子数为2mol, 【分析】
2 2
故B正确,不选; 根据图像,曲线①代表的粒子的分布系数随着 NaOH的滴入逐渐减小,曲线②代表的粒子的分布系数随着
C.充电时,阳极上H O转化为O ,负极上Zn(OH)2-转化为Zn,电池总反应为: NaOH的滴入逐渐增大;当加入40mLNaOH溶液时,溶液的pH在中性发生突变,且曲线②代表的粒子达到最
2 2 4
大值接近1;没有加入NaOH时,pH为1,说明H A第一步完全电离,第二步部分电离,曲线①代表δ(HA-),
2
2Zn(OH)2-=2Zn+O +4OH-+2H O,故C正确,不选;
4 2 2 0.1000mol/L40mL
曲线②代表δ(A2-),根据反应2NaOH+H A=Na A+2H O,c(H A)= =0.1000mol/L,据此分
2 2 2 2
220.00mL
D.充电时,正极即为阳极,电极反应式为:2H O-4e-=4H++O ,溶液中H+浓度增大,溶液中
2 2
析作答。
c(H+)•c(OH-)=K ,温度不变时,K 不变,因此溶液中OH-浓度降低,故D错误,符合题意;
W W 【详解】A.根据分析,曲线①代表δ(HA-),曲线②代表δ(A2-),A错误;B.当加入40.00mLNaOH溶液时,溶液的pH发生突变,说明恰好完全反应,结合分析,根据反应 (1)“酸浸氧化”需要加热,其原因是___________。
0.1000mol/L40mL
2NaOH+H A=Na A+2H O,c(H A)= =0.1000mol/L,B错误; (2)“酸浸氧化”中,VO+和VO2+被氧化成VO,同时还有___________离子被氧化。写出VO+转化为VO反应
2 2 2 2 220.00mL 2 2
C.由于H A第一步完全电离,则HA-的起始浓度为0.1000mol/L,根据图像,当V =0时,HA-的分布系数 的离子方程式___________。
2 NaOH
c(A2-)c(H+) (3)“中和沉淀”中,钒水解并沉淀为V O xH O,随滤液②可除去金属离子K+、Mg2+、Na+、___________,以
为0.9,溶液的pH=1,A2-的分布系数为0.1,则HA-的电离平衡常数K = = 2 5 2
a c(HA-)
及部分的___________。
0.1000mol/L0.10.1000mol/L
≈1×10-2,C正确;
0.1000mol/L0.9 (4)“沉淀转溶”中,V O xH O转化为钒酸盐溶解。滤渣③的主要成分是___________。
2 5 2
D.用酚酞作指示剂,酚酞变色的pH范围为8.2~10,终点时溶液呈碱性,c(OH-)>c(H+),溶液中的电荷守恒为
(5)“调pH”中有沉淀生产,生成沉淀反应的化学方程式是___________。
c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-),则c(Na+)>2c(A2-)+c(HA-),D错误;
(6)“沉钒”中析出NH VO 晶体时,需要加入过量NH Cl,其原因是___________。
4 3 4
答案选C。
【答案】 (1). 加快酸浸和氧化反应速率(促进氧化完全) (2). Fe2+ (3). VO++MnO +2H+=VO+
2 2
【点睛】本题的难点是判断H A的电离,根据pH的突变和粒子分布分数的变化确定H A的电离方程式为
2 2
+Mn2++H O (4). Mn2+ (5). Fe3+、Al3+ (6). Fe(OH) (7). NaAlO +HCl+H O=NaCl+Al(OH) ↓或
H A=H++A2-,HA-⇌H++A2-。 2 3 2 2 3
2
Na[Al(OH) ]+HCl= NaCl+Al(OH) ↓+H O (8). 利用同离子效应,促进NH VO 尽可能析出完全
三、非选择题:共 174分,第 22~32 题为必考题,每个试题考生都必须作答。第 33~38 题为选考 4 3 2 4 3
【解析】
题,考生根据要求作答。
【分析】
(一)必考题:共 129分。
黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO 、Fe O ,用30%H SO
8.钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO 、 2 3 4 2 4
2
和MnO “酸浸氧化”时VO+和VO2+被氧化成VO+,Fe O 与硫酸反应生成的Fe2+被氧化成Fe3+,SiO 此过程中
Fe 3 O 4 。采用以下工艺流程可由黏土钒矿制备NH 4 VO 3 。 2 2 3 4 2
不反应,滤液①中含有VO+、K+、Mg2+、Al3+、Fe3+、Mn2+、SO2-;滤液①中加入 NaOH调节 pH=3.0~3.1,
2 4
钒水解并沉淀为V O ·xH O,根据表中提供的溶液中金属离子开始沉淀和完全沉淀的pH,此过程中Fe3+部分转
2 5 2
化为Fe(OH) 沉淀,部分Al3+转化为Al(OH) 沉淀,滤液②中含有K+、Na+、Mg2+、Al3+、Fe3+、Mn2+、SO2-,
3 3 4
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
滤饼②中含V O ·xH O、Fe(OH) 、Al(OH) ,滤饼②中加入NaOH使pH>13,V O ·xH O转化为钒酸盐溶解,
2 5 2 3 3 2 5 2
金属离子 Fe3+ Fe2+ Al3+ Mn2+
Al(OH) 转化为 NaAlO ,则滤渣③的主要成分为 Fe(OH) ;滤液③中含钒酸盐、偏铝酸钠,加入 HCl调
3 2 3
pH=8.5,NaAlO 转化为Al(OH) 沉淀而除去;最后向滤液④中加入NH Cl“沉钒”得到NH VO 。
开始沉淀pH 1.9 7.0 3.0 8.1 2 3 4 4 3
【详解】(1)“酸浸氧化”需要加热,其原因是:升高温度,加快酸浸和氧化反应速率(促进氧化完全),故答案
完全沉淀pH 3.2 9.0 4.7 10.1
为:加快酸浸和氧化反应速率(促进氧化完全);
(2)“酸浸氧化”中,钒矿粉中的Fe O 与硫酸反应生成FeSO 、Fe (SO ) 和水,MnO 具有氧化性,Fe2+具有还原
3 4 4 2 4 3 2
性,则VO+和VO2+被氧化成VO+的同时还有Fe2+被氧化,反应的离子方程式为
2
回答下列问题:MnO +2Fe2++4H+=Mn2++2Fe3++2H O;VO+转化为VO+时,钒元素的化合价由+3价升至+5价,1molVO+失去 (2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移
2 2 2
率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择____________作为电解质。
2mol电子,MnO 被还原为Mn2+,Mn元素的化合价由+4价降至+2价,1molMnO 得到2mol电子,根据得失
2 2
阳离子 u∞×108/(m2·s−1·V−1) 阴离子 u∞×108/(m2·s−1·V−1)
电子守恒、原子守恒和电荷守恒,VO+转化为VO+反应的离子方程式为VO++MnO +2H+=VO++Mn2++H O,故
2 2 2 2
答案为:Fe2+,VO++MnO +2H+=VO++Mn2++H O; Li+ 4.07 HCO 4.61
2 2 2 3
(3)根据分析,“中和沉淀”中,钒水解并沉淀为V O ·xH O,随滤液②可除去金属离子K+、Mg2+、Na+、Mn2+,
2 5 2 Na+ 5.19 NO 7.40
3
以及部分的Fe3+、Al3+,故答案为:Mn2+,Fe3+、Al3+;
(4)根据分析,滤渣③的主要成分是Fe(OH) ,故答案为:Fe(OH) ; Ca2+ 6.59 Cl− 7.91
3 3
(5)“调pH”中有沉淀生成,是NaAlO 与HCl反应生成Al(OH) 沉淀,生成沉淀反应的化学方程式是
2 3
K+ 7.62 SO2 8.27
4
NaAlO +HCl+H O=NaCl+Al(OH) ↓或Na[Al(OH) ]+HCl= NaCl+Al(OH) ↓+H O,故答案为:
2 2 3 4 3 2
NaAlO +HCl+H O=NaCl+Al(OH) ↓或Na[Al(OH) ]+HCl= NaCl+Al(OH) ↓+H O。
2 2 3 4 3 2
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________电极溶液中。
(6)“沉钒”中析出NH VO 晶体时,需要加入过量NH Cl,其原因是:增大NH +离子浓度,利用同离子效应,促
4 3 4 4
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L−1。石墨电极上未见Fe析出。可知,石墨
进NH VO 尽可能析出完全,故答案为:利用同离子效应,促进NH VO 尽可能析出完全。
4 3 4 3
电极溶液中c(Fe2+)=________。
【点睛】本题以黏土钒矿制备NH VO 的工艺流程为载体,考查流程的分析、物质的分离和提纯、反应方程式
4 3
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为_______,铁电极的电极反应式为_______。因此,验证
的书写等,解题的关键是根据物质的流向分析每一步骤的作用和目的。
了Fe2+氧化性小于________,还原性小于________。
9.为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
(6)实验前需要对铁电极表面活化。在FeSO 溶液中加入几滴Fe (SO ) 溶液,将铁电极浸泡一段时间,铁电极表
4 2 4 3
面被刻蚀活化。检验活化反应完成的方法是_______。
【答案】 (1). 烧杯、量筒、托盘天平 (2). KCl (3). 石墨 (4). 0.09mol/L (5). Fe3++e-=Fe2+
(6). Fe-2e-=Fe2+ (7). Fe3+ (8). Fe (9). 取活化后溶液少许于试管中,加入KSCN溶液,若溶液不出现血
红色,说明活化反应完成
回答下列问题: 【解析】
(1)由FeSO 4 ·7H 2 O固体配制0.10 mol·L−1 FeSO 4 溶液,需要的仪器有药匙、玻璃棒、_________(从下列图中选 【分析】
择,写出名称)。
(1)根据物质的量浓度溶液的配制步骤选择所用仪器;
(2)~(5)根据题给信息选择合适的物质,根据原电池工作的原理书写电极反应式,并进行计算,由此判断氧化
性、还原性的强弱;
(6)根据刻蚀活化的原理分析作答。
【详解】(1)由FeSO ·7H O固体配制0.10mol·L-1FeSO 溶液的步骤为计算、称量、溶解并冷却至室温、移液、
4 2 4
洗涤、定容、摇匀、装瓶、贴标签,由FeSO ·7H O固体配制0.10mol·L-1FeSO 溶液需要的仪器有药匙、托盘天
4 2 4平、合适的量筒、烧杯、玻璃棒、合适的容量瓶、胶头滴管,故答案为:烧杯、量筒、托盘天平。
(2)Fe2+、Fe3+能与HCO- 反应,Ca2+能与SO2-反应,FeSO 、Fe (SO ) 都属于强酸弱碱盐,水溶液呈酸性,酸性
3 4 4 2 4 3
条件下NO-能与Fe2+反应,根据题意“盐桥中阴、阳离子不与溶液中的物质发生化学反应”,盐桥中阴离子不可
3
以选择HCO- 、NO-,阳离子不可以选择Ca2+,另盐桥中阴、阳离子的迁移率(u∞)应尽可能地相近,根据表
3 3
中数据,盐桥中应选择KCl作为电解质,故答案为:KCl。
(3)电流表显示电子由铁电极流向石墨电极,则铁电极为负极,石墨电极为正极,盐桥中阳离子向正极移动,则 (2)当SO (g)、O (g)和N (g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa
2 2 2
盐桥中的阳离子进入石墨电极溶液中,故答案为:石墨。 压强下,SO 平衡转化率α随温度的变化如图所示。反应在5.0MPa、550℃时的α=__________,判断的依据是
2
(4)根据(3)的分析,铁电极的电极反应式为Fe-2e-=Fe2+,石墨电极上未见Fe析出,石墨电极的电极反应式为 __________。影响α的因素有__________。
Fe3++e-=Fe2+,电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02mol/L,根据得失电子守恒,石墨
电极溶液中c(Fe2+)增加0.04mol/L,石墨电极溶液中c(Fe2+)=0.05mol/L+0.04mol/L=0.09mol/L,故答案为:
0.09mol/L。
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为Fe3++e-=Fe2+,铁电极的电极反应式为Fe-2e-=Fe2+;电
池总反应为Fe+2Fe3+=3Fe2+,根据同一反应中,氧化剂的氧化性强于氧化产物、还原剂的还原性强于还原产
物,则验证了Fe2+氧化性小于Fe3+,还原性小于Fe,故答案为:Fe3++e-=Fe2+ ,Fe-2e-=Fe2+ ,Fe3+,Fe。
(6)在FeSO 溶液中加入几滴Fe (SO ) 溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化,发生的反应为
4 2 4 3
(3)将组成(物质的量分数)为2m% SO (g)、m% O (g)和q% N (g)的气体通入反应器,在温度t、压强p条件下进
Fe+ Fe (SO ) =3FeSO ,要检验活化反应完成,只要检验溶液中不含Fe3+即可,检验活化反应完成的方法是:取 2 2 2
2 4 3 4
行反应。平衡时,若SO 转化率为α,则SO 压强为___________,平衡常数K =___________(以分压表示,分
活化后溶液少许于试管中,加入KSCN溶液,若溶液不出现血红色,说明活化反应完成,故答案为:取活化后 2 3 p
压=总压×物质的量分数)。
溶液少许于试管中,加入KSCN溶液,若溶液不变红,说明活化反应完成。
α
(4)研究表明,SO 催化氧化的反应速率方程为:v=k( −1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高
【点睛】本题的难点是第(2)题盐桥中电解质的选择和第(6)实验方法的设计,要充分利用题给信息和反应的原理 2 α′
解答。 而增大;α为SO 平衡转化率,α'为某时刻SO 转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代
2 2
1
入上述速率方程,得到v~t曲线,如图所示。
10.硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关键工序是SO 的催化氧化:SO (g)+ O (g)
2 2 2
2
钒催化剂SO (g) ΔH=−98 kJ·mol−1。回答下列问题:
3
(1)钒催化剂参与反应的能量变化如图所示,V O (s)与SO (g)反应生成VOSO (s)和V O (s)的热化学方程式为:
2 5 2 4 2 4
_________。
曲线上v最大值所对应温度称为该α'下反应的最适宜温度t 。tt 后,v逐渐下降。原因
m m m
是__________________________。【答案】 (1). 2V O (s)+ 2SO (g)⇌ 2VOSO (s)+ V O (s) ∆H= -351 kJ∙mol-1 (2). 0.975 (3). 该反应气体 1
2 5 2 4 2 4 SO + O 矾 催化 剂 SO
2 2 2 3
分子数减少,增大压强,α提高。所以,该反应在 550℃、压强为 5.0MPa>2.5MPa=p 2 的,所以 p 1 =5.0MPa 起始量(mol) 2m m 0
2mp 2m
(4). 反 应 物 ( N 和 O ) 的 起 始 浓 度 ( 组 成 )、 温 度 、 压 强 (5). (6). 变化量(mol) 2m m
2 2
100m
2m
平衡量(mol) 2m(1-) m(1)
0.5 平衡时气体的总物质的量为n(总)= 2m(1-α)+m(1-α)+2mαmol+q mol,则SO 的物质的量分数为
11.5 mp (7). 升高温度,k增大使v逐渐提高,但α降低使v逐渐下降。当t<t m ,k增大对 3
100m nSO
2mmol 2m
3 100% 100% 100%。该反应在恒压容
n总 2m1m12mmolq mol 100m
v的提高大于α引起的降低;当t>t ,k增大对v的提高小于α引起的降低
m
【解析】 2mp 2m1 p m1 p
器中进行,因此,SO 的分压p(SO )= ,p(SO )= ,p(O )= ,在该条件下,
3 3 2 2
【分析】 100m 100m 100m
1
根据盖斯定律,用已知的热化学方程式通过一定的数学运算,可以求出目标反应的反应热;根据压强对化学平
SO (g)+ O (g)⇌2SO (g) 的K =
2 2 3 p
2
衡的影响,分析图中数据找到所需要的数据;根据恒压条件下总压不变,求出各组分的分压,进一步可以求出
2mp
平衡常数;根据题中所给的速率公式,分析温度对速率常数及二氧化硫的转化率的影响,进一步分析对速率的
pSO
3
100m
影响。
pSO
2
p0.5O
2
2m1p
m1p
0.5
11.5
mp
0.5 。
100m 100m 100m
【详解】(1)由题中信息可知:
1 0.8
①SO 2 (g)+ O 2 (g)⇌SO 3 (g) ∆H= -98kJ∙mol-1 (4) 由于该反应是放热反应,温度升高后α降低。由题中信息可知,v=k 1 1n,升高温度,k增
2
②V O (s)+ SO (g)⇌V O (s)+ SO (g) ∆H = -24kJ∙mol-1
2 4 3 2 5 2 2 大使v逐渐提高,但α降低使v逐渐下降。当t<t ,k增大对v的提高大于α引起的降低;当t>t ,k增大对
m m
③V O (s)+ 2SO (g)⇌2VOSO (s) ∆H = -399kJ∙mol-1
2 4 3 4 1 v的提高小于α引起的降低。
根据盖斯定律可知,③-②2得2V O (s)+ 2SO (g)⇌ 2VOSO (s)+ V O (s),则∆H= ∆H -2∆H =( -399kJ∙mol-1)-( -
2 5 2 4 2 4 1 2 【点睛】本题有关化学平衡常数的计算是一个难点,尤其题中给的都是字母型数据,这无疑增大了难度。这也
24kJ∙mol-1)2= -351kJ∙mol-1,所以该反应的热化学方程式为:2V O (s)+ 2SO (g)⇌ 2VOSO (s)+ V O (s) ∆H= -
2 5 2 4 2 4 是对考生的意志的考验,只要巧妙假设、小心求算,还是可以得到正确结果的,毕竟有关化学平衡的计算是一
351 kJ∙mol-1;
种熟悉的题型。本题的另一难点是最后一问,考查的是速率公式与化学平衡的综合理解,需要明确化学反应速
1
(2) SO (g)+ O (g)⇌SO (g),该反应是一个气体分子数减少的放热反应,故增大压强可以使化学平衡向正反应
2 2 3 率与速率常数及平衡转化率之间的函数关系,才能作出正确的解答。所以,耐心和细心才是考好的保证。
2
方向移动。因此,在相同温度下,压强越大,SO 的平衡转化率越大,所以,该反应在550℃、压强为5.0MPa (二)选考题:共 45分。请考生从 2道物理题、2道化学题、2道生物题中每科任选一题作答。如
2
条件下,SO 的平衡转化率一定高于相同温度下、压强为2.5MPa的,因此,p =5.0MPa,由图中数据可知, 果多做,则每科按所做的第一题计分。
2 1
α=0.975。影响α的因素就是影响化学平衡移动的因素,主要有反应物(N 和O )的浓度、温度、压强等。 11.Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔
2 2
(3)假设原气体的物质的量为100mol,则SO 、O 和N 的物质的量分别为2m mol、m mol和q mol, 化学奖。回答下列问题:
2 2 2
2m+m+q=3m+q=100,SO 的平衡转化率为α,则有下列关系: (1)基态Fe2+与Fe3+离子中未成对的电子数之比为_________。
2
(2)Li及其周期表中相邻元素的第一电离能(I )如表所示。I (Li)> I (Na),原因是_________。I (Be)> I (B)>
1 1 1 1 1
I (Li),原因是________。
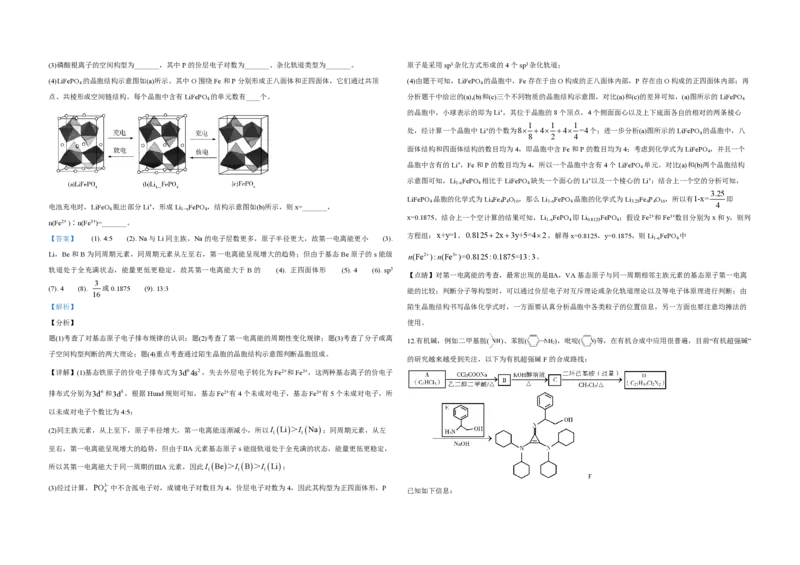
1(3)磷酸根离子的空间构型为_______,其中P的价层电子对数为_______、杂化轨道类型为_______。 原子是采用sp3杂化方式形成的4个sp3杂化轨道;
(4)LiFePO 的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶 (4)由题干可知,LiFePO 的晶胞中,Fe存在于由O构成的正八面体内部,P存在由O构成的正四面体内部;再
4 4
点、共棱形成空间链结构。每个晶胞中含有LiFePO 的单元数有____个。 分析题干中给出的(a),(b)和(c)三个不同物质的晶胞结构示意图,对比(a)和(c)的差异可知,(a)图所示的LiFePO
4 4
的晶胞中,小球表示的即为Li+,其位于晶胞的8个顶点,4个侧面面心以及上下底面各自的相对的两条棱心
1 1 1
处,经计算一个晶胞中Li+的个数为8 4 4 =4个;进一步分析(a)图所示的LiFePO 的晶胞中,八
4
8 2 4
面体结构和四面体结构的数目均为4,即晶胞中含Fe和P的数目均为4;考虑到化学式为LiFePO ,并且一个
4
晶胞中含有的Li+,Fe和P的数目均为4,所以一个晶胞中含有4个LiFePO 单元。对比(a)和(b)两个晶胞结构
4
示意图可知,Li FePO 相比于LiFePO 缺失一个面心的Li+以及一个棱心的Li+;结合上一个空的分析可知,
1-x 4 4
3.25
LiFePO 晶胞的化学式为Li Fe P O ,那么Li FePO 晶胞的化学式为Li Fe P O ,所以有1-x= 即
4 4 4 4 16 1-x 4 3.25 4 4 16
4
电池充电时,LiFeO 脱出部分Li+,形成Li FePO ,结构示意图如(b)所示,则x=_______,
4 1−x 4
x=0.1875。结合上一个空计算的结果可知,Li FePO 即Li FePO ;假设Fe2+和Fe3+数目分别为x和y,则列
n(Fe2+ )∶n(Fe3+)=_______。 1-x 4 0.8125 4
方程组:x+y=1,0.81252x3y+5=42,解得x=0.8125,y=0.1875,则Li FePO 中
【答案】 (1). 4:5 (2). Na与Li同主族,Na的电子层数更多,原子半径更大,故第一电离能更小 (3). 1-x 4
Li,Be和B为同周期元素,同周期元素从左至右,第一电离能呈现增大的趋势;但由于基态Be原子的s能级 n(Fe2):n(Fe3)=0.8125:0.1875=13:3。
轨道处于全充满状态,能量更低更稳定,故其第一电离能大于B的 (4). 正四面体形 (5). 4 (6). sp3
【点睛】对第一电离能的考查,最常出现的是ⅡA,ⅤA基态原子与同一周期相邻主族元素的基态原子第一电离
3
(7). 4 (8). 或0.1875 (9). 13:3
能的比较;判断分子等构型时,可以通过价层电子对互斥理论或杂化轨道理论以及等电子体原理进行判断;由
16
【解析】 陌生晶胞结构书写晶体化学式时,一方面要认真分析晶胞中各类粒子的位置信息,另一方面也要注意均摊法的
【分析】 使用。
题(1)考查了对基态原子电子排布规律的认识;题(2)考查了第一电离能的周期性变化规律;题(3)考查了分子或离
12.有机碱,例如二甲基胺( )、苯胺( ),吡啶( )等,在有机合成中应用很普遍,目前“有机超强碱”
子空间构型判断的两大理论;题(4)重点考查通过陌生晶胞的晶胞结构示意图判断晶胞组成。
的研究越来越受到关注,以下为有机超强碱F的合成路线:
【详解】(1)基态铁原子的价电子排布式为3d64s2,失去外层电子转化为Fe2+和Fe3+,这两种基态离子的价电子
排布式分别为3d6和3d5,根据Hund规则可知,基态Fe2+有4个未成对电子,基态Fe3+有5个未成对电子,所
以未成对电子个数比为4:5;
(2)同主族元素,从上至下,原子半径增大,第一电离能逐渐减小,所以I Li>I Na ;同周期元素,从左
1 1
至右,第一电离能呈现增大的趋势,但由于ⅡA元素基态原子s能级轨道处于全充满的状态,能量更低更稳定,
所以其第一电离能大于同一周期的ⅢA元素,因此I Be>I B>I Li ;
1 1 1
(3)经过计算,PO3中不含孤电子对,成键电子对数目为4,价层电子对数为4,因此其构型为正四面体形,P
4 已知如下信息:①H C=CH CCl 3 COONa Δ
2 2 乙二醇二甲醚/△ +KOH +KCl+H O。
2
醇
② +RNH
NaOH
2 2HCl
(3)由C的分子结构可知其所含官能团有碳碳双键和氯原子。
③苯胺与甲基吡啶互为芳香同分异构体
(4) C( )与过量的二环己基胺发生生成D,D与E发生信息②的反应生成F,由F的分子结构可
回答下列问题:
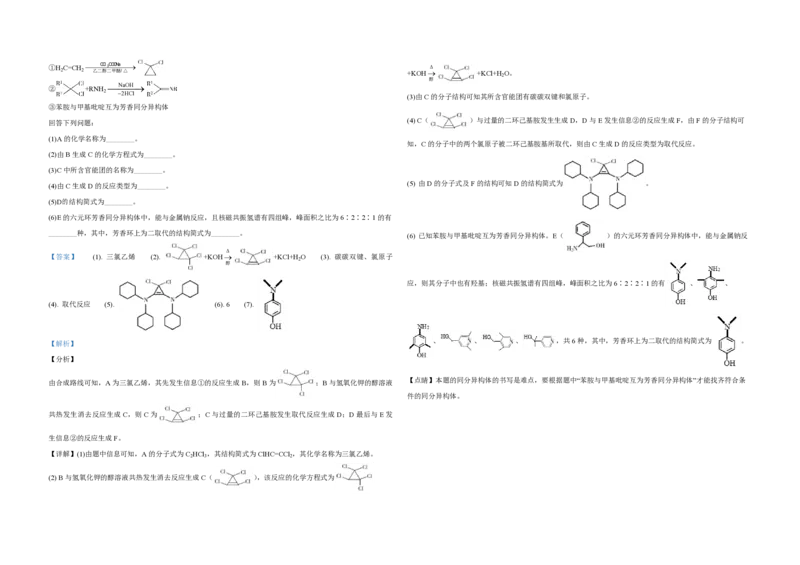
(1)A的化学名称为________。
知,C的分子中的两个氯原子被二环己基胺基所取代,则由C生成D的反应类型为取代反应。
(2)由B生成C的化学方程式为________。
(3)C中所含官能团的名称为________。
(5) 由D的分子式及F的结构可知D的结构简式为 。
(4)由C生成D的反应类型为________。
(5)D的结构简式为________。
(6)E的六元环芳香同分异构体中,能与金属钠反应,且核磁共振氢谱有四组峰,峰面积之比为6∶2∶2∶1的有
________种,其中,芳香环上为二取代的结构简式为________。
(6) 已知苯胺与甲基吡啶互为芳香同分异构体。E( )的六元环芳香同分异构体中,能与金属钠反
Δ
【答案】 (1). 三氯乙烯 (2). +KOH +KCl+H O (3). 碳碳双键、氯原子
2
醇
应,则其分子中也有羟基;核磁共振氢谱有四组峰,峰面积之比为6∶2∶2∶1的有 、 、
(4). 取代反应 (5). (6). 6 (7).
、 、 、 ,共6种,其中,芳香环上为二取代的结构简式为 。
【解析】
【分析】
【点睛】本题的同分异构体的书写是难点,要根据题中“苯胺与甲基吡啶互为芳香同分异构体”才能找齐符合条
由合成路线可知,A为三氯乙烯,其先发生信息①的反应生成B,则B为 ;B与氢氧化钾的醇溶液
件的同分异构体。
共热发生消去反应生成C,则C为 ;C与过量的二环己基胺发生取代反应生成D;D最后与E发
生信息②的反应生成F。
【详解】(1)由题中信息可知,A的分子式为C HCl ,其结构简式为ClHC=CCl ,其化学名称为三氯乙烯。
2 3 2
(2) B与氢氧化钾的醇溶液共热发生消去反应生成C( ),该反应的化学方程式为