文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
主题三 物质的组成与结构
专题 11 构成物质的微粒 元素
01考情透视·目标导航
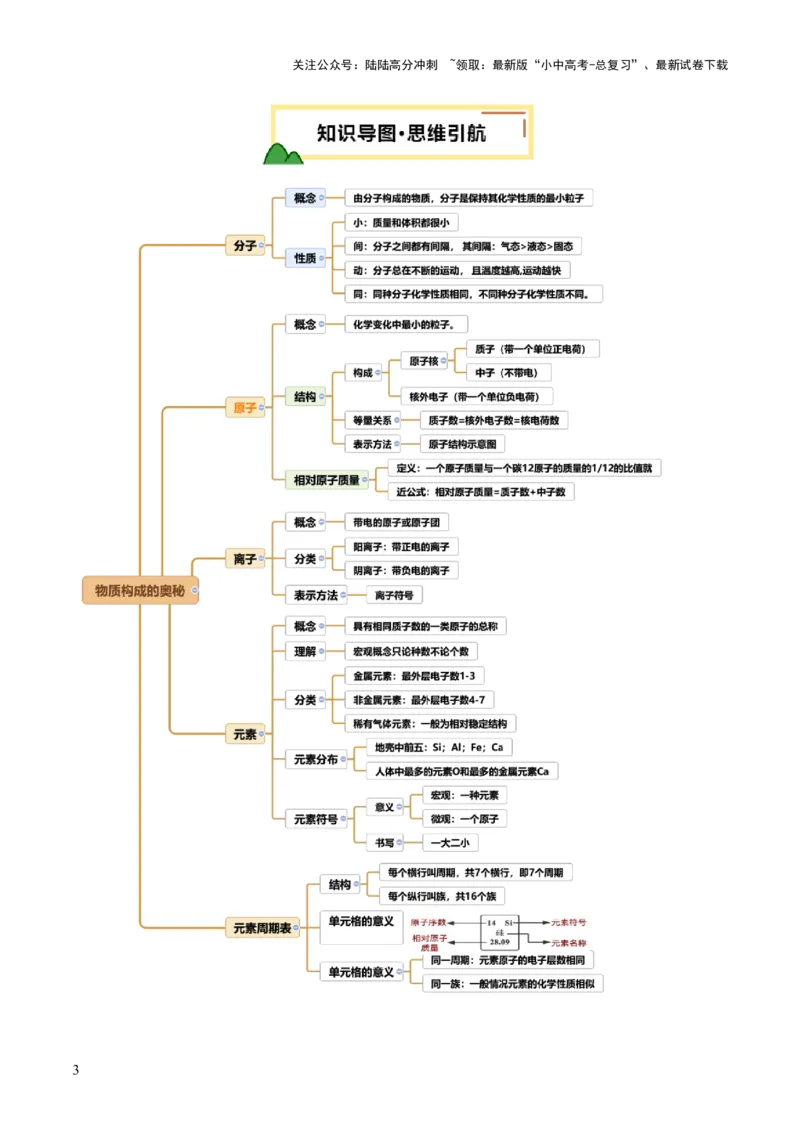
02知识导图·思维引航
03考点突破·考法探究
考点一 分子
考点二 原子和离子
考点三 元素
考点四 元素周期表
04题型精研·考向洞悉
题型一 分子
考向01 由分子构成的物质
考向02 用粒子的性质解释常见现象
题型二 原子和离子
考向01 原子的构成
考向02 离子
考向03 原子(离子)的结构示意图
考向04 相对原子质量
考向05 由原子、离子构成的物质
题型三 元素
考向01 元素的概念及理解
考向02 元素的分布
考向03 元素的分类
考向04 元素符号及意义
题型四 元素周期表
考向01 元素周期表的结构及规律
考向02 元素周期表信息与结构示意图综合考查
跨学科实践活动 制作模型并展示科学家探索物质组成与结构的历程
考点 课标要求 命题预测
原子、分子、离子、元素是中考必考内
掌握分子的概念,理解原子的概念,了解
分子
容,分值为 2~7 分,题型主要以选择
微粒的共性,能从微观的角度解释化学变化的
题、填空题及简答题的形式呈现,在综合
实质。
原子和离子 命题中也会出现。预计 2025年中考中,
了解原子的结构,熟练运用原子核外电子
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
分子以分子的性质为主要考点进行考查,
原子以原子结构为主要考点进行考查,离
子以离子符号、离子所带的电荷为主要考
元素
点进行考查,元素以元素的宏观意义,联
排布的基本规律,理解离子的概念并能判断阴 系到化合价、元素质量的计算为主要考点
阳离子,画出前20号元素的原子核外电子排布 进行考查。
元素周期表
示意图。
识记地壳中含量前五位元素,理解元素的
概念,理解元素符号的含义。认识元素周期表
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点一 分子
一、分子
1、概念
分子:由分子构成的物质分子是保持其化学性质的最小粒子。
原子:化学变化中最小的粒子。
2、认识微观粒子的基本特征(以分子为例)
(1)分子质量和体积都很小;
(2)分子之间都有间隔;一般情况下,同种物质不同状态的分子间隔:气态>液态>固态。温度升高,分
子间隔增大;压强增大,分子间隔缩小。
(3)分子总在不断的运动,且温度越高,运动越快。
(4)保持物质化学性质的微粒,决定于构成该物质的微粒是什么,如由分子构成的物质,保持其化学性
质的最小微粒就是分子,由原子构成的物质,保持其化学性质的最小微粒就是原子。保持水的化学性质的
粒子是水分子;保持铁的化学性质的粒子是铁原子。同种分子化学性质相同,不同种分子化学性质不同。
3、分子与原子的区别与联系:
区别:在化学变化中分子还可以再分,原子不可再分;
联系:分子是由原子构成的,在化学变化中,分子分裂成原子,原子重新组合成新的分子。
1.“分子大,原子小”的说法是错误:原子不一定比分子小,世界最大的原子是钫原子(Fr,半径
1.53A),
最小的分子是氢分子(H,半径1.15A)。
2
2.分子是由原子构成的,但原子只能构成分子的说法错误,原子也可以直接构成物质(比如:金属、非
金属固体单质和稀有气体都是由原子构成。)
1.(2024·青海西宁)物质的微粒观是重要的化学观念之一。下列关于宏观事实的微观解释正确的是
A.液态水变成水蒸气——分子体积变大
B.臭氧和氧气化学性质不同——分子构成不同
C.水银温度计汞柱升高——分子间隔增大
D.分离液态空气制氧气——分子可以再分
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点二 原子和离子
一、原子发现史
1、道尔顿:原子不可再分,是最小的实心球体。
2、汤姆森:英国科学家汤姆森发现了电子,认为原子在一定的条件下是可分的。并设计了一个原子模
型,认为原子像葡萄干布丁,其中葡萄干是带负电的电子,布丁是带正电的物质。
3、卢瑟福:α粒子轰击金箔实验
(1)现象:①大部分α粒子穿过金箔,不改变原来方向;
②部分α粒子改变了原来前进的方向;
③甚至有极少数α粒子被反弹回来。
(2)现象分析: ①大多数α粒子能顺利穿过金箔,说明原子内部有很大的空间。
②带正电的α粒子与带正电的原子核产生斥力,方向偏转。
③极少数α粒子被反弹过来说原子核的质量比α粒子大很多。
(3)结论:原子是由原子核和核外电子构成。
二、原子结构
原子核(带正电) 质子(带正电)
1、原子(不显电性) 中子(不带电)
核外电子(带负电)
2、核电荷数:原子核所带电荷数。
3、原子质量几乎全部集中在原子核上,但原子核体积很小,原子的体积由核外电子决定。
4、在原子中,质子数=核外电子数=核电荷数
三、相对原子质量
1、定义:一个原子质量与一个 碳 1 2 原子 的质量的1/12 的比值就是相对原子质量。
2、近似算法公式:相对原子质量=质子数+中子数。
3、理解 (1)相对原子质量不是个质量是个比值;
(2)有单位,是“1”常省略不写;
(3)相对原子质量之比等于原子实际质量之比;
(4)引入相对原子质量是为了书写、记忆和运算方便。
四、原子核外电子的排布
1、在多电子的原子中,核外电子的能量不同,能量高的离核远,能量低的离核近。通常把电子在离核远
近不同的区域运动称为电子的分层排布。
2、排布规律:(1)第1层最多2 个电子;(2)第2层最多8 个电子;(3)最外层最多8 个。
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
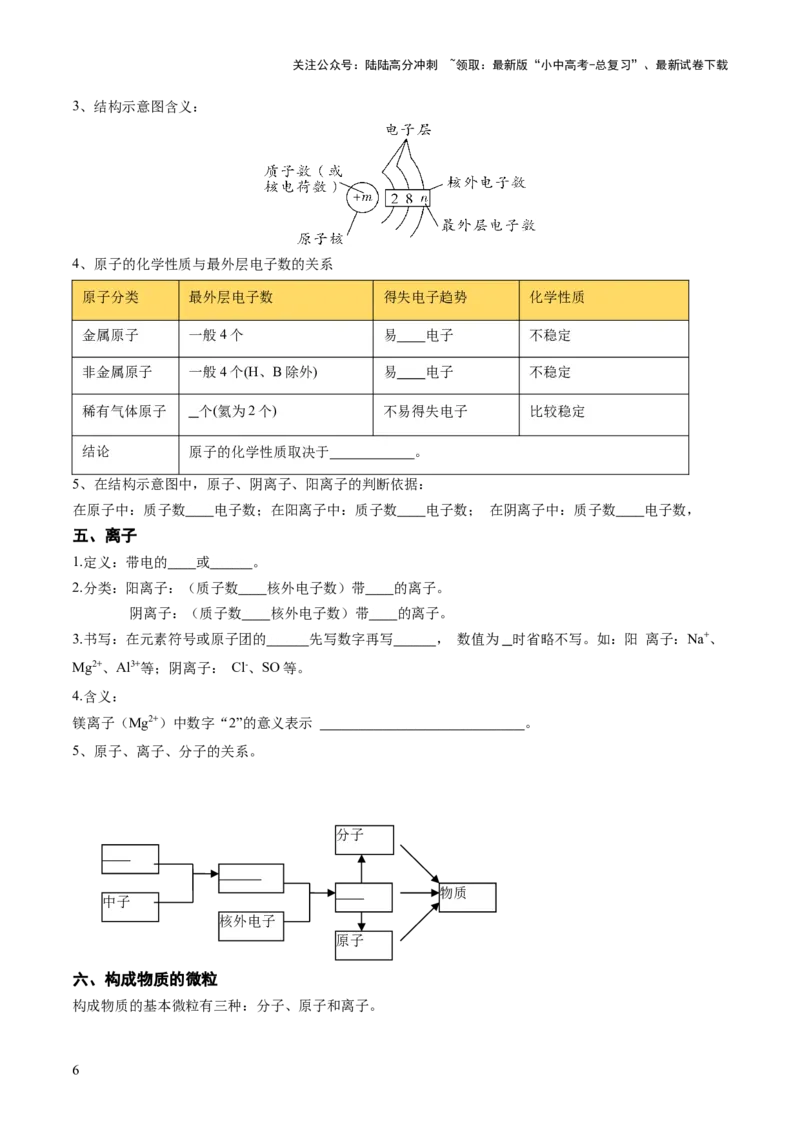
3、结构示意图含义:
4、原子的化学性质与最外层电子数的关系
原子分类 最外层电子数 得失电子趋势 化学性质
金属原子 一般4个 易失去电子 不稳定
非金属原子 一般4个(H、B除外) 易得到电子 不稳定
稀有气体原子 8 个(氦为2个) 不易得失电子 比较稳定
结论 原子的化学性质取决于最外层电子数。
5、在结构示意图中,原子、阴离子、阳离子的判断依据:
在原子中:质子数等于电子数;在阳离子中:质子数大于电子数; 在阴离子中:质子数小于电子数,
五、离子
1.定义:带电的原子或原子团。
2.分类:阳离子:(质子数大于核外电子数)带正电的离子。
阴离子:(质子数小于核外电子数)带负电的离子。
3.书写:在元素符号或原子团的右上角先写数字再写正负号, 数值为1 时省略不写。如:阳 离子:Na+、
Mg2+、Al3+等;阴离子: Cl-、SO等。
4.含义:
镁离子(Mg2+)中数字“2”的意义表示 一个镁离子带两个单位的正电荷 。
5、原子、离子、分子的关系。
分子
质子
原子核
原子 物质
中子
核外电子
原子
六、构成物质的微粒
构成物质的基本微粒有三种:分子、原子和离子。
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1、由原子构成的物质有:
种类 示例 构成微粒 物质符号 符号书写特点
①金属单质 铜 铜原子 Cu
铁 铁原子 Fe
②大多数的固态非金属单质 石墨 碳原子 C
元素符号
(常温) 红磷 磷原子 P
③稀有气体 氦气 氦原子 He
氩气 氩原子 Ar
2、由分子构成的物质有:
种类 示例 构成微粒 物质符号
①大多数的气态单质(常 氧气 氧分子 O
2
温) 足球烯 足球烯分子 C
60
②大多数的非金属氧化物 水 水分子 HO
2
二氧化碳 二氧化碳分子 CO
2
③酸 盐酸 盐酸分子或氯化氢分子 HCl
硫酸 硫酸分子 HSO
2 4
3、由离子构成的物质:
种类 示例 构成微粒
①大多数的金属氧化物 氧化镁 氧离子和镁离子
②大多数的碱 氢氧化钠 钠离子和氢氧根离子
③大多数的盐 氯化钠 氯离子和钠离子
硫酸铜 铜离子和硫酸根离子
1.原子由原子核和核外电子构成,原子核由质子和中子构成。但是原子核内一定有质子,不一定有中子。
(如普通氢原子就无中子)。
2.相对原子质量不是个质量是个比值;有单位,是“1”常省略不写;
3.最外层电子数为8的粒子不一定是稀有气体原子,也可能是阳离子或阴离子;稳定结构的原子最外层电
子数不一定是8。(如第一层为最外层,则只有2 个电子,例如氦原子)
1.(2024·四川巴中)我国探月工程嫦娥五号返回器曾携带1731g月壤样品返回地球。月壤中含量丰富的
氦-3可作为核聚变燃料,其原子核是由2个质子和1个中子构成的,氦-3的原子结构示意图为
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A. B. C. D.
2.(2024·北京·中考真题)为实现高效光催化分解水制氢,科研人员开展 纳米复合光催化材料的研
究。铌(Nb)在元素周期表中的原子序数是41,下列关于Nb的说法不正确的是( )
A.质子数是41 B.核电荷数是41
C.原子质量是41 D.核外电子数是41
考点三 元素
一、元素
1、定义:具有相同质子数的一类原子的总称(元素是宏观概念只论种数不论个数)。
注意:元素的根本区别是质子数不同;质子数决定元素的种类,同种元素的原子质子数一定相同。
2、分类:
(1)金属元素:“钅”(金和汞除外);最外层电子数1-3;
(2)非金属元素:“气”“氵”“石””;最外层电子数4-7;
(3)稀有气体元素:He、Ne、Ar;最外层电子数8(He、2个);
3、元素符号:
(1)书写:拉丁字母;
(2)书写原则:“一大二小”一个字母的大写,二个字母的第一个大写,第二个小写。
(3)意义:
①宏观:一种元素。
②微观:一个原子。
③由原子构成的物质:其元素符号还表示一种物质。
④元素符号前出现数字:只表示微观意义。
如:H:表示氢元素,一个氢原子; Fe:表示铁元素,一个铁原子,铁这种物质。
4、元素分布:
(1)地壳中元素含量由高到低是O、Si、Al、Fe、Ca。地壳中含量最多的元素是O 和最多的金属元素
Al;
(2)海水中最多的元素O 和最多的金属元素是Na;
(3)空气中含量最多的元素N;
(3)人体中最多的元素O 和最多的金属元素Ca;
(4)最原始的元素H,即相对原子质量最小的元素;
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1.元素是宏观概念只论种数不论个数。元素符号(表示一种元素;一个原子)前面出现了数字,就只表示
微观概念(几个原子)。
2.是否为同种元素,只需要看质子数是否相同。而元素的化学性质由最外层电子数决定,化学性质相似,
则最外层电子数一样。
3.元素符号的书写原则(可以概括为“一大二小”),必须书写规范。
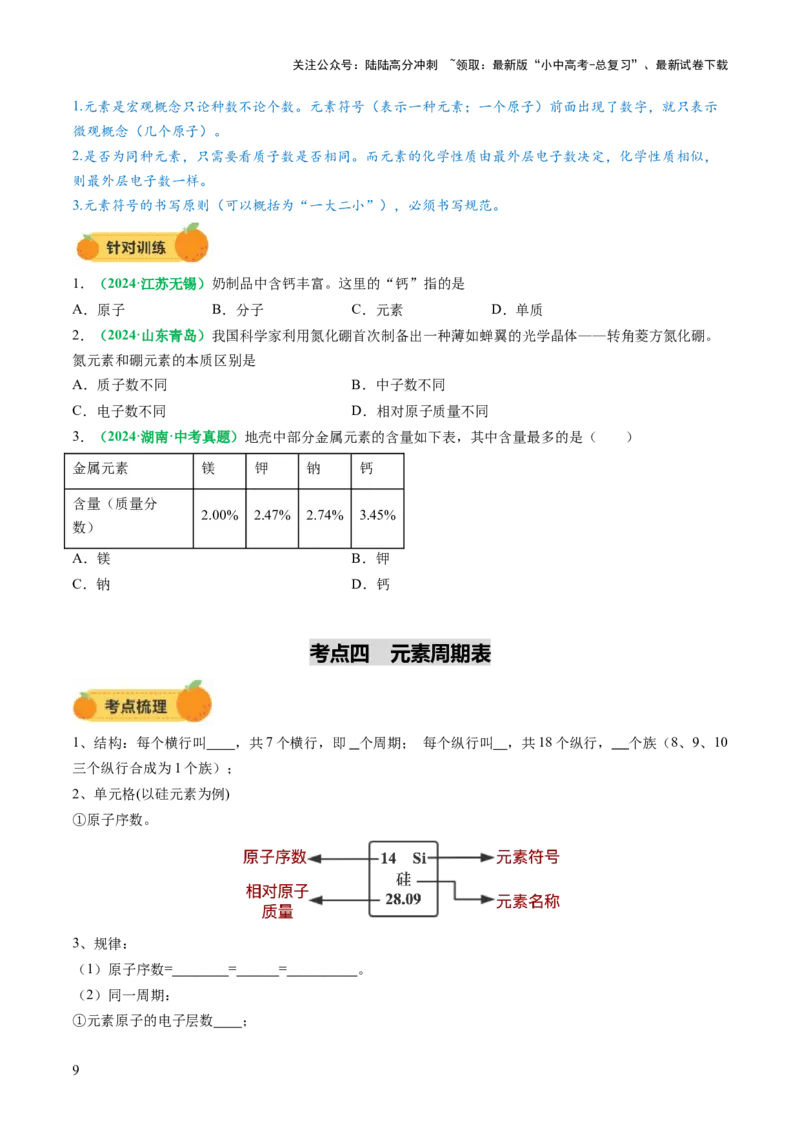
1.(2024·江苏无锡)奶制品中含钙丰富。这里的“钙”指的是
A.原子 B.分子 C.元素 D.单质
2.(2024·山东青岛)我国科学家利用氮化硼首次制备出一种薄如蝉翼的光学晶体——转角菱方氮化硼。
氮元素和硼元素的本质区别是
A.质子数不同 B.中子数不同
C.电子数不同 D.相对原子质量不同
3.(2024·湖南·中考真题)地壳中部分金属元素的含量如下表,其中含量最多的是( )
金属元素 镁 钾 钠 钙
含量(质量分
2.00% 2.47% 2.74% 3.45%
数)
A.镁 B.钾
C.钠 D.钙
考点四 元素周期表
1、结构:每个横行叫周期,共7个横行,即7 个周期; 每个纵行叫族,共18个纵行,16 个族(8、9、10
三个纵行合成为1个族);
2、单元格(以硅元素为例)
①原子序数。
3、规律:
(1)原子序数=核电荷数=质子数=核外电子数。
(2)同一周期:
①元素原子的电子层数相同;
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
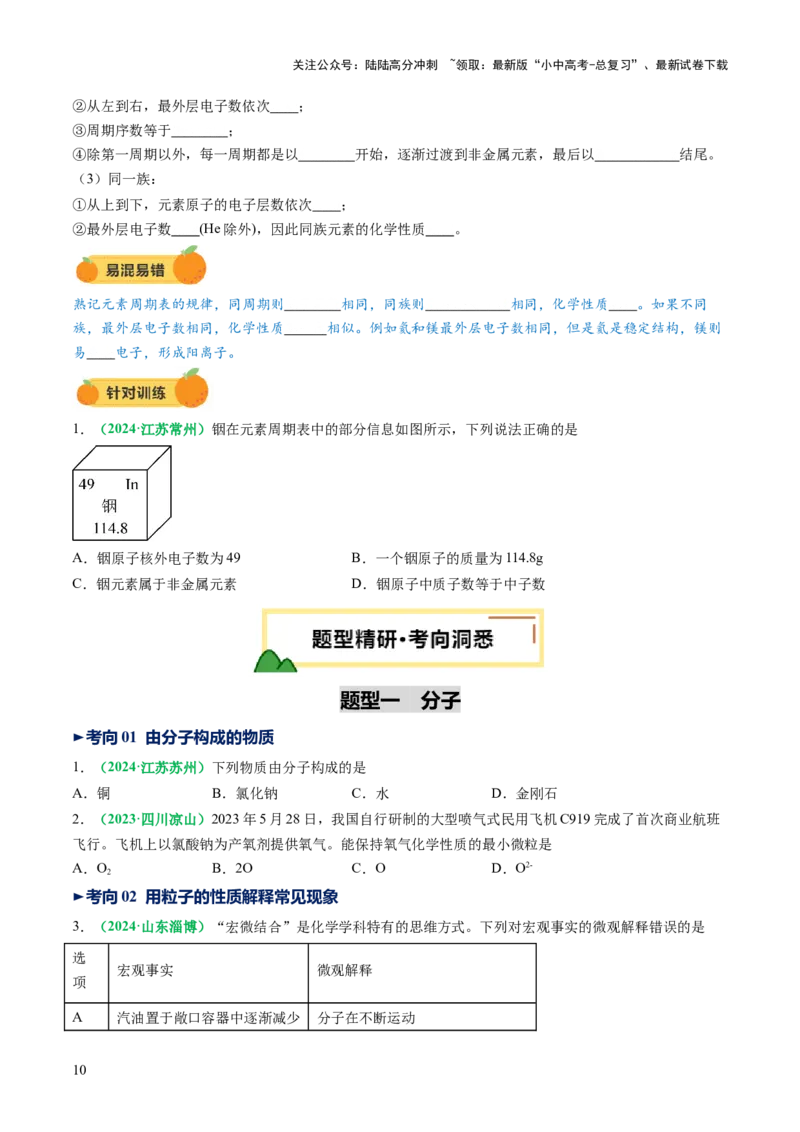
②从左到右,最外层电子数依次增加;
③周期序数等于电子层数;
④除第一周期以外,每一周期都是以金属元素开始,逐渐过渡到非金属元素,最后以稀有气体元素结尾。
(3)同一族:
①从上到下,元素原子的电子层数依次增加;
②最外层电子数相同(He除外),因此同族元素的化学性质相似。
熟记元素周期表的规律,同周期则电子层数相同,同族则最外层电子数相同,化学性质相似。如果不同
族,最外层电子数相同,化学性质不一定相似。例如氦和镁最外层电子数相同,但是氦是稳定结构,镁则
易失去电子,形成阳离子。
1.(2024·江苏常州)铟在元素周期表中的部分信息如图所示,下列说法正确的是
A.铟原子核外电子数为49 B.一个铟原子的质量为114.8g
C.铟元素属于非金属元素 D.铟原子中质子数等于中子数
题型一 分子
►考向01 由分子构成的物质
1.(2024·江苏苏州)下列物质由分子构成的是
A.铜 B.氯化钠 C.水 D.金刚石
2.(2023·四川凉山)2023年5月28日,我国自行研制的大型喷气式民用飞机C919完成了首次商业航班
飞行。飞机上以氯酸钠为产氧剂提供氧气。能保持氧气化学性质的最小微粒是
A.O B.2O C.O D.O2-
2
►考向02 用粒子的性质解释常见现象
3.(2024·山东淄博)“宏微结合”是化学学科特有的思维方式。下列对宏观事实的微观解释错误的是
选
宏观事实 微观解释
项
A 汽油置于敞口容器中逐渐减少 分子在不断运动
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B 碳酸分解生成水和二氧化碳 化学反应前后,分子种类发生改变
C 气体压缩储存于钢瓶中 压强增大,气体分子变小
D 氧气和臭氧化学性质不同 分子结构不同
4.(2024·四川自贡)我国是茶文化的发源地,中国茶清香四溢。从微观角度解释闻到香味的原因是
A.分子的质量和体积都很小
B.分子可以分成原子
C.分子之间有间隙
D.分子在不断运动
5.(2024·青海)湿衣服晾干,从微观角度解释正确的是
A.分子的体积变大
B.分子分解成原子
C.分子在不断运动
D.分子消失
题型二 原子和分子
►考向01 原子的构成
6.(2024·北京)为实现高效光催化分解水制氢,科研人员开展 纳米复合光催化材料的研究。铌
(Nb)在元素周期表中的原子序数是41,下列关于Nb的说法不正确的是
A.质子数是41 B.核电荷数是41 C.原子质量是41 D.核外电子数是41
►考向02 离子
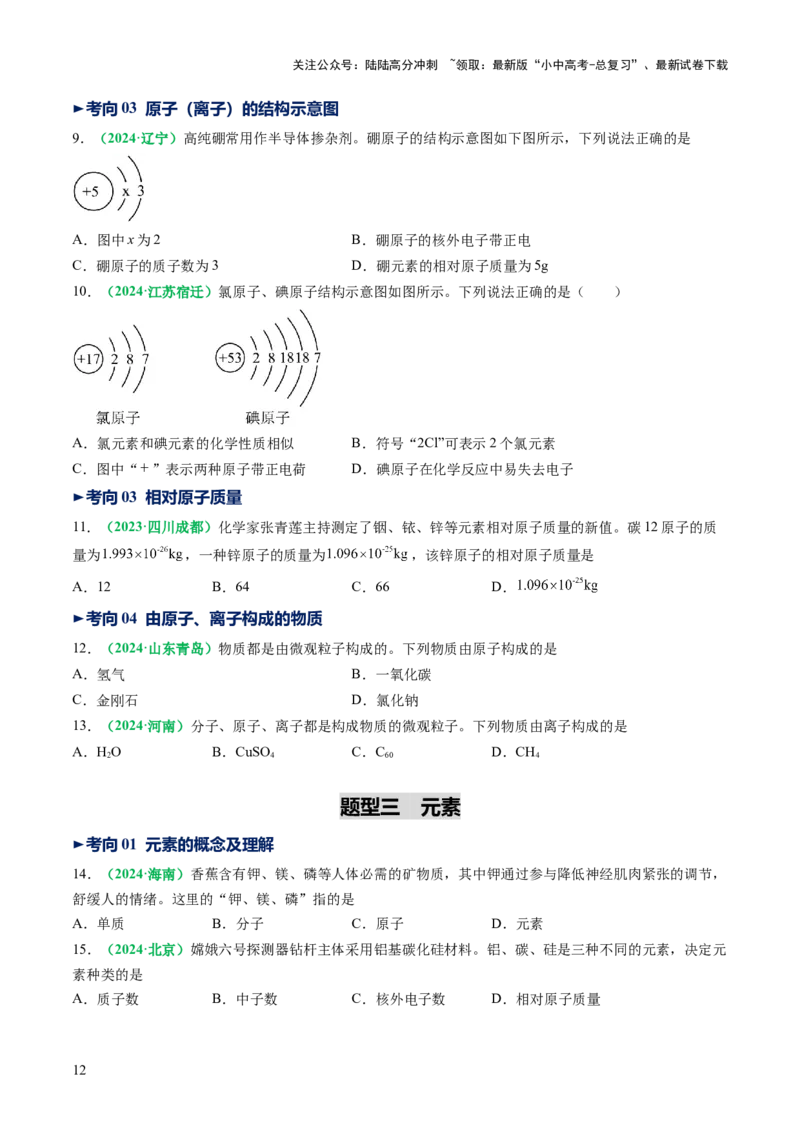
7.(2024·云南)如图为金属钠与氯气反应生成氯化钠的示意图,下列说法错误的是
A.每个氯离子带一个单位负电荷
B.钠原子在该反应中形成了阴离子
C.氯化钠是由钠离子和氯离子构成的
D.钠离子和氯离子的结构都相对稳定
8.(2024·辽宁)下列选项中,表示两个钠离子的是
A. B.Na C. D.
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
►考向03 原子(离子)的结构示意图
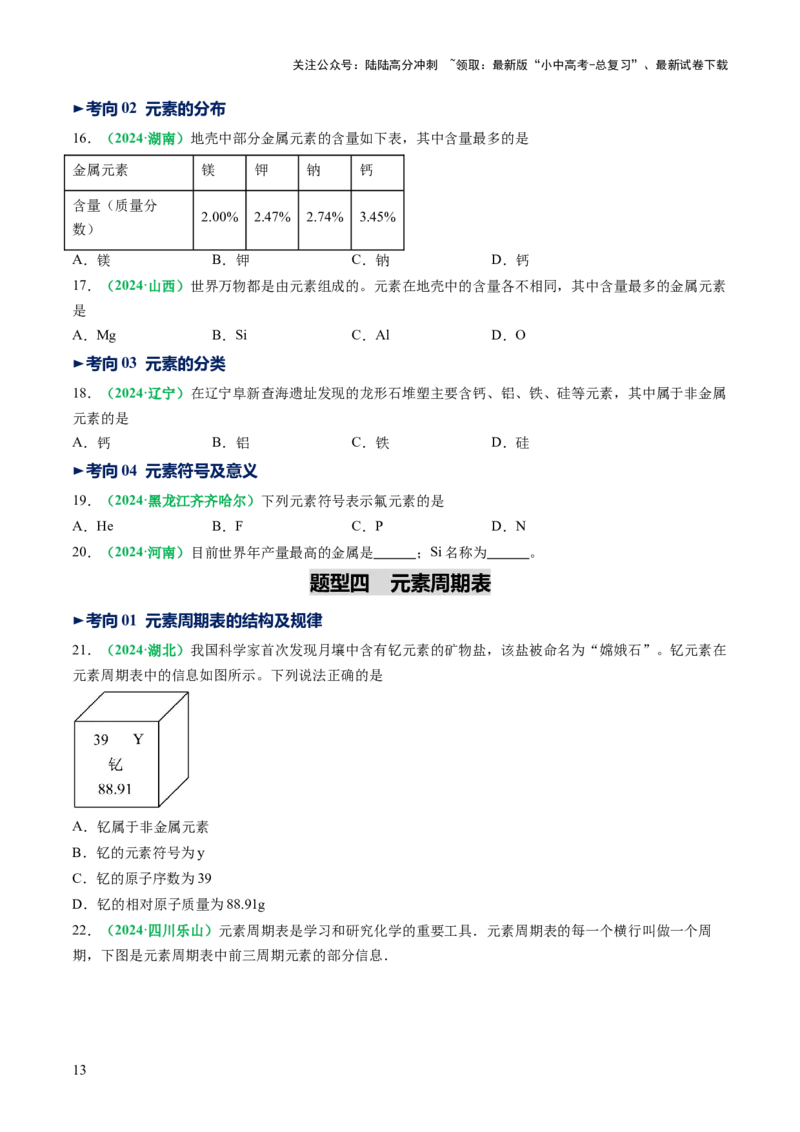
9.(2024·辽宁)高纯硼常用作半导体掺杂剂。硼原子的结构示意图如下图所示,下列说法正确的是
A.图中x为2 B.硼原子的核外电子带正电
C.硼原子的质子数为3 D.硼元素的相对原子质量为5g
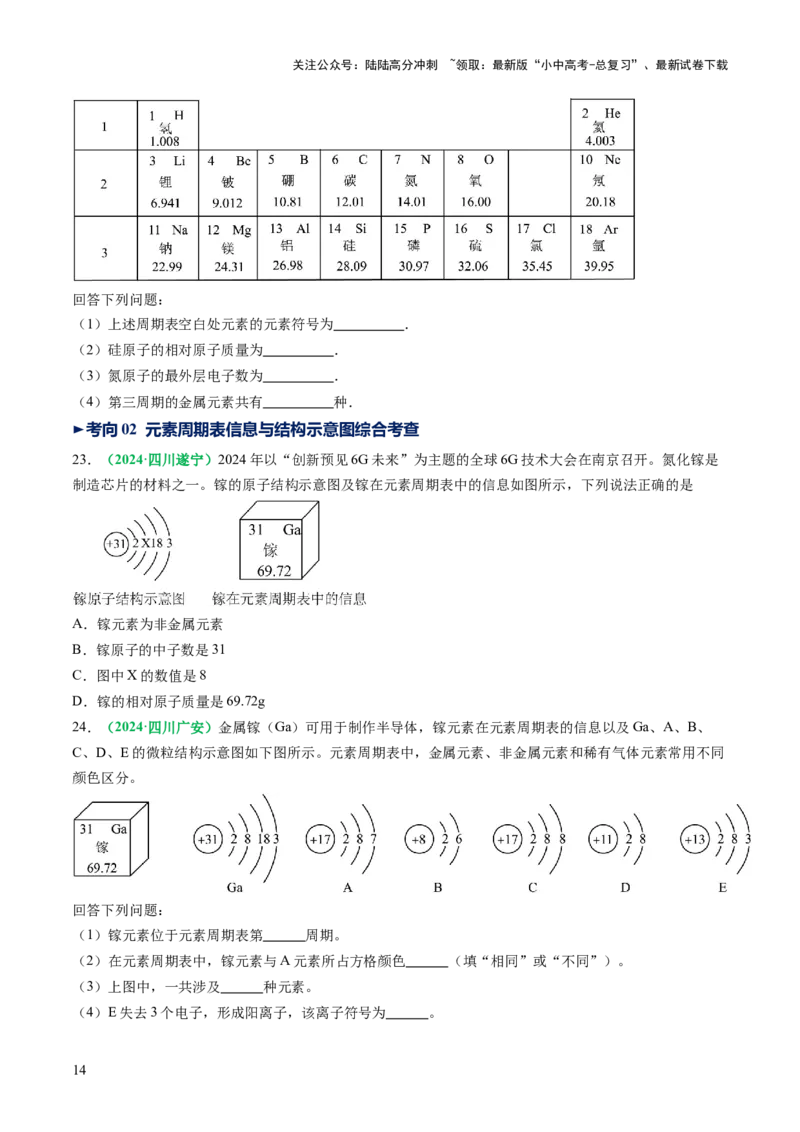
10.(2024·江苏宿迁)氯原子、碘原子结构示意图如图所示。下列说法正确的是( )
A.氯元素和碘元素的化学性质相似 B.符号“2Cl”可表示2个氯元素
C.图中“ ”表示两种原子带正电荷 D.碘原子在化学反应中易失去电子
►考向03 相对原子质量
11.(2023·四川成都)化学家张青莲主持测定了铟、铱、锌等元素相对原子质量的新值。碳12原子的质
量为 ,一种锌原子的质量为 ,该锌原子的相对原子质量是
A.12 B.64 C.66 D.
►考向04 由原子、离子构成的物质
12.(2024·山东青岛)物质都是由微观粒子构成的。下列物质由原子构成的是
A.氢气 B.一氧化碳
C.金刚石 D.氯化钠
13.(2024·河南)分子、原子、离子都是构成物质的微观粒子。下列物质由离子构成的是
A.HO B.CuSO C.C D.CH
2 4 60 4
题型三 元素
►考向01 元素的概念及理解
14.(2024·海南)香蕉含有钾、镁、磷等人体必需的矿物质,其中钾通过参与降低神经肌肉紧张的调节,
舒缓人的情绪。这里的“钾、镁、磷”指的是
A.单质 B.分子 C.原子 D.元素
15.(2024·北京)嫦娥六号探测器钻杆主体采用铝基碳化硅材料。铝、碳、硅是三种不同的元素,决定元
素种类的是
A.质子数 B.中子数 C.核外电子数 D.相对原子质量
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
►考向02 元素的分布
16.(2024·湖南)地壳中部分金属元素的含量如下表,其中含量最多的是
金属元素 镁 钾 钠 钙
含量(质量分
2.00% 2.47% 2.74% 3.45%
数)
A.镁 B.钾 C.钠 D.钙
17.(2024·山西)世界万物都是由元素组成的。元素在地壳中的含量各不相同,其中含量最多的金属元素
是
A.Mg B.Si C.Al D.O
►考向03 元素的分类
18.(2024·辽宁)在辽宁阜新查海遗址发现的龙形石堆塑主要含钙、铝、铁、硅等元素,其中属于非金属
元素的是
A.钙 B.铝 C.铁 D.硅
►考向04 元素符号及意义
19.(2024·黑龙江齐齐哈尔)下列元素符号表示氟元素的是
A.He B.F C.P D.N
20.(2024·河南)目前世界年产量最高的金属是 ;Si名称为 。
题型四 元素周期表
►考向01 元素周期表的结构及规律
21.(2024·湖北)我国科学家首次发现月壤中含有钇元素的矿物盐,该盐被命名为“嫦娥石”。钇元素在
元素周期表中的信息如图所示。下列说法正确的是
A.钇属于非金属元素
B.钇的元素符号为y
C.钇的原子序数为39
D.钇的相对原子质量为88.91g
22.(2024·四川乐山)元素周期表是学习和研究化学的重要工具.元素周期表的每一个横行叫做一个周
期,下图是元素周期表中前三周期元素的部分信息.
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
回答下列问题:
(1)上述周期表空白处元素的元素符号为 .
(2)硅原子的相对原子质量为 .
(3)氮原子的最外层电子数为 .
(4)第三周期的金属元素共有 种.
►考向02 元素周期表信息与结构示意图综合考查
23.(2024·四川遂宁)2024年以“创新预见6G未来”为主题的全球6G技术大会在南京召开。氮化镓是
制造芯片的材料之一。镓的原子结构示意图及镓在元素周期表中的信息如图所示,下列说法正确的是
A.镓元素为非金属元素
B.镓原子的中子数是31
C.图中X的数值是8
D.镓的相对原子质量是69.72g
24.(2024·四川广安)金属镓(Ga)可用于制作半导体,镓元素在元素周期表的信息以及Ga、A、B、
C、D、E的微粒结构示意图如下图所示。元素周期表中,金属元素、非金属元素和稀有气体元素常用不同
颜色区分。
回答下列问题:
(1)镓元素位于元素周期表第 周期。
(2)在元素周期表中,镓元素与A元素所占方格颜色 (填“相同”或“不同”)。
(3)上图中,一共涉及 种元素。
(4)E失去3个电子,形成阳离子,该离子符号为 。
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
跨学科实践活动
制作模型并展示科学家探索物质组成与结构的历程
【内容结构】
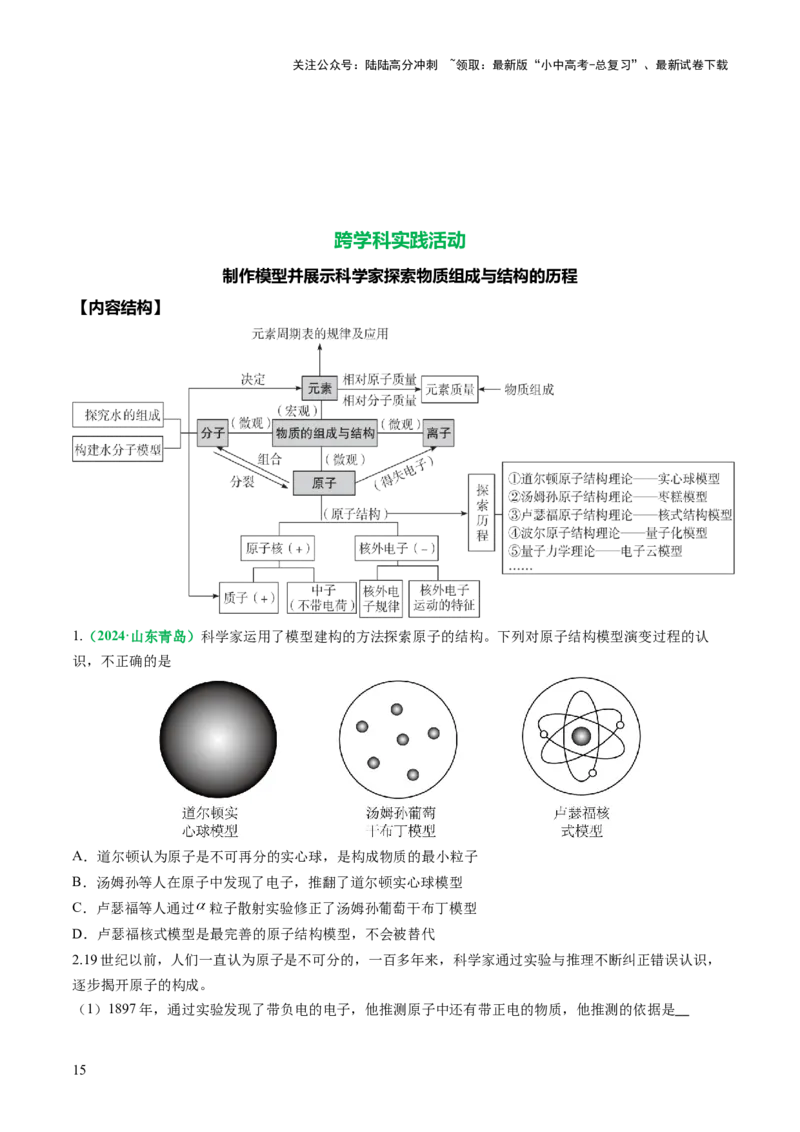
1.(2024·山东青岛)科学家运用了模型建构的方法探索原子的结构。下列对原子结构模型演变过程的认
识,不正确的是
A.道尔顿认为原子是不可再分的实心球,是构成物质的最小粒子
B.汤姆孙等人在原子中发现了电子,推翻了道尔顿实心球模型
C.卢瑟福等人通过 粒子散射实验修正了汤姆孙葡萄干布丁模型
D.卢瑟福核式模型是最完善的原子结构模型,不会被替代
2.19世纪以前,人们一直认为原子是不可分的,一百多年来,科学家通过实验与推理不断纠正错误认识,
逐步揭开原子的构成。
(1)1897年,通过实验发现了带负电的电子,他推测原子中还有带正电的物质,他推测的依据是
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
。
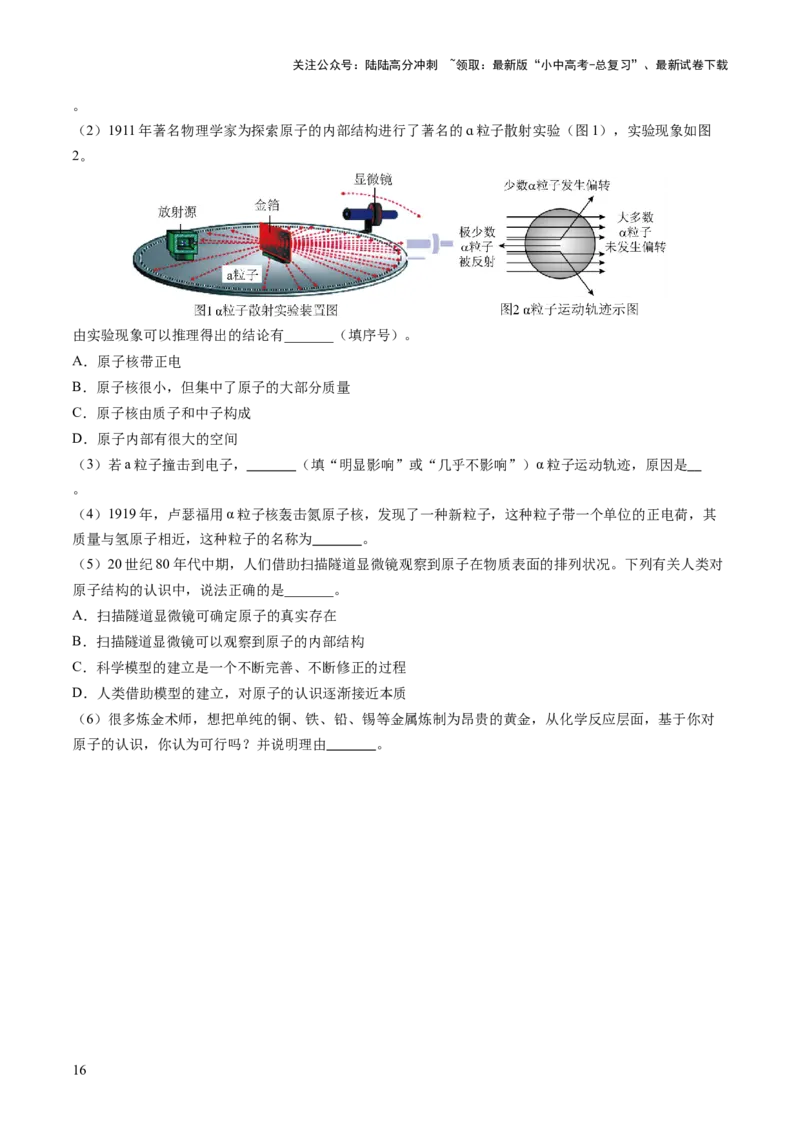
(2)1911年著名物理学家为探索原子的内部结构进行了著名的ɑ粒子散射实验(图1),实验现象如图
2。
由实验现象可以推理得出的结论有_______(填序号)。
A.原子核带正电
B.原子核很小,但集中了原子的大部分质量
C.原子核由质子和中子构成
D.原子内部有很大的空间
(3)若a粒子撞击到电子, (填“明显影响”或“几乎不影响”)α粒子运动轨迹,原因是
。
(4)1919年,卢瑟福用α粒子核轰击氮原子核,发现了一种新粒子,这种粒子带一个单位的正电荷,其
质量与氢原子相近,这种粒子的名称为 。
(5)20世纪80年代中期,人们借助扫描隧道显微镜观察到原子在物质表面的排列状况。下列有关人类对
原子结构的认识中,说法正确的是_______。
A.扫描隧道显微镜可确定原子的真实存在
B.扫描隧道显微镜可以观察到原子的内部结构
C.科学模型的建立是一个不断完善、不断修正的过程
D.人类借助模型的建立,对原子的认识逐渐接近本质
(6)很多炼金术师,想把单纯的铜、铁、铅、锡等金属炼制为昂贵的黄金,从化学反应层面,基于你对
原子的认识,你认为可行吗?并说明理由 。
16