文档内容
江苏省 2023 年普通高中学业水平选择性考试
化学试题
本试卷共 100分,考试时间 75分钟。
可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 Mg-24 S-32 Cl-35.5 K-39 V-51 Fe-56
一、单项选择题:共 13题,每题 3分,共 39分。每题只有一个选项最符合题意。
1.我国提出2060年实现碳中和的目标,体现了大国担当。碳中和中的碳是指( )
A.碳原子 B.二氧化碳 C.碳元素 D.含碳物质
2.反应NH Cl+NaNO NaCl+N +2H O应用于石油开采。下列说法正确的是( )
4 2 2 2
A.NH+的电子式为 B.NO-中N元素的化合价为+5
4 2
C.N 分子中存在NN键 D.H O为非极性分子
2 2
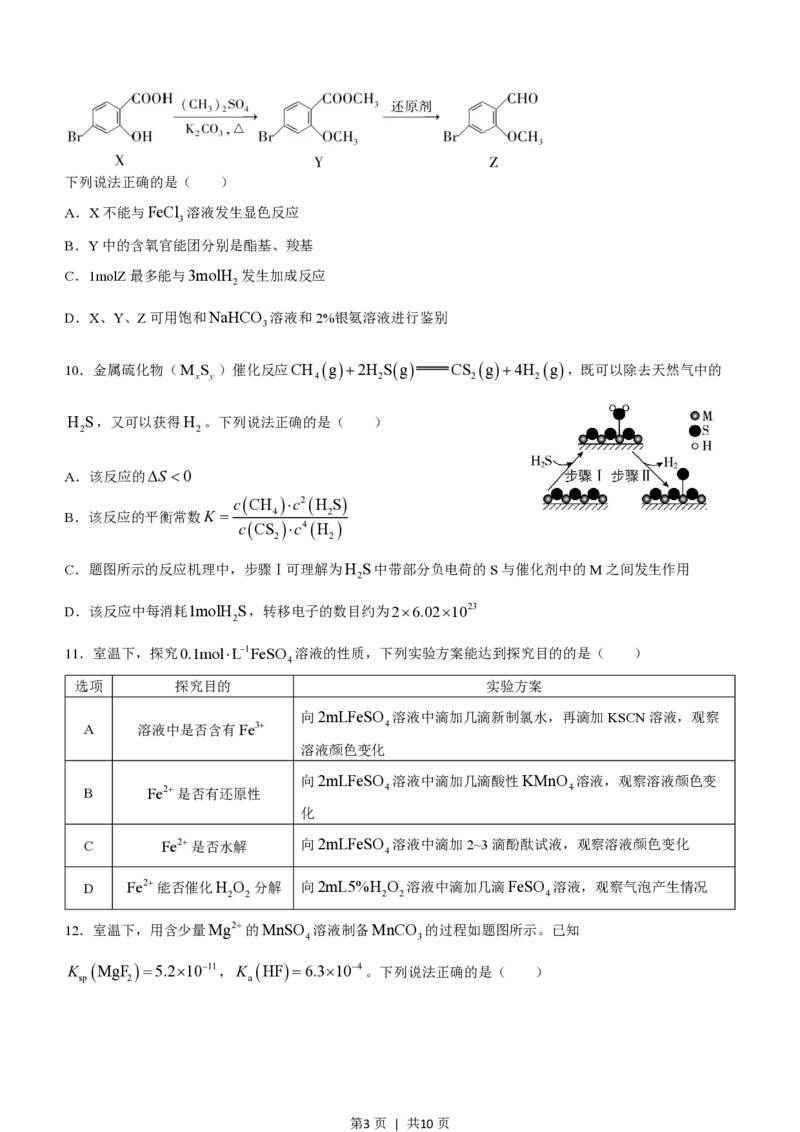
3.实验室制取Cl 的实验原理及装置均正确的是( )
2
A. 制取Cl B. 除去Cl 中的HCl
2 2
C. 收集Cl D. 吸收尾气中的Cl
2 2
4.元素C、Si、Ge位于周期表中ⅣA族。下列说法正确的是( )
A.原子半径:rC>rSi>rGe B.第一电离能:I C> I Si> I Ge
1 1 1
C.碳单质、晶体硅、SiC均为共价晶体 D.可在周期表中元素Si附近寻找新半导体材料
阅读下列材料,完成5~7题:
氢元素及其化合物在自然界广泛存在且具有重要应用。1H、2H、3H是氢元素的3种核素,基态H原子
1 1 1
1s1的核外电子排布,使得H既可以形成H+又可以形成H-,还能形成H O、H O 、NH 、 N H 、
2 2 2 3 2 4
CaH 等重要化合物;水煤气法、电解水、光催化分解水都能获得H ,如水煤气法制氢反应中,H Og
2 2 2
与足量Cs反应生成1molH g和1molCOg吸收131.3kJ的热量。H 在金属冶炼、新能源开发、碳中
2 2
第1页 | 共10页和等方面具有重要应用,如HCO-在催化剂作用下与H 反应可得到HCOO-。我国科学家在氢气的制备和
3 2
应用等方面都取得了重大成果。
5.下列说法正确的是( )
A.1H、2H、3H都属于氢元素
1 1 1
B.NH+和H O的中心原子轨道杂化类型均为sp2
4 2
C.H O 分子中的化学键均为极性共价键
2 2
D.CaH 晶体中存在Ca与H 之间的强烈相互作用
2 2
6.下列化学反应表示正确的是( )
A.水煤气法制氢:Cs+H Og H g+COg DH =-131.3kJ×mol-1
2 2
催化剂
B.HCO-催化加氢生成HCOO-的反应:HCO- +H HCOO- +H O
3 3 2 2
C.电解水制氢的阳极反应:2H O-2e- H +2OH-
2 2
D.CaH 与水反应:CaH +2H O CaOH +H
2 2 2 2 2
7.下列物质结构与性质或物质性质与用途具有对应关系的是( )
A.H 具有还原性,可作为氢氧燃料电池的燃料
2
B.氨极易溶于水,液氨可用作制冷剂
C.H O分子之间形成氢键,H Og的热稳定性比H Sg的高
2 2 2
D. N H 中的N原子与H+形成配位键, N H 具有还原性
2 4 2 4
8.氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A.实验室探究稀硝酸与铜反应的气态产物:HNO 稀¾C¾u®NO¾O¾2®NO
3 2
B.工业制硝酸过程中的物质转化:N ¾¾O¾2 ¾®NO¾H¾2 O¾®HNO
2 放电或高温 3
催化剂
C.汽车尾气催化转化器中发生的主要反应:2NO+2CO N +2CO
2 2
△
D.实验室制备少量NH 的原理:2NH Cl+CaOH CaCl +2NH +2H O
3 4 2 2 3 2
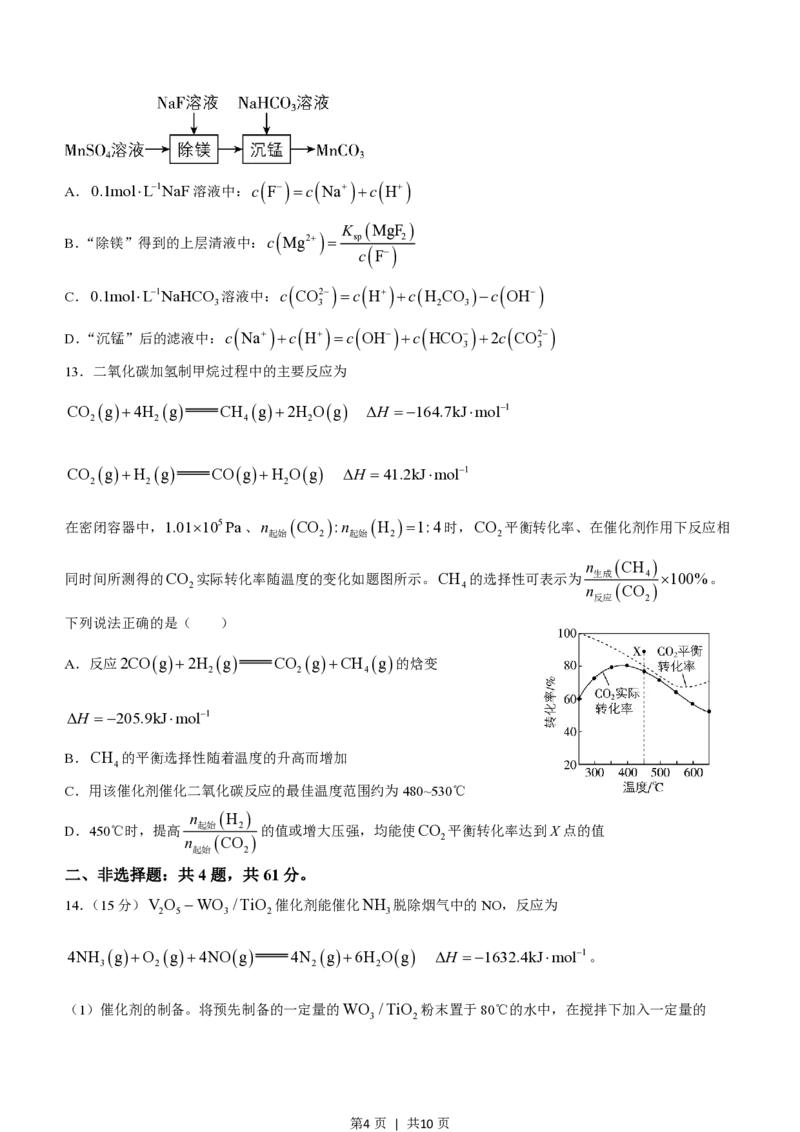
9.化合物Z是合成药物非奈利酮的重要中间体,其合成路线如下:
第2页 | 共10页下列说法正确的是( )
A.X不能与FeCl 溶液发生显色反应
3
B.Y中的含氧官能团分别是酯基、羧基
C.1molZ最多能与3molH 发生加成反应
2
D.X、Y、Z可用饱和NaHCO 溶液和2%银氨溶液进行鉴别
3
10.金属硫化物(M S )催化反应CH g+2H Sg CS g+4H g,既可以除去天然气中的
x y 4 2 2 2
H S,又可以获得H 。下列说法正确的是( )
2 2
A.该反应的DS <0
cCH ×c2H S
B.该反应的平衡常数K = 4 2
cCS ×c4H
2 2
C.题图所示的反应机理中,步骤Ⅰ可理解为H S中带部分负电荷的S与催化剂中的M之间发生作用
2
D.该反应中每消耗1molH S,转移电子的数目约为2´6.02´1023
2
11.室温下,探究0.1mol×L-1FeSO 溶液的性质,下列实验方案能达到探究目的的是( )
4
选项 探究目的 实验方案
向2mLFeSO 溶液中滴加几滴新制氯水,再滴加KSCN溶液,观察
A 溶液中是否含有Fe3+ 4
溶液颜色变化
向2mLFeSO 溶液中滴加几滴酸性KMnO 溶液,观察溶液颜色变
B Fe2+是否有还原性 4 4
化
C Fe2+是否水解 向2mLFeSO 溶液中滴加2~3滴酚酞试液,观察溶液颜色变化
4
D Fe2+能否催化H O 分解 向2mL5%H O 溶液中滴加几滴FeSO 溶液,观察气泡产生情况
2 2 2 2 4
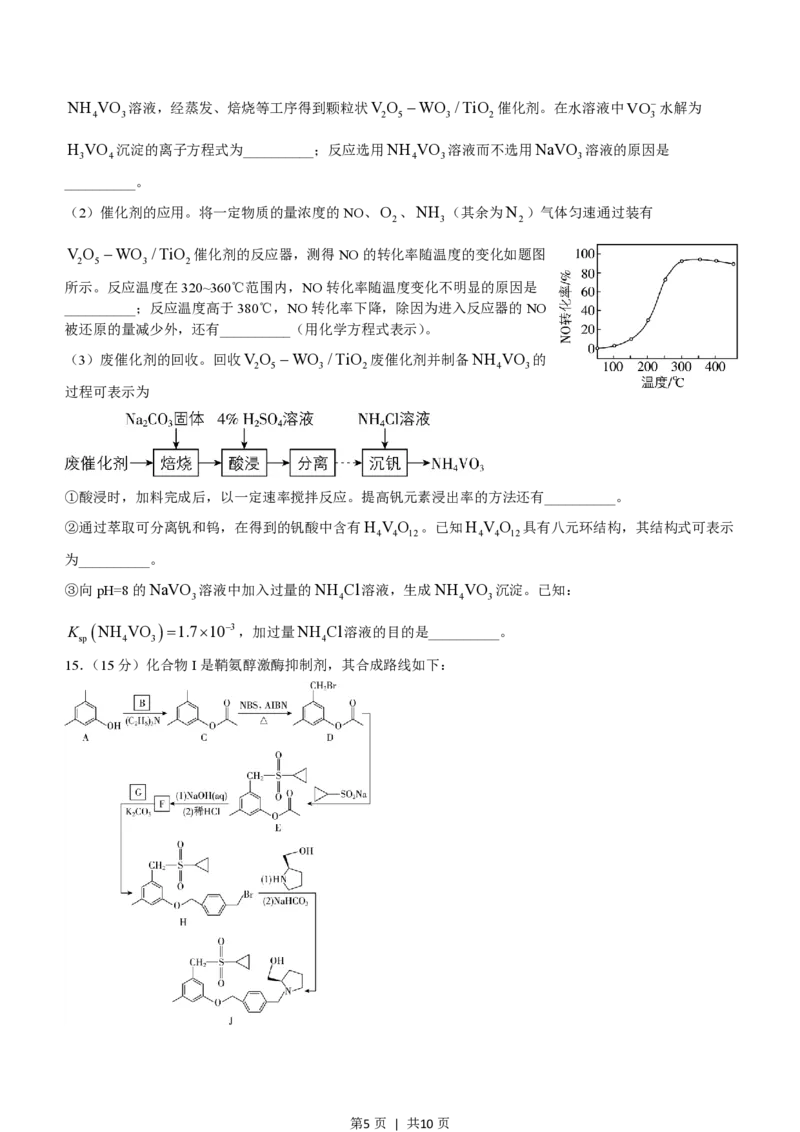
12.室温下,用含少量Mg2+的MnSO 溶液制备MnCO 的过程如题图所示。已知
4 3
K MgF =5.2´10-11,K HF=6.3´10-4。下列说法正确的是( )
sp 2 a
第3页 | 共10页A.0.1mol×L-1NaF溶液中:c F- =c Na+ +c H+
K MgF
B.“除镁”得到的上层清液中:c Mg2+ = sp 2
c
F-
C.0.1mol×L-1NaHCO 溶液中:c CO2- =c H+ +cH CO -c OH-
3 3 2 3
D.“沉锰”后的滤液中:c
Na+
+c
H+
=c
OH-
+c
HCO-
+2c
CO2-
3 3
13.二氧化碳加氢制甲烷过程中的主要反应为
CO g+4H g CH g+2H Og DH =-164.7kJ×mol-1
2 2 4 2
CO g+H g COg+H Og DH =41.2kJ×mol-1
2 2 2
在密闭容器中,1.01´105Pa、n CO :n H =1:4时,CO 平衡转化率、在催化剂作用下反应相
起始 2 起始 2 2
n CH
同时间所测得的CO 实际转化率随温度的变化如题图所示。CH 的选择性可表示为 生成 4 ´100%。
2 4 n CO
反应 2
下列说法正确的是( )
A.反应2COg+2H g CO g+CH g的焓变
2 2 4
DH =-205.9kJ×mol-1
B.CH 的平衡选择性随着温度的升高而增加
4
C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃
n H
D.450℃时,提高 起始 2 的值或增大压强,均能使CO 平衡转化率达到X点的值
n CO 2
起始 2
二、非选择题:共 4题,共 61分。
14.(15分)VO -WO /TiO 催化剂能催化NH 脱除烟气中的NO,反应为
2 5 3 2 3
4NH g+O g+4NOg 4N g+6H Og DH =-1632.4kJ×mol-1。
3 2 2 2
(1)催化剂的制备。将预先制备的一定量的WO /TiO 粉末置于80℃的水中,在搅拌下加入一定量的
3 2
第4页 | 共10页NH VO 溶液,经蒸发、焙烧等工序得到颗粒状VO -WO /TiO 催化剂。在水溶液中VO-水解为
4 3 2 5 3 2 3
H VO 沉淀的离子方程式为__________;反应选用NH VO 溶液而不选用NaVO 溶液的原因是
3 4 4 3 3
__________。
(2)催化剂的应用。将一定物质的量浓度的NO、O 、NH (其余为N )气体匀速通过装有
2 3 2
VO -WO /TiO 催化剂的反应器,测得NO的转化率随温度的变化如题图
2 5 3 2
所示。反应温度在320~360℃范围内,NO转化率随温度变化不明显的原因是
__________;反应温度高于380℃,NO转化率下降,除因为进入反应器的NO
被还原的量减少外,还有__________(用化学方程式表示)。
(3)废催化剂的回收。回收VO -WO /TiO 废催化剂并制备NH VO 的
2 5 3 2 4 3
过程可表示为
①酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有__________。
②通过萃取可分离钒和钨,在得到的钒酸中含有H V O 。已知H V O 具有八元环结构,其结构式可表示
4 4 12 4 4 12
为__________。
③向pH=8的NaVO 溶液中加入过量的NH Cl溶液,生成NH VO 沉淀。已知:
3 4 4 3
K NH VO =1.7´10-3,加过量NH Cl溶液的目的是__________。
sp 4 3 4
15.(15分)化合物I是鞘氨醇激酶抑制剂,其合成路线如下:
第5页 | 共10页(1)化合物A的酸性比环己醇的__________(填“强”或“弱”或“无差别”)。
(2)B的分子式为C H OCl,可由乙酸与SOCl 反应合成,B的结构简式为__________。
2 3 2
(3)A→C中加入C H N是为了结构反应中产生的__________(填化学式)。
2 5 3
(4)写出同时满足下列条件的C的一种同分异构体的结构简式:__________。碱性条件水解后酸化生成两
种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使2%酸性KMnO 溶液褪色;加热条件
4
下,铜催化另一产物与氧气反应,所得有机产物的核磁共振氢谱中只有1个峰。
(5)G的分子式为C H Br ,F→H的反应类型为__________。
8 8 2
(6)写出以 、 和CH =CH 为原料制备 的合成路线流图(须用
2 2
NBS和AlBN,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
16.(15分)实验室模拟“镁法工业烟气脱硫”并制备MgSO ×H O,其实验过程可表示为
4 2
(1)在搅拌下向氧化镁浆料中匀速缓慢通入SO 气体,生成MgSO ,反应为
2 3
MgOH +H SO MgSO +2H O
2 2 3 3 2
其平衡常数K与K éMgOH ù、K MgSO 、K H SO 、K H SO 的代数关系式为K =
sp ë 2 û sp 3 a1 2 3 a2 2 3
__________;下列实验操作一定能提高氧化镁浆料吸收SO 效率的有__________(填序号)。
2
A.水浴加热氧化镁浆料
B.加快搅拌速率
C.降低通入SO 气体的速率
2
D.通过多孔球泡向氧化镁浆料中通SO
2
(2)在催化剂作用下MgSO 被O 氧化为MgSO 。已知MgSO 的溶解度为0.57g(20℃),O 氧化溶液
3 2 4 3 2
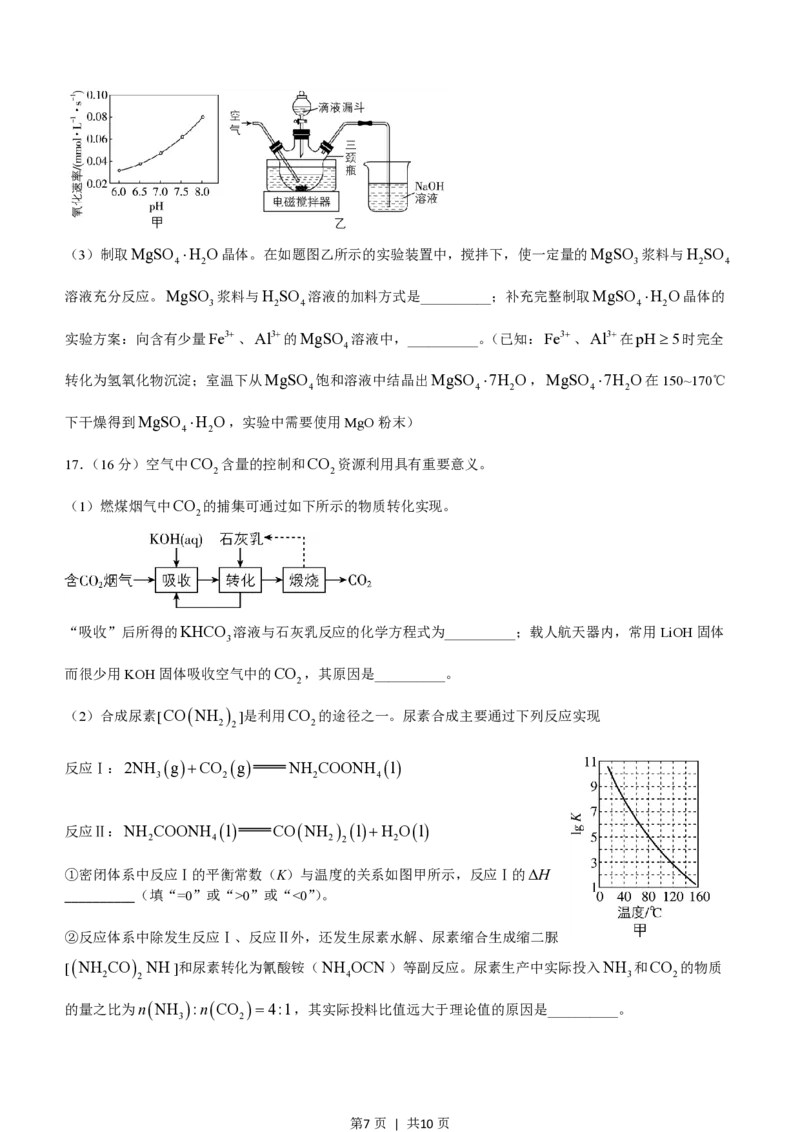
中SO2-的离子方程式为__________;在其他条件相同时,以负载钴的分子筛为催化剂,浆料中MgSO 被
3 3
O 氧化的速率随pH的变化如题图甲所示。在pH=6~8范围内,pH增大,浆料中MgSO 的氧化速率增大,
2 3
其主要原因是__________。
第6页 | 共10页(3)制取MgSO ×H O晶体。在如题图乙所示的实验装置中,搅拌下,使一定量的MgSO 浆料与H SO
4 2 3 2 4
溶液充分反应。MgSO 浆料与H SO 溶液的加料方式是__________;补充完整制取MgSO ×H O晶体的
3 2 4 4 2
实验方案:向含有少量Fe3+、Al3+的MgSO 溶液中,__________。(已知:Fe3+、Al3+在pH³5时完全
4
转化为氢氧化物沉淀;室温下从MgSO 饱和溶液中结晶出MgSO ×7H O,MgSO ×7H O在150~170℃
4 4 2 4 2
下干燥得到MgSO ×H O,实验中需要使用MgO粉末)
4 2
17.(16分)空气中CO 含量的控制和CO 资源利用具有重要意义。
2 2
(1)燃煤烟气中CO 的捕集可通过如下所示的物质转化实现。
2
“吸收”后所得的KHCO 溶液与石灰乳反应的化学方程式为__________;载人航天器内,常用LiOH固体
3
而很少用KOH固体吸收空气中的CO ,其原因是__________。
2
(2)合成尿素[CONH ]是利用CO 的途径之一。尿素合成主要通过下列反应实现
2 2 2
反应Ⅰ:2NH g+CO g NH COONH l
3 2 2 4
反应Ⅱ:NH COONH l CONH l+H Ol
2 4 2 2 2
①密闭体系中反应Ⅰ的平衡常数(K)与温度的关系如图甲所示,反应Ⅰ的DH
__________(填“=0”或“>0”或“<0”)。
②反应体系中除发生反应Ⅰ、反应Ⅱ外,还发生尿素水解、尿素缩合生成缩二脲
[ NH CO NH]和尿素转化为氰酸铵(NH OCN)等副反应。尿素生产中实际投入NH 和CO 的物质
2 2 4 3 2
的量之比为nNH :nCO =4:1,其实际投料比值远大于理论值的原因是__________。
3 2
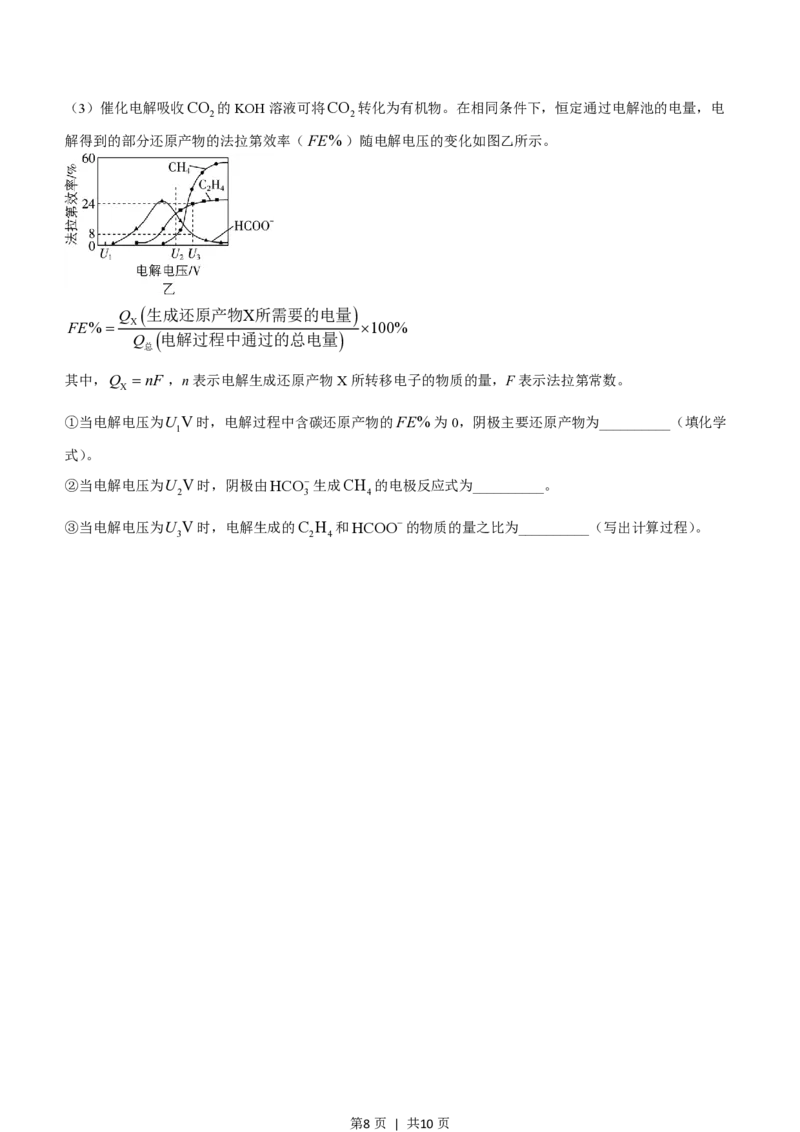
第7页 | 共10页(3)催化电解吸收CO 的KOH溶液可将CO 转化为有机物。在相同条件下,恒定通过电解池的电量,电
2 2
解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图乙所示。
Q 生成还原产物X所需要的电量
FE%= X ´100%
Q 电解过程中通过的总电量
总
其中,Q =nF ,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
X
①当电解电压为U V时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为__________(填化学
1
式)。
②当电解电压为U V时,阴极由HCO-生成CH 的电极反应式为__________。
2 3 4
③当电解电压为U V时,电解生成的C H 和HCOO-的物质的量之比为__________(写出计算过程)。
3 2 4
第8页 | 共10页第9页 | 共10页第10页 | 共10页