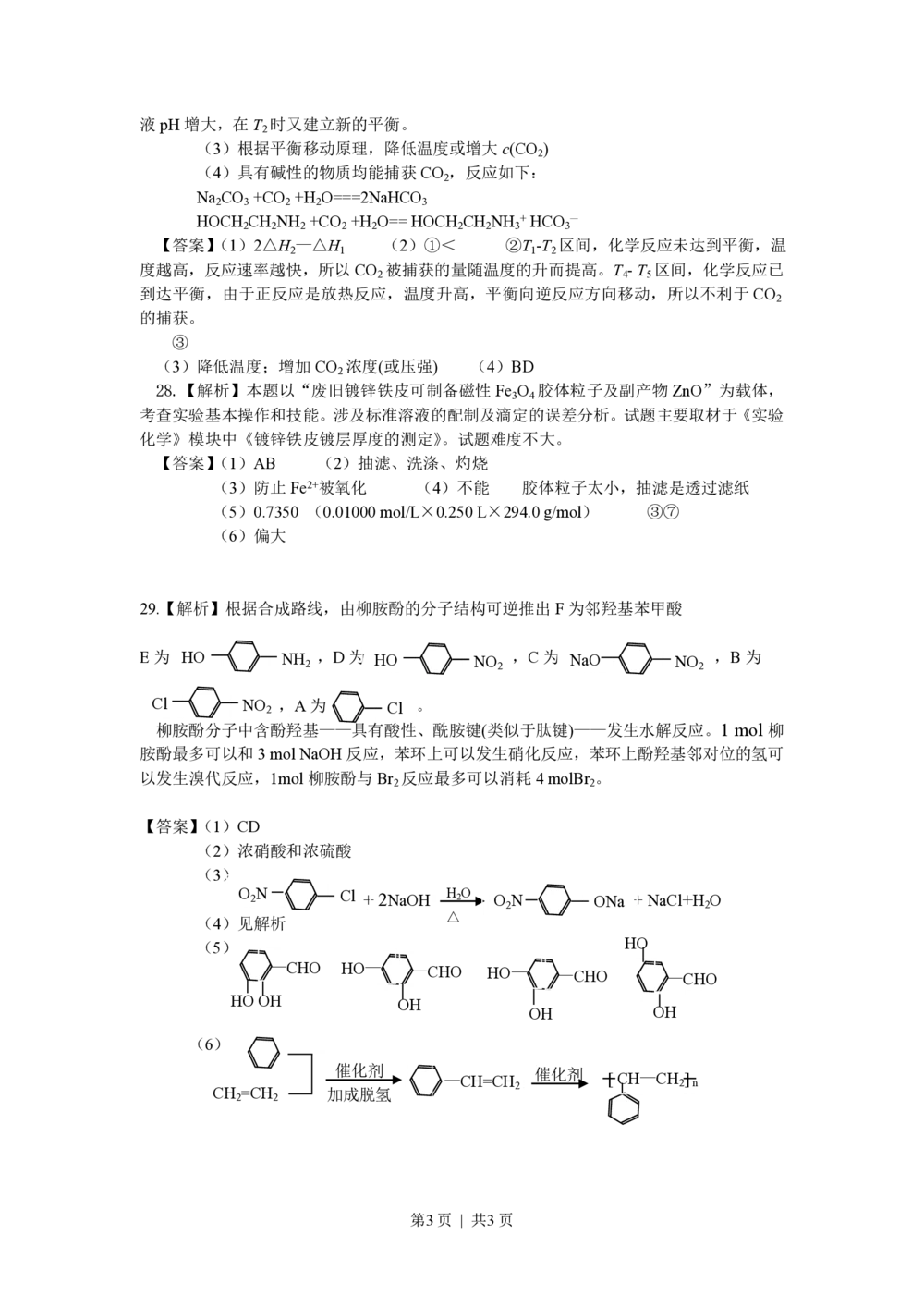文档内容
2013 年浙江高考化学试卷参考答案
7、B【解析】A选项:氢氧燃料电池要求电极必须多孔具有很强的吸附能力,并具一定的
催化作用,同时增大气固的接触面积,提高反应速率。C选项:As和P同主族。甲基环氧
乙烷与二氧化碳在一定条件下反应生成聚碳酸酯,原子利用率达到100%,生成的聚碳酸酯
易降解生成无毒无害物质,所以此反应符合绿色化学原则。B选项:pH计可用于酸碱中和
滴定终点的判断。
8、C【解析】A选项:实验室从海带提取单质碘缺少了氧化过程,萃取后还要分液。B选
项:用乙醇和浓H SO 制备乙烯时必须使温度迅速提高至约170℃,不可能是水浴加热(水
2 4
浴加热温度最高只能达到100℃)。D选项:蛋白质溶液中加入饱和(NH ) SO 溶液发生盐析
4 2 4
(盐析是可逆过程,不破坏蛋白质的生理活性,加水后又溶解),蛋白质溶液中加入CuSO 等
4
重金属盐溶液变性析出(变性是不可逆过程,蛋白质失去了生理活性,加水不再溶解)。C
选项:通常认为是Cl—替换氧化铝中的O2—而形成可溶性的氯化物,所以铝表面的氧化膜易
被Cl—破坏。
9、A【解析】由“X元素的原子内层电子数是最外层电子数的一半”可推出X为C,因此Y
为O,Z为Si,W为S,Q为Cl。A选项:Na和S可形成类似于Na O 的Na S 。Z与Y
2 2 2 2
组成的物质是SiO ,SiO 是原子晶体,熔融时不能导电。C选项:S得电子能力比Cl弱。D
2 2
选项:C、O元素都能形成多种同素异形体。
10、D【解析】A选项:题给化合物正确的名称为2,2,4,5-四甲基-3,3-二乙基己烷。B选项:
苯甲酸的分子式为C H O ,可将分子式变形为C H ·CO ,因此等物质的量的苯和苯甲酸完
7 6 2 6 6 2
全燃烧消耗氧气的量相等。C选项:苯不能使酸性高锰酸钾溶液褪色。
11、D
【解析】电解的电极反应为:阳极 2I——2e—== I 左侧溶液变蓝色
2
3I +6OH—==IO —+5I—+3H O 一段时间后,蓝色变浅
2 3 2
阴离子交换膜 向右侧移动
阴极 2H O+2e—==H ↑+2OH— 右侧放出氢气
2 2
如果用阳离子交换膜代替阴离子交换膜:
电极反应为:阳极 2I——2e—== I 多余K+
2
通过阳离子交换膜迁移至阴极
阴极 2H O+2e—==H ↑+2OH— 保证两边溶液呈电中性
2 2
12、B【解析】浓度均为0.1000 mol/L的三种酸HX、HY、HZ,根据滴定曲线0点三种酸
的pH可得到HZ是强酸,HY和HX是弱酸,但酸性:HY>HX。因此,同温同浓度时,
三种酸的导电性:HZ>HY>HX。B选项:当NaOH溶液滴加到10 mL时,溶液中c(HY)
≈c(Y—),即K (HY)≈c(H+)=10—pH=10—5。C选项:用NaOH溶液滴定至HX恰好完全反应
a
时,HY早被完全中和,所得溶液是NaY和NaX混合溶液,但因酸性:HY>HX,即X—的
水解程度大于Y—,溶液中c(Y—)>c(X—)。D选项:HY与HZ混合,溶液的电荷守恒式为:
c(H+)= c(Y—)+ c(Z—) +c(OH—),又根据HY的电离平衡常数:
c(H+)·c(Y—) K (HY)·c(HY)
a
K (HY)= 即有:c(Y—)=
a c(HY) c(H+)
K (HY)·c(HY) c(Y—)
a
所以达平衡后:c(H+)= + c(Z—) +c(OH—)
c(H+)
13、C【解析】A选项:因加入了NaOH (aq)和Na CO (aq),在滤液中引入了Na+,不能根
c(Y—) 2 3
据滤液焰色反应的黄色火焰判断试液是否含Na+。B选项:试液是葡萄糖酸盐溶液,其中一
定含葡萄糖酸根,葡萄糖能发生银镜反应,葡萄糖酸根不能发生银镜反应。D选项:溶液加
第1页 | 共3页入H O
2 2
后再滴加KSCN(aq)显血红色,不能证明葡萄糖酸盐试液中是否含Fe2+。正确的方法是:在
溶液中滴加KSCN(aq)不显血红色,再滴入滴加H O 显血红色,证明溶液中只含Fe2+。若此
2 2
前各步均没有遇到氧化剂,则可说明葡萄糖酸盐试液中只含Fe2+。C选项:根据“控制溶液
pH=4时,Fe(OH) 沉淀完全,Ca2+、Mg2+不沉淀”信息,在过滤除去Fe(OH) 的滤液中分别
3 3
加入NH ·H O(aq)和Na CO (aq),加入NH ·H O(aq)不产生沉淀说明滤液中不含Mg2+,加入
3 2 2 3 3 2
Na CO (aq)产生白色沉淀,说明滤液中含Ca2+。
2 3
26、【解析】“单质气体丙在标准状态下的密度为1.25 g/L”——丙为N ,化合物乙分解得到
2
H 和N ,化合物乙为NH H,NH H有NH +和H—构成的离子化合物。6.00 g化合物甲分解
2 2 4 4 4
得到短周期元素的金属单质和0.3 molH ,而短周期元素的金属单质的质量为5.4 g;化合物
2
甲与水反应生成的白色沉淀可溶于NaOH溶液,说明该沉淀可能是Al(OH) ,进而可判定化
3
催化剂
△
合物甲为AlH 3 。涉及的反应为: △
a.甲、乙受热分解:2AlH =======2Al+3H ↑ 2NH H=========N ↑+5H ↑
3 2 4 2 2
b.甲与水反应: 2AlH +6H O==2Al(OH) +6H ↑
3 2 3 2
△
c. 2NH H+5CuO======5Cu+ N ↑+5H O
4 2 2
d. 化合物甲与乙可能发生的反应:2AlH + 2NH H ======2Al+N ↑+8H ↑
3 4 2 2
化合物甲和乙的组成中都含—1价H,—1价H还原性很强,可发生氧化还原反应产生H ;
2
且2Al+3化合价降低6,2NH H 中8H+1化合价降低8,化合价共降低14;2AlH 中6H—1和
4 3
2NH H中2H—化合价升高8,2NH H中2N—3化合价升高6,化合价共升高14。
4 4
NH H电子式:
4
第(4)题的实验设计是1992年全国高考题的再现:Cu+在酸性溶液中不稳定,可发生自
身氧化还原反应生成Cu2+和Cu。现有浓硫酸、浓硝酸、稀硫酸、稀硝酸、FeCl 稀溶液及
3
pH试纸,而没有其它试剂。简述如何用最简便的实验方法来检验CuO经氢气还原所得到的
红色产物中是否含有碱性氧化物Cu O。
2
实验方案设计的关键是Cu O溶解而Cu不溶解:①Cu O为碱性氧化物;②不能选用具有
2 2
强氧化性的试剂,否则Cu被氧化为Cu2+。
实验方案设计的表述:简述操作步骤,复述实验现象,根据现象作出判断。
【答案】取少量反应产物,滴加足量稀硫酸,若溶液由无色变为蓝色,证明产物Cu中含
有Cu O;若溶液不变蓝色,证明产物Cu中不含Cu O。
2 2
27.【解析】(1)将反应Ⅰ倒过来书写:
(NH ) CO (aq) 2NH (l)+ H O (l)+ CO (g) —△H
4 2 3 3 2 2 1
将反应Ⅱ×2:
+) 2NH (l)+ 2H O (l)+ 2CO (g) 2NH HCO (aq) 2△H
3 2 2 4 3 2
得:(NH ) CO (aq) + H O (l)+ CO (g) 2NH HCO (aq) △H =2△H —△H
4 2 3 2 2 4 3 3 2 1
(2)由图1可知:在温度为T 时反应达平衡,此后温度升高,c(CO )增大,平衡
3 2
逆向移动,说明反应Ⅲ是放热反应(△H <0)。在T 前反应未建立平衡,
3 3
无论在什么温度下(NH ) CO (aq)总是捕获CO ,故c(CO )减小。
4 2 3 2 2
反应Ⅲ在温度为T 时建立平衡后(由图2可知:溶液pH不随
1
时间变化而变化),迅速上升到T 并维持温度不变,平衡逆向移动,溶
2
第2页 | 共3页液pH增大,在T 时又建立新的平衡。
2
(3)根据平衡移动原理,降低温度或增大c(CO )
2
(4)具有碱性的物质均能捕获CO ,反应如下:
2
Na CO +CO +H O===2NaHCO
2 3 2 2 3
HOCH CH NH +CO +H O== HOCH CH NH + HCO —
2 2 2 2 2 2 2 3 3
【答案】(1)2△H —△H (2)①< ②T -T 区间,化学反应未达到平衡,温
2 1 1 2
度越高,反应速率越快,所以CO 被捕获的量随温度的升而提高。T - T 区间,化学反应已
2 4 5
到达平衡,由于正反应是放热反应,温度升高,平衡向逆反应方向移动,所以不利于CO
2
的捕获。
③
(3)降低温度;增加CO 浓度(或压强) (4)BD
2
28.【解析】本题以“废旧镀锌铁皮可制备磁性Fe O 胶体粒子及副产物ZnO”为载体,
3 4
考查实验基本操作和技能。涉及标准溶液的配制及滴定的误差分析。试题主要取材于《实验
化学》模块中《镀锌铁皮镀层厚度的测定》。试题难度不大。
【答案】(1)AB (2)抽滤、洗涤、灼烧
(3)防止Fe2+被氧化 (4)不能 胶体粒子太小,抽滤是透过滤纸
(5)0.7350 (0.01000 mol/L×0.250 L×294.0 g/mol) ③⑦
(6)偏大
29.【解析】根据合成路线,由柳胺酚的分子结构可逆推出F为邻羟基苯甲酸
E为 H O NH 2 ,D为 H O NO 2 ,C为 N a O NO 2 ,B为
C l NO 2 ,A为 Cl 。
柳胺酚分子中含酚羟基——具有酸性、酰胺键(类似于肽键)——发生水解反应。1 mol柳
胺酚最多可以和3 mol NaOH反应,苯环上可以发生硝化反应,苯环上酚羟基邻对位的氢可
以发生溴代反应,1mol柳胺酚与Br 反应最多可以消耗4 molBr 。
2 2
【答案】(1)CD
(2)浓硝酸和浓硫酸
(3)
O 2 N Cl + 2NaOH H 2 O O N ONa + NaCl+H O
2 2
△
(4)见解析 a
(5) HO
—CHO HO— —CHO HO— —CHO —CHO
HO OH OH
OH OH
(6)
催化剂 —CH=CH
2
催化剂 [ CH—CH
2
]
n
CH =CH 加成脱氢
2 2
第3页 | 共3页