文档内容
年 月“八省联考”考前猜想卷
2025 1
化 学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 Li7 C12 O16 Na23 Cl35.5 Mn55 Co59 Zn65 Co59
第 卷
Ⅰ
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.2024年11月12日上午10时,万众瞩目的2024年中国航空航天博览会在珠海金湾机场盛大开幕,
我国歼-35A战斗机成明星装备。下列说法正确的是( )
A.航展首日中国空军军机在空中拉出的彩色烟带属于丁达尔效应
B.战斗机的隐形涂层含石墨烯(石墨的单层结构),12g石墨烯中含有1.5molσ键
C.战斗机的玻璃纤维雷达罩、聚碳酸酯舱盖、芳纶蜂窝材料都属于有机高分子材料
D.由于硬铝材料密度小、强度低,具有较好的抗腐蚀能力,可用作飞机外壳材料
2.下列化学用语表述不 . 正 . 确 . 的是( )
A.天然橡胶的结构简式:
B.基态Fe2+的价层电子排布式为3d54s1
C.OF 分子的VSEPR模型:
2
D.基态N原子2p能级电子轨道表示式:
3.下列说法正确的是( )
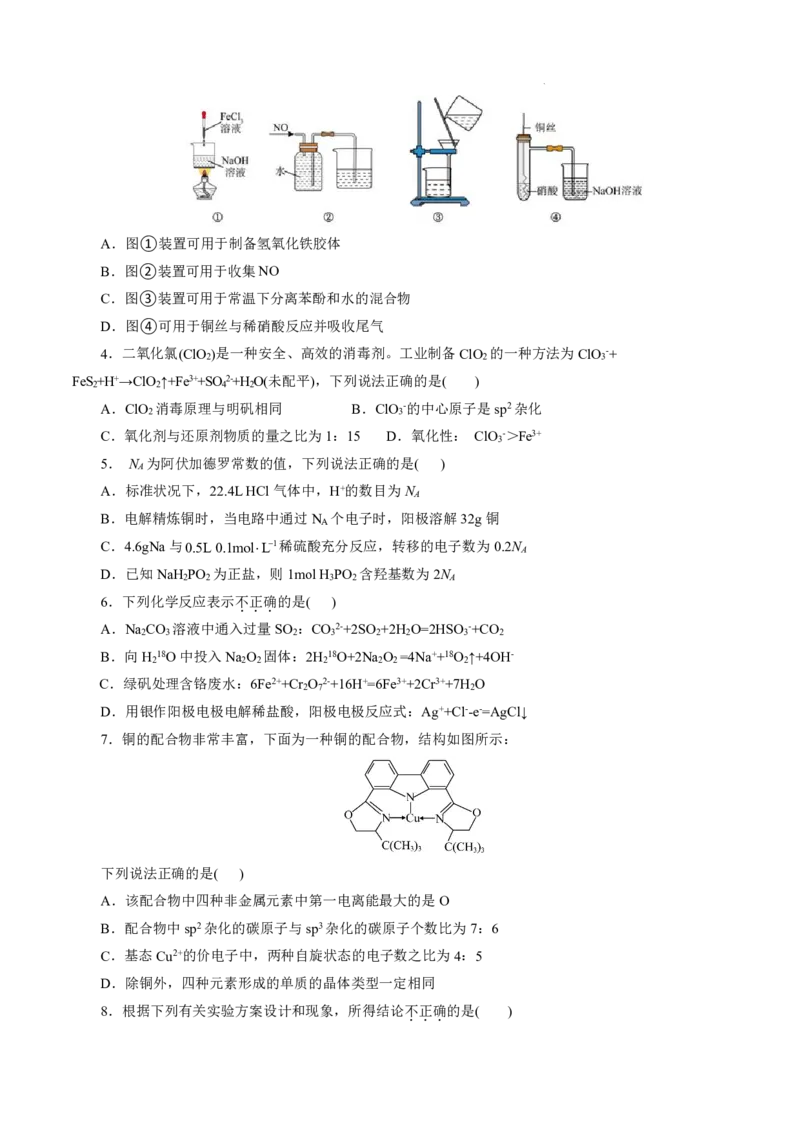
学科网(北京)股份有限公司A.图①装置可用于制备氢氧化铁胶体
B.图②装置可用于收集NO
C.图③装置可用于常温下分离苯酚和水的混合物
D.图④可用于铜丝与稀硝酸反应并吸收尾气
4.二氧化氯(ClO )是一种安全、高效的消毒剂。工业制备ClO 的一种方法为ClO -+
2 2 3
FeS+H+→ClO ↑+Fe3++SO2-+HO(未配平),下列说法正确的是( )
2 2 4 2
A.ClO 消毒原理与明矾相同 B.ClO -的中心原子是sp2杂化
2 3
C.氧化剂与还原剂物质的量之比为1:15 D.氧化性: ClO ->Fe3+
3
5. N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.标准状况下,22.4LHCl气体中,H+的数目为N
A
B.电解精炼铜时,当电路中通过N 个电子时,阳极溶解32g铜
A
C.4.6gNa与0.5L 0.1molL1稀硫酸充分反应,转移的电子数为0.2N
A
D.已知NaH PO 为正盐,则1molH PO 含羟基数为2N
2 2 3 2 A
6.下列化学反应表示不 . 正 . 确 . 的是( )
A.Na CO 溶液中通入过量SO :CO 2-+2SO +2H O=2HSO -+CO
2 3 2 3 2 2 3 2
B.向H 18O中投入Na O 固体:2H 18O+2Na O =4Na++18O ↑+4OH-
2 2 2 2 2 2 2
C.绿矾处理含铬废水:6Fe2++Cr O 2-+16H+=6Fe3++2Cr3++7H O
2 7 2
D.用银作阳极电极电解稀盐酸,阳极电极反应式:Ag++Cl--e-=AgCl↓
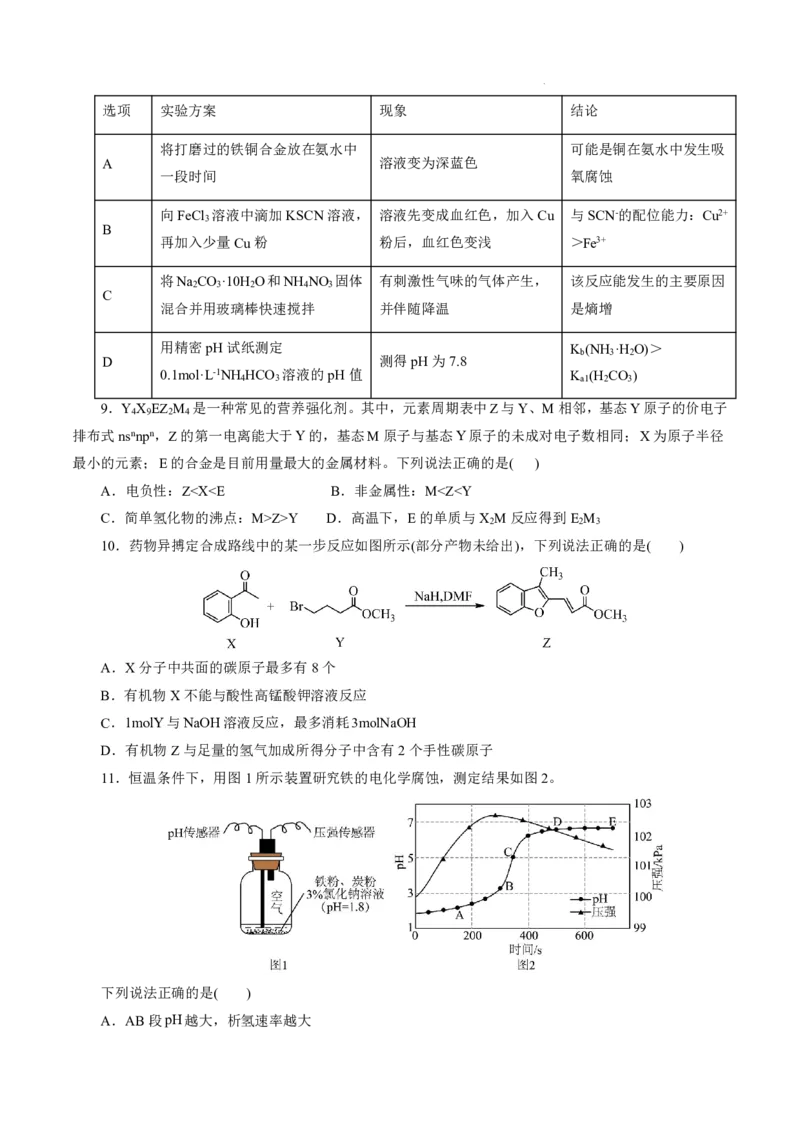
7.铜的配合物非常丰富,下面为一种铜的配合物,结构如图所示:
下列说法正确的是( )
A.该配合物中四种非金属元素中第一电离能最大的是O
B.配合物中sp2杂化的碳原子与sp3杂化的碳原子个数比为7:6
C.基态Cu2+的价电子中,两种自旋状态的电子数之比为4:5
D.除铜外,四种元素形成的单质的晶体类型一定相同
8.根据下列有关实验方案设计和现象,所得结论不 . 正 . 确 . 的是( )
学科网(北京)股份有限公司选项 实验方案 现象 结论
将打磨过的铁铜合金放在氨水中 可能是铜在氨水中发生吸
A 溶液变为深蓝色
一段时间 氧腐蚀
向FeCl 溶液中滴加KSCN溶液, 溶液先变成血红色,加入Cu 与SCN-的配位能力:Cu2+
3
B
再加入少量Cu粉 粉后,血红色变浅 >Fe3+
将Na CO ·10H O和NH NO 固体 有刺激性气味的气体产生, 该反应能发生的主要原因
2 3 2 4 3
C
混合并用玻璃棒快速搅拌 并伴随降温 是熵增
用精密pH试纸测定 K (NH ·H O)>
b 3 2
D 测得pH为7.8
0.1mol·L-1NH 4 HCO 3 溶液的pH值 K a1 (H 2 CO 3 )
9.Y X EZ M 是一种常见的营养强化剂。其中,元素周期表中Z与Y、M相邻,基态Y原子的价电子
4 9 2 4
排布式nsnnpn,Z的第一电离能大于Y的,基态M原子与基态Y原子的未成对电子数相同;X为原子半径
最小的元素;E的合金是目前用量最大的金属材料。下列说法正确的是( )
A.电负性:ZZ>Y D.高温下,E的单质与X M反应得到E M
2 2 3
10.药物异搏定合成路线中的某一步反应如图所示(部分产物未给出),下列说法正确的是( )
A.X分子中共面的碳原子最多有8个
B.有机物X不能与酸性高锰酸钾溶液反应
C.1molY与NaOH溶液反应,最多消耗3molNaOH
D.有机物Z与足量的氢气加成所得分子中含有2个手性碳原子
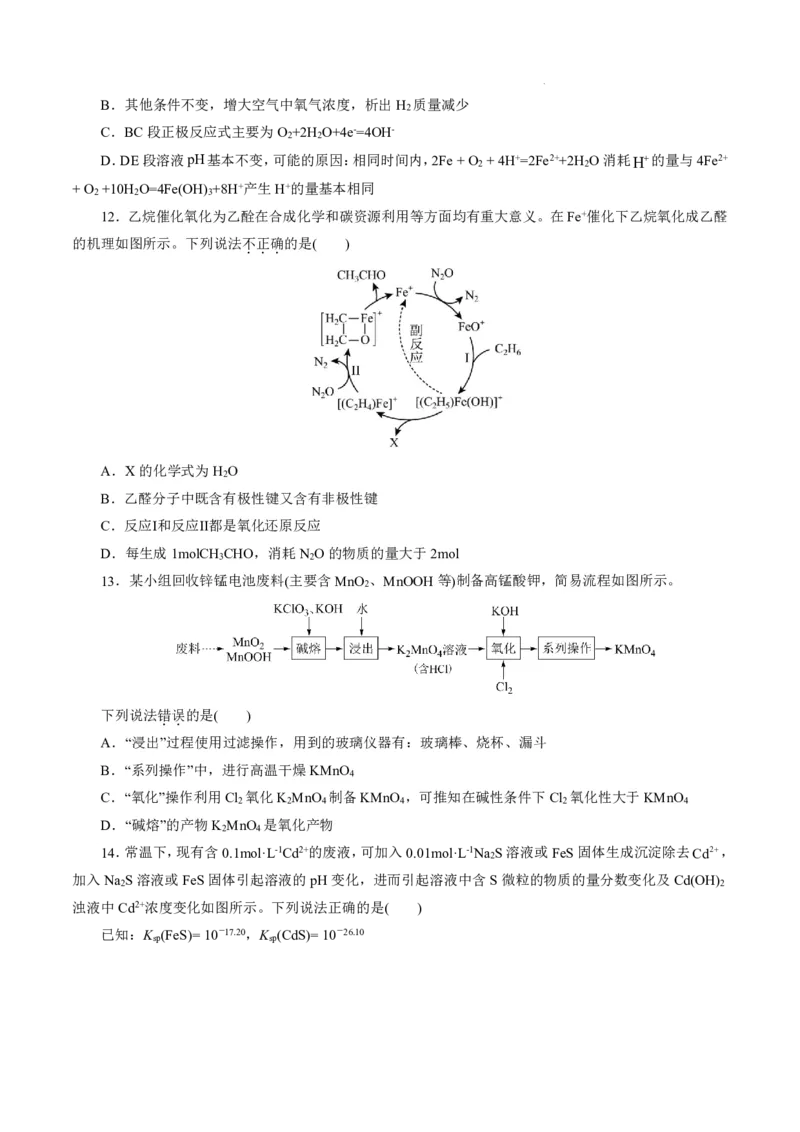
11.恒温条件下,用图1所示装置研究铁的电化学腐蚀,测定结果如图2。
下列说法正确的是( )
A.AB段pH越大,析氢速率越大
学科网(北京)股份有限公司B.其他条件不变,增大空气中氧气浓度,析出H 质量减少
2
C.BC段正极反应式主要为O +2H O+4e-=4OH-
2 2
D.DE段溶液pH基本不变,可能的原因:相同时间内,2Fe+O
2
+4H+=2Fe2++2H
2
O消耗H的量与4Fe2+
+O +10H O=4Fe(OH) +8H+产生H+的量基本相同
2 2 3
12.乙烷催化氧化为乙酫在合成化学和碳资源利用等方面均有重大意义。在Fe+催化下乙烷氧化成乙醛
的机理如图所示。下列说法不 . 正 . 确 . 的是( )
A.X的化学式为H O
2
B.乙醛分子中既含有极性键又含有非极性键
C.反应Ⅰ和反应Ⅱ都是氧化还原反应
D.每生成1molCH CHO,消耗N O的物质的量大于2mol
3 2
13.某小组回收锌锰电池废料(主要含MnO 、MnOOH等)制备高锰酸钾,简易流程如图所示。
2
下列说法错 . 误 . 的是( )
A.“浸出”过程使用过滤操作,用到的玻璃仪器有:玻璃棒、烧杯、漏斗
B.“系列操作”中,进行高温干燥KMnO
4
C.“氧化”操作利用Cl 氧化K MnO 制备KMnO ,可推知在碱性条件下Cl 氧化性大于KMnO
2 2 4 4 2 4
D.“碱熔”的产物K MnO 是氧化产物
2 4
14.常温下,现有含0.1mol·L-1Cd2+的废液,可加入0.01mol·L-1Na
2
S溶液或FeS固体生成沉淀除去Cd2,
加入Na S溶液或FeS固体引起溶液的pH变化,进而引起溶液中含S微粒的物质的量分数变化及Cd(OH)
2 2
浊液中Cd2+浓度变化如图所示。下列说法正确的是( )
已知:K (FeS)=10-17.20,K (CdS)=10-26.10
sp sp
学科网(北京)股份有限公司A.0.01mol·L-1Na S溶液中:c(Na+)>c(S2-)>c(OH―)>c(HS-)
2
B.加适量Na S固体可使废液中Cd2+浓度由b点变到a点
2
C.由图1和图2得知,当溶液的pH=10,发生的反应为Cd2++2HS-=CdS+H S
2
D.向废液中加入FeS固体,可使c(Cd2+)<10-9.9mol·L-1
第 卷
II
二、非选择题:本题共4小题,共58分。
15.(15分)铬酰氯是一种无机化合物,化学式为CrO Cl ,熔点-96.5℃,沸点117℃,常温下为深红棕
2 2
色液体,放置在空气中会迅速挥发并水解,主要在有机合成中作氧化剂、氯化剂和溶剂。在实验室中可由
重铬酸钾、浓硫酸与氯化钠反应得到铬酰氯,反应机理为:浓硫酸先分别与重铬酸钾和氯化钠反应生成CrO
3
和氯化氢气体两种中间产物,然后CrO 迅速与氯化氢气体反应生成铬酰氯。实验装置如下(夹持装置略):
3
回答下列问题:
(1)A的名称是 。B的进水口为 (填“a”或“b”)。
(2)浓硫酸在反应前应装入冰箱中冷却至0℃左右,其目的是 。
(3)写出CrO 与氯化氢气体反应生成铬酰氯的化学反应方程式 。
3
(4)投料时,加入过量氯化钠粉末可以显著增大铬酰氯的产率,原因是 。
(5)反应结束后,用电热套加热装置A,收集117℃左右的馏分,收集装置选用冰水浴的目的
是 。
(6)图中C装置未画出,应为下列装置中的哪一种 (填标号),该装置的作用是 。
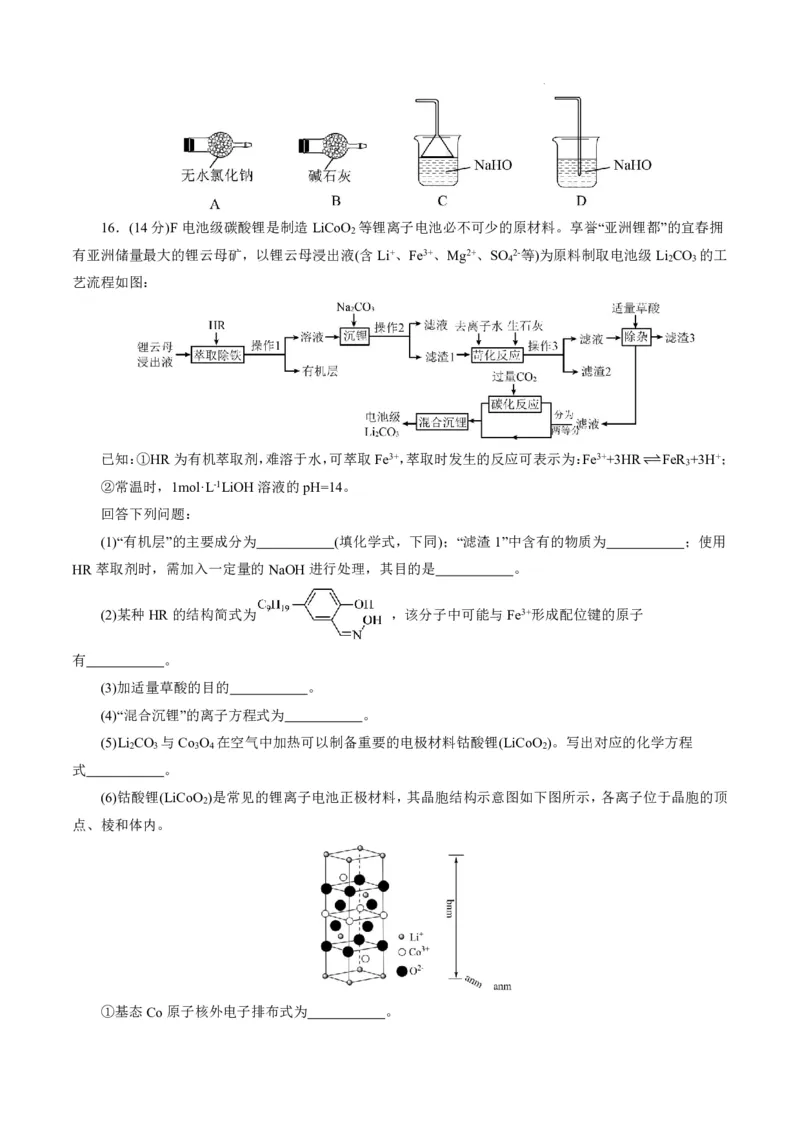
学科网(北京)股份有限公司16.(14分)F电池级碳酸锂是制造LiCoO 等锂离子电池必不可少的原材料。享誉“亚洲锂都”的宜春拥
2
有亚洲储量最大的锂云母矿,以锂云母浸出液(含Li+、Fe3+、Mg2+、SO 2-等)为原料制取电池级Li CO 的工
4 2 3
艺流程如图:
已知:①HR为有机萃取剂,难溶于水,可萃取Fe3+,萃取时发生的反应可表示为:Fe3++3HRFeR +3H+;
3
②常温时,1mol·L-1LiOH溶液的pH=14。
回答下列问题:
(1)“有机层”的主要成分为 (填化学式,下同);“滤渣1”中含有的物质为 ;使用
HR萃取剂时,需加入一定量的NaOH进行处理,其目的是 。
(2)某种HR的结构简式为 ,该分子中可能与Fe3+形成配位键的原子
有 。
(3)加适量草酸的目的 。
(4)“混合沉锂”的离子方程式为 。
(5)Li CO 与Co O 在空气中加热可以制备重要的电极材料钴酸锂(LiCoO )。写出对应的化学方程
2 3 3 4 2
式 。
(6)钴酸锂(LiCoO )是常见的锂离子电池正极材料,其晶胞结构示意图如下图所示,各离子位于晶胞的顶
2
点、棱和体内。
①基态Co原子核外电子排布式为 。
学科网(北京)股份有限公司②该晶胞密度为 g·cm-3。(写出计算式,阿伏加德罗常数为N )
A
17.(14分)绿色能源是未来能源发展的方向,积极发展氢能,是实现“碳达峰、碳中和”的重要举措,可
以用以下方法制备氢气。
I.甲烷和水蒸气催化制氢气。主要反应如下:
i.CH (g)+H O(g) CO(g)+3H (g) △H=+206.2kJ•mol-1
4 2 2
ii.CO(g)+H O(g) CO (g)+H (g) △H=-41.2kJ•mol-1
2 2 2
(1)反应CH (g)+CO (g) 2CO(g)+2H (g)的△H= kJ•mol-1。
4 2 2
(2)在容积不变的绝热密闭容器中发生反应i,下列能说明反应达到平衡状态的是 (填标号)。
A.气体混合物的密度不再变化 B.CH 消耗速率和H 的生成速率相等
4 2
C.CO的浓度保持不变 D.气体平均相对分子质量不再变化
E.体系的温度不再发生变化
(3)恒定压强为P MPa时,将n(CH ):n(H O)=1:3的混合气体投入反应器中发生反应i和ii,平衡时,
0 4 2
各组分的物质的量分数与温度的关系如图所示。
①图中表示CO 的物质的量分数与温度的变化曲线是 (填字母)。
2
②结合图中数据,其他条件不变,若要H 的产量最大,最适宜的反应温度是 (填标号)。
2
A.550~600℃ B.650~700℃ C.750~800℃
在其他条件不变的情况下,向体系中加入CaO可明显提高平衡体系中H 的含量,原因是 。
2
③600℃时,反应ii的平衡常数的计算式为K = (K 是以分压表示的平衡常数,分压=总压×物质
p p
的量分数)。
Ⅱ.电解法制氢气。某科研小组设计如图所示电解池,利用CO 和H O在碱性电解液中制备水煤气(H 、
2 2 2
CO),产物中H 和CO的物质的量之比为1∶1。
2
(4)电极B是 极,生成水煤气的电极反应式为 。
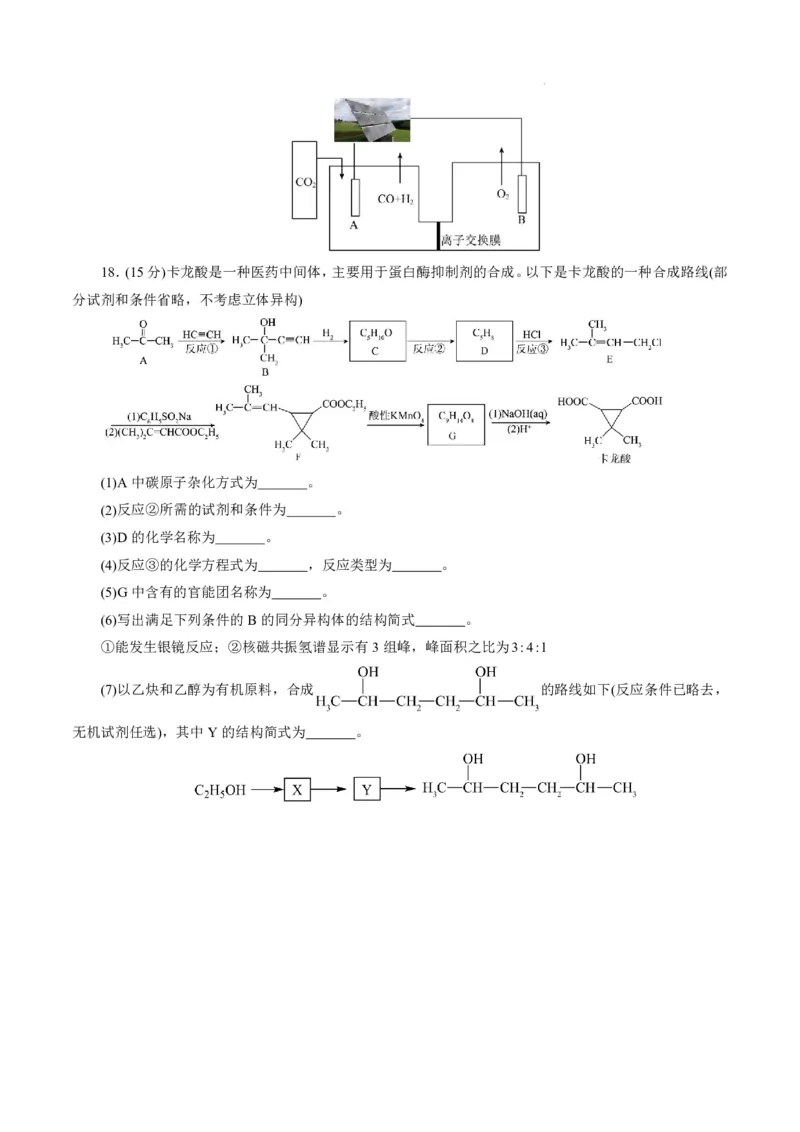
学科网(北京)股份有限公司18.(15分)卡龙酸是一种医药中间体,主要用于蛋白酶抑制剂的合成。以下是卡龙酸的一种合成路线(部
分试剂和条件省略,不考虑立体异构)
(1)A中碳原子杂化方式为 。
(2)反应②所需的试剂和条件为 。
(3)D的化学名称为 。
(4)反应③的化学方程式为 ,反应类型为 。
(5)G中含有的官能团名称为 。
(6)写出满足下列条件的B的同分异构体的结构简式 。
①能发生银镜反应;②核磁共振氢谱显示有3组峰,峰面积之比为3:4:1
(7)以乙炔和乙醇为有机原料,合成 的路线如下(反应条件已略去,
无机试剂任选),其中Y的结构简式为 。
学科网(北京)股份有限公司