文档内容
丰台区 2020—2021 学年度第一学期期末练习
初三化学
2021.01
相对原子质量:H1 C12 N14 O16 Na23 Si28
第一部分选择题(共25分)
(每小题只有1个选项符合题意。共25个小题,每小题1分)
1. 空气成分中,体积分数最大的是( )
A. 氮气 B. 二氧化碳 C. 氧气 D. 稀有气体
2. 下列元素中,属于金属元素的是
A. 氖 B. 氧 C. 锌 D. 磷
3. 下列物质属于氧化物的是( )
A. O B. H O C. NaCl D. H SO
2 2 2 4
4. 下列物质在氧气中燃烧,火星四射、生成黑色固体的是
A. 红磷 B. 木炭 C. 酒精 D. 铁丝
5. 下列物质放入水中,能形成溶液的是
A. 白糖 B. 牛奶 C. 面粉 D. 花生油
6. 下列金属中,金属活动性最强的是( )
A. 镁 B. 铜 C. 铁 D. 银
7. 热干面是武汉的传统小吃。下列制作热干面的主要操作中,属于过滤的是( )
A.调酱 B.煮面 C.捞面 D.拌面
A. A B. B C. C D. D
8. 碳元素与氧元素的本质区别是
A. 质子数不同 B. 电子数不同 C. 中子数不同 D. 最外层电子数不同9. 下列做法不利于保护环境的是( )
A. 将垃圾分类投放
B. 出行乘坐公共交通工具
.
C 随意丢弃废旧电池
D. 无纸化办公
10. 下列符号中,表示两个氢原子的是
A. H B. 2H C. 2H D.
2 2
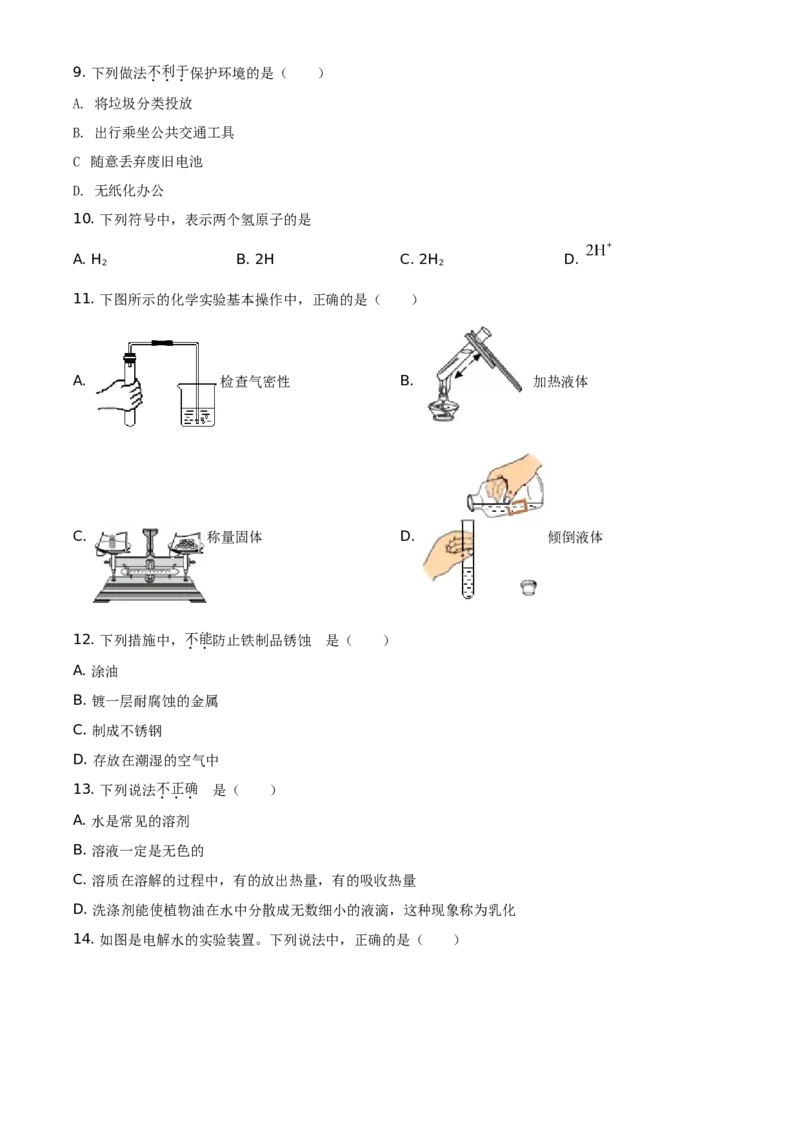
11. 下图所示的化学实验基本操作中,正确的是( )
A. 检查气密性 B. 加热液体
C. 称量固体 D. 倾倒液体
12. 下列措施中,不能防止铁制品锈蚀 的是( )
A. 涂油
B. 镀一层耐腐蚀的金属
C. 制成不锈钢
D. 存放在潮湿的空气中
13. 下列说法不正确 的是( )
A. 水是常见的溶剂
B. 溶液一定是无色的
C. 溶质在溶解的过程中,有的放出热量,有的吸收热量
D. 洗涤剂能使植物油在水中分散成无数细小的液滴,这种现象称为乳化
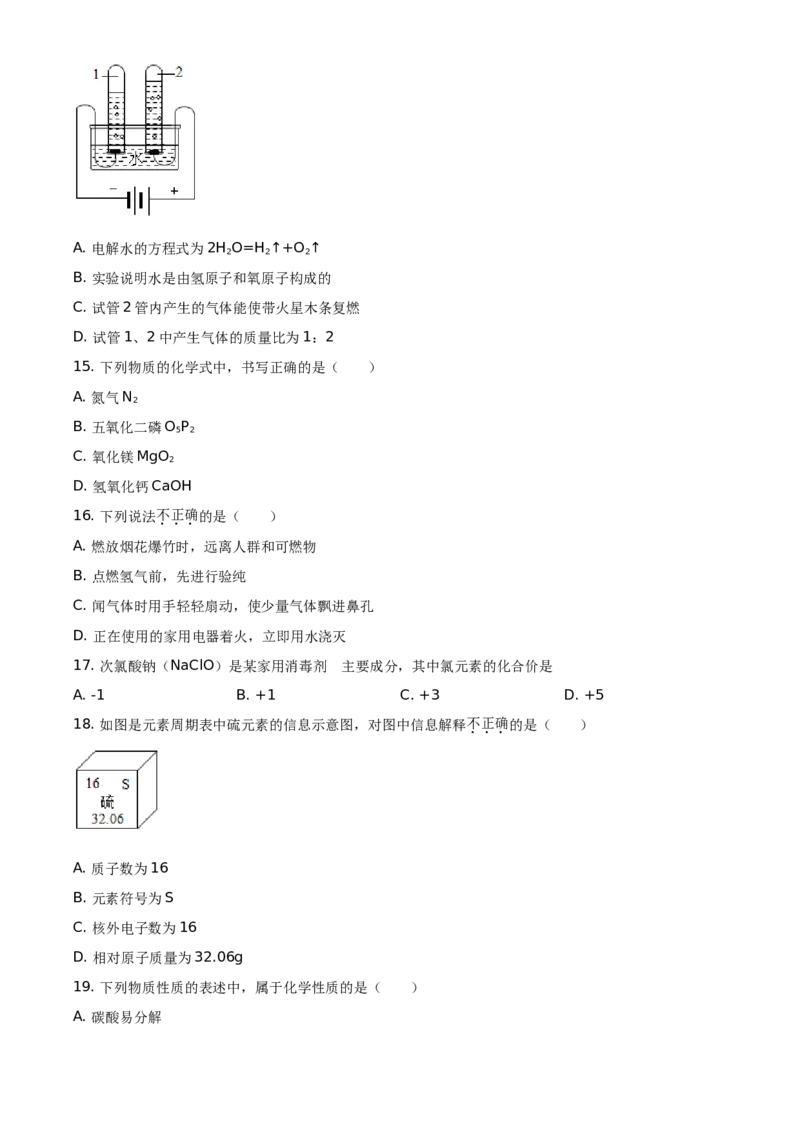
14. 如图是电解水的实验装置。下列说法中,正确的是( )A. 电解水的方程式为2H O=H ↑+O ↑
2 2 2
B. 实验说明水是由氢原子和氧原子构成的
C. 试管2管内产生的气体能使带火星木条复燃
D. 试管1、2中产生气体的质量比为1:2
15. 下列物质的化学式中,书写正确的是( )
A. 氮气N
2
B. 五氧化二磷O P
5 2
C. 氧化镁MgO
2
D. 氢氧化钙CaOH
16. 下列说法不正确的是( )
A. 燃放烟花爆竹时,远离人群和可燃物
B. 点燃氢气前,先进行验纯
C. 闻气体时用手轻轻扇动,使少量气体飘进鼻孔
D. 正在使用的家用电器着火,立即用水浇灭
17. 次氯酸钠(NaClO)是某家用消毒剂 的主要成分,其中氯元素的化合价是
A. -1 B. +1 C. +3 D. +5
18. 如图是元素周期表中硫元素的信息示意图,对图中信息解释不正确的是( )
A. 质子数为16
B. 元素符号为S
C. 核外电子数为16
D. 相对原子质量为32.06g
19. 下列物质性质的表述中,属于化学性质的是( )
A. 碳酸易分解B. 铝呈银白色
C. 氢气难溶于水
D. 氧气无色无味
20. 固体碘受热升华,下列关于此过程的说法正确的是
A. 碘分子质量变大 B. 碘分子间的间隔变大
C. 碘分子体积变小 D. 碘分子运动速率不变
21. 实验室用过氧化氢溶液制取氧气 ,关于该反应说法错误的是( )
A. MnO 为催化剂
2
B. 属于分解反应
C. 反应前后分子种类不变
D. 反应前后原子种类不变
22. 下列实验目的所对应的实验操作中,不正确的是( )
选项 实验目的 实验操作
A 鉴别硬水和软水 加入肥皂水
B 鉴别O 和CO 伸入燃着的木条
2 2
C 除去Cu粉中的Fe粉 加足量稀盐酸,过滤
D 除去CO 中的CO 通入足量澄清石灰水
2
A. A B. B C. C D. D
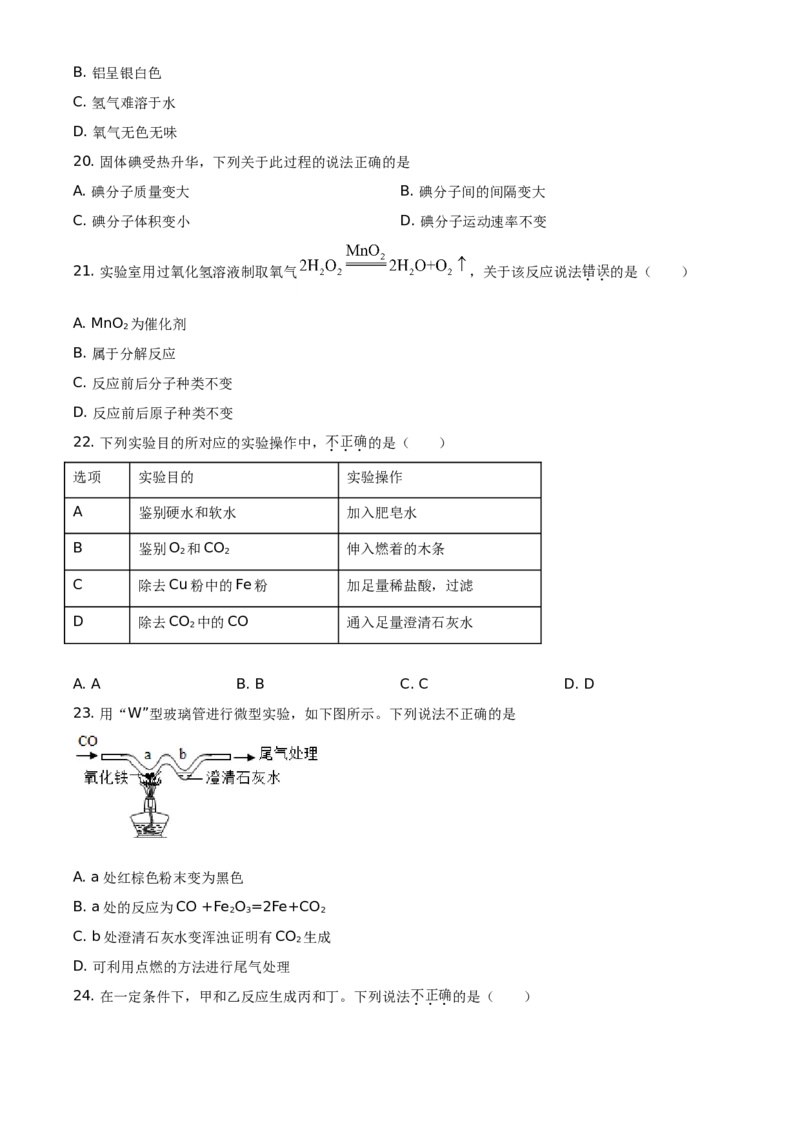
23. 用“W”型玻璃管进行微型实验,如下图所示。下列说法不正确的是
A. a处红棕色粉末变为黑色
B. a处的反应为CO +Fe O =2Fe+CO
2 3 2
C. b处澄清石灰水变浑浊证明有CO 生成
2
D. 可利用点燃的方法进行尾气处理
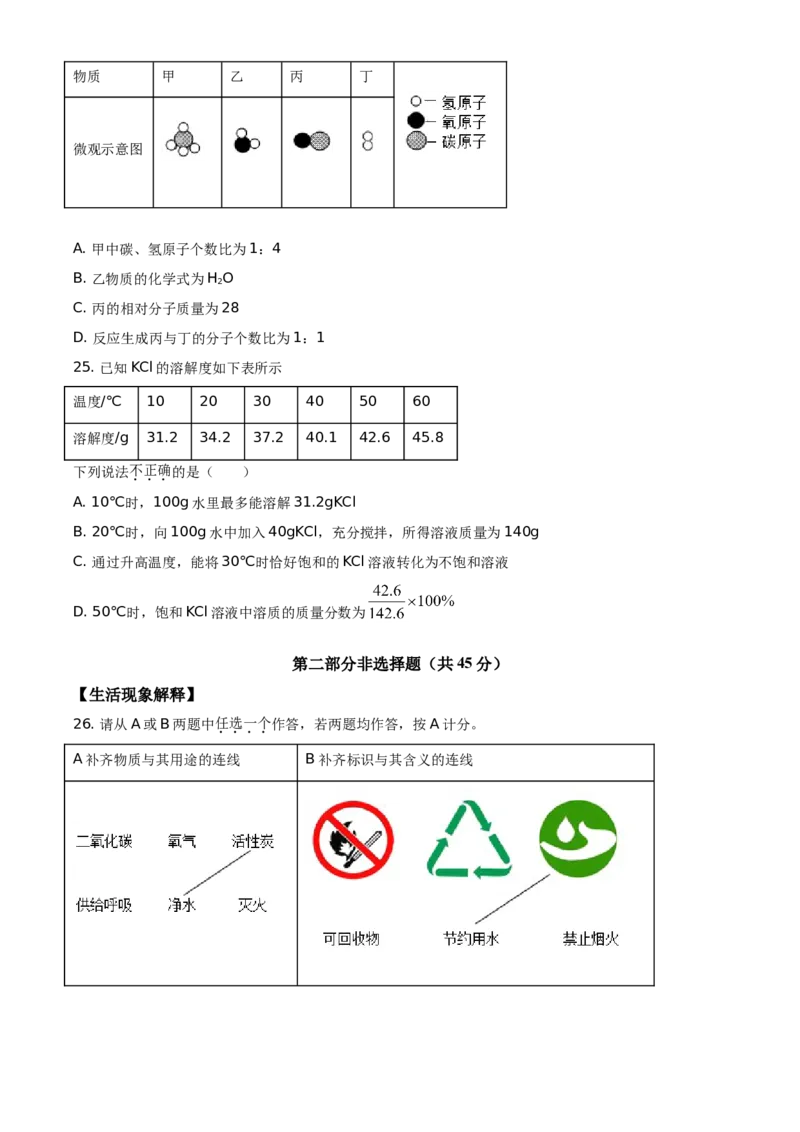
24. 在一定条件下,甲和乙反应生成丙和丁。下列说法不正确的是( )物质 甲 乙 丙 丁
微观示意图
A. 甲中碳、氢原子个数比为1:4
B. 乙物质的化学式为H O
2
C. 丙的相对分子质量为28
D. 反应生成丙与丁的分子个数比为1:1
25. 已知KCl的溶解度如下表所示
温度/℃ 10 20 30 40 50 60
溶解度/g 31.2 34.2 37.2 40.1 42.6 45.8
下列说法不正确的是( )
A. 10℃时,100g水里最多能溶解31.2gKCl
B. 20℃时,向100g水中加入40gKCl,充分搅拌,所得溶液质量为140g
C. 通过升高温度,能将30℃时恰好饱和的KCl溶液转化为不饱和溶液
D. 50℃时,饱和KCl溶液中溶质的质量分数为
第二部分非选择题(共45分)
【生活现象解释】
26. 请从A或B两题中任选一个作答,若两题均作答,按A计分。
A补齐物质与其用途的连线 B补齐标识与其含义的连线27. 2020年11月24日,嫦娥五号成功发射,将实现中国首次月球无人采样返回,标志着中国航天又取
得重大突破。高致密碳化硅(SiC)特种陶瓷常用作月基光学望远镜的主要材料。
(1)SiC属于___________。
A单质 B化合物 C纯净物 D混合物
(2)SiC中硅元素与碳元素的质量比为___________。
28. 目前使用的燃料大多来自化石燃料。
(1)化石燃料包括天然气、石油、___________。
(2)天然气的主要成分是甲烷(CH ),甲烷燃烧的化学方程式为___________。
4
【科普阅读理解】
29. 阅读下面的科普短文。
硒(Se)是人体内重要的微量元素之一,在抗氧化、延缓机体衰老等方面发挥重要作用。
含硒丰富的食物有水产品、动物内脏、蘑菇、富硒大米、白菜心等。摄入硒过少可能会导致克山病的发生,
而过高会引起中毒,导致腹泻、失明、脱发、甚至死亡。
人体中硒主要通过土壤-植物-机体食物链摄入。我国土壤中硒含量严重不均衡,因此国内对富硒食品进行
了许多开发与研究。施用含硒肥料,可提高植物中硒的含量。
食物中硒主要以硒酸钠(Na SeO )、亚硒酸钠(Na SeO )、植物活性硒形式存在。硒含量的检测可采
2 4 2 3
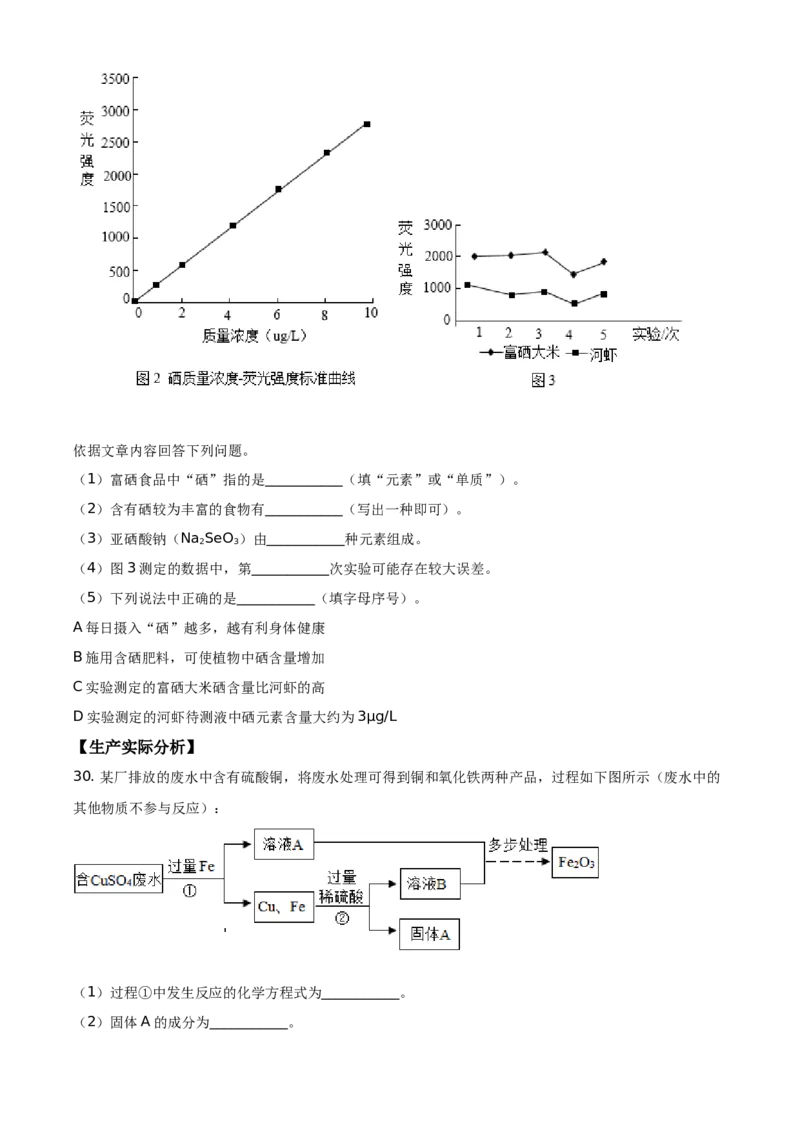
取荧光光谱法,在相同条件下,将待测液荧光强度与标准曲线(图2)对比,即可快速获取结果。将10g
某富硒大米、河虾样品分别制成1L待测液,进行5次实验,测得数据如下(见图3)。依据文章内容回答下列问题。
(1)富硒食品中“硒”指的是___________(填“元素”或“单质”)。
(2)含有硒较为丰富的食物有___________(写出一种即可)。
(3)亚硒酸钠(Na SeO )由___________种元素组成。
2 3
(4)图3测定的数据中,第___________次实验可能存在较大误差。
(5)下列说法中正确的是___________(填字母序号)。
A每日摄入“硒”越多,越有利身体健康
B施用含硒肥料,可使植物中硒含量增加
C实验测定的富硒大米硒含量比河虾的高
D实验测定的河虾待测液中硒元素含量大约为3μg/L
【生产实际分析】
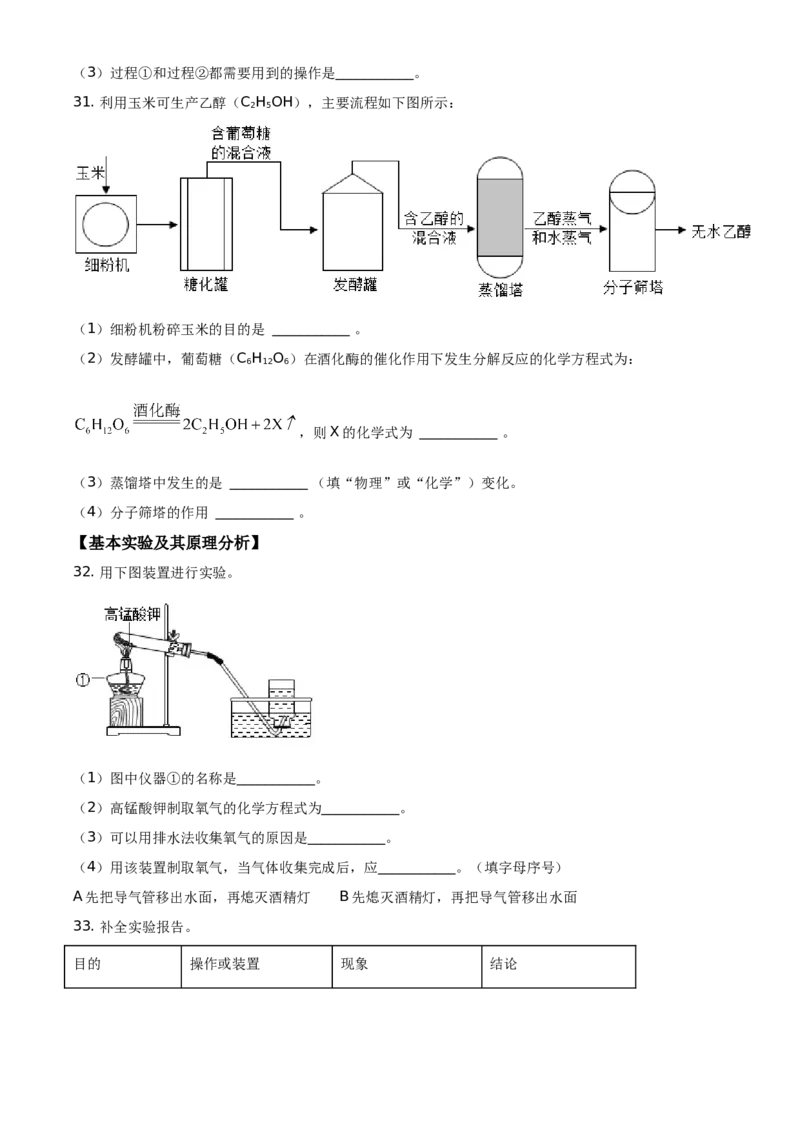
30. 某厂排放的废水中含有硫酸铜,将废水处理可得到铜和氧化铁两种产品,过程如下图所示(废水中的
其他物质不参与反应):
(1)过程①中发生反应的化学方程式为___________。
(2)固体A的成分为___________。(3)过程①和过程②都需要用到的操作是___________。
31. 利用玉米可生产乙醇(C H OH),主要流程如下图所示:
2 5
(1)细粉机粉碎玉米的目的是 ___________ 。
(2)发酵罐中,葡萄糖(C H O )在酒化酶的催化作用下发生分解反应的化学方程式为:
6 12 6
,则X的化学式为 ___________ 。
(3)蒸馏塔中发生的是 ___________ (填“物理”或“化学”)变化。
(4)分子筛塔的作用 ___________ 。
【基本实验及其原理分析】
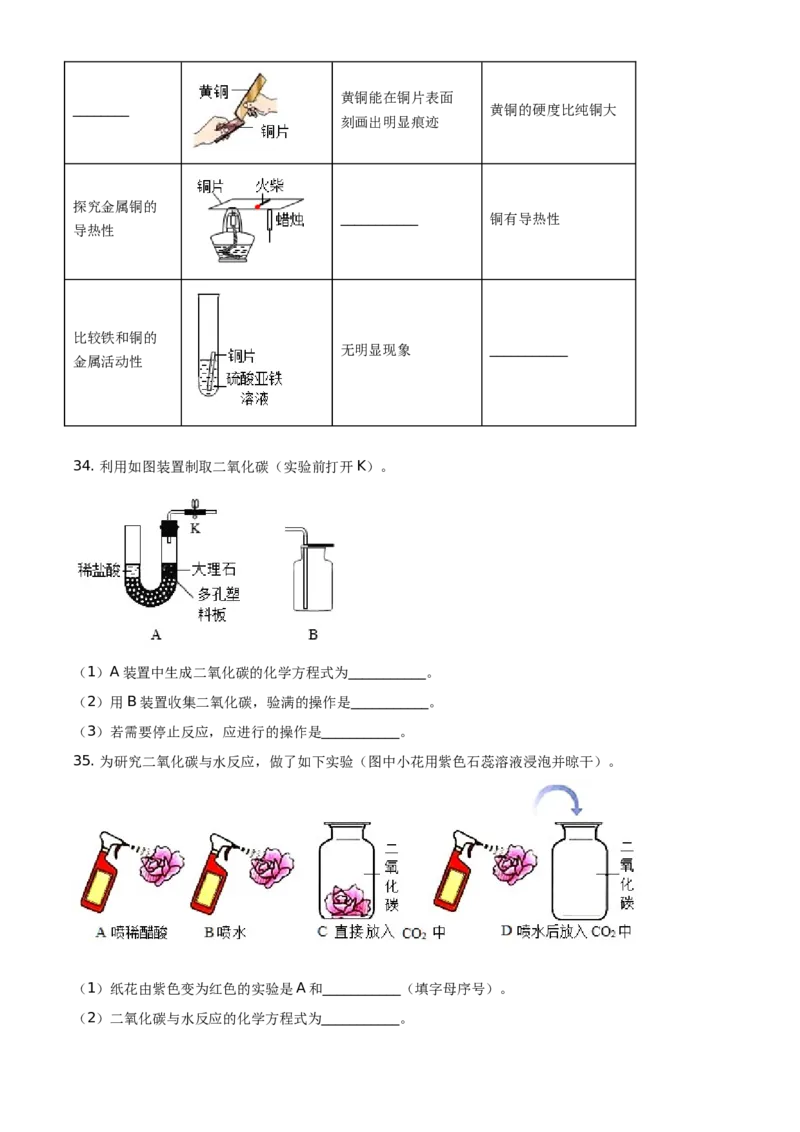
32. 用下图装置进行实验。
(1)图中仪器①的名称是___________。
(2)高锰酸钾制取氧气的化学方程式为___________。
(3)可以用排水法收集氧气的原因是___________。
(4)用该装置制取氧气,当气体收集完成后,应___________。(填字母序号)
A先把导气管移出水面,再熄灭酒精灯 B先熄灭酒精灯,再把导气管移出水面
33. 补全实验报告。
目的 操作或装置 现象 结论黄铜能在铜片表面
________ 黄铜的硬度比纯铜大
刻画出明显痕迹
探究金属铜的
___________ 铜有导热性
导热性
比较铁和铜的
无明显现象 ___________
金属活动性
34. 利用如图装置制取二氧化碳(实验前打开K)。
(1)A装置中生成二氧化碳的化学方程式为___________。
(2)用B装置收集二氧化碳,验满的操作是___________。
(3)若需要停止反应,应进行的操作是___________。
35. 为研究二氧化碳与水反应,做了如下实验(图中小花用紫色石蕊溶液浸泡并晾干)。
(1)纸花由紫色变为红色的实验是A和___________(填字母序号)。
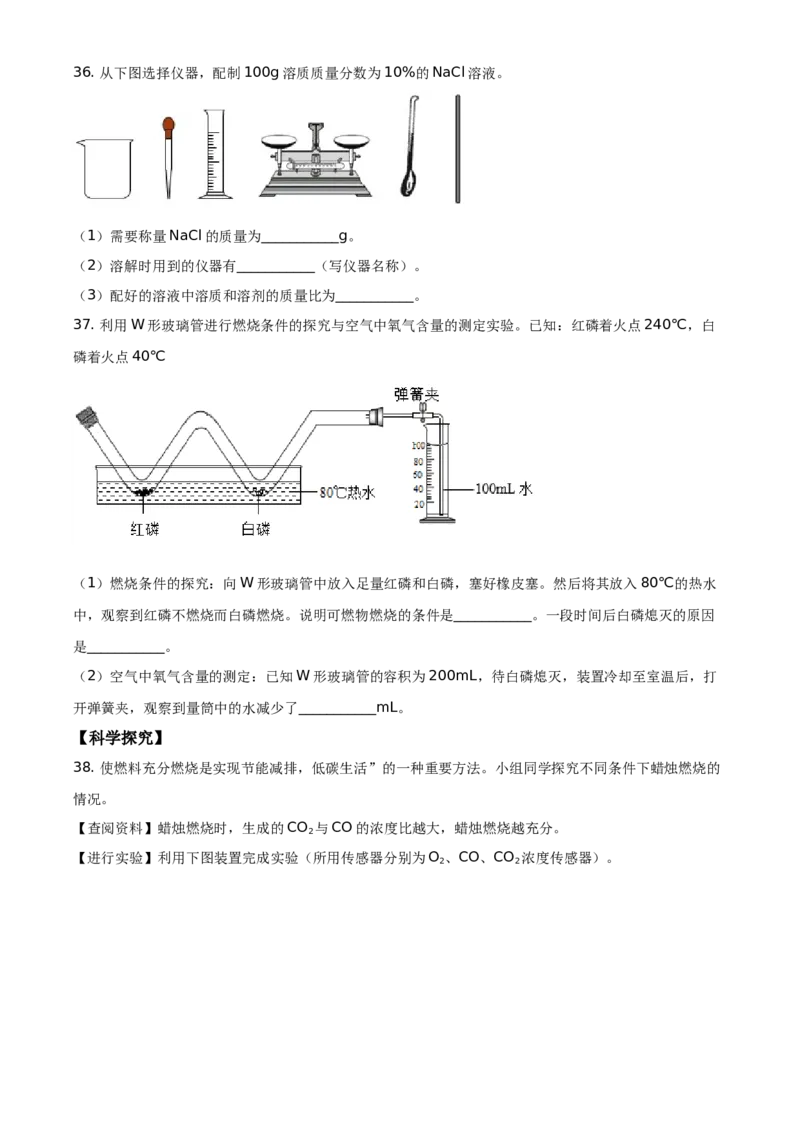
(2)二氧化碳与水反应的化学方程式为___________。36. 从下图选择仪器,配制100g溶质质量分数为10%的NaCl溶液。
(1)需要称量NaCl的质量为___________g。
(2)溶解时用到的仪器有___________(写仪器名称)。
(3)配好的溶液中溶质和溶剂的质量比为___________。
37. 利用W形玻璃管进行燃烧条件的探究与空气中氧气含量的测定实验。已知:红磷着火点240℃,白
磷着火点40℃
(1)燃烧条件的探究:向W形玻璃管中放入足量红磷和白磷,塞好橡皮塞。然后将其放入80℃的热水
中,观察到红磷不燃烧而白磷燃烧。说明可燃物燃烧的条件是___________。一段时间后白磷熄灭的原因
是___________。
(2)空气中氧气含量的测定:已知W形玻璃管的容积为200mL,待白磷熄灭,装置冷却至室温后,打
开弹簧夹,观察到量筒中的水减少了___________mL。
【科学探究】
38. 使燃料充分燃烧是实现节能减排,低碳生活”的一种重要方法。小组同学探究不同条件下蜡烛燃烧的
情况。
【查阅资料】蜡烛燃烧时,生成的CO 与CO的浓度比越大,蜡烛燃烧越充分。
2
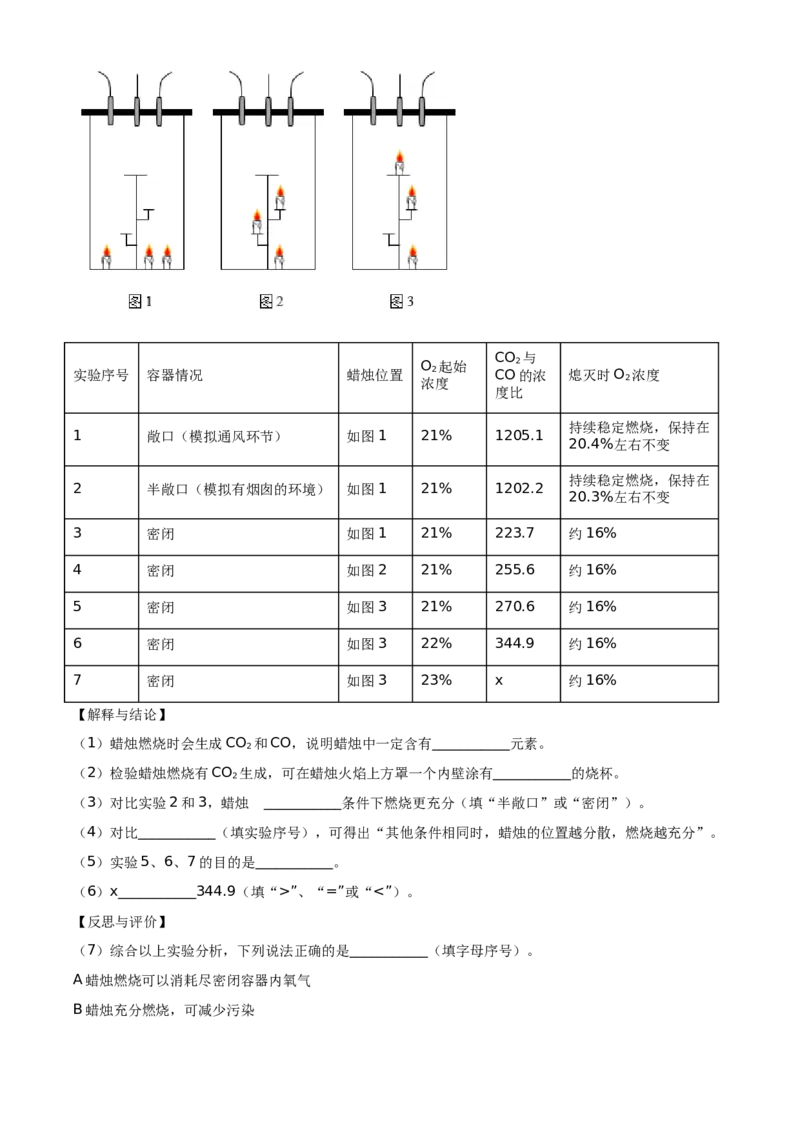
【进行实验】利用下图装置完成实验(所用传感器分别为O 、CO、CO 浓度传感器)。
2 2CO 与
O 起始 2
实验序号 容器情况 蜡烛位置 2 CO的浓 熄灭时O 浓度
浓度 2
度比
持续稳定燃烧,保持在
1 敞口(模拟通风环节) 如图1 21% 1205.1
20.4%左右不变
持续稳定燃烧,保持在
2 半敞口(模拟有烟囱的环境) 如图1 21% 1202.2
20.3%左右不变
3 密闭 如图1 21% 223.7 约16%
4 密闭 如图2 21% 255.6 约16%
5 密闭 如图3 21% 270.6 约16%
6 密闭 如图3 22% 344.9 约16%
7 密闭 如图3 23% x 约16%
【解释与结论】
(1)蜡烛燃烧时会生成CO 和CO,说明蜡烛中一定含有___________元素。
2
(2)检验蜡烛燃烧有CO 生成,可在蜡烛火焰上方罩一个内壁涂有___________的烧杯。
2
(3)对比实验2和3,蜡烛 在___________条件下燃烧更充分(填“半敞口”或“密闭”)。
(4)对比___________(填实验序号),可得出“其他条件相同时,蜡烛的位置越分散,燃烧越充分”。
(5)实验5、6、7的目的是___________。
(6)x___________344.9(填“>”、“=”或“<”)。
【反思与评价】
(7)综合以上实验分析,下列说法正确的是___________(填字母序号)。
A蜡烛燃烧可以消耗尽密闭容器内氧气
B蜡烛充分燃烧,可减少污染C实验1中氧气浓度基本不变,是因为分子在不断运动
D燃料在氧气浓度较高的富氧空气中燃烧,能起到节能减排的作用
【生产实际定量分析】
39. 叠氮化钠(NaN )可用作汽车安全气囊的气源,产生气体的原理是:
3
2NaN +CuO=Na O+3N ↑+Cu。计算130gNaN 完全反应生成N 的质量。
3 2 2 3 2本试卷的题干、答案和解析均由组卷网(http://zujuan.xkw.com)专业教师团队编校出品。
登录组卷网可对本试卷进行单题组卷、细目表分析、布置作业、举一反三等操作。
试卷地址:在组卷网浏览本卷
组卷网是学科网旗下的在线题库平台,覆盖小初高全学段全学科、超过900万精品解析试题。
关注组卷网服务号,可使用移动教学助手功能(布置作业、线上考试、加入错题本、错题训练)。
学科网长期征集全国最新统考试卷、名校试卷、原创题,赢取丰厚稿酬,欢迎合作。
钱老师 QQ:537008204 曹老师 QQ:713000635