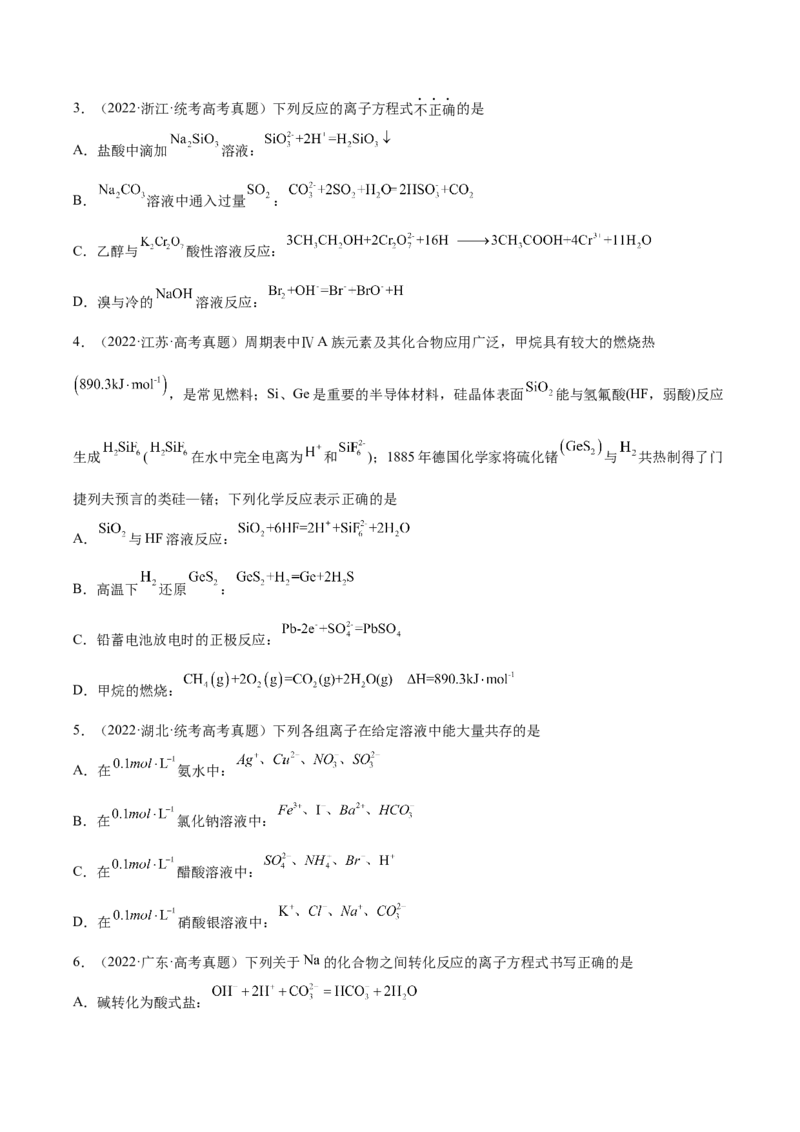文档内容
查补易混易错 04 离子反应
离子反应从微观上建立了认识化学反应的新视角,是电离模型的重要应用,为化学的微观研究奠定了重要
的基础。《课程标准》)要求学生通过实验事实认识离子反应及其发生的条件,能用离子方程式正确表示典
型物质的主要化学性质,该部分知识要求学生能对反应进行"宏观—微观—符号"三重表征分析微观实质,
并能用离子方程式进行符号表征,培养"宏观辨识与微观探析"的核心素养。离子反应贯穿在整个高中化学
教学之中,是每年高考命题中必然要涉及的知识点之一,主要包括离子方程式的书写(或正误判断)、离
子共存及离子的推导(可能出现在非选择题,对离子是否存在要知其然还要知其所以然),在非选择题中
也经常考离子方程式的书写,已知部分反应物和生成物,特别要注意的就是溶液的酸碱环境。
易错01离子方程式正误判断
(1)离子方程式正误判断时,要看是否符合客观事实,如铁与稀盐酸反应:3Fe+6H+=2Fe3++3H↑,书
2
写错误的原因是铁与稀盐酸反应生成Fe2+。
(2)要看拆分是否正确,如石灰石与稀盐酸反应:CO2- +2H+ = CO ↑+ H O,书写错误的原因是难溶的
3 2 2
CaCO 不能拆写;向NaHCO 溶液中滴加盐酸:CO2—+2H+===H O+CO↑,书写错误的原因是弱酸酸式
3 3 3 2 2
根离子HCO —不能拆写;NaO固体与水反应:O2—+HO===2OH-,书写错误的原因是氧化物NaO不能
3 2 2 2
拆写;醋酸溶液与水垢中的CaCO 反应:CaCO +2H+===Ca2++HO+CO↑,书写错误的原因是弱酸醋酸
3 3 2 2
(CHCOOH)不能拆写;Mg(OH) 和稀盐酸的反应:OH-+H+===H O,书写错误的原因是难溶的
3 2 2
Mg(OH) 不能拆写。
2
(3)要看是否符合原子守恒和电荷守恒,如氯化铁溶液与铜反应:Fe3++Cu== Fe2++Cu2+,书写错误的原因
是左右两边电荷不守恒;如金属钠与水反应:Na+HO== Na++OH– +H ↑,书写错误的原因是反应前后H原
2 2
子的数目不等。
(4)要看是否漏写离子反应,如Ba(OH) 溶液与硫酸铜溶液反应:Ba2++SO2-=BaSO ↓,书写错误的原
2 4 4
因是漏掉Cu2+与OH-生成Cu(OH) 沉淀。要看是否符合题设条件,如过量的NaHCO 溶液与Ca(OH) 溶液混
2 3 2
合:HCO - +Ca2+ +OH- = CaCO ↓+ H O,书写错误的原因是该离子方程式表示的是NaHCO 溶液与过量的
3 3 2 3
Ca(OH) 溶液混合。(5)要看是否符合组成,如稀硫酸与 Ba(OH) 溶液反应:H++SO2–+Ba2++OH–==
2 2 4
BaSO↓+H O,书写错误的原因是离子的个数比应与化学式中的组成不一致。
4 2
(6)要看离子方程式的条件注明是否正确,如制取氢氧化铁胶体:Fe3++3HO =Fe(OH) ↓+3H+,书写错
2 3误的原因是未标注加热符号。
易错02离子共存
(1)因生成弱电解质而不能大量共存的离子组:H+与CO、HCO、SO、HSO、S2-、HS-等易挥发的弱酸
的酸根不能共存;OH-与H+、NH、HCO、HSO、HS-、HPO、HPO等不能大量共存。
2
(2)因生成沉淀而不能大量共存的离子组:H+与SiO、AlO等不能大量共存;SO与Ba2+、Ca2+、Ag+等
不能大量共存;CO与Ba2+、Ca2+、Mg2+、Ag+、Cu2+、Zn2+等不能大量共存;S2-与Cu2+、Pb2+、Fe2+、
Hg2+、Ag+等不能大量共存;OH-与Mg2+、Al3+、Fe2+、Fe3+、Cu2+、Ag+、Zn2+等不能大量共存。
(3)因发生氧化还原反应而不能大量共存的离子组:在酸性条件下,NO与I-、Br-、Fe2+、S2-、HS-、
SO、HSO等不能共存,MnO与I-、Br-、Cl-、S2-、HS-、SO、HSO、Fe2+等不能大量共存,ClO-与Fe2
+、I-、S2-、HS-、SO、HSO等不能大量共存,S2-与SO等不能大量共存(碱性条件下可以共存);在碱性
条件下,ClO-与I-、Br-、Cl-、S2-等还原性比较强的离子不能大量共存,MnO与I-、Br-、Cl-、S2-等
还原性比较强的离子不能大量共存;
Fe3+与S2-、HS-、SO、HSO、I-等还原性比较强的离子不能大量共存,MnO与乙醇、苯酚、乙醛等还原
性比较强的分子不能大量共存。
(4)因水解相互促进而不能大量共存的离子组:Al3+与AlO、HCO、CO、HS-、S2-、SO、HSO、SiO、
ClO-、C HO-等不能大量共存;Fe3+与AlO、HCO、CO、SiO、ClO-等不能共存。
6 5
(5)因发生络合反应而不能大量共存的离子组:Fe3+和SCN-、C HO-不能大量共存;Ag+与NH在碱性
6 5
条件下不能大量共存。(1)一色——溶液颜色:
离子 Cu2+ Fe3+ Fe2+ MnO
溶液颜色 蓝色 黄色 浅绿色 紫红色
(2)二性——溶液的酸碱性
①在强酸性溶液中,OH-及弱酸根阴离子(如CO、ClO-、SO、S2-、CHCOO-等)不能大量存在。
3
②在强碱性溶液中,H+及弱碱阳离子(如NH、Al3+、Cu2+、Mg2+、Zn2+、Fe3+等)不能大量存在。
③如HCO、HS-、HSO、HPO、HPO等,在强酸性或强碱性溶液中均不能大量存在。
2
(3)三特殊——三种特殊情况
①AlO与HCO不能大量共存:AlO+HCO+HO===Al(OH) ↓+CO。
2 3
②“NO+H+”组合具有强氧化性,能与S2-、Fe2+、I-、SO等还原性的离子发生氧化还原反应而不能大
量共存。
③NH与CHCOO-、CO,Mg2+与HCO等组合中,虽然两种离子都能水解且水解相互促进,但总的水解
3
程度仍很小,它们在溶液中仍能大量共存。
(4)四反应——四种反应类型反应类型 不能大量共存的离子
如Ca2+ 、Ba2+与CO 、SO、SO;SiO与H+;Ag+与Cl-等不
生成沉淀
能大量共存
复分解 生成气体及易
H+与CO 、HCO、S2-、SO;NH和OH-等不能大量共存
反应 挥发性物质
生成弱
H+与OH-、ClO-、F-、CHCOO-等不能大量共存
3
电解质
Fe3+与S2-、I-等;MnO、ClO-在酸性、碱性、中性条件下与I
氧化还原反应
-、Fe2+、SO不能大量共存
相互促进的水解反应 Al3+、Fe3+与AlO、HCO、CO 等相互促进水解,不能大量共存
络合反应 Fe3+与SCN-;Ag+与NH ·H O不能大量共存
3 2
1.(2022·北京·高考真题)下列方程式与所给事实不相符的是
A.加热 固体,产生无色气体:
B.过量铁粉与稀硝酸反应,产生无色气体:
C.苯酚钠溶液中通入 ,出现白色浑浊:
D.乙醇、乙酸和浓硫酸混合加热,产生有香味的油状液体:
2.(2022·浙江·统考高考真题)下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
3 2
B.将少量NO 通入NaOH溶液:2NO +2OH-= + +H O
2 2 2
C.将少量SO 通入NaClO溶液:SO +H O+2ClO-= +2HClO
2 2 2
D.向氨水中滴入少量硝酸银溶液:Ag++2NH·H O= +2H O
3 2 23.(2022·浙江·统考高考真题)下列反应的离子方程式不正确的是
A.盐酸中滴加 溶液:
B. 溶液中通入过量 :
C.乙醇与 酸性溶液反应:
D.溴与冷的 溶液反应:
4.(2022·江苏·高考真题)周期表中ⅣA族元素及其化合物应用广泛,甲烷具有较大的燃烧热
,是常见燃料;Si、Ge是重要的半导体材料,硅晶体表面 能与氢氟酸(HF,弱酸)反应
生成 ( 在水中完全电离为 和 );1885年德国化学家将硫化锗 与 共热制得了门
捷列夫预言的类硅—锗;下列化学反应表示正确的是
A. 与HF溶液反应:
B.高温下 还原 :
C.铅蓄电池放电时的正极反应:
D.甲烷的燃烧:
5.(2022·湖北·统考高考真题)下列各组离子在给定溶液中能大量共存的是
A.在 氨水中:
B.在 氯化钠溶液中:
C.在 醋酸溶液中:
D.在 硝酸银溶液中:
6.(2022·广东·高考真题)下列关于 的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:B.碱转化为两种盐:
C.过氧化物转化为碱:
D.盐转化为另一种盐:
7.(2022·福建·统考高考真题)实验室需对少量污染物进行处理。以下处理方法和对应的反应方程式均错
误的是
A.用硫磺处理洒落在地上的水银:
B.用盐酸处理银镜反应后试管内壁的金属银:
C.用烧碱溶液吸收蔗糖与浓硫酸反应产生的刺激性气体:
D.用烧碱溶液吸收电解饱和食盐水时阳极产生的气体:
8.(2023·辽宁大连·统考一模)下列离子方程式书写正确的是
A.向 溶液中加入稀硫酸:
B.用亚硫酸钠溶液吸收少量氯气:
C.Fe与稀硝酸反应,当 时:
D.用过量苯酚溶液与碳酸钠溶液反应:2 + 2 +H O+CO
2 2
9.(2023·广东惠州·统考一模)下列有关铁及其化合物转化过程中的离子方程式书写正确的是
A.氧化亚铁溶于稀硝酸:
B.铁溶于盐酸:
C.醋酸除铁锈:
D.三氯化铁腐蚀铜板:
10.(2023·吉林长春·统考三模)能正确表示下列反应的离子方程式是A. 溶液中滴入 溶液:
B. 溶液中通入 ,溶液变为黄绿色:
C. 溶液中加入少量盐酸:
D.泡沫灭火器的反应原理:
11.(2023春·重庆沙坪坝·高三重庆一中校考阶段练习)经过指定操作后,下列各组溶液中离子还能大量
共存的是
A.加入 : 、 、Na+、
B.加入FeCl : 、 、 、
3
C.加入AgCl: 、F-、Na+、
D.通入SO :ClO-、Cl-、 、K+
2
12.(2023·广东佛山·统考二模)氯元素的单质及化合物之间可互相转化。下列反应的离子方程式书写错
误的是
A.单质转化为两种盐:
B.盐转化为酸:
C.酸转化为单质和盐:
D.两种盐转化为单质:
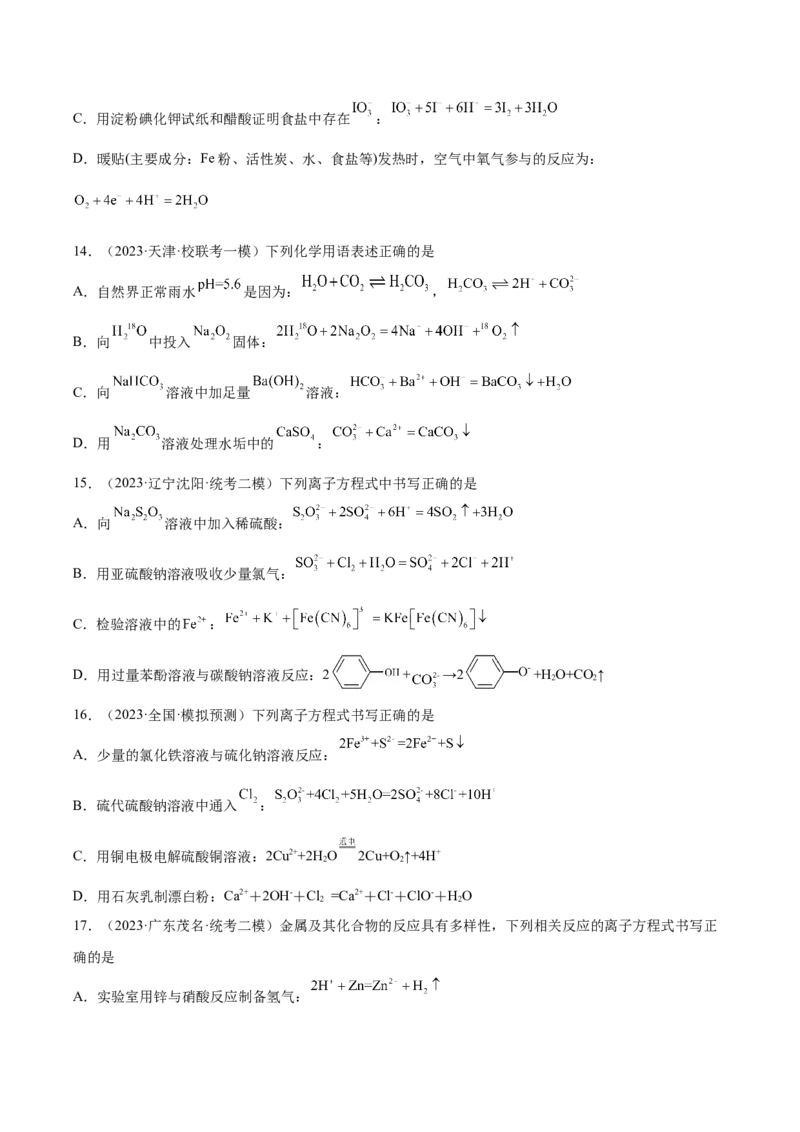
13.(2023·广东梅州·统考二模)下列解释事实的离子方程式书写正确的是
A.用含铝粉和氢氧化钠的疏通剂疏通管道:
B.用氯化铁溶液蚀刻覆铜板:C.用淀粉碘化钾试纸和醋酸证明食盐中存在 :
D.暖贴(主要成分:Fe粉、活性炭、水、食盐等)发热时,空气中氧气参与的反应为:
14.(2023·天津·校联考一模)下列化学用语表述正确的是
A.自然界正常雨水 是因为: ,
B.向 中投入 固体:
C.向 溶液中加足量 溶液:
D.用 溶液处理水垢中的 :
15.(2023·辽宁沈阳·统考二模)下列离子方程式中书写正确的是
A.向 溶液中加入稀硫酸:
B.用亚硫酸钠溶液吸收少量氯气:
C.检验溶液中的 :
D.用过量苯酚溶液与碳酸钠溶液反应:2 + →2 +H O+CO↑
2 2
16.(2023·全国·模拟预测)下列离子方程式书写正确的是
A.少量的氯化铁溶液与硫化钠溶液反应:
B.硫代硫酸钠溶液中通入 :
C.用铜电极电解硫酸铜溶液:2Cu2++2H O 2Cu+O ↑+4H+
2 2
D.用石灰乳制漂白粉:Ca2++2OH-+Cl =Ca2++Cl-+ClO-+HO
2 2
17.(2023·广东茂名·统考二模)金属及其化合物的反应具有多样性,下列相关反应的离子方程式书写正
确的是
A.实验室用锌与硝酸反应制备氢气:B.腐蚀电路板的刻蚀液再生:
C.用含有 和铝粉的管道疏通剂疏通管道;
D.用 、 和 制备小苏打:
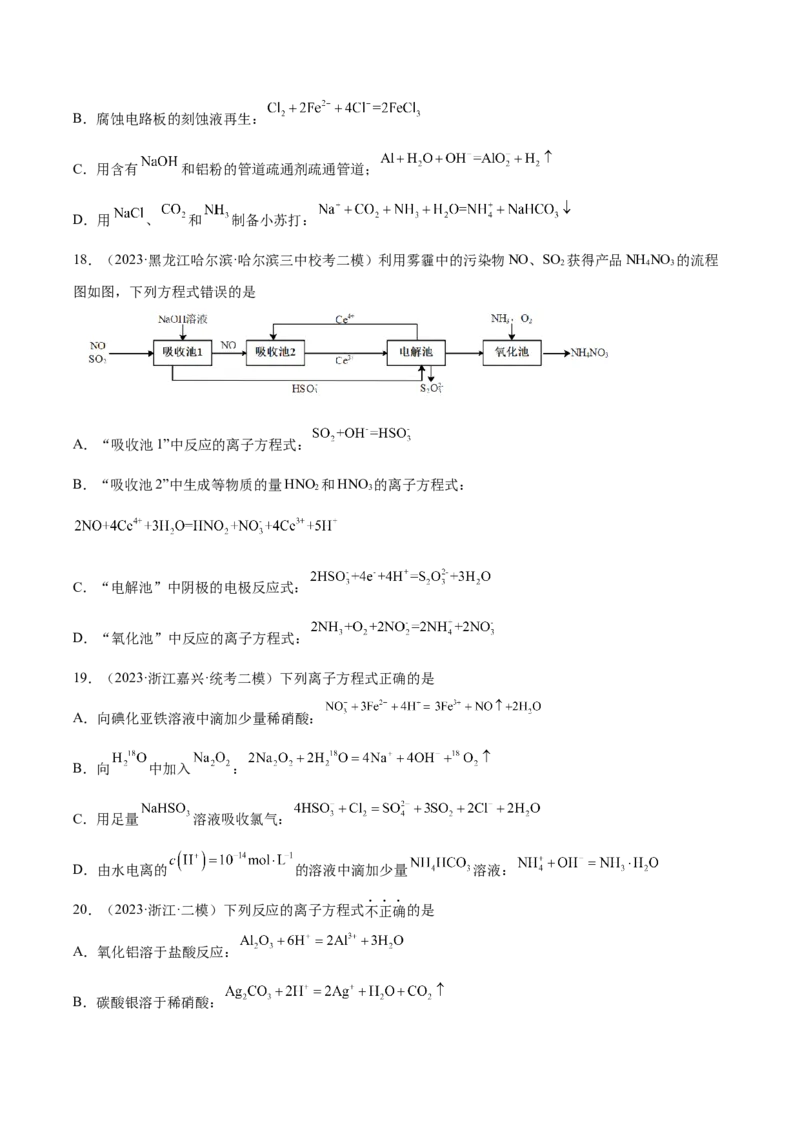
18.(2023·黑龙江哈尔滨·哈尔滨三中校考二模)利用雾霾中的污染物NO、SO 获得产品NH NO 的流程
2 4 3
图如图,下列方程式错误的是
A.“吸收池1”中反应的离子方程式:
B.“吸收池2”中生成等物质的量HNO 和HNO 的离子方程式:
2 3
C.“电解池”中阴极的电极反应式:
D.“氧化池”中反应的离子方程式:
19.(2023·浙江嘉兴·统考二模)下列离子方程式正确的是
A.向碘化亚铁溶液中滴加少量稀硝酸:
B.向 中加入 :
C.用足量 溶液吸收氯气:
D.由水电离的 的溶液中滴加少量 溶液:
20.(2023·浙江·二模)下列反应的离子方程式不正确的是
A.氧化铝溶于盐酸反应:
B.碳酸银溶于稀硝酸:C.次氯酸溶液见光分解:
D. 溶液中通入少量氯气:
21.(2023·湖南·校联考二模)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。 的一
种制备方法如图所示。下列说法错误的是
A.“富集”是为了提高 的浓度
B.“转化”产生的沉淀是Ag
C.“氧化”通入氯气越多越好
D.“氧化”主要发生的离子反应为
22.(2023·辽宁·校联考二模)下列离子方程式书写正确的是
A.Fe与稀硝酸反应,当n(Fe):n(HNO)=1:1时,3Fe+2NO +8H+=3Fe2++2NO↑+4HO
3 2
B.NaSO 溶液与稀HSO 反应的离子方程式:SO +2SO +6H+=4SO↑+3H O
2 2 3 2 4 2 2 2
C.向饱和NaCO 溶液中通入过量CO:CO +CO +H O=2HCO
2 3 2 2 2
D.CuSO 与过量浓氨水反应的离子方程式:Cu2++2NH•H O=Cu(OH) ↓+2NH
4 3 2 2
23.(2023春·湖南长沙·高三雅礼中学校考阶段练习)有一澄清透明的溶液,只可能含有大量的Fe3+、
Fe2+、H+、Al3+、AlO 、CO 、NO 七种离子中的几种,向该溶液中逐滴滴入1mol•L-1NaOH溶液一定体
积后才产生沉淀。则下列判断正确的是
A.溶液中可能含有AlO B.溶液中可能含有Fe2+
C.溶液中一定不含Al3+ D.溶液中一定含有NO
24.(2023·河南郑州·统考二模)化学创造美好生活。下列劳动项目所涉及反应的离子方程式错误的是A.工程师用FeS除去废水中的Hg2+ :FeS(s) + Hg2+ (aq) = HgS(s) + Fe2+ (aq)
B.消防员使用泡沫灭火器灭火:A13+ +3 = Al(OH) ↓+3CO ↑
3 2
C.环保人员用漂白粉溶液脱除废气中的SO :Ca2++2ClO- +SO+H O=CaSO↓+2HClO
2 2 2 3
D.工人用醋酸处理水垢中的氢氧化镁:Mg(OH) + 2CHCOOH= 2CH COO-+Mg2+ +2H O
2 3 3 2
25.(2022·湖南·高考真题)下列离子方程式正确的是
A. 通入冷的 溶液:
B.用醋酸和淀粉 溶液检验加碘盐中的 :
C. 溶液中加入 产生沉淀:
D. 溶液与少量的 溶液混合: