文档内容
高中知识手册
高中化学
每天进步一点点C 目录
ONTENTS
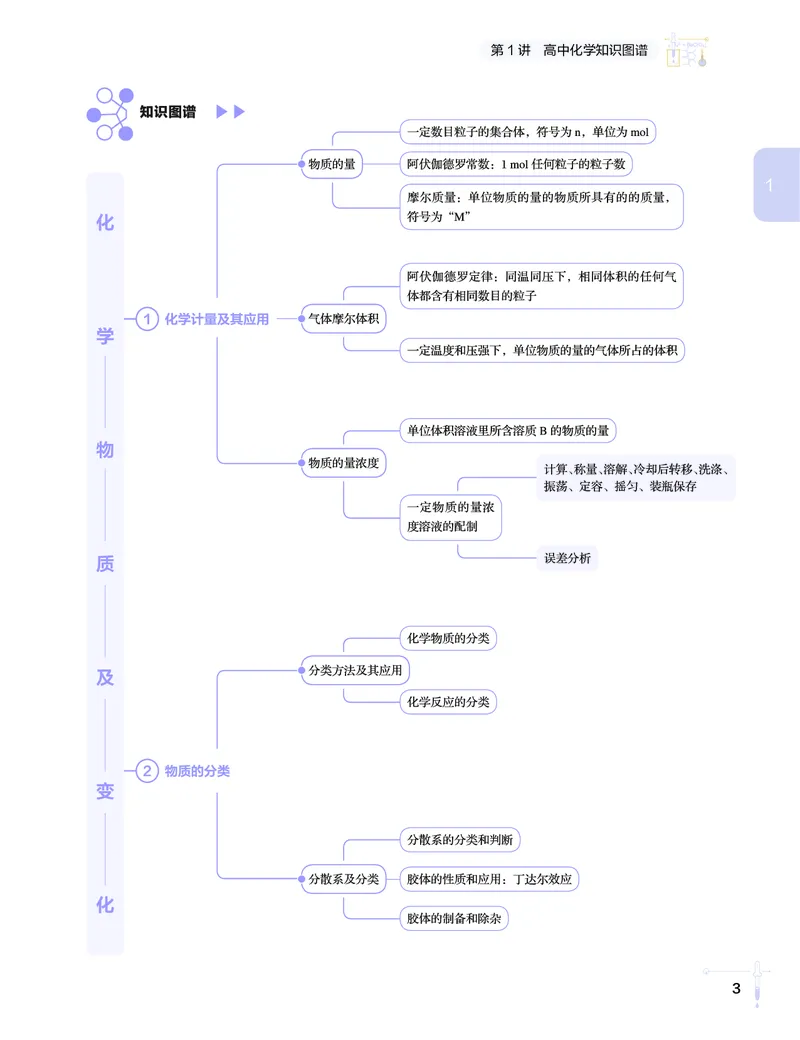
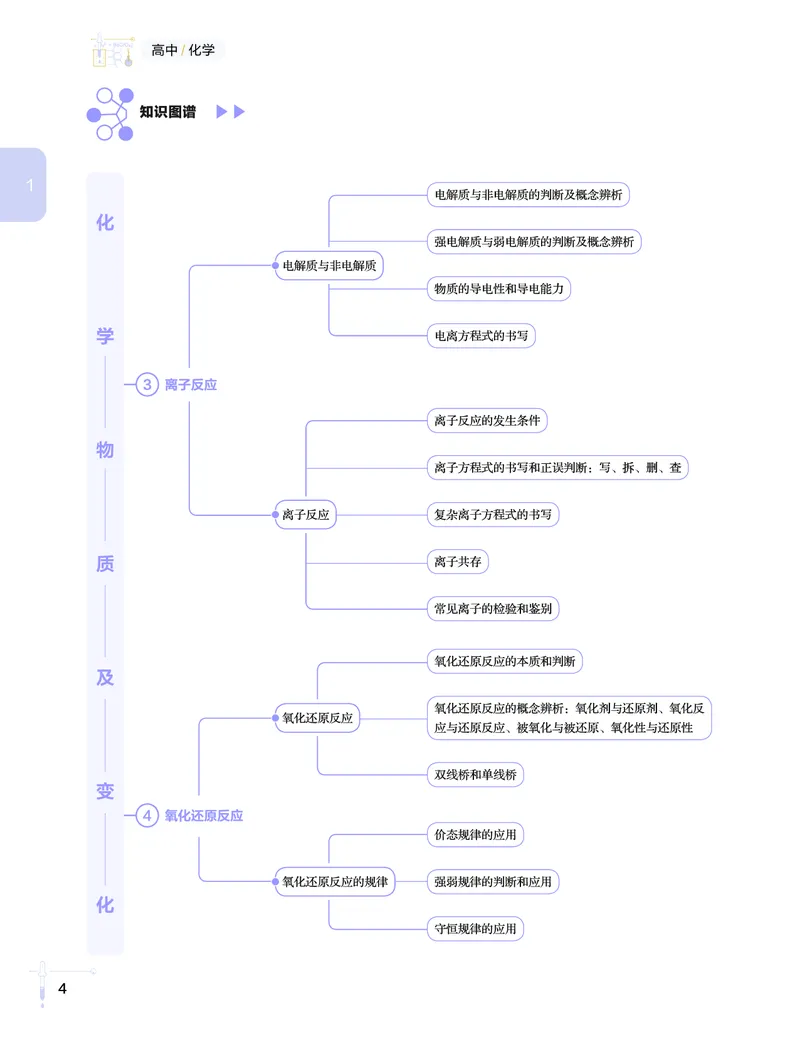
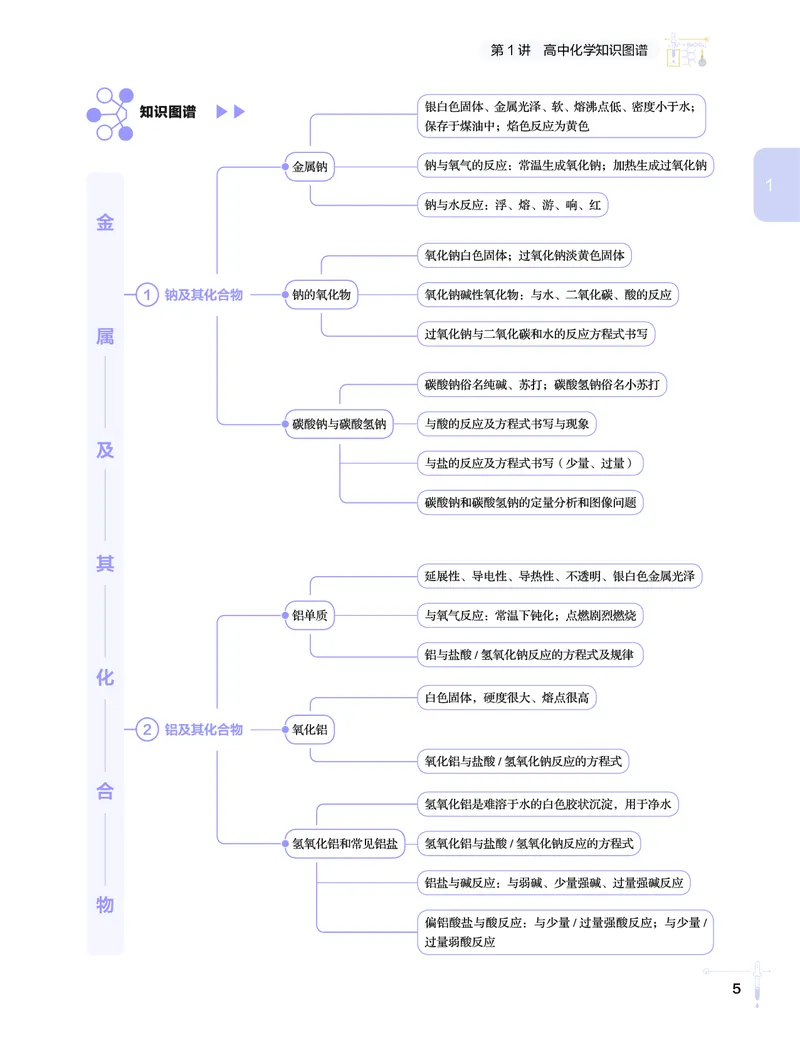
第 1 讲 高中化学知识图谱
第 2 讲 课本方程式
模块1 必修一(新人教) 19
模块2 必修二(新人教) 22
模块3 电化学 24
模块4 有机化学基础 26
第 3 讲 近三年高考方程式
模块1 2020年高考 29
模块2 2019年高考 32
模块3 2018年高考 35第1讲
高中化学知识图谱
第 1 讲
高中化学知识图谱第1讲 高中化学知识图谱
1
3高中/化学
1
4第1讲 高中化学知识图谱
1
5高中/化学
1
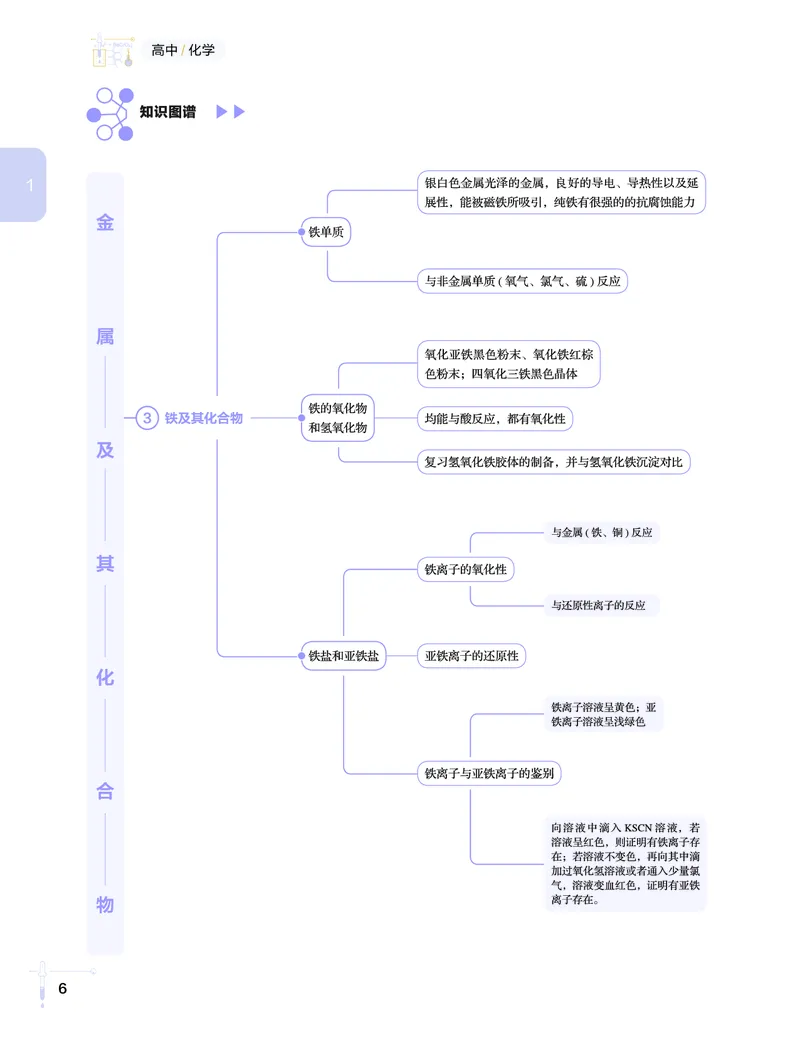
6第1讲 高中化学知识图谱
1
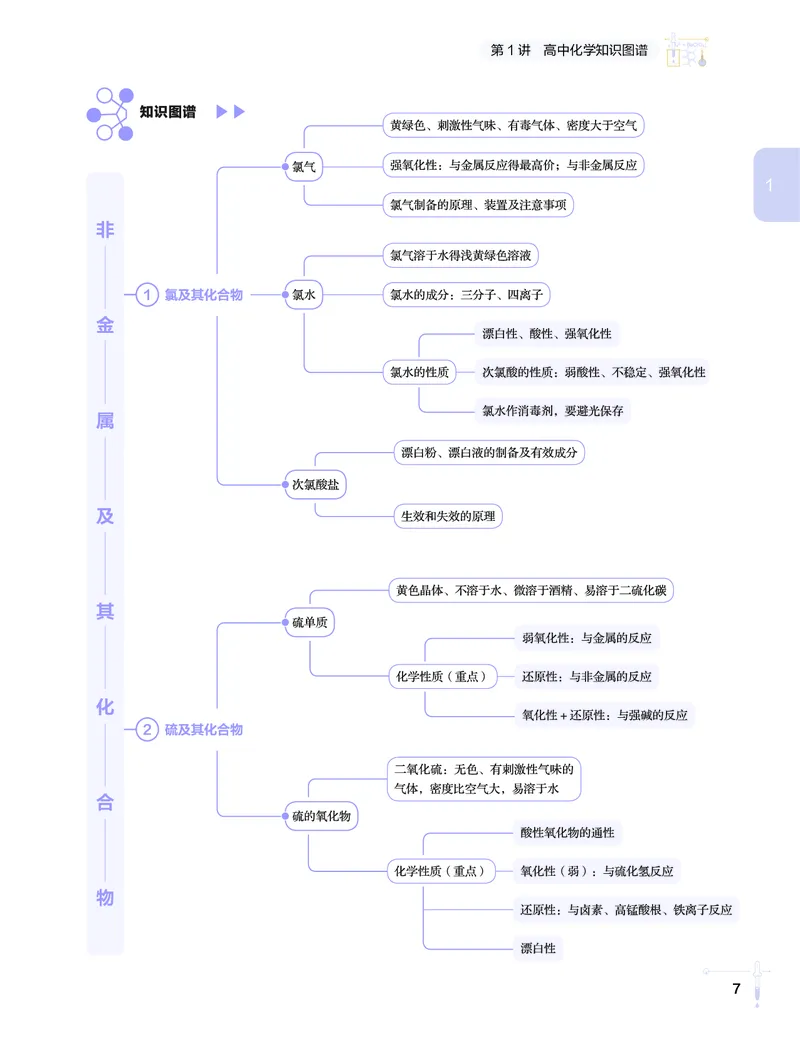
7高中/化学
1
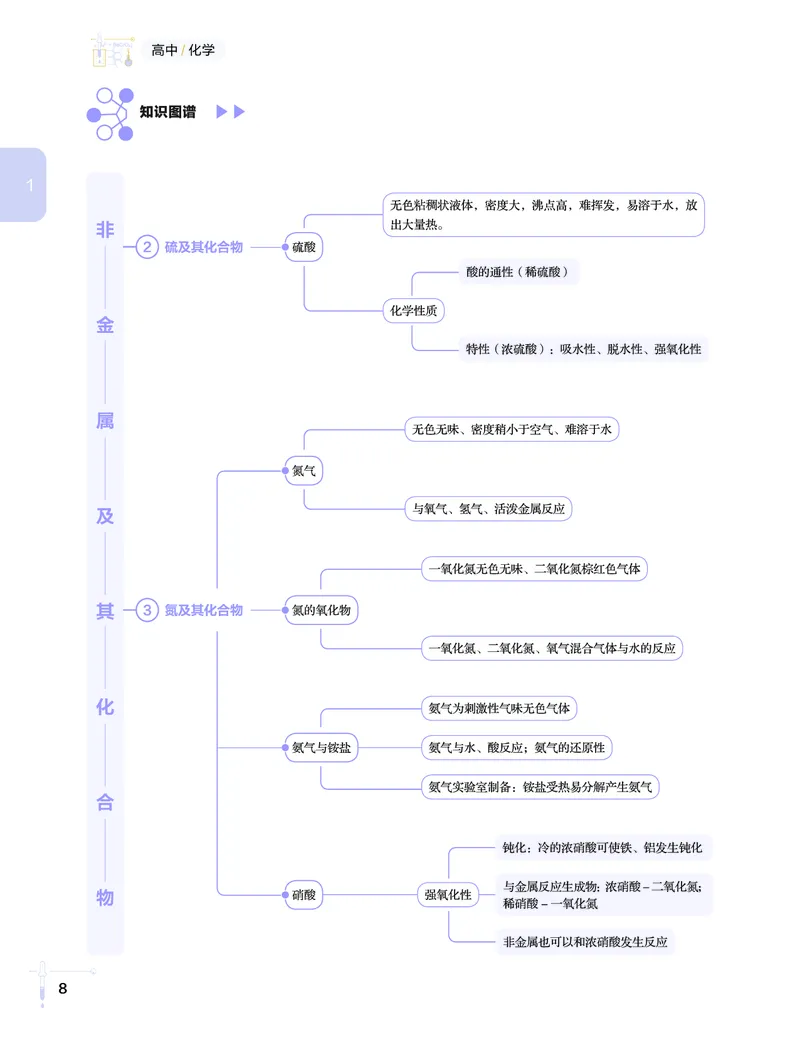
8第1讲 高中化学知识图谱
1
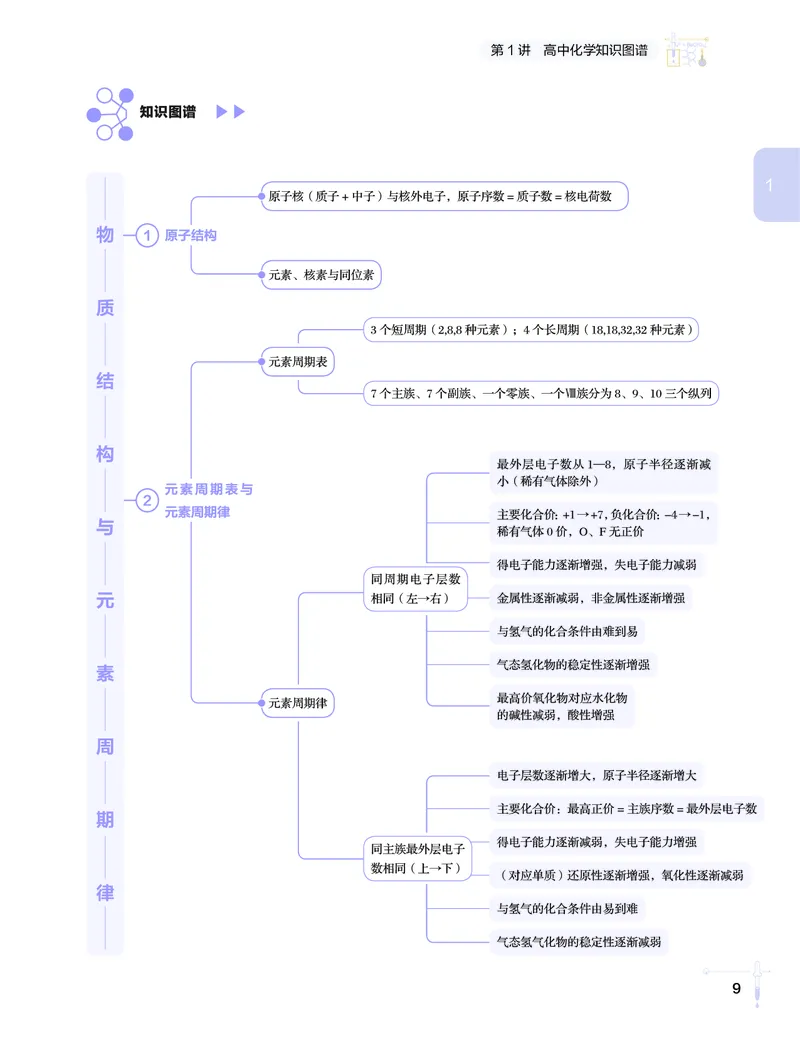
9高中/化学
1
10第1讲 高中化学知识图谱
1
11高中/化学
1
12第1讲 高中化学知识图谱
1
13高中/化学
1
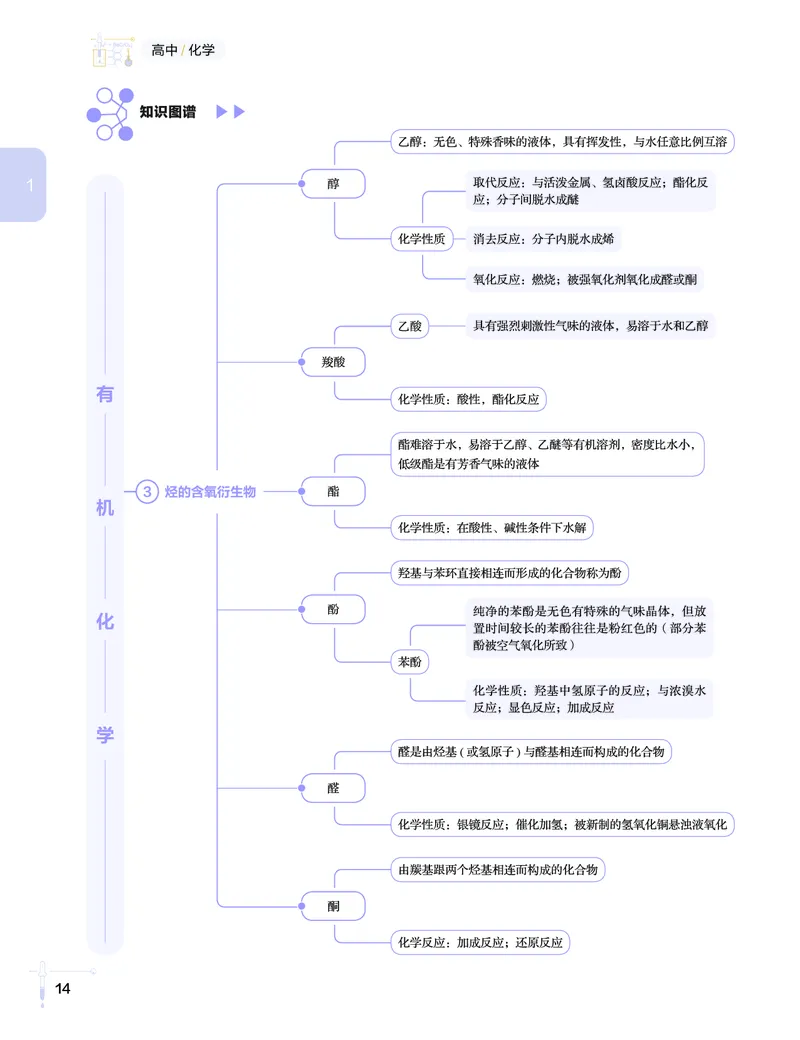
14第1讲 高中化学知识图谱
1
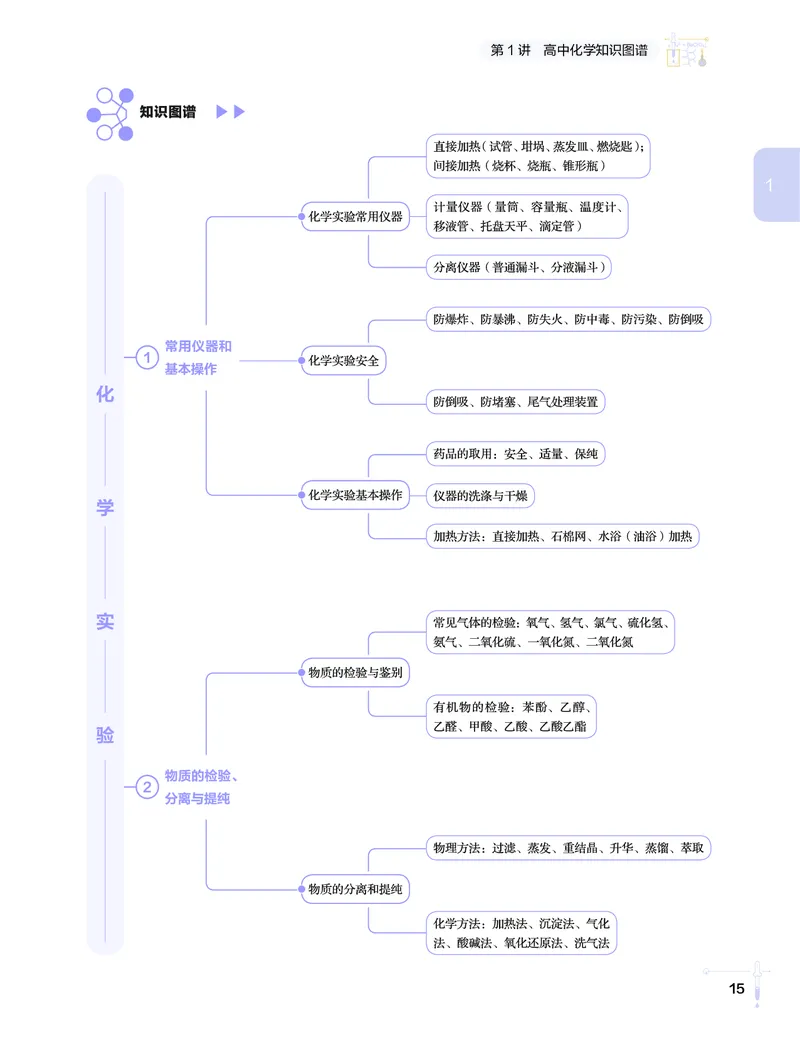
15高中/化学
1
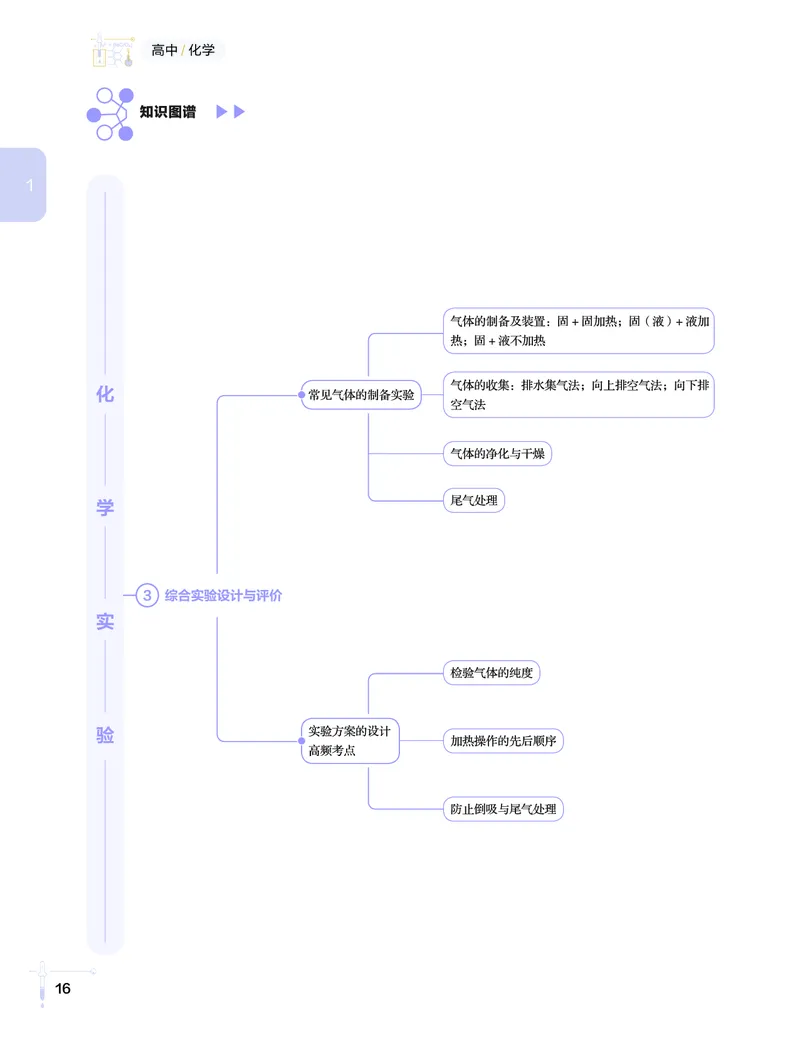
16第1讲 高中化学知识图谱
1
C H E M I S T RY
17第2讲
课本方程式
第 2 讲
课本方程式第2讲 课本方程式
模块 1
必修一(新人教)
1
知识精讲
2
电离方程式:
1
NaCl===Na++Cl-
2 KNO 3 ===K++NO- 3
3
HCl===H++Cl-
5 H 2 SO 4 ===2H++SO2 4 -
6 HNO 3 ===H++NO- 3
离子方程式:
7
Ba2++SO2
4
-===BaSO
4
#
8 H++OH-===H 2 O
9
Zn+2H+===Zn2++H
2
"
氧化还原反应:
10 Fe+CuSO 4 ===FeSO 4 +Cu
∆
11 2Na+Cl 2 ===2NaCl
点燃
12 H 2 +Cl 2 ===2HCl
∆
13 CuO+H 2 ===Cu+H 2 O
钠及其化合物:
14 4Na+O 2 ===2Na 2 O
∆
15 2Na+O 2 ===Na 2 O 2
16 2Na+2H 2 O===2NaOH+H 2 "
17 2Na 2 O 2 +2H 2 O===4NaOH+O 2 "
18 2Na 2 O 2 +2CO 2 ===2Na 2 CO 3 +O 2
∆
19 2NaHCO 3 ===Na 2 CO 3 +H 2 O+CO 2 "
19高中/化学
氯及其化合物:
∆
20 2Na+Cl 2 ===2NaCl
∆
21 2Fe+3Cl 2 ===2FeCl 3
∆
22 Cu+Cl 2 ===CuCl 2
点燃
23 H 2 +Cl 2 ===2HCl
24 Cl 2 +H 2 O===HCl+HClO
光照
2 25 2HClO=== 2HCl+O 2 "
26 Cl 2 +2NaOH===NaCl+NaClO+H 2 O
27 2Cl 2 +2Ca(OH) 2 ===Ca(ClO) 2 +CaCl 2 +2H 2 O
∆
28 MnO 2 +4HCl(浓)===MnCl 2 +Cl 2 "+2H 2 O
29
Ag++Cl-===AgCl#
30 2Ag++CO2 3 -===Ag 2 CO 3 #
31 Ag 2 CO 3 +2H+===2Ag++CO 2 "+H 2 O
铁及其化合物
高温
32 3Fe+4H 2 O(g)===Fe 3 O 4 +4H 2
33 FeO+2H+===Fe2++H 2 O
34 Fe 2 O 3 +6H+===2Fe3++H 2 O
35 FeSO 4 +2NaOH===Fe(OH) 2 #+Na 2 SO 4
36 4Fe(OH) 2 +O 2 +2H 2 O===4Fe(OH) 3
∆
37 2Fe(OH) 3 ===Fe 2 O 3 +3H 2 O
38
2Fe3++Fe===3Fe2+
39
2Fe2++Cl
2
===2Fe3++2Cl-
铝及其化合物
40 Al 2 O 3 +6HCl===2AlCl 3 +3H 2 O
41 2Al+6HCl===2AlCl 3 +3H 2 "
42 2Al+2NaOH+2H 2 O===2NaAlO 2 +3H 2 "
43 Al 2 O 3 +2NaOH===2NaAlO 2 +H 2 O
20第2讲 课本方程式
物质结构与元素周期律:
∆
44 4Li+O 2 ===2Li 2 O
∆
45 2Na+O 2 ===Na 2 O 2
46 2Na+2H 2 O===2NaOH+H 2 "
47 2K+2H 2 O===2KOH+H 2 "
48 2NaBr+Cl 2 ===2NaCl+Br 2
2
21高中/化学
模块 2
必修二(新人教)
2
知识精讲
2
硫及其化合物:
∆
1 S+Fe===FeS
∆
2 S+2Cu===Cu 2 S
∆
3 S+H 2 ===H 2 S
点燃
4 S+O 2 ===SO 2
5 SO 2 +H 2 O⇌H 2 SO 3
6 2SO 2 +O 2
催⇌化剂
2SO 3
∆
7 SO 3 +H 2 O===H 2 SO 4
8 SO 2 +2H 2 S===3S+2H 2 O
∆
9 Cu+2H 2 SO 4 (浓)===CuSO 4 +SO 2 "+2H 2 O
∆
10 C+2H 2 SO 4 (浓)===CO 2 "+2SO 2 "+2H 2 O
氮及其化合物
点燃
11 N 2 +3Mg===Mg 3 N 2
放电或高温
12 N 2 +O 2 === 2NO
13 N 2 +3H 2
高温⇌高压
2NH 3
催化剂
14 2NO+O 2 ===2NO 2
15 3NO 2 +H 2 O===2HNO 3 +NO
16 NH 3 +H 2 O⇌NH 3 (cid:1)H 2 O⇌NH+ 4 +OH-
17 NH 3 +HCl===NH 4 Cl
催化剂
18 4NH 3 +5O 2 ===4NO+6H 2 O
∆
∆
19 NH 4 Cl===NH 3 "+HCl"
∆
20 NH 4 HCO 3 ===NH 3 "+H 2 O+CO 2 "
∆
21 2NH 4 Cl+Ca(OH) 2 ===CaCl 2 +2H 2 O+2NH 3
∆
22 NH+ 4 +OH-===NH 3 "+H 2 O
∆
23 4HNO 3 ===4NO 2 "+O 2 "+2H 2 O
或光照
22第2讲 课本方程式
24 Cu+4HNO 3 (浓)===Cu(NO 3 ) 2 +2NO 2 "+2H 2 O
25 3Cu+8HNO 3 (稀)===3Cu(NO 3 ) 2 +2NO"+4H 2 O
无机非金属材料:
高温
26 SiO 2 +2C===Si+2CO"
有机化合物:
2
27 CH 4 +2O 2
(cid:0)点(cid:0)燃!CO
2 +2H 2 O
28 C 3 H 8 +5O 2
(cid:0)点(cid:0)燃!3CO
2 +4H 2 O
29 CH 4 +Cl 2
(cid:0)光!CH
3 Cl+HCl
30 CH 3 Cl+Cl 2
(cid:0)光!CH
2 Cl 2 +HCl
31 CH 2 Cl 2 +Cl 2
(cid:0)光!CHCl
3 +HCl
32 CHCl 3 +Cl 2
(cid:0)光!CCl
4 +HCl
33 C 2 H 4 +3O 2
(cid:0)点(cid:0)燃!2CO
2 +2H 2 O
34 CH 2 =CH 2 +H 2 (cid:0)催(cid:0)(cid:0)化(cid:0)剂!CH 3 (cid:0)CH 3
△
35 CH 2 =CH 2 +H 2 O(cid:0)(cid:0)催(cid:0)化(cid:0)剂(cid:0)!CH 3 (cid:0)CH 2 (cid:0)OH
加热加压
36 2CH 3 CH 2 OH+2Na!(cid:0) 2CH 3 CH 2 ONa+H 2 "
37 CH 3 CH 2 OH+3O 2
(cid:0)点(cid:0)燃!2CO
2 +3H 2 O
38 2CH 3 CH 2 OH+O 2
(cid:0)催(cid:0)(cid:0)化(cid:0)剂!2CH
3 CHO+2H 2 O
△
39 CH 3 COOH+C 2 H 5 OH
浓⇌硫酸
CH 3 COOC 2 H 5 +H 2 O
∆
化学与可持续发展:
∆
40 2HgO===2Hg+O 2 "
∆
41 2Ag 2 O===4Ag+O 2 "
电解
42 MgCl 2 (熔融)===Mg+Cl 2 "
43 2Al 2 O 3 (熔融)= 电 = 解 =4Al+3O 2 "
冰晶石
电解
44 2NaCl(熔融)===2Na+Cl 2 "
高温
45 Fe 2 O 3 +2Al===2Fe+Al 2 O 3
高温
46 C+H 2 O(g)===CO+H 2
23高中/化学
模块 3
电化学
3
知识精讲
2
1 锌铜原电池:
负极:Zn(cid:0)2e-===Zn2+
正极:Cu2++2e-===Cu
总反应:Zn+Cu2+===Zn2++Cu
2 碱性锌锰电池:
负极:Zn+2OH-(cid:0)2e-===Zn(OH)
2
正极:2MnO +2H O+2e-===2MnO(OH)+2OH-
2 2
总反应:Zn+2MnO +2H O===2MnO(OH)+Zn(OH)
2 2 2
3 铅酸蓄电池:
负极:Pb+SO2-(cid:0)2e-===PbSO
4 4
正极:PbO +4H++SO2-+2e-===PbSO +2H O
2 4 4 2
总反应:Pb+PbO +2H SO ===2PbSO +2H O
2 2 4 4 2
4 氢氧燃料电池:
负极:2H (cid:0)4e-===4H+
2
正极:O +4H++4e-===2H O
2 2
总反应:2H +O ===2H O
2 2 2
5 电解氯化铜:
阳极:2Cl-(cid:0)2e-===Cl "
2
阴极:Cu2++2e-===Cu
电解
总反应:Cu2++2Cl-===Cu+Cl "
2
6 电解饱和食盐水:
阳极:2Cl-(cid:0)2e-===Cl "
2
阴极:2H O+2e-===H "+2OH-
2 2
电解
总反应:2Cl-+2H O===Cl "+H "+2OH-
2 2 2
7 电解熔融氯化钠:
阳极:2Cl-(cid:0)2e-===Cl "
2
阴极:Na++e-===Na
电解
总反应:2NaCl(熔融)===2Na+Cl "
2
24第2讲 课本方程式
8 析氢腐蚀:
负极:Fe(cid:0)2e-===Fe2+
正极:2H++2e-===H "
2
总反应:Fe+2H+===Fe2++H "
2
9 吸氧腐蚀:
负极:Fe(cid:0)2e-===Fe2+
正极:2H O+O +4e-===4OH-
2 2
总反应:2Fe+O 2 +2H 2 O===2Fe(OH) 2 2
25高中/化学
模块 4
有机化学基础
4
知识精讲
2
有机化合物:
1 2CH 3 CH 2 OH+2Na!(cid:0) 2CH 3 CH 2 ONa+H 2 "
∆
2 CH 3 CH 2 OH+HBr(cid:0)!CH 3 CH 2 Br+H 2 O
3 CH(cid:17)CH+Br 2 !(cid:0) CHBr=CHBr
4 CHBr=CHBr+Br 2 !(cid:0) CHBr 2 (cid:0)CHBr 2
5 CH(cid:17)CH+H 2 (cid:0)催(cid:0)(cid:0)化(cid:0)剂!CH 2 =CH 2
∆
6
CH(cid:17)CH+HCl(cid:0)催(cid:0)(cid:0)化(cid:0)剂!CH
2 =CHCl
∆
7
CH(cid:17)CH+H
2
O(cid:0)催(cid:0)(cid:0)化(cid:0)剂!CH
3
(cid:0)CHO
∆
8
9
10
11
12
13 C 2 H 5 (cid:0)Br+NaOH(cid:0)水!C 2 H 5 (cid:0)OH+NaBr
∆
14 CH 3 CH 2 Br+NaOH(cid:0)乙(cid:0)醇!CH 2 =CH 2 "+NaBr+H 2 O
∆
15 CH 3 CH 2 OH(cid:0)浓(cid:0)(cid:0)硫(cid:0)酸!CH 2 =CH 2 "+H 2 O
170℃
16 2CH 3 CH 2 OH(cid:0)浓(cid:0)(cid:0)硫(cid:0) ◦ 酸!C 2 H 5 (cid:0)O(cid:0)C 2 H 5 +H 2 O
140 C
17
26第2讲 课本方程式
18
19
20 CH 3 CHO+H 2
(cid:0)催(cid:0)(cid:0)化(cid:0)剂!CH
3 CH 2 OH
2
∆
21 CH 3 CHO+HCN!(cid:0) CH 3 CH(OH)CN
∆
22 CH 3 CHO+2[Ag(NH 3 ) 2 ]OH(cid:0)!CH 3 COONH 4 +2Ag#+3NH 3 +H 2 O
∆
23 CH 3 CHO+2Cu(OH) 2 +NaOH(cid:0)!CH 3 COONa+Cu 2 O#+3H 2 O
24 2CH 3 CHO+O 2
(cid:0)催(cid:0)(cid:0)化(cid:0)剂!2CH
3 COOH
∆
25 CH 3 COCH 3 +H 2
(cid:0)催(cid:0)(cid:0)化(cid:0)剂!CH
3 CH(OH)CH 3
∆
26 CH 3 COOH+C 2 H 5 OH
浓⇌硫酸
CH 3 COOC 2 H 5 +H 2 O
∆
27 CH 3 COOC 2 H 5 +H 2 O
稀⇌硫酸
CH 3 COOH+C 2 H 5 OH
∆
∆
28 CH 3 COOC 2 H 5 +NaOH(cid:0)!CH 3 COONa+C 2 H 5 OH
∆
29 RCONH 2 +H 2 O+HCl(cid:0)!RCOOH+NH 4 Cl
∆
30 RCONH 2 +NaOH(cid:0)!RCOONa+NH 3 "
27第3讲
近三年高考方程式
第 3 讲
近三年高考方程式第3讲 近三年高考方程式
模块 1
2020 年高考
1
知识精讲
2020 年全国统一高考化学试卷(新课标 Ⅰ)
1 甲醇羰基化反应为 CH 3 OH+CO===CH 3 CO 2 H
2 CH 3 OH+HI===CH 3 I+H 2 O
3
3 锌-二氧化碳水介质电池:
放电时,负极反应为:Zn(cid:0)2e-+4OH-===Zn(OH) 2-
4
充电时,电池总反应为:2Zn(OH) 2-===2Zn+O "+4OH-+2H O
4 2 2
4 VO++2H++MnO 2 ===VO+ 2 +Mn2++H 2 O
5 HCl+NaAl(OH) 4 ===Al(OH) 3 #+NaCl+H 2 O
6 用原电池验证不同化合价铁的氧化还原能力:
石墨电极:Fe3++e-===Fe2+
铁电极:Fe(cid:0)2e-===Fe2+
7 2V 2 O 5 (s)+2SO 2 (g)===2VOSO 4 (s)+V 2 O 4 (s) ∆H=-351kJ(cid:1)mol-1
2020 年全国统一高考化学试卷(新课标 Ⅱ)
1 H 2 CO 3 ⇌H++HCO- 3
2 银-氧化钨电致变色器总反应:WO 3 +xAg===Ag x WO 3
3 2Cl 2 +HgO===Cl 2 O+HgCl 2
4 NaHCO 3 +NaHSO 4 ===Na 2 SO 4 +CO 2 "+H 2 O
5 ClO-+Cl-+2H+===Cl 2 "+H 2 O
6 2MnO- 4 +5H 2 C 2 O 4 +6H+===2Mn2++10CO 2 "+8H 2 O
7 2CH 4
(cid:0)高(cid:0)温!C
2 H 6 +H 2
8 电解二氧化碳阴极:CO 2 +2e-===CO+O2-
9
金属卤化物光电材料:2Eu3++Pb===2Eu2++Pb2+、2Eu2++I
2
===2Eu3++2I-
2020 年全国统一高考化学试卷(新课标 Ⅲ)
1 3SO2 3 -+Cl 2 +H 2 O===2HSO- 3 +2Cl-+SO2 4 -
2 碱性硼化钒-空气电池:
硼化钒电极:VB +16OH-(cid:0)11e-===VO3-+2B(OH) -+4H O
2 4 4 2
29高中/化学
电池总反应:4VB +11O +20OH-+6H O===8B(OH) -+4VO3-
2 2 2 4 4
冰水
3 Cl 2 +2OH-===ClO-+Cl-+H 2 O
4 AlO- 2 +H++H 2 O===Al(OH) 3 #
5 2Ni2++ClO-+4OH-===2NiOOH#+Cl-+H 2 O
2020 年北京市高考化学试卷
1 用碳酸钠溶液处理锅炉水垢:CaSO 4 (s)+CO2 3 -⇌CaCO 3 (s)+SO2 4 -
2 湿润的淀粉碘化钾试纸遇氯气变蓝:Cl 2 +2I-===2Cl-+I 2
高温
3 铝粉和氧化铁组成的铝热剂用于焊接钢轨:2Al+Fe 2 O 3 ===Al 2 O 3 +2Fe
4 淡黄色的过氧化钠敞口放置变成白色:2Na 2 O 2 +2CO 2 ===2Na 2 CO 3 +O 2
3
2Na O +2H O===4NaOH+O ";2NaOH+CO ===Na CO +H O
2 2 2 2 2 2 3 2
∆
5 2Ba(NO 3 ) 2 ===2BaO+O 2 "+4NO 2 "
6 BaO 2 +2HCl===BaCl 2 +H 2 O 2
7 电解制备过氧化氢阴极反应:O 2 +2H++2e-===H 2 O 2
8 HC(cid:17)CCH 2 OH+CH 3 COOH 浓⇌硫酸 CH 3 COOCH 2 C(cid:17)CH+H 2 O
∆
9 HAuCl 4 ⇌H++AuCl- 4
10 3Cu+8HNO 3 (稀)===3Cu(NO 3 ) 2 +2NO"+4H 2 O
11 溶金反应:Au+4NaCl+5HNO 3 ===HAuCl 4 +2H 2 O+NO"+4NaNO 3
12 MnO 2 +4H++2Fe2+===Mn2++2Fe3++2H 2 O
13 电解制备二氧化锰:Mn2+(cid:0)2e-+2H 2 O===MnO 2 +4H+
∆
14 4Na 2 SO 3 ===Na 2 S+3Na 2 SO 4
15
S2-+Cu2+===CuS#
16
S2
x
-+2H+===H
2
S"+(x-1)S#
2020 年海南省高考化学试卷
1 Cu2++4NH 3 (cid:1)H 2 O===[Cu(NH 3 ) 4 ] 2++4H 2 O
2 燃料电池正极:O 2 +4e-(cid:0)4H+===2H 2 O
高温
3 Fe 2 O 3 +3CO===2Fe+3CO 2
4 S 2 O2 8 -+H 2 O⇌HSO- 5 +H++SO2 4 -
5 2Na+2H 2 O===2NaOH+H 2 "
30第3讲 近三年高考方程式
2020 年江苏省高考化学试卷
1 Cl 2 +H 2 O⇌H++Cl-+HClO
2 3NO 2 +H 2 O===2H++2NO- 3 +NO
3 AlO- 2 +CO 2 +2H 2 O===Al(OH) 3 #+HCO- 3
4 硝酸银与过量氨水反应:Ag++3NH 3 (cid:1)H 2 O===Ag(NH 3 ) + 2 +OH-+NH+ 4 +2H 2 O
5 牺牲阳极保护法的阴极反应:2H 2 O+2e-===H 2 "+2OH-
6 2NH 3 +H 2 O+SO 2 ===SO2 3 -+2NH+ 4
7 ZnSO 3 +SO 2 +H 2 O===Zn2++2HSO- 3
冰水
8 Cl 2 +2OH-===Cl-+ClO-+H 2 O
9 Fe2++HCO- 3 +NH 3 (cid:1)H 2 O===FeCO 3 #+NH+ 4 +H 2 O
催化剂 3
10 HCO- 3 +H 2 === HCOO-+H 2 O
11 HCOOH 燃料电池负极:HCOO-(cid:0)2e-+2OH-===HCO- 3 +H 2 O
12 2HCOOH+2OH-+O 2 ===2HCO- 3 +2H 2 O
2020 年山东省高考化学试卷
1 MgO+2NH 4 Cl===MgCl 2 +2NH 3 "+H 2 O
2 微生物脱盐电池负极:CH 3 COO-+2H 2 O(cid:0)8e-===2CO 2 "+7H+
3 电解制备双氧水阳极:2H 2 O(cid:0)4e-===4H++O 2 "
4 MnO 2 +BaS+H 2 O===Ba(OH) 2 +MnO+S
5 Mn2++HCO- 3 +NH 3 (cid:1)H 2 O===MnCO 3 #+NH+ 4 +H 2 O
6 CH 3 COOH+CH 3 CH 2 OH
浓⇌硫酸
CH 3 COOC 2 H 5 +H 2 O
∆
7 Ca(ClO) 2 +4HCl===CaCl 2 +2Cl 2 "+2H 2 O
2020 年天津市高考化学试卷
1 碳酸钙与稀硝酸反应:CaCO 3 +2H+===Ca2++CO 2 "+H 2 O
2
硫酸亚铁溶液与溴水:2Fe2++Br
2
===2Fe3++2Br-
3 氢氧化钠与过量草酸溶液反应:H 2 C 2 O 4 +OH-===HC 2 O- 4 +H 2 O
4 C 6 H 5 O-+CO 2 +H 2 O===C 6 H 5 OH+HCO- 3
5 熔融钠-硫电池总反应:2Na+xS
放⇌电
Na 2 S x
充电
放电时正极反应:xS+2Na++2e-===Na S
2 x
6 2Co(OH) 3 +6H++2Cl-===2Co2++Cl 2 "+6H 2 O
7 制备硫酸镍:3Ni+3H 2 SO 4 +2HNO 3 ===3NiSO 4 +2NO"+4H 2 O
31高中/化学
模块 2
2019 年高考
2
知识精讲
2019 年全国统一高考化学试卷(新课标 Ⅰ)
1 利用生物燃料电池原理研究室温下氨的合成,阴极区,在氢化酶作用下发生反应:
H +2MV2+===2H++2MV+
2
3
2 NH 3 +NH 4 HCO 3 ===(NH 4 ) 2 CO 3
3 2Mg2++3CO2 3 -+2H 2 O===Mg(OH) 2 (cid:1)MgCO 3 #+2HCO- 3
2019 年全国统一高考化学试卷(新课标 Ⅱ)
1 向硫酸铜溶液中加入足量锌粉,溶液蓝色消失:Zn+CuSO 4 ===Cu+ZnSO 4
2 澄清石灰水久置后出现白色固体:Ca(OH) 2 +CO 2 ===CaCO 3 #+H 2 O
3 过氧化钠在空气中放置后由淡黄色变为白色:2Na 2 O 2 +2CO 2 ===2Na 2 CO 3 +O 2
4 向氢氧化镁悬浊液中滴加足量氯化铁溶液出现红褐色沉淀:3Mg(OH) 2 +2FeCl 3 ===2Fe(OH) 3 +3MgCl 2
900-1200℃
5 BaSO 4 +4C === BaS+4CO"
6 CO+H 2 O===CO 2 +H 2
7
Ba2++S2-+Zn2++SO2
4
-===ZnS(cid:1)BaSO
4
#
2019 年全国统一高考化学试卷(新课标 Ⅲ)
1 3D-Zn-NiOOH 二次电池:
总反应:Zn(s)+2NiOOH(s)+H O(l)
放⇌电
ZnO(s)+2Ni(OH) (s)
2 2
充电
充电时阳极反应:Ni(OH) (s)+OH-(aq)(cid:0)e-===NiOOH(s)+H O(l)
2 2
放电时负极反应:Zn(s)+2OH-(aq)(cid:0)2e-===ZnO(s)+H O(l)
2
2 MnO 2 +MnS+2H 2 SO 4 ===2MnSO 4 +S+2H 2 O
3 MgF ⇌Mg2++2F-
2
4 Mn2++2HCO- 3 ===MnCO 3 #+CO 2 "+H 2 O
5 在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主
要包括电化学过程和化学过程,负极区发生的反应有:Fe3++e-===Fe2+;4Fe2++O +4H+===4Fe3++2H O
2 2
32第3讲 近三年高考方程式
2019 年北京市高考化学试卷
1
氯化钠溶于水:NaCl===Na++Cl-
电解
2 电解氯化铜溶液:CuCl 2 ===Cu+Cl 2 "
3 乙酸在水中电离:CH 3 COOH⇌CH 3 COO-+H+
4 氢气与氯气反应能量变化:H 2 (g)+Cl 2 (g)===2HCl(g) ∆H=-183kJ(cid:1)mol-1
5 草酸有酸性:Ca(OH) 2 +H 2 C 2 O 4 ===CaC 2 O 4 #+2H 2 O
6 草酸酸性大于碳酸:NaHCO 3 +H 2 C 2 O 4 ===NaHC 2 O 4 +CO 2 "+H 2 O
7 草酸有还原性:2MnO- 4 +5H 2 C 2 O 4 +6H+===2Mn2++10CO 2 "+8H 2 O
8 草酸可发生酯化反应:HOOCCOOH+2C 2 H 5 OH
浓⇌硫酸
C 2 H 5 OOCCOOC 2 H 5 +2H 2 O
∆
9 BrO- 3 +5Br-+6H+===3Br 2 +3H 2 O 3
催化剂
10 CH 4 +2H 2 O(g) === 4H 2 +CO 2
11 CO 2 +CaO===CaCO 3
12 电解水制氢,产生氢气的电极方程式:2H 2 O+2e-===H 2 "+2OH-
∆
13 Cu+2H 2 SO 4 (浓)===CuSO 4 +SO 2 "+2H 2 O
14 亚硫酸银溶于氨水:Ag 2 SO 3 +4NH 3 (cid:1)H 2 O===2Ag(NH 3 ) + 2 +SO2 3 -+4H 2 O
15 Ag 2 SO 4 (s)⇌2Ag++SO2 4 -
16 2Ag++SO 2 +H 2 O===Ag 2 SO 3 #+2H+
2019 年海南省高考化学试卷
1 银-锌电池
总反应:Ag O+Zn+H O===2Ag+Zn(OH)
2 2 2
负极:Zn+2OH-(cid:0)2e-===Zn(OH)
2
正极:Ag O+H O+2e-===2Ag+2OH-
2 2
2
向溴化亚铁溶液中通入过量氯气:4Br-+2Fe2++3Cl
2
===2Fe3++2Br
2
+6Cl-
3 向碳酸钠溶液中通入少量二氧化碳:CO2 3 -+CO 2 +H 2 O===2HCO- 3
4 向碘化钾溶液中加入少量双氧水:2H++2I-+H 2 O 2 ===I 2 +2H 2 O
5 向硫化钠溶液中通入过量二氧化硫:2S2-+5SO 2 +2H 2 O===3S#+4HSO- 3
6 ZnS 2 O 4 +Na 2 CO 3 ===ZnCO 3 #+Na 2 S 2 O 4
7 锂-二氧化硫电池:
正极:2SO +2e-===S O2-
2 2 4
总反应:2Li+2SO ===Li S O
2 2 2 4
∆
8 2NH 4 Cl+Ca(OH) 2 ===CaCl 2 +2NH 3 "+2H 2 O
33高中/化学
2019 年江苏省高考化学试卷
1 室温下用稀氢氧化钠溶液吸收氯气:Cl 2 +2OH-===ClO-+Cl-+H 2 O
2 用铝粉和氢氧化钠溶液反应制取少量氢气:2Al+2OH-+2H 2 O===2AlO- 2 +3H 2 "
3 室温下用稀硝酸溶解铜:3Cu+2NO- 3 +8H+===3Cu2++2NO"+4H 2 O
4 向硅酸钠溶液中滴加稀盐酸:SiO2 3 -+2H+===H 2 SiO 3 #
5
吸氧腐蚀负极:Fe(cid:0)2e-===Fe2+
催化剂
6 2NH 3 +2O 2 ===N 2 O+3H 2 O
∆
7 3HClO+2NO+H 2 O===3Cl-+2NO- 3 +5H+
8 过氧化氢氧化亚铁离子:2Fe2++H 2 O 2 +2H+===2Fe3++2H 2 O
9 HCO- 3 +NH 3 (cid:1)H 2 O===NH+ 4 +CO2 3 -+H 2 O
3 400-600 ◦ C
10 CaC 2 O 4 === CaCO 3 +CO"
11 电解二氧化碳制甲酸阴极:CO 2 +H++2e-===HCOO-
2019 年天津市高考化学试卷
1 向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解:Mg(OH) 2 +2NH+ 4 ===Mg2++2NH 3 (cid:1)H 2 O
2 向沸水中滴加饱和氯化铁溶液得到红褐色液体:Fe3++3H 2 O===3H++Fe(OH) 3 (胶体)
3 二氧化硫使酸性高锰酸钾溶液褪色:5SO 2 +2MnO- 4 +2H 2 O===5SO2 4 -+2Mn2++4H+
4 氧化亚铁溶于稀硝酸:3FeO+10H++NO- 3 ===3Fe3++NO"+5H 2 O
5 锌-碘溴液流电池正极反应:I 2 Br-+2e-===2I-+Br-
6 SbCl 3 +H 2 O⇌SbOCl#+2HCl
◦
300 C
7 Si(s)+3HCl(g)===SiHCl 3 (g)+H 2 (g) ∆H=-225kJ(cid:1)mol-1
8 惰性电极电解 KOH 溶液制备氢气阴极:2H 2 O+2e-===H 2 "+2OH-
34第3讲 近三年高考方程式
模块 3
2018 年高考
3
知识精讲
2018 年全国统一高考化学试卷(新课标 Ⅰ)
1 二氧化碳 + 硫化氢协同转化装置:
阴极的电极反应:CO +2H++2e-===CO+H O
2 2
3
协同转化总反应:CO +H S===CO+H O+S
2 2 2
2
Zn+2Cr3+===Zn2++2Cr2+
3 2NaHSO 3 ===Na 2 S 2 O 5 +H 2 O
4 三室膜电解制备焦亚硫酸钠,阳极反应:2H 2 O(cid:0)4e-===O 2 "+4H+
5 S 2 O2 5 -+2I 2 +3H 2 O===2SO2 4 -+4I-+6H+
2018 年全国统一高考化学试卷(新课标 Ⅱ)
1 钠-二氧化碳二次电池:
总反应:3CO +4Na⇌2Na CO +C
2 2 3
放电时,正极反应为:3CO +4e-===2CO2-+C
2 3
充电时,负极反应为:Na++e-===Na
高温
2 2ZnS+3O 2 ===2ZnO+2SO 2
3
Cd2++Zn===Cd+Zn2+
4
电解硫酸锌阴极反应:Zn2++2e-===Zn
5 3FeC 2 O 4 +2K 3 [Fe(CN) 6 ]===Fe 3 [Fe(CN) 6 ] 2 #+3K 2 C 2 O 4
2018 年全国统一高考化学试卷(新课标 Ⅲ)
1 KH(IO 3 ) 2 +KOH===2KIO 3 +H 2 O
2 电解制备碘酸钾阴极:2H 2 O+2e-===2OH-+H 2 "
3 2SiHCl 3 +3H 2 O===(HSiO) 2 O+6HCl
∆
4 CH 2 ClC(cid:17)CH+NaCN(cid:0)!NCCH 2 C(cid:17)CH+NaCl
35高中/化学
2018 年北京市高考化学试卷
1 硬脂酸与乙醇的酯化反应:C 17 H 35 COOH+C 2 H1 5 8OH 浓⇌硫 ∆ 酸 C 17 H 35 CO18OC 2 H 5 +H 2 O
2 常温下,0.1mol(cid:1)L-1 氨水的 pH=11.1:NH 3 (cid:1)H 2 O⇌NH+ 4 +OH-
3
电解精炼铜阴极反应:Cu2++2e-===Cu
4
亚硫酸钠溶液中存在水解平衡:SO2
3
-+H
2
O⇌HSO-
3
+OH-
5 CH 2 =CHCH 3 +Cl 2
(cid:0)高(cid:0)温!CH
2 =CHCH 2 Cl+HCl
6 CH 2 OHCHOHCH 2
OH(cid:0)浓(cid:0)(cid:0)硫(cid:0)酸!CH
2 =CHCHO+2H 2 O
∆
∆ 1
7 2Ca 5 (PO 4 ) 3 F+10H 2 SO 4 +5H 2 O===10CaSO 4 (cid:1) H 2 O+6H 3 PO 4 +2HF
2
8 BaCO 3 +SO2 4 -+2H 3 PO 4 ===BaSO 4 +CO 2 "+H 2 O+2H 2 PO- 4
3 9 3SO 2 (g)+2H 2 O(g)===2H 2 SO 4 (l)+S(s) ∆H=-254kJ(cid:1)mol-1
10 I 2 +2H 2 O+SO 2 ===4H++SO2 4 -+2I-
11 2MnO- 4 +10Cl-+16H+===5Cl 2 "+2Mn2++8H 2 O
12 Cl 2 +2KOH===KCl+KClO+H 2 O
13 4FeO2 4 -+20H+===4Fe3++3O 2 "+10H 2 O
2018 年海南省高考化学试卷
1 镁氧电池
总反应式:2Mg+O +2H O===2Mg(OH)
2 2 2
负极:Mg(cid:0)2e-+2OH-===Mg(OH) #
2
正极:O +4e-+2H O===4OH-
2 2
2 N 2 +3H 2
催⇌化剂
2NH 3
高温高压
3 Cu+H 2 O 2 +H 2 SO 4 ===CuSO 4 +2H 2 O
4
Cu+2Fe3+===Cu2++2Fe2+
5 CH 4 +Cl 2
(cid:0)光(cid:0)照!CH
3 Cl+HCl
点燃
6 4Na+3CO 2 ===2Na 2 CO 3 +C
2018 年江苏省高考化学试卷
1
饱和碳酸钠溶液与硫酸钙固体反应:CO2
3
-+CaSO
4
⇌CaCO
3
+SO2
4
-
2 酸化碘酸钠和碘化钠的混合溶液:5I-+IO- 3 +6H+===3I 2 +3H 2 O
3 次氯酸钾与氢氧化铁反应:3ClO-+2Fe(OH) 3 +4OH-===2FeO2 4 -+3Cl-+5H 2 O
通电
4
电解饱和食盐水:2Cl-+2H
2
O===2OH-+H
2
"+Cl
2
"
36第3讲 近三年高考方程式
5 SO 2 +OH-===HSO- 3
∆
6 3Cl 2 +6OH-===ClO- 3 +5Cl-+3H 2 O
7 电解亚硝酸溶液阳极:HNO 2 (cid:0)2e-+H 2 O===3H++NO- 3
8 2HNO 2 +(NH 2 ) 2 CO===2N 2 "+CO 2 "+3H 2 O
2018 年天津市高考化学试卷
1 2Mg(OH) 2 +2SO 2 +O 2 ===2MgSO 4 +2H 2 O
2 2NO+3H 2 O 2 ===2H++2NO- 3 +2H 2 O
3 氧气辅助的铝-二氧化碳电池:
负极:Al(cid:0)3e-===Al3+
正极:6O +6e-===6O-;6CO +6O-===3C O2-+6O 3
2 2 2 2 2 4 2
总反应:2Al+6CO ===Al (C O )
2 2 2 4 3
37高中/化学
3
C H E M I S T RY
38