文档内容
【基础知识】电解池及金属的电化学腐蚀与防护
考点一 电解原理
【必备知识】
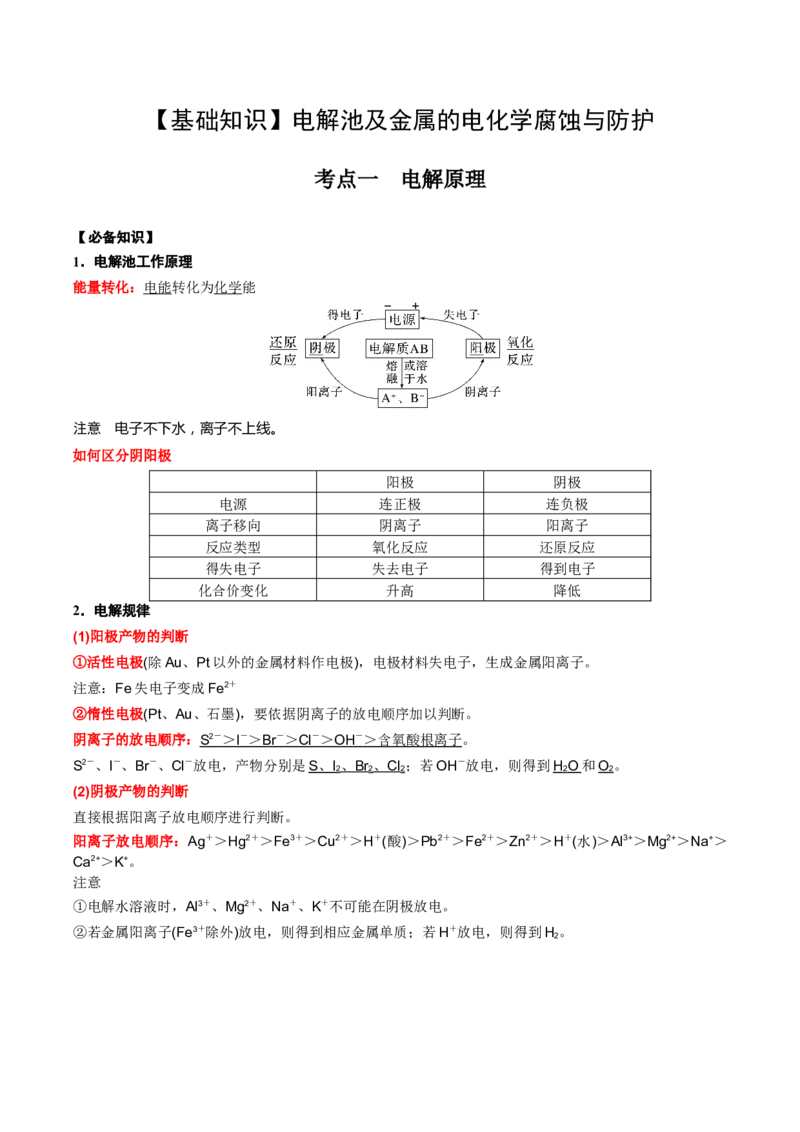
1.电解池工作原理
能量转化:电能转化为化学能
注意 电子不下水,离子不上线。
如何区分阴阳极
阳极 阴极
电源 连正极 连负极
离子移向 阴离子 阳离子
反应类型 氧化反应 还原反应
得失电子 失去电子 得到电子
化合价变化 升高 降低
2.电解规律
(1)阳极产物的判断
①活性电极(除Au、Pt以外的金属材料作电极),电极材料失电子,生成金属阳离子。
注意:Fe失电子变成Fe2+
②惰性电极(Pt、Au、石墨),要依据阴离子的放电顺序加以判断。
阴离子的放电顺序: S 2 - > I - > Br - > C l - > OH - >含氧酸根离子 。
S2-、I-、Br-、Cl-放电,产物分别是 S 、 I 、 B r 、 C l ;若OH-放电,则得到H O 和O 。
2 2 2 2 2
(2)阴极产物的判断
直接根据阳离子放电顺序进行判断。
阳离子放电顺序:Ag+>Hg2+>Fe3+>Cu2+>H+(酸)>Pb2+>Fe2+>Zn2+>H+(水)>Al3+>Mg2+>Na+>
Ca2+>K+。
注意
①电解水溶液时,Al3+、Mg2+、Na+、K+不可能在阴极放电。
②若金属阳离子(Fe3+除外)放电,则得到相应金属单质;若H+放电,则得到H 。
23.常例分析
完成下表(电极为惰性电极)
溶液 溶液复原
类型 实例 电极反应式
pH变化 方法
阳极:2HO-4e-===4H++O↑
2 2
HSO 阴极:4H++4e-===2H↑ 减小
2 4 2
总反应:2HO=====2H↑+O↑
2 2 2
阳极:4OH--4e-===2HO+O↑
2 2
电解
NaOH 阴极:4HO+4e-===2H↑+4OH- 增大 加水
2 2
水型
总反应:2HO=====2H↑+O↑
2 2 2
阳极:2HO-4e-===4H++O↑
2 2
KNO 阴极:4HO+4e-===2H↑+4OH- 不变
3 2 2
总反应:2HO=====2H↑+O↑
2 2 2
阳极:2Cl--2e-===Cl↑
2
通入 HC l
HCl 阴极:2H++2e-===H↑ 增大
2
气体
电解电 总反应:2H++2Cl-=====H↑+Cl↑
2 2
解质型 阳极:2Cl--2e-===Cl↑
2
加 CuC l
CuCl 阴极:Cu2++2e-===Cu - 2
2
固体
总反应:Cu2++2Cl-=====Cu+Cl↑
2
阳极:2Cl--2e-===Cl↑
2
通入 HC l
NaCl 阴极:2HO+2e-===H↑+2OH- 增大
2 2
气体
总反应:2Cl-+2HO=====H↑+Cl↑+2OH
放氢生 2 2 2
碱型 阳极:2Cl--2e-===Cl 2 ↑
通入 HC l
MgCl 阴极:2HO+Mg2++2e-===H ↑+Mg(OH)↓ 增大
2 2 2 2
气体
总反应:MgCl +2HO=====Cl↑+H↑+Mg(OH)↓
2 2 2 2 2
阳极:2HO-4e-===4H++O↑ 加入
2 2
AgNO 阴极:4Ag++4e-===4Ag 减小 Ag O 固
3 2
总反应:4Ag++2HO=====4Ag+O↑+4H+ 体
放氧生 2 2
酸型 阳极:2H 2 O-4e-===O 2 ↑+4H+ 加CuO
CuSO 阴极:2Cu2++4e-===2Cu 减小 或
4
总反应:2CuSO 4 +2H 2 O=====2Cu+O 2 ↑+2H 2 SO 4 CuCO 3
注意 电解质溶液的复原,应遵循“出什么加什么”(即一般加入阴极产物与阳极产物形成的化合物)的原
则。【基础练习】
1、用惰性电极电解下列各组中的三种电解质溶液,在电解的过程中,溶液的pH依次为升高、不变、降低
的是( )
A.AgNO CuCl Cu(NO ) B.KCl NaSO CuSO
3 2 3 2 2 4 4
C.CaCl KOH NaNO D.HCl HNO KSO
2 3 3 2 4
【答案】 B
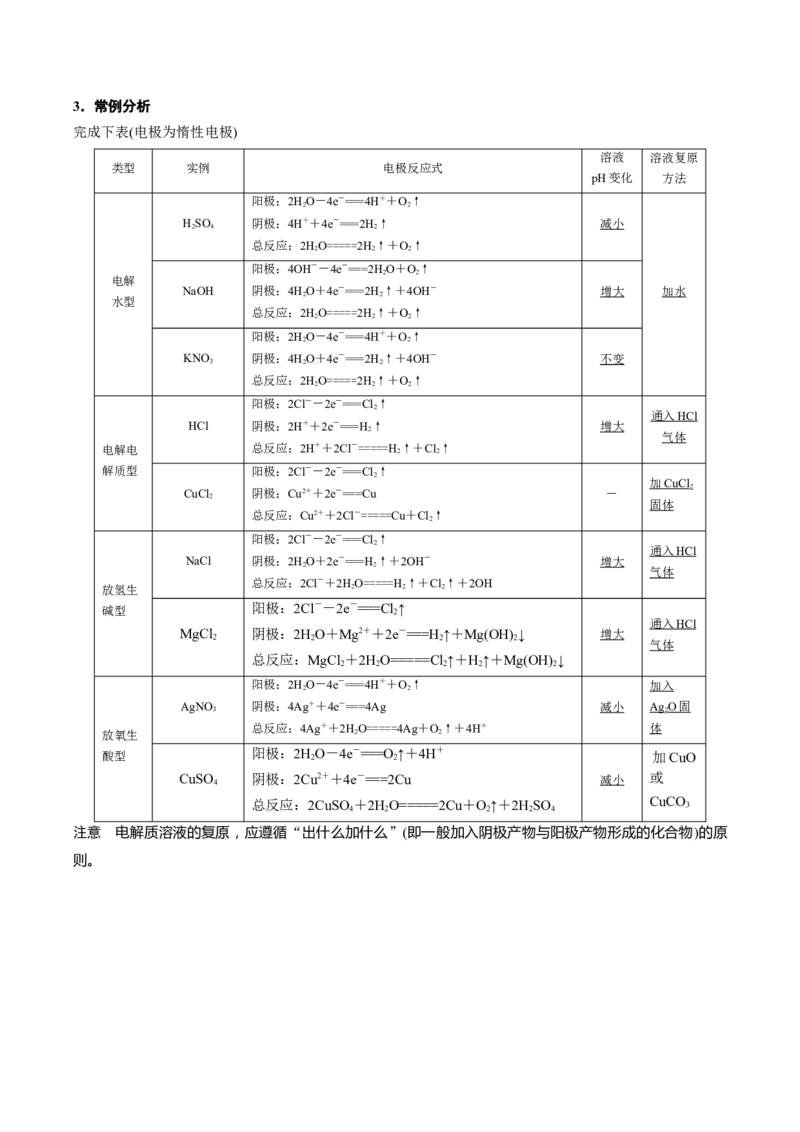
2、(2016·全国1)三室式电渗析法处理含NaSO 废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,
2 4
在直流电场的作用下,两膜中间的Na+和S 可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔
室。下列叙述正确的是 ( )
A.通电后中间隔室的SO2-离子向正极迁移,正极区溶液pH增大
4
B.该法在处理含NaSO 废水时可以得到NaOH和HSO 产品
2 4 2 4
C.负极反应为2HO-4e- O+4H+,负极区溶液pH降低
2 2
D.当电路中通过1 mol电子的电量时,会有0.5 mol的O 生成
2
【答案】B
【详解】在负极区发生的电极反应为4HO+4e- 2H↑+4OH-,在正极区发生的电极反应为2HO-4e-
2 2 2
O↑+4H+,故正极区pH减小,A选项错误;Na+移向负极区,生成NaOH,SO2-移向正极区,生成HSO ,B选项正
2 4 2 4
确;根据负极区电极反应可知C选项错误;每通过1 mol 电子,有0.25 mol O 生成,D选项错误。
2
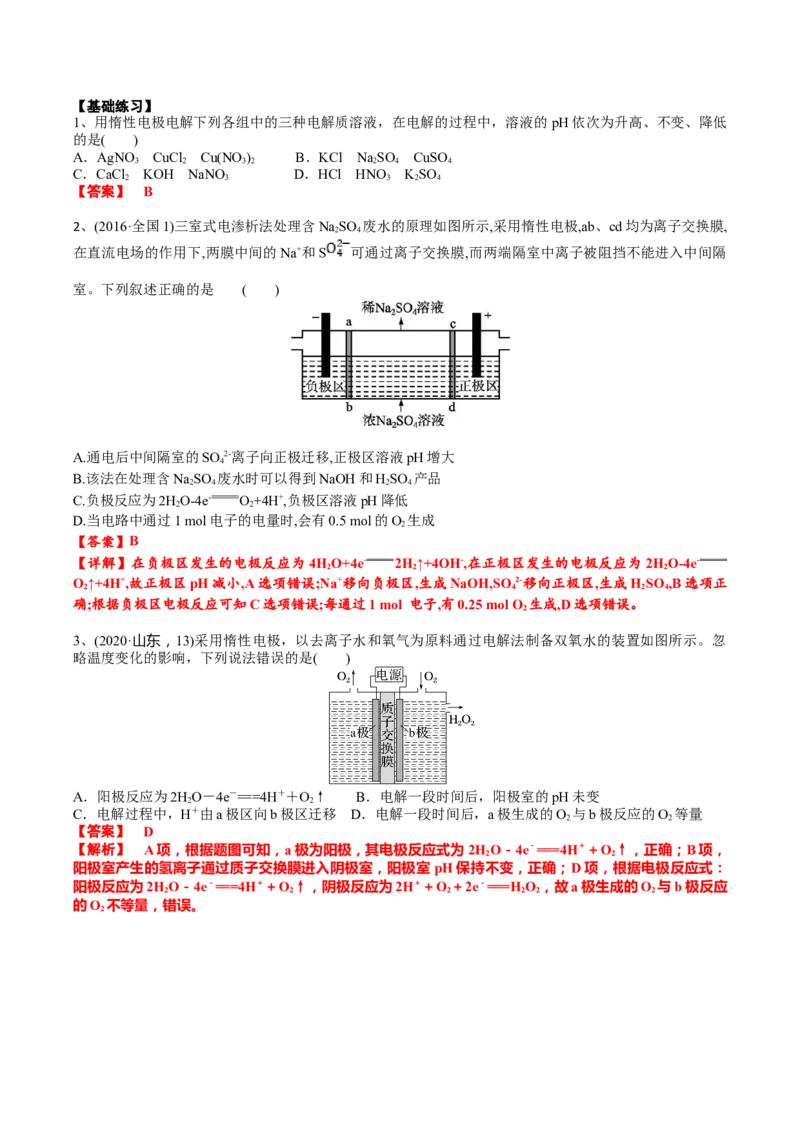
3、(2020·山东,13)采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如图所示。忽
略温度变化的影响,下列说法错误的是( )
A.阳极反应为2HO-4e-===4H++O↑ B.电解一段时间后,阳极室的pH未变
2 2
C.电解过程中,H+由a极区向b极区迁移 D.电解一段时间后,a极生成的O 与b极反应的O 等量
2 2
【答案】 D
【解析】 A项,根据题图可知,a极为阳极,其电极反应式为2HO-4e-===4H++O↑,正确;B项,
2 2
阳极室产生的氢离子通过质子交换膜进入阴极室,阳极室 pH保持不变,正确;D项,根据电极反应式:
阳极反应为2HO-4e-===4H++O↑,阴极反应为2H++O +2e-===HO ,故a极生成的O 与b极反应
2 2 2 2 2 2
的O 不等量,错误。
24、(2021·全国乙卷,12)沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却水排放
并降低冷却效率。为解决这一问题,通常在管道口设置一对惰性电极(如图所示),通入一定的电流。
下列叙述错误的是( )
A.阳极发生将海水中的Cl-氧化生成Cl 的反应 B.管道中可以生成氧化灭杀附着生物的NaClO
2
C.阴极生成的H 应及时通风稀释安全地排入大气 D.阳极表面形成的Mg(OH) 等积垢需要定期清理
2 2
【答案】 D
【解析】 根据题干信息分析可知,阳极区海水中的Cl-会优先失去电子生成Cl ,发生氧化反应,A正确;
2
设置的装置为电解池原理,阳极区生成的Cl 与阴极区生成的OH-在管道中会发生反应生成NaCl、NaClO
2
和HO,其中NaClO具有强氧化性,可氧化灭杀附着的生物,B正确;因为H 是易燃性气体,所以阴极
2 2
区生成的H 需及时通风稀释,安全地排入大气,以排除安全隐患,C正确;阴极的电极反应式为2HO+
2 2
2e-===H↑+2OH-,会使海水中的Mg2+沉淀积垢,所以阴极表面会形成Mg(OH) 等积垢,需要定期清
2 2
理,D错误。
5、(2022·海南,9)一种采用HO(g)和N(g)为原料制备NH (g)的装置示意图如下。
2 2 3
下列有关说法正确的是( )
A.在b电极上,N 被还原 B.金属Ag可作为a电极的材料
2
C.改变工作电源电压,反应速率不变 D.电解过程中,固体氧化物电解质中O2-不断减少
【答案】 A
【解析】 由装置示意图可知,b电极上N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,
2 3
因此b为阴极,电极反应式为N +3HO+6e-===2NH +3O2-,a为阳极,电极反应式为2O2--4e-
2 2 3
===O ,据此分析解答。由分析可得,在b电极上,N 被还原,A正确;a为阳极,若金属Ag作为a的电
2 2
极材料,则金属Ag优先失去电子,B错误;改变工作电源的电压,导致电流大小改变,反应速率也会改
变,C错误;电解过程中,阴极电极反应式为2N+6HO+12e-===4NH +6O2-,阳极电极反应式为6O2-
2 2 3
-12e-===3O,因此固体氧化物电解质中O2-不会减少,D错误。
2
6、(2020·全国卷)电致变色器件可智能调控太阳光透过率,从而实现节能。如图是某电致变色器件的示意
图。当通电时,Ag+注入无色WO 薄膜中,生成AgWO ,器件呈现蓝色,对于该变化过程,下列叙述
3 x 3
错误的是( )
A.Ag为阳极 B.Ag+由银电极向变色层迁移
C.W元素的化合价升高 D.总反应为WO +xAg===AgxWO
3 3
【答案】C
【详解】根据题给信息,通电时Ag+注入无色WO 薄膜中,生成Ag WO ,可判断Ag为阳极,失去电子
3 x 3
发生氧化反应,Ag-e-===Ag+,Ag+通过固体电解质向变色层迁移,总反应为WO +xAg===Ag WO ,
3 x 3
A、B、D项均正确;WO 得xe-生成WO,W元素的化合价降低,C项错误。
37、(2021·海南)液氨中存在平衡:2NH NH ++NH -。如图所示为电解池装置,以KNH 的液氨溶液为电解
3 4 2 2
液,电解过程中a、b两个惰性电极上都有气泡产生。下列有关说法正确的是 ( )
A.b电极连接的是电源的负极 B.a电极的反应为2NH +2e- H +2NH -
3 2 2
C.电解过程中,阴极附近K+浓度减小 D.理论上两极产生的气体物质的量之比为1∶1
【答案】B
【详解】根据图示可知:在b电极上产生N,N元素化合价升高,失去电子,发生氧化反应,所以b电极为阳极,
2
连接电源的正极,A项错误;电极a上产生H,H元素得到电子化合价降低,发生还原反应,所以a电极为阴极,
2
电极反应式为:2NH+2e- H+2N ,B项正确;电解过程中,阴极附近产生N ,使溶液中阴离子浓度增大,
3 2
为维持溶液电中性,阳离子K+会向阴极区定向移动,最终导致阴极区K+浓度增大,C项错误;反应每产生1 mol
H,转移2 mol电子,反应每产生1 mol N ,转移6 mol电子,故阴极产生的H 与阳极产生的N 的物质的量之比
2 2 2 2
是3∶1,D项错误。
8、(2021·湖北)Na Cr O 的酸性水溶液随着H+浓度的增大会转化为CrO 。电解法制备CrO 的原理如图所
2 2 7 3 3
示。下列说法错误的是 ( )
A.电解时只允许H+通过离子交换膜 B.生成O 和H 的质量比为8∶1
2 2
C.电解一段时间后阴极区溶液OH-的浓度增大 D.CrO 的生成反应为:Cr O2-+2H+ 2CrO+H O
3 2 7 3 2
【答案】A
【详解】根据左侧电极上生成O,右侧电极上生成H,可知左侧电极为阳极,发生反应:2H O-4e- 4H++O ↑,
2 2 2 2
右侧电极为阴极,发生反应:2H O+2e- 2OH-+H ↑;由题意知,左室中Na CrO 随着H+浓度增大转化为
2 2 2 2 7
CrO :Cr O2-+2H+ 2CrO +H O,因此阳极生成的H+不能通过离子交换膜。由以上分析可知,电解时通过
3 2 7 3 2
离子交换膜的是Na+,A项说法错误;根据各电极上转移电子数相等,由阳极反应和阴极反应可知生成O 和H
2 2
的物质的量之比为1∶2,其质量比为8∶1,B项说法正确;根据阴极反应可知,电解一段时间后阴极区溶液OH-的
浓度增大,C项说法正确;电解过程中阳极区H+的浓度增大,Na CrO 转化为CrO 的反应为CrO2-+2H+
2 2 7 3 2 7
2CrO +H O,D项说法正确。
3 2