文档内容
【基础知识】分子结构与性质
考点七 分子间作用力
【必备知识】
1、范德华力、氢键的对比
范德华力 氢键
作用微粒 分子或原子(稀有气体分子) H与N、O、F等电负性很大的原子
分类 分子内氢键和分子间氢键
特征 无方向性和饱和性 有饱和性和方向性
强度 化学键>氢键>范德华力
①组成和结构相似的物质,相对分子 X—H…Y强弱与X和Y的电负性有
影响其强度的因素 质量越大,范德华力越大; 关。
②分子的极性越大,范德华力越大。 电负性越强,氢键越强。
对物质性质的影响 主要影响物理性质(如熔、沸点)
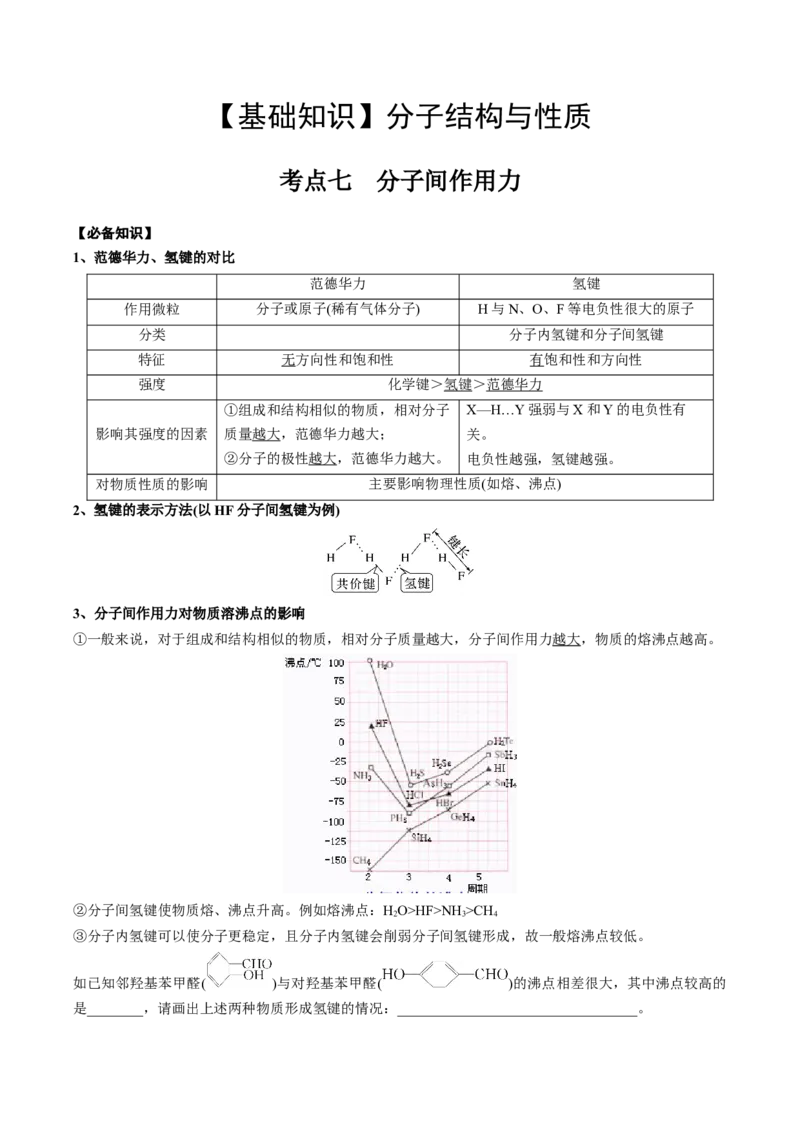
2、氢键的表示方法(以HF分子间氢键为例)
3、分子间作用力对物质溶沸点的影响
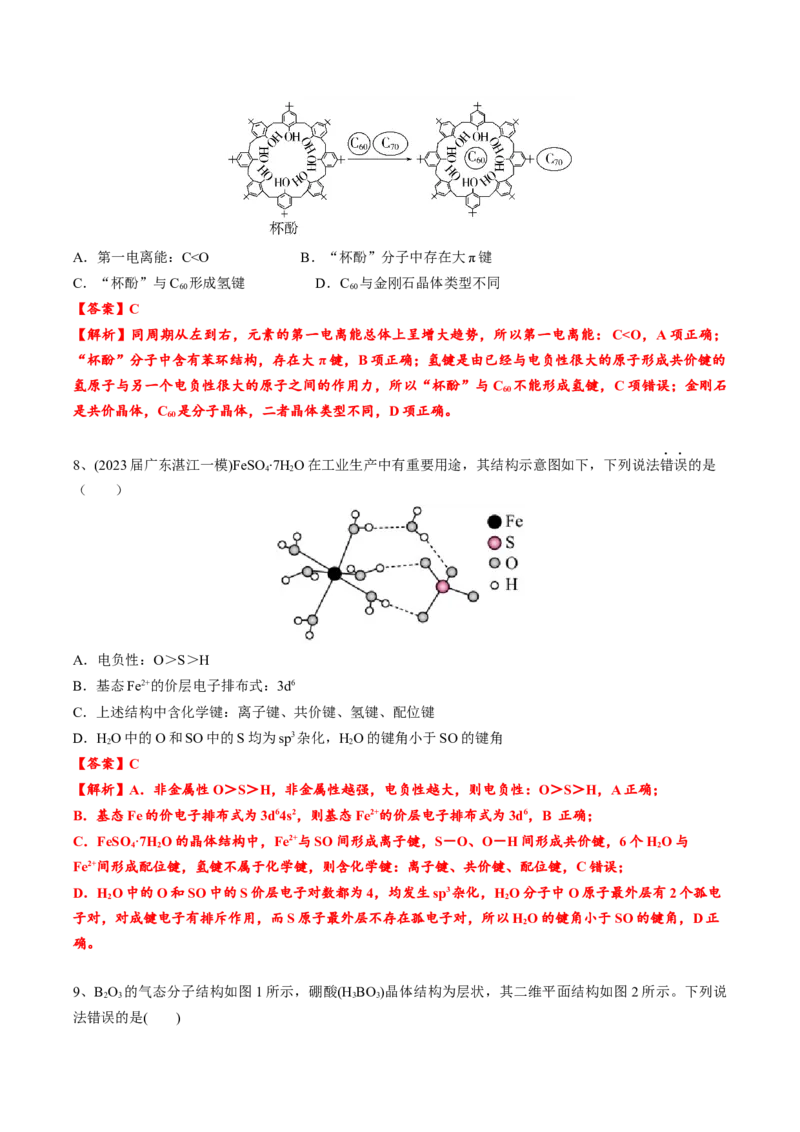
①一般来说,对于组成和结构相似的物质,相对分子质量越大,分子间作用力越大,物质的熔沸点越高。
②分子间氢键使物质熔、沸点升高。例如熔沸点:HO>HF>NH >CH
2 3 4
③分子内氢键可以使分子更稳定,且分子内氢键会削弱分子间氢键形成,故一般熔沸点较低。
如已知邻羟基苯甲醛( )与对羟基苯甲醛( )的沸点相差很大,其中沸点较高的
是________,请画出上述两种物质形成氢键的情况:__________________________________。【答案】 邻羟基苯甲醛形成分子内氢键: ;对羟基苯甲醛形成分子间氢键:
4、氢键对分子其他性质的影响
(1)氨极易液化,因为NH 分子液化时形成分子间氢键。
3
(2)水结冰时体积膨胀、密度减小,因为结冰时形成氢键。
(3)溶质与溶剂若能形成氢键,能增大溶解度。比如NH 极易溶于水,小分子醇能与水以任意比互溶。
3
例、有关物质的熔、沸点,解答下列问题。
(1)有机物A( )的结构可以表示为 (虚线表示氢键),而有机物B( )只能形成分子间
氢键。工业上用水蒸气蒸馏法将 A和B进行分离,首先被蒸出的成分是______________________,原因
是:________________________________________________________________________。
(2)[2019·新课标Ⅲ]苯胺( )的晶体类型是__________。苯胺( )与甲苯(
)的相对分子质量相近,但苯胺的熔点(-5.9 ℃)、沸点(184.4 ℃)分别高于甲苯的熔点(-95.0
℃)、沸点(111 ℃),原因是____________________________。
(3)S 的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为
8
________________。
(4)在CO 低压合成甲醇反应(CO +3H===CH OH+HO)所涉及的4种物质中,沸点从高到低的顺序为
2 2 2 3 2
____________________________,原因是_________________________________________。
【答案】 (1)A A易形成分子内氢键,B易形成分子间氢键,所以B的沸点比A的高
(2)分子晶体 苯胺分子间存在氢键
(3)S 相对分子质量大,分子间范德华力大
8
(4)H O>CH OH>CO >H HO与CH OH均为极性分子,HO中氢键比甲醇多;CO 与H 均为非极性
2 3 2 2 2 3 2 2 2
分子,CO 相对分子质量较大,范德华力较大
2
【易错辨析】
1、氢键是一种特殊的化学键( )2、卤素单质、卤素氢化物、卤素碳化物(即CX)的熔、沸点均随着相对分子质量的增大而增大( )
4
3、氨水中氨分子与水分子间形成了氢键( )
4、可燃冰(CH·8H O)中甲烷分子与水分子之间形成了氢键( )
4 2
5、HO比HS稳定是因为水分子间存在氢键( )
2 2
6、氢键的存在一定能使物质的熔、沸点升高( )
7、NH 的稳定性很强,是因为其分子间能形成氢键。( )
3
8、C的氢化物沸点低于O的氢化物,因为HO含有氢键。( )
2
9、范德华力非常微弱,破坏范德华力不需要消耗能量。( )
10、HO 分子间存在氢键。( )
2 2
11、氢键具有方向性和饱和性。( )
12、乙醇分子和水分子间只存在范德华力。( )
【答案】 1.× 2.× 3.√ 4.× 5.× 6.× 7.× 8.× 9.× 10.√ 11.√ 12.×
【跟踪练习】
1、下列物质能形成氢键,且形成的氢键最强的是( )
A、甲醇 B、NH C、冰 D、(HF)
3 n
【答案】D
2、氨气溶于水时,大部分NH 与HO以氢键(用“…”表示)结合形成NH ·H O分子,根据氨水的性质可
3 2 3 2
推知NH ·H O的结构式为( )
3 2
【答案】D
3、下列关于化学键及晶体的说法中,不正确的是( )
A. Cl 、Br 、I 的沸点逐渐升高,是因为分子间作用力越来越大
2 2 2
B. NaOH和NH Cl化学键类型相同
4
C. N 和CCl 两种分子中,每个原子的最外层都具有8电子稳定结构
2 4
D. 石英晶体是共价晶体,其分子式为SiO
2
【答案】D
4、下列现象与氢键有关的是( )
①HF的熔、沸点比ⅦA族其他元素氢化物的高 ②乙醇可以和水以任意比互溶
③冰的密度比液态水的密度小 ④水分子高温下也很稳定
⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低A.②③④⑤ B.①②③⑤ C.①②③④ D.①②③④⑤
【答案】B
5、液氨、液氯、清洗剂、萃取剂等重点品种使用企业和白酒企业,应加强储罐区、危化品库房、危化品
输送等的管理,确保化工生产安全。下列说法正确的是( )
A.液氨中只存在范德华力
B.液氨分子间作用力强,所以其稳定性大于PH
3
C.液氯挥发导致人体吸入后中毒,是因为液氯分子中的共价键键能较小
D.萃取剂CCl 的沸点高于CH 的沸点
4 4
【答案】 D
【解析】 液氨中还存在共价键、氢键等作用力,A项错误;分子间作用力只影响物质的物理性质,与其
稳定性无关,B项错误;由于液氯中Cl 分子间的作用力弱,液氯沸点低,极易挥发而被人体吸入引起中
2
毒,与共价键键能大小无关,C项错误;由于CCl 与CH 结构相似,且均为共价化合物,CCl 的相对分
4 4 4
子质量大于CH ,其沸点也高于CH 的沸点,D项正确。
4 4
6、“冰面为什么滑?”,这与冰层表面的结构有关(如图)。下列有关说法错误的是( )
A.由于氢键的存在,水分子的稳定性好,高温下也很难分解
B.第一层固态冰中,水分子间通过氢键形成空间网状结构
C.第二层“准液体”中,水分子间形成氢键的机会比固态冰中少
D.当高于一定温度时,“准液体”中的水分子与下层冰连接的氢键断裂,产生“流动性的水分子”,使
冰面变滑
【答案】 A
【解析】 水分子的稳定性好,是由水分子内氢氧共价键的键能决定的,与分子间形成的氢键无关,A错
误;固态冰中,1个水分子与周围的4个水分子通过氢键相连接,从而形成空间网状结构,B正确;“准
液体”中,水分子间的距离不完全相等,所以 1个水分子与少于4个的水分子间形成氢键,形成氢键的机
会比固态冰中少,C正确;当温度达到一定数值时,“准液体”中的水分子与下层冰连接的氢键被破坏,
使一部分水分子能够自由流动,从而产生“流动性的水分子”,造成冰面变滑,D正确。
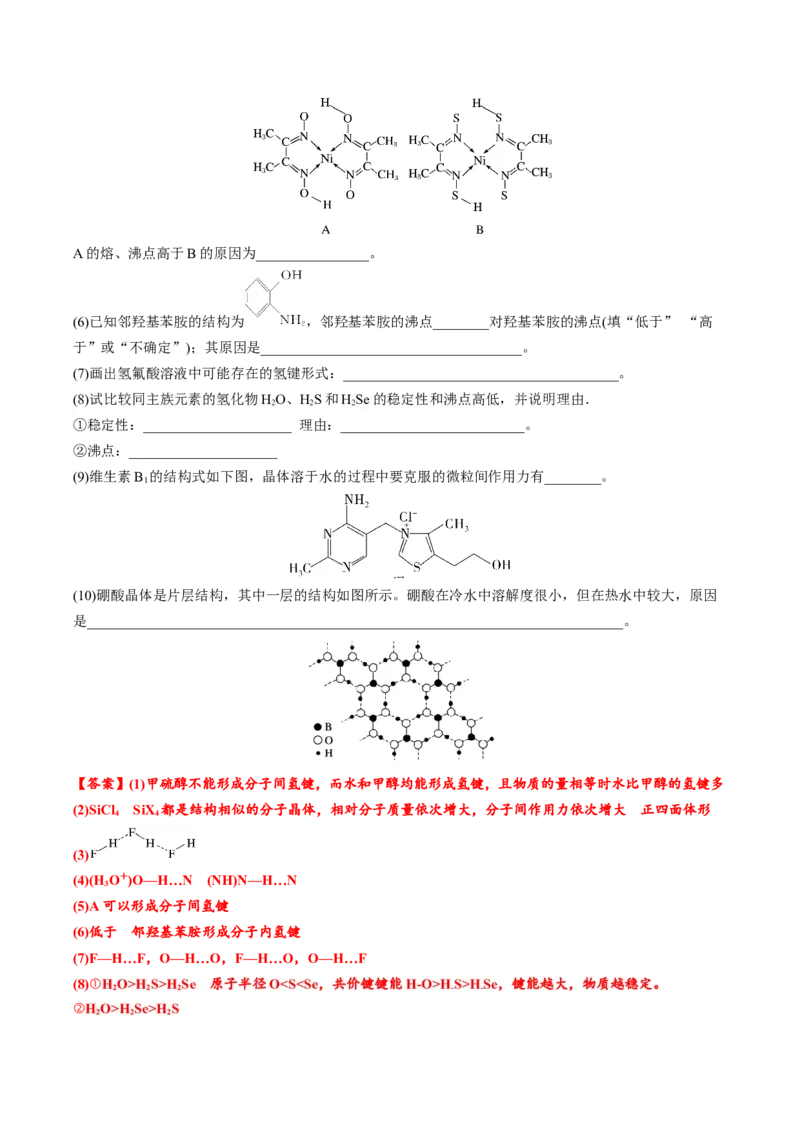
7、(2022·苏州实验中学月考)利用超分子可分离C 和C 。将C 、C 混合物加入一种空腔大小适配C 的
60 70 60 70 60
“杯酚”中进行分离的流程如图。下列说法错误的是( )A.第一电离能:CH S>H Se 原子半径OHS>HSe,键能越大,物质越稳定。
2 2 2 - -
②HO>H Se>H S
2 2 2(9)离子键、氢键、范德华力
(10)硼酸在冷水中存在分子间氢键,缔合在一起,溶解度小。加热时,氢键被破坏,与水形成氢键,溶解
度增大。