文档内容
一、选择题
1.(2018·高考全国卷Ⅱ)下列实验过程可以达到实验目的的是( )
编号 实验目的 实验过程
称取4.0 g固体NaOH于烧杯中,加入少量蒸
A 配制0.400 0 mol·L-1的NaOH溶液
馏水溶解,转移至250 mL容量瓶中定容
向盛有2 mL黄色氯化铁溶液的试管中滴加
B 探究维生素C的还原性
浓的维生素C溶液,观察颜色变化
向稀盐酸中加入锌粒,将生成的气体依次通
C 制取并纯化氢气
过NaOH溶液、浓硫酸和KMnO 溶液
4
向2支盛有5 mL不同浓度NaHSO 溶液的试
3
D 探究浓度对反应速率的影响 管中同时加入2 mL 5%H O 溶液,观察实验
2 2
现象
解析:选B。NaOH固体溶解后需冷却至室温才能转移至250 mL容量瓶中,且需用蒸馏水
洗涤烧杯内壁和玻璃棒2~3次,洗涤液并入容量瓶,然后定容,A项不能达到实验目的;实验
中若观察到FeCl 溶液的黄色逐渐褪去,且溶液变成浅绿色,说明维生素C具有还原性,B项
3
能达到实验目的;通过NaOH溶液可除去H 中混有的少量HCl杂质,再经浓硫酸干燥即可得
2
到H,没有必要经过KMnO 溶液,C项不能达到实验目的;NaHSO 溶液与HO 溶液的反应
2 4 3 2 2
没有明显实验现象,无法判断反应进行的快慢,D项不能达到实验目的。
2.(2019·宜宾一诊)下列实验操作能达到实验目的的是( )
实验目的 实验操作
A 检验溶液中的Fe2+ 先滴加新制氯水,再滴加KSCN溶液
配制0.5 mol/L的 量取50 mL 1.0 mol/L HSO 溶液,倒入小
2 4
B
HSO 溶液 烧杯中,再加入50 mL水稀释
2 4
加热乙醇和浓硫酸的混合液,将气体通入
C 验证乙烯的生成
酸性KMnO 溶液
4
D 除去乙酸乙酯中混有的乙酸 用过量饱和碳酸钠溶液洗涤后分液
解析:选D。先滴加新制氯水,可氧化亚铁离子,原溶液中可能含铁离子,则检验亚铁离子
时应先加KSCN无现象,后加氯水变红色,A错误。配制0.5 mol/L 的HSO 溶液,需要在容
2 4
量瓶中配制,在烧杯中稀释后转移到容量瓶中定容,且应将浓硫酸加入水中稀释,B错误。乙
烯及挥发的乙醇均会使酸性高锰酸钾褪色,则不能检验乙烯,C错误。乙酸与碳酸钠反应后,
与乙酸乙酯分层,然后分液可分离, D正确。
3.(2019·郑州高三模拟)下列各组物质,不用任何试剂即可鉴别的是( )
A.NaCl、NaBr、KI三种无色溶液
B.HCl、NaCl、NaNO 、NaCO 四种溶液
3 2 3
C.NaBr、HCl、KCl三种溶液
D.淀粉、淀粉碘化钾、碘化钾、溴水四种溶液
解析:选D。NaCl、NaBr、KI三种无色溶液要用AgNO 溶液鉴别,选项A不符合题意;
3
HCl、NaCl、NaNO 、NaCO 四种溶液两两混合,依据互滴法可鉴别HCl和NaCO,剩余的
3 2 3 2 3
NaCl和NaNO 两种溶液需用AgNO 溶液鉴别,选项B不符合题意;NaBr、HCl、KCl三种溶液
3 3
需先用NaCO 溶液鉴别出HCl,再用AgNO 溶液鉴别出NaBr和KCl,选项C不符合题意;淀
2 3 3
粉、淀粉碘化钾、碘化钾、溴水四种溶液中溴水有颜色,溴水与碘化钾溶液反应生成碘单质,溶液颜色加深,溴水与淀粉碘化钾溶液反应生成碘单质,碘单质与淀粉反应使溶液呈蓝色,剩余
的为淀粉溶液,选项D符合题意。
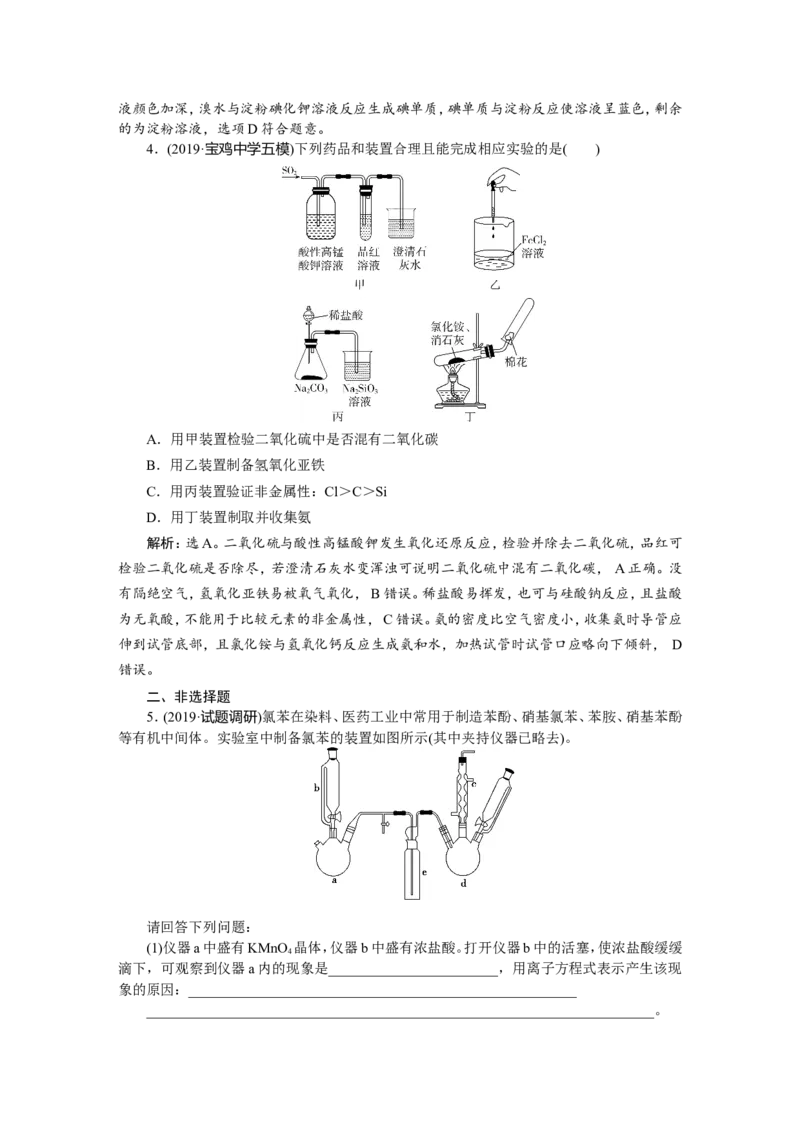
4.(2019·宝鸡中学五模)下列药品和装置合理且能完成相应实验的是( )
A.用甲装置检验二氧化硫中是否混有二氧化碳
B.用乙装置制备氢氧化亚铁
C.用丙装置验证非金属性:Cl>C>Si
D.用丁装置制取并收集氨
解析:选A。二氧化硫与酸性高锰酸钾发生氧化还原反应,检验并除去二氧化硫,品红可
检验二氧化硫是否除尽,若澄清石灰水变浑浊可说明二氧化硫中混有二氧化碳, A正确。没
有隔绝空气,氢氧化亚铁易被氧气氧化, B错误。稀盐酸易挥发,也可与硅酸钠反应,且盐酸
为无氧酸,不能用于比较元素的非金属性, C错误。氨的密度比空气密度小,收集氨时导管应
伸到试管底部,且氯化铵与氢氧化钙反应生成氨和水,加热试管时试管口应略向下倾斜, D
错误。
二、非选择题
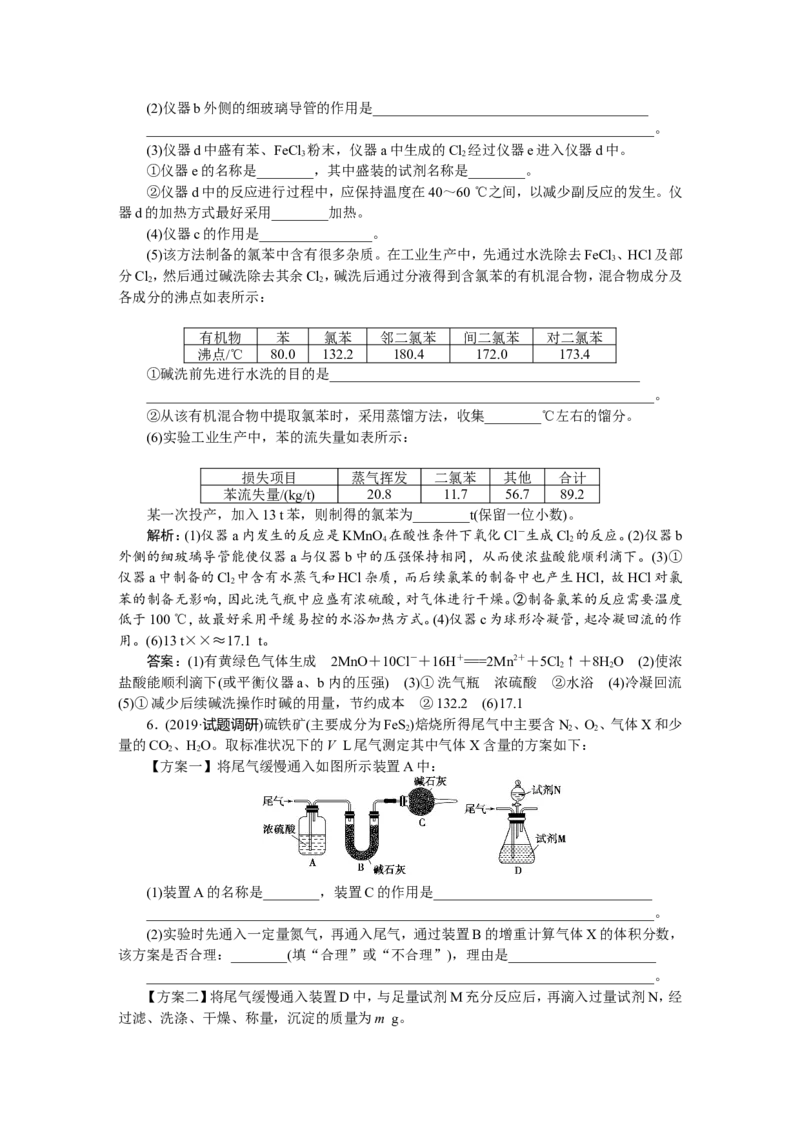
5.(2019·试题调研)氯苯在染料、医药工业中常用于制造苯酚、硝基氯苯、苯胺、硝基苯酚
等有机中间体。实验室中制备氯苯的装置如图所示(其中夹持仪器已略去)。
请回答下列问题:
(1)仪器a中盛有KMnO 晶体,仪器b中盛有浓盐酸。打开仪器b中的活塞,使浓盐酸缓缓
4
滴下,可观察到仪器a内的现象是________________________,用离子方程式表示产生该现
象的原因:_______________________________________________________
________________________________________________________________________。(2)仪器b外侧的细玻璃导管的作用是_______________________________________
________________________________________________________________________。
(3)仪器d中盛有苯、FeCl 粉末,仪器a中生成的Cl 经过仪器e进入仪器d中。
3 2
①仪器e的名称是________,其中盛装的试剂名称是________。
②仪器d中的反应进行过程中,应保持温度在40~60 ℃之间,以减少副反应的发生。仪
器d的加热方式最好采用________加热。
(4)仪器c的作用是________________。
(5)该方法制备的氯苯中含有很多杂质。在工业生产中,先通过水洗除去FeCl 、HCl及部
3
分Cl,然后通过碱洗除去其余Cl,碱洗后通过分液得到含氯苯的有机混合物,混合物成分及
2 2
各成分的沸点如表所示:
有机物 苯 氯苯 邻二氯苯 间二氯苯 对二氯苯
沸点/℃ 80.0 132.2 180.4 172.0 173.4
①碱洗前先进行水洗的目的是____________________________________________
________________________________________________________________________。
②从该有机混合物中提取氯苯时,采用蒸馏方法,收集________℃左右的馏分。
(6)实验工业生产中,苯的流失量如表所示:
损失项目 蒸气挥发 二氯苯 其他 合计
苯流失量/(kg/t) 20.8 11.7 56.7 89.2
某一次投产,加入13 t苯,则制得的氯苯为________t(保留一位小数)。
解析:(1)仪器a内发生的反应是KMnO 在酸性条件下氧化Cl-生成Cl 的反应。(2)仪器b
4 2
外侧的细玻璃导管能使仪器a与仪器b中的压强保持相同,从而使浓盐酸能顺利滴下。(3)①
仪器a中制备的Cl 中含有水蒸气和HCl杂质,而后续氯苯的制备中也产生HCl,故HCl对氯
2
苯的制备无影响,因此洗气瓶中应盛有浓硫酸,对气体进行干燥。②制备氯苯的反应需要温度
低于100 ℃,故最好采用平缓易控的水浴加热方式。(4)仪器c为球形冷凝管,起冷凝回流的作
用。(6)13 t××≈17.1 t。
答案:(1)有黄绿色气体生成 2MnO+10Cl-+16H+===2Mn2++5Cl↑+8HO (2)使浓
2 2
盐酸能顺利滴下(或平衡仪器a、b内的压强) (3)①洗气瓶 浓硫酸 ②水浴 (4)冷凝回流
(5)①减少后续碱洗操作时碱的用量,节约成本 ②132.2 (6)17.1
6.(2019·试题调研)硫铁矿(主要成分为FeS)焙烧所得尾气中主要含N、O、气体X和少
2 2 2
量的CO、HO。取标准状况下的V L尾气测定其中气体X含量的方案如下:
2 2
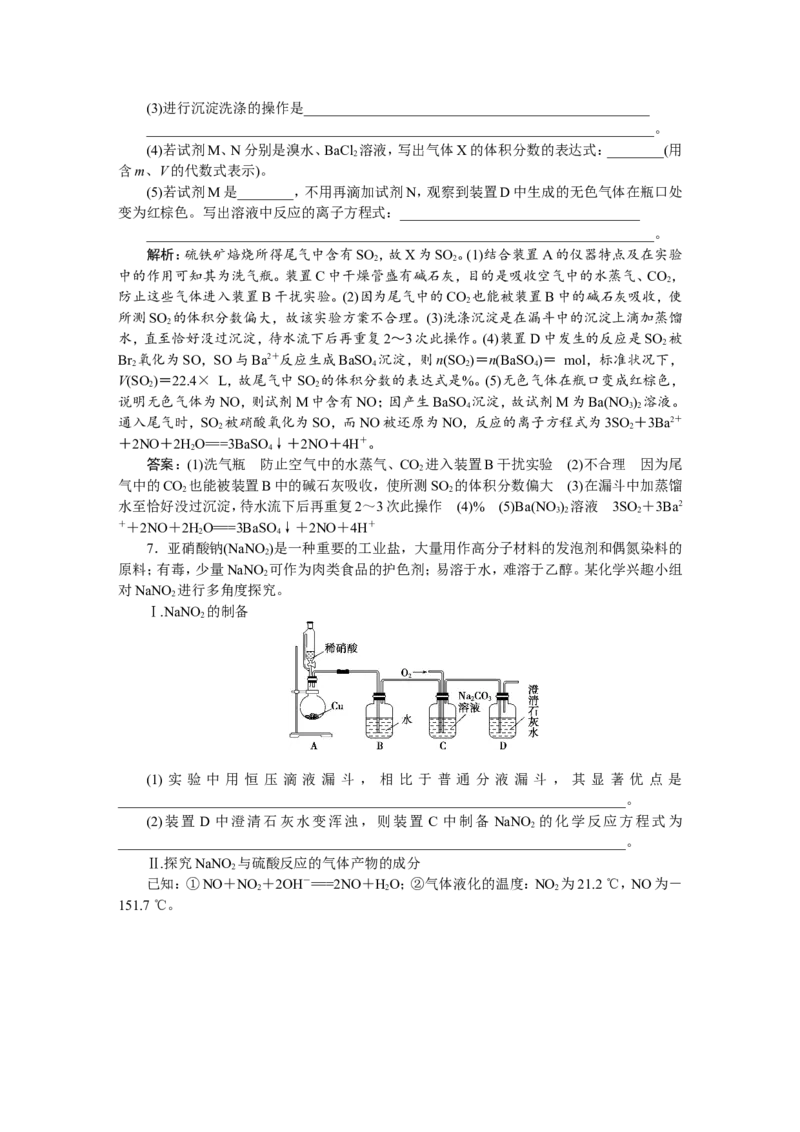
【方案一】将尾气缓慢通入如图所示装置A中:
(1)装置A的名称是________,装置C的作用是_______________________________
________________________________________________________________________。
(2)实验时先通入一定量氮气,再通入尾气,通过装置B的增重计算气体X的体积分数,
该方案是否合理:________(填“合理”或“不合理”),理由是_____________________
________________________________________________________________________。
【方案二】将尾气缓慢通入装置D中,与足量试剂M充分反应后,再滴入过量试剂N,经
过滤、洗涤、干燥、称量,沉淀的质量为m g。(3)进行沉淀洗涤的操作是_________________________________________________
________________________________________________________________________。
(4)若试剂M、N分别是溴水、BaCl 溶液,写出气体X的体积分数的表达式:________(用
2
含m、V的代数式表示)。
(5)若试剂M是________,不用再滴加试剂N,观察到装置D中生成的无色气体在瓶口处
变为红棕色。写出溶液中反应的离子方程式:__________________________________
________________________________________________________________________。
解析:硫铁矿焙烧所得尾气中含有SO ,故X为SO 。(1)结合装置A的仪器特点及在实验
2 2
中的作用可知其为洗气瓶。装置C中干燥管盛有碱石灰,目的是吸收空气中的水蒸气、CO,
2
防止这些气体进入装置B干扰实验。(2)因为尾气中的CO 也能被装置B中的碱石灰吸收,使
2
所测SO 的体积分数偏大,故该实验方案不合理。(3)洗涤沉淀是在漏斗中的沉淀上滴加蒸馏
2
水,直至恰好没过沉淀,待水流下后再重复2~3次此操作。(4)装置D中发生的反应是SO 被
2
Br 氧化为SO,SO与Ba2+反应生成BaSO 沉淀,则n(SO )=n(BaSO)= mol,标准状况下,
2 4 2 4
V(SO )=22.4× L,故尾气中SO 的体积分数的表达式是%。(5)无色气体在瓶口变成红棕色,
2 2
说明无色气体为NO,则试剂M中含有NO;因产生BaSO 沉淀,故试剂M为Ba(NO ) 溶液。
4 3 2
通入尾气时,SO 被硝酸氧化为SO,而NO被还原为NO,反应的离子方程式为3SO +3Ba2+
2 2
+2NO+2HO===3BaSO ↓+2NO+4H+。
2 4
答案:(1)洗气瓶 防止空气中的水蒸气、CO 进入装置B干扰实验 (2)不合理 因为尾
2
气中的CO 也能被装置B中的碱石灰吸收,使所测SO 的体积分数偏大 (3)在漏斗中加蒸馏
2 2
水至恰好没过沉淀,待水流下后再重复2~3次此操作 (4)% (5)Ba(NO ) 溶液 3SO +3Ba2
3 2 2
++2NO+2HO===3BaSO ↓+2NO+4H+
2 4
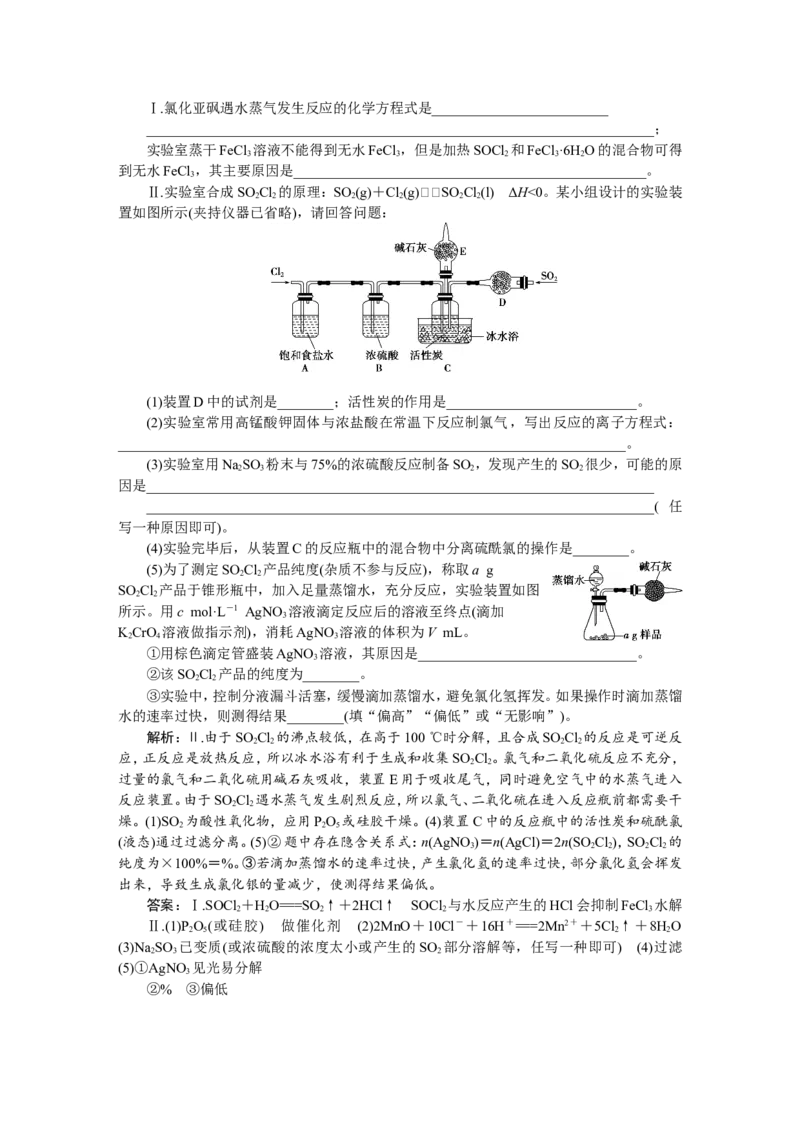
7.亚硝酸钠(NaNO )是一种重要的工业盐,大量用作高分子材料的发泡剂和偶氮染料的
2
原料;有毒,少量NaNO 可作为肉类食品的护色剂;易溶于水,难溶于乙醇。某化学兴趣小组
2
对NaNO 进行多角度探究。
2
Ⅰ.NaNO 的制备
2
(1) 实 验 中 用 恒 压 滴 液 漏 斗 , 相 比 于 普 通 分 液 漏 斗 , 其 显 著 优 点 是
________________________________________________________________________。
(2)装置 D 中澄清石灰水变浑浊,则装置 C 中制备 NaNO 的化学反应方程式为
2
________________________________________________________________________。
Ⅱ.探究NaNO 与硫酸反应的气体产物的成分
2
已知:①NO+NO +2OH-===2NO+HO;②气体液化的温度:NO 为21.2 ℃,NO为-
2 2 2
151.7 ℃。(3)反应前打开弹簧夹,先通入一段时间的N,目的是___________________________
2
________________________________________________________________________。
(4)为了检验装置A中生成的气体产物,仪器的连接顺序(按从左到右的顺序连接)为A、
C、________、________、________。
(5)在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,装置A中产生红棕色气体。
①确认装置A中产生的气体含有NO,依据的现象是__________________________
________________________________________________________________________。
②装置E的作用是_____________________________________________________。
(6)如果没有装置C,对实验结论造成的影响是_____________________________
________________________________________________________________________。
(7) 通 过 上 述 实 验 探 究 过 程 , 可 得 出 装 置 A 中 反 应 的 离 子 方 程 式 是
________________________________________________________________________。
解析:Ⅰ.(1)恒压滴液漏斗连接反应仪器,平衡滴液漏斗与烧瓶中的压强,有利于漏斗中
反应液的顺利滴下。(2)装置D中澄清石灰水变浑浊,说明反应中有CO 生成,故反应的化学
2
方程式为4NO+O+2NaCO===4NaNO +2CO。Ⅱ.(3)反应前通入N,目的是排出装置中的
2 2 3 2 2 2
空气,防止可能产生的NO与O 反应生成NO 。(4)若气体产物中含有NO ,装置E可使NO 液
2 2 2 2
化,达到除去气体产物中NO 的目的;若气体产物中含有NO,则装置D中通入O,生成红棕
2 2
色的NO ;装置B可吸收有毒尾气,故仪器连接顺序为A、C、E、D、B。(5)①装置A中产生
2
NO,则装置D中通入O 时,NO转化为NO ,现象是烧瓶内气体由无色变为红棕色。②NO 液
2 2 2
化温度较高,故装置E可使NO 液化。(6)装置C可除去混合气体中的水蒸气,以防水蒸气与
2
NO 反应生成NO,从而无法确定气体产物中是否存在NO。(7)根据上述分析可知,NaNO 与
2 2
硫酸反应生成NO和NO ,故反应的离子方程式为2NO+2H+===NO↑+NO↑+HO。
2 2 2
答案:Ⅰ.(1)平衡滴液漏斗与烧瓶中的压强,有利于稀硝酸顺利滴下 (2)4NO+O +
2
2NaCO===4NaNO +2CO Ⅱ.(3)防止可能产生的NO被空气中的O 氧化成NO ,干扰气体
2 3 2 2 2 2
产物的检验 (4)E D B (5)①装置D中通入氧气后,气体由无色变为红棕色 ②冷凝,使
NO 完全液化 (6)水蒸气会与NO 反应产生NO,造成对NO的来源认识不清 (7)2NO+2H
2 2
+===NO↑+NO↑+HO
2 2
8.氯化亚砜(SOCl )和硫酰氯(SO Cl)在空气中遇水蒸气发生剧烈反应,并产生大量白雾。
2 2 2
SO Cl 常做氯化剂或氯磺化剂,用于制造药品、染料和表面活性剂,其部分性质如表所示:
2 2
物质 物理性质 化学性质
熔点:-54.1 ℃;
SO Cl 100 ℃以上分解生成SO 和Cl
2 2 沸点:69.1 ℃ 2 2Ⅰ.氯化亚砜遇水蒸气发生反应的化学方程式是_________________________
________________________________________________________________________;
实验室蒸干FeCl 溶液不能得到无水FeCl ,但是加热SOCl 和FeCl ·6H O的混合物可得
3 3 2 3 2
到无水FeCl ,其主要原因是__________________________________________________。
3
Ⅱ.实验室合成SO Cl 的原理:SO (g)+Cl(g)SO Cl(l) ΔH<0。某小组设计的实验装
2 2 2 2 2 2
置如图所示(夹持仪器已省略),请回答问题:
(1)装置D中的试剂是________;活性炭的作用是___________________________。
(2)实验室常用高锰酸钾固体与浓盐酸在常温下反应制氯气,写出反应的离子方程式:
________________________________________________________________________。
(3)实验室用NaSO 粉末与75%的浓硫酸反应制备SO ,发现产生的SO 很少,可能的原
2 3 2 2
因是________________________________________________________________________
________________________________________________________________________( 任
写一种原因即可)。
(4)实验完毕后,从装置C的反应瓶中的混合物中分离硫酰氯的操作是________。
(5)为了测定SO Cl 产品纯度(杂质不参与反应),称取a g
2 2
SO Cl 产品于锥形瓶中,加入足量蒸馏水,充分反应,实验装置如图
2 2
所示。用c mol·L-1 AgNO 溶液滴定反应后的溶液至终点(滴加
3
KCrO 溶液做指示剂),消耗AgNO 溶液的体积为V mL。
2 4 3
①用棕色滴定管盛装AgNO 溶液,其原因是_______________________________。
3
②该SO Cl 产品的纯度为________。
2 2
③实验中,控制分液漏斗活塞,缓慢滴加蒸馏水,避免氯化氢挥发。如果操作时滴加蒸馏
水的速率过快,则测得结果________(填“偏高”“偏低”或“无影响”)。
解析:Ⅱ.由于SO Cl 的沸点较低,在高于100 ℃时分解,且合成SO Cl 的反应是可逆反
2 2 2 2
应,正反应是放热反应,所以冰水浴有利于生成和收集SO Cl。氯气和二氧化硫反应不充分,
2 2
过量的氯气和二氧化硫用碱石灰吸收,装置E用于吸收尾气,同时避免空气中的水蒸气进入
反应装置。由于SO Cl 遇水蒸气发生剧烈反应,所以氯气、二氧化硫在进入反应瓶前都需要干
2 2
燥。(1)SO 为酸性氧化物,应用PO 或硅胶干燥。(4)装置C中的反应瓶中的活性炭和硫酰氯
2 2 5
(液态)通过过滤分离。(5)②题中存在隐含关系式:n(AgNO)=n(AgCl)=2n(SO Cl),SO Cl 的
3 2 2 2 2
纯度为×100%=%。③若滴加蒸馏水的速率过快,产生氯化氢的速率过快,部分氯化氢会挥发
出来,导致生成氯化银的量减少,使测得结果偏低。
答案:Ⅰ.SOCl +HO===SO↑+2HCl↑ SOCl 与水反应产生的HCl会抑制FeCl 水解
2 2 2 2 3
Ⅱ.(1)P O(或硅胶) 做催化剂 (2)2MnO+10Cl-+16H+===2Mn2++5Cl↑+8HO
2 5 2 2
(3)Na SO 已变质(或浓硫酸的浓度太小或产生的SO 部分溶解等,任写一种即可) (4)过滤
2 3 2
(5)①AgNO 见光易分解
3
②% ③偏低