文档内容
专项提能特训 5 非金属及其化合物对环境的影响
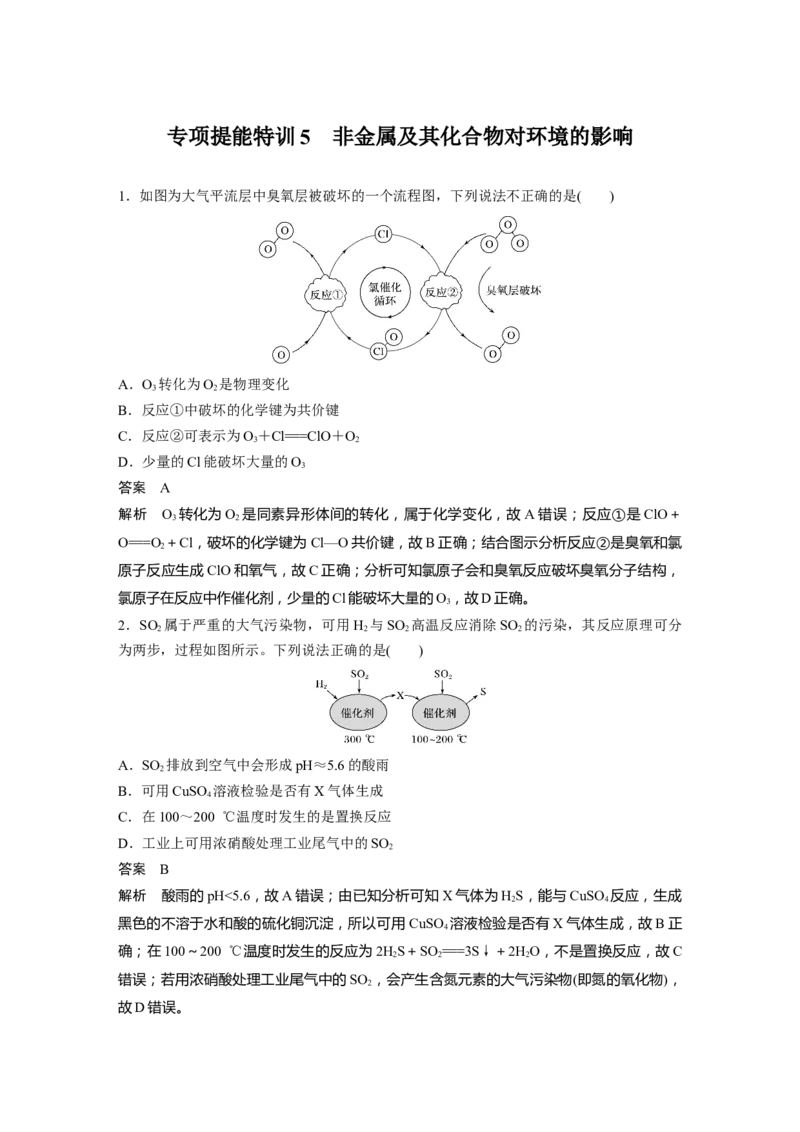
1.如图为大气平流层中臭氧层被破坏的一个流程图,下列说法不正确的是( )
A.O 转化为O 是物理变化
3 2
B.反应①中破坏的化学键为共价键
C.反应②可表示为O+Cl===ClO+O
3 2
D.少量的Cl能破坏大量的O
3
答案 A
解析 O 转化为O 是同素异形体间的转化,属于化学变化,故A错误;反应①是ClO+
3 2
O===O +Cl,破坏的化学键为Cl—O共价键,故B正确;结合图示分析反应②是臭氧和氯
2
原子反应生成ClO和氧气,故C正确;分析可知氯原子会和臭氧反应破坏臭氧分子结构,
氯原子在反应中作催化剂,少量的Cl能破坏大量的O,故D正确。
3
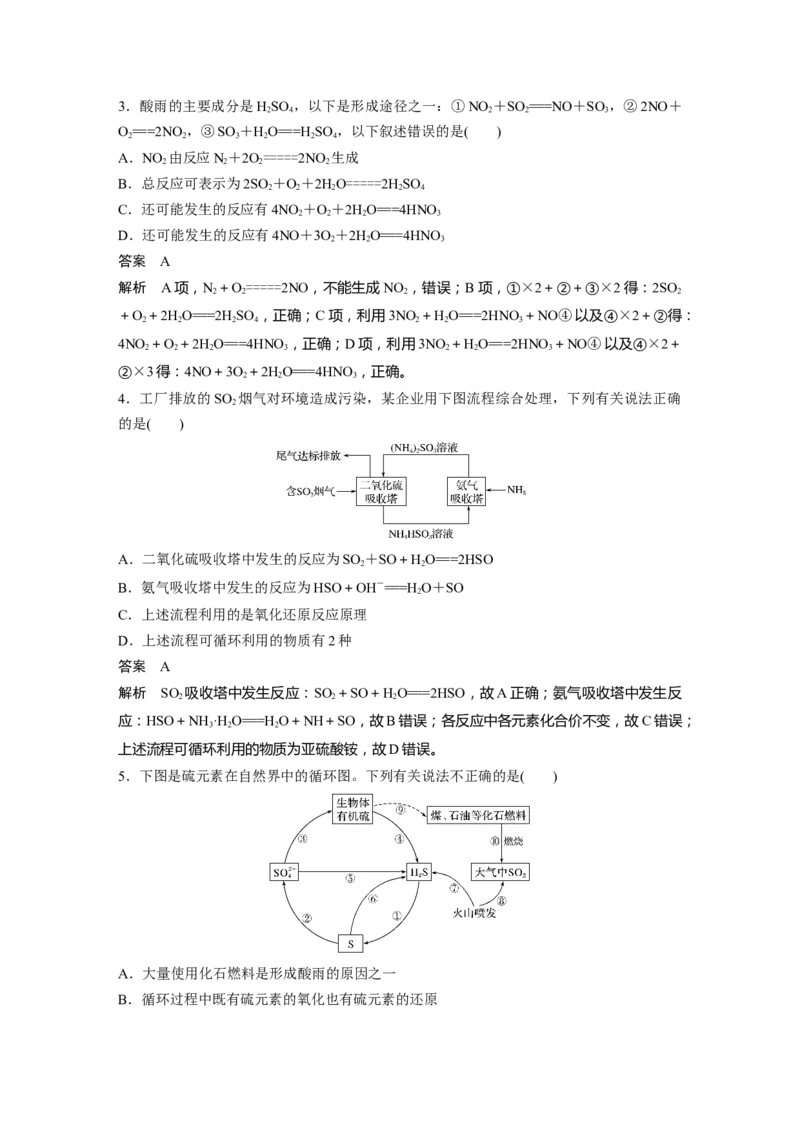
2.SO 属于严重的大气污染物,可用H 与SO 高温反应消除SO 的污染,其反应原理可分
2 2 2 2
为两步,过程如图所示。下列说法正确的是( )
A.SO 排放到空气中会形成pH≈5.6的酸雨
2
B.可用CuSO 溶液检验是否有X气体生成
4
C.在100~200 ℃温度时发生的是置换反应
D.工业上可用浓硝酸处理工业尾气中的SO
2
答案 B
解析 酸雨的pH<5.6,故A错误;由已知分析可知X气体为HS,能与CuSO 反应,生成
2 4
黑色的不溶于水和酸的硫化铜沉淀,所以可用 CuSO 溶液检验是否有X气体生成,故B正
4
确;在100~200 ℃温度时发生的反应为2HS+SO ===3S↓+2HO,不是置换反应,故C
2 2 2
错误;若用浓硝酸处理工业尾气中的SO ,会产生含氮元素的大气污染物(即氮的氧化物),
2
故D错误。3.酸雨的主要成分是HSO ,以下是形成途径之一:①NO +SO ===NO+SO ,②2NO+
2 4 2 2 3
O===2NO ,③SO +HO===HSO ,以下叙述错误的是( )
2 2 3 2 2 4
A.NO 由反应N+2O=====2NO 生成
2 2 2 2
B.总反应可表示为2SO +O+2HO=====2HSO
2 2 2 2 4
C.还可能发生的反应有4NO +O+2HO===4HNO
2 2 2 3
D.还可能发生的反应有4NO+3O+2HO===4HNO
2 2 3
答案 A
解析 A项,N +O=====2NO,不能生成NO ,错误;B项,①×2+②+③×2得:2SO
2 2 2 2
+O +2HO===2HSO ,正确;C项,利用3NO +HO===2HNO +NO④以及④×2+②得:
2 2 2 4 2 2 3
4NO +O +2HO===4HNO ,正确;D项,利用3NO +HO===2HNO +NO④以及④×2+
2 2 2 3 2 2 3
②×3得:4NO+3O+2HO===4HNO,正确。
2 2 3
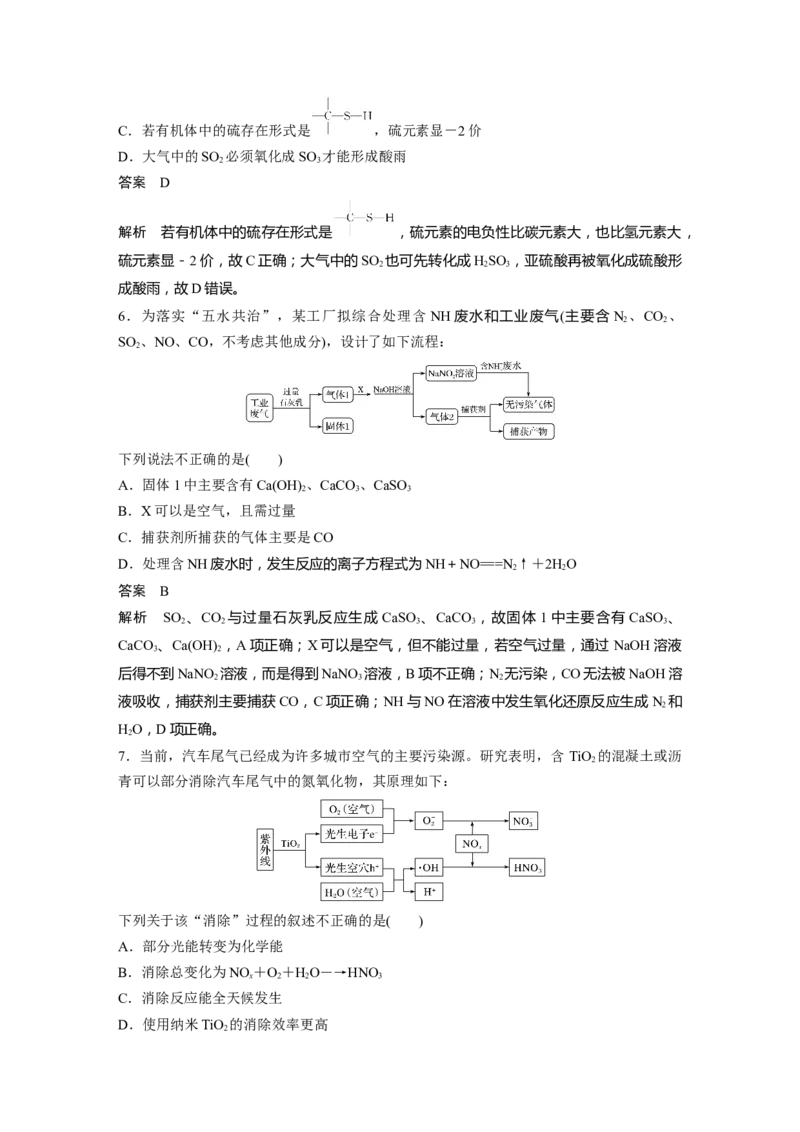
4.工厂排放的SO 烟气对环境造成污染,某企业用下图流程综合处理,下列有关说法正确
2
的是( )
A.二氧化硫吸收塔中发生的反应为SO +SO+HO===2HSO
2 2
B.氨气吸收塔中发生的反应为HSO+OH-===HO+SO
2
C.上述流程利用的是氧化还原反应原理
D.上述流程可循环利用的物质有2种
答案 A
解析 SO 吸收塔中发生反应:SO +SO+HO===2HSO,故A正确;氨气吸收塔中发生反
2 2 2
应:HSO+NH ·H O===HO+NH+SO,故B错误;各反应中各元素化合价不变,故C错误;
3 2 2
上述流程可循环利用的物质为亚硫酸铵,故D错误。
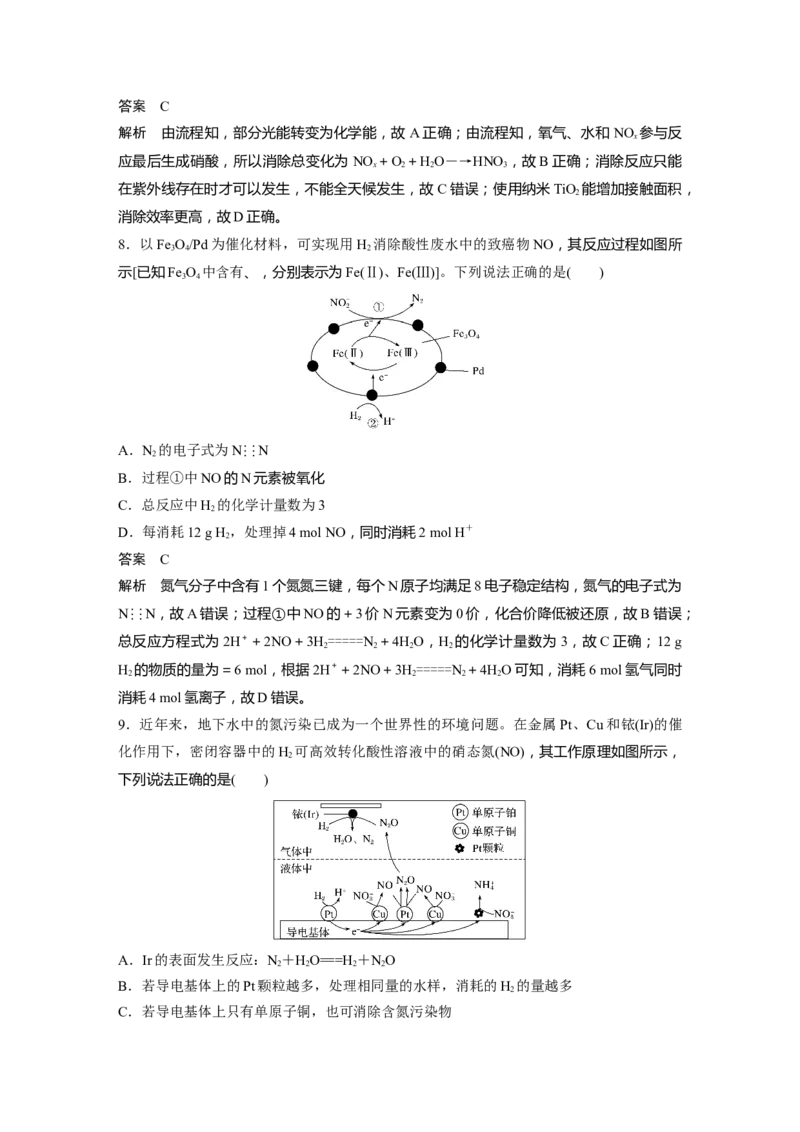
5.下图是硫元素在自然界中的循环图。下列有关说法不正确的是( )
A.大量使用化石燃料是形成酸雨的原因之一
B.循环过程中既有硫元素的氧化也有硫元素的还原C.若有机体中的硫存在形式是 ,硫元素显-2价
D.大气中的SO 必须氧化成SO 才能形成酸雨
2 3
答案 D
解析 若有机体中的硫存在形式是 ,硫元素的电负性比碳元素大,也比氢元素大,
硫元素显-2价,故C正确;大气中的SO 也可先转化成HSO ,亚硫酸再被氧化成硫酸形
2 2 3
成酸雨,故D错误。
6.为落实“五水共治”,某工厂拟综合处理含 NH废水和工业废气(主要含N 、CO 、
2 2
SO 、NO、CO,不考虑其他成分),设计了如下流程:
2
下列说法不正确的是( )
A.固体1中主要含有Ca(OH) 、CaCO 、CaSO
2 3 3
B.X可以是空气,且需过量
C.捕获剂所捕获的气体主要是CO
D.处理含NH废水时,发生反应的离子方程式为NH+NO===N↑+2HO
2 2
答案 B
解析 SO 、CO 与过量石灰乳反应生成 CaSO 、CaCO ,故固体1中主要含有 CaSO 、
2 2 3 3 3
CaCO 、Ca(OH) ,A项正确;X可以是空气,但不能过量,若空气过量,通过 NaOH溶液
3 2
后得不到NaNO 溶液,而是得到NaNO 溶液,B项不正确;N 无污染,CO无法被NaOH溶
2 3 2
液吸收,捕获剂主要捕获CO,C项正确;NH与NO在溶液中发生氧化还原反应生成N 和
2
HO,D项正确。
2
7.当前,汽车尾气已经成为许多城市空气的主要污染源。研究表明,含 TiO 的混凝土或沥
2
青可以部分消除汽车尾气中的氮氧化物,其原理如下:
下列关于该“消除”过程的叙述不正确的是( )
A.部分光能转变为化学能
B.消除总变化为NO+O+HO―→HNO
x 2 2 3
C.消除反应能全天候发生
D.使用纳米TiO 的消除效率更高
2答案 C
解析 由流程知,部分光能转变为化学能,故 A正确;由流程知,氧气、水和 NO 参与反
x
应最后生成硝酸,所以消除总变化为NO+O +HO―→HNO ,故B正确;消除反应只能
x 2 2 3
在紫外线存在时才可以发生,不能全天候发生,故C错误;使用纳米TiO 能增加接触面积,
2
消除效率更高,故D正确。
8.以Fe O/Pd为催化材料,可实现用H 消除酸性废水中的致癌物NO,其反应过程如图所
3 4 2
示[已知Fe O 中含有、,分别表示为Fe(Ⅱ)、Fe(Ⅲ)]。下列说法正确的是( )
3 4
A.N 的电子式为N⋮⋮N
2
B.过程①中NO的N元素被氧化
C.总反应中H 的化学计量数为3
2
D.每消耗12 g H,处理掉4 mol NO,同时消耗2 mol H+
2
答案 C
解析 氮气分子中含有1个氮氮三键,每个N原子均满足8电子稳定结构,氮气的电子式为
N⋮⋮N,故A错误;过程①中NO的+3价N元素变为0价,化合价降低被还原,故B错误;
总反应方程式为2H++2NO+3H=====N +4HO,H 的化学计量数为3,故C正确;12 g
2 2 2 2
H 的物质的量为=6 mol,根据2H++2NO+3H=====N +4HO可知,消耗6 mol氢气同时
2 2 2 2
消耗4 mol氢离子,故D错误。
9.近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属 Pt、Cu和铱(Ir)的催
化作用下,密闭容器中的H 可高效转化酸性溶液中的硝态氮(NO),其工作原理如图所示,
2
下列说法正确的是( )
A.Ir的表面发生反应:N+HO===H+NO
2 2 2 2
B.若导电基体上的Pt颗粒越多,处理相同量的水样,消耗的H 的量越多
2
C.若导电基体上只有单原子铜,也可消除含氮污染物D.若导电基体上的Pt颗粒增多,有利于降低溶液中的含氮量
答案 B
解析 由原理的示意图可知,Ir的表面发生反应:H +NO===N +HO,故A错误;Pt颗
2 2 2 2
粒使NO转化为NH,需得到更多的电子,故消耗的H 更多,故B正确;若导电基体上只有
2
单原子铜,不能形成原电池,所以不能消除含氮污染物,故C错误;由原理的示意图可知,
若导电基体上的Pt颗粒增多,则NO会更多的转化成铵根,不利于降低溶液中的含氮量,
故D错误。
10.(2019·江苏,16)NO、NO和NO 等氮氧化物是空气污染物,含有氮氧化物的尾气需处
2 2
理后才能排放。
(1)N O的处理。NO是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 NO分解。NH
2 2 2 3
与O 在加热和催化剂作用下生成NO的化学方程式为________________________________。
2 2
(2)NO和NO 的处理。已除去NO的硝酸尾气可用NaOH溶液吸收,主要反应为
2 2
NO+NO +2OH-===2NO+HO
2 2
2NO +2OH-===NO+NO+HO
2 2
①下列措施能提高尾气中NO和NO 去除率的有______(填字母)。
2
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到 NaNO 晶体,该晶体中的主要杂质是
2
____________(填化学式);吸收后排放的尾气中含量较高的氮氧化物是________(填化学式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相
同,NO转化为NO的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
① 在 酸 性 NaClO 溶 液 中 , HClO 氧 化 NO 生 成 Cl - 和 NO , 其 离 子 方 程 式 为
_________________。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是_____________________________。
答案 (1)2NH +2O=====NO+3HO
3 2 2 2
(2)①BC ②NaNO NO
3
(3)①3HClO+2NO+HO===3Cl-+2NO+5H+
2
②溶液pH越小,溶液中HClO的浓度越大,氧化NO的能力越强
解析 (1)NH 被O 氧化生成NO,N元素从-3价升至+1价,1 mol NH 失去4 mol e-,O
3 2 2 3
元素从0价降至-2价,1 mol O 得到4 mol e-,根据N和O元素得失电子守恒及原子守恒
2配平方程式。(2)①A项,通入尾气速率过快时,尾气吸收不充分,错误;B项,采用气、液
逆流方式吸收尾气时,尾气吸收会更充分,正确;C项,补充NaOH溶液,c(OH-)增大,能
更充分的吸收尾气,正确。②NO 与NaOH反应可生成NaNO 、NaNO 和水,所以NaNO
2 2 3 2
晶体中会混有NaNO 杂质。由吸收尾气的主要反应可知,NO 吸收更充分,故吸收后排放
3 2
的尾气中NO的含量较高。(3)①HClO氧化NO生成NO,自身被还原为Cl-,根据得失电子
守恒、原子守恒、电荷守恒配平方程式。②氧化NO的是HClO,NaClO在酸性条件下会生
成HClO,所以pH越小,溶液中HClO的浓度越大,NO转化率越高。