文档内容
18 应用“等效平衡”判断平衡移动的结果
1.等效平衡的含义
在一定条件下(恒温恒容或恒温恒压)下,同一可逆反应体系,不管是从正反应开始,还是从
逆反应开始,还是正、逆反应同时投料,达到化学平衡状态时,任何相同组分的百分含量
(质量分数、物质的量分数、体积分数等)均相同。
2.等效平衡的判断方法
(1)恒温恒容条件下反应前后体积改变的反应
判断方法:极值等量即等效。
例如:2SO (g)+O(g)2SO (g)
2 2 3
① 2 mol 1 mol 0
② 0 0 2 mol
③ 0.5 mol 0.25 mol 1.5 mol
④ a mol b mol c mol
上述①②③三种配比,按化学方程式的化学计量数关系均转化为反应物,则 SO 均为2
2
mol,O 均为1 mol,三者建立的平衡状态完全相同。
2
④中a、b、c三者的关系满足:c+a=2,+b=1,即与上述平衡等效。
(2)恒温恒压条件下反应前后体积改变的反应
判断方法:极值等比即等效。
例如:2SO (g)+O(g)2SO (g)
2 2 3
① 2 mol 3 mol 0
② 1 mol 3.5 mol 2 mol
③ a mol b mol c mol
按化学方程式的化学计量数关系均转化为反应物,则①②中=,故互为等效平衡。
③中a、b、c三者关系满足:=,即与①②平衡等效。
(3)恒温条件下反应前后体积不变的反应
判断方法:无论是恒温恒容,还是恒温恒压,只要极值等比即等效,因为压强改变对该类反
应的化学平衡无影响。
例如:H(g)+I(g)2HI(g)
2 2
① 1 mol 1 mol 0
② 2 mol 2 mol 1 mol
③ a mol b mol c mol
①②两种情况下,n(H )∶n(I)=1∶1,故互为等效平衡。
2 2
③中a、b、c三者关系满足∶=1∶1或a∶b=1∶1,c≥0,即与①②平衡等效。3.虚拟“中间态”法构建等效平衡
(1)构建恒温恒容平衡思维模式
新平衡状态可认为是两个原平衡状态简单的叠加并压缩而成,相当于增大压强。
(2)构建恒温恒压平衡思维模式(以气体物质的量增加的反应为例,见图示)
新平衡状态可以认为是两个原平衡状态简单的叠加,压强不变,平衡不移动。
对于以下三个反应,从反应开始进行到达到平衡后,保持温度、体积不变,按要求回答下列
问题。
(1)PCl (g)PCl (g)+Cl(g)
5 3 2
再充入 PCl (g),平衡向________方向移动,达到平衡后,PCl (g)的转化率________,
5 5
PCl (g)的百分含量______。
5
答案 正反应 减小 增大
(2)2HI(g)I(g)+H(g)
2 2
再充入HI(g),平衡向________方向移动,达到平衡后,HI的分解率________,HI的百分含
量________。
答案 正反应 不变 不变
(3)2NO (g)NO(g)
2 2 4
再充入NO (g),平衡向________方向移动,达到平衡后,NO (g)的转化率________,NO (g)
2 2 2
的百分含量________。
答案 正反应 增大 减小
(4)mA(g)+nB(g)pC(g)
同等倍数的加入A(g)和B(g),平衡正向移动,达到平衡后,①m+n>p,A、B的转化率都
增大,体积分数都减小;②m+n=p,A、B的转化率、体积分数都不变;③m+n2p
甲 丙 乙
B.SO 的质量m:m =m >2m
3 甲 丙 乙
C.c(SO )与c(O )之比为k:k =k >k
2 2 甲 丙 乙
D.反应放出或吸收热量的数值Q:Q =Q >2Q
甲 丙 乙
答案 B
解析 因为反应2SO (g)+O(g)2SO (g)在恒温、恒容的条件下进行。根据等效平衡的原
2 2 3
理可知,甲与丙最后达到平衡时SO 、O 、SO 的物质的量、容器内的压强、SO 与O 的比
2 2 3 2 2
值都相同;乙相当于在甲容器达到平衡后,将容器的体积瞬间扩大为原来的2倍。设甲达到
平衡时容器内的压强为p ,此时容器内瞬间压强减小为,此时平衡向逆反应方向移动,气
甲
体的物质的量增加,SO 的质量减小,所以容器内气体的压强增大,则p >,则2p >p =p
3 乙 乙 甲
,SO 的质量,m =m >2m ,A错、B对;当甲容器达到平衡后瞬间将容器体积扩大 2
丙 3 甲 丙 乙
倍,平衡向逆反应方向移动,但是生成的SO 与O 的物质的量之比为2∶1,这与开始两者
2 2
加入的物质的量之比相同,所以在此过程中SO 与O 的物质的量之比一直是2∶1不变,C
2 2
错;甲与丙为等效平衡,但达到平衡时,甲容器中SO 的转化率与丙容器中SO 的转化率不
2 3
一定相等,即Q 不一定等于Q ,D错。
甲 丙
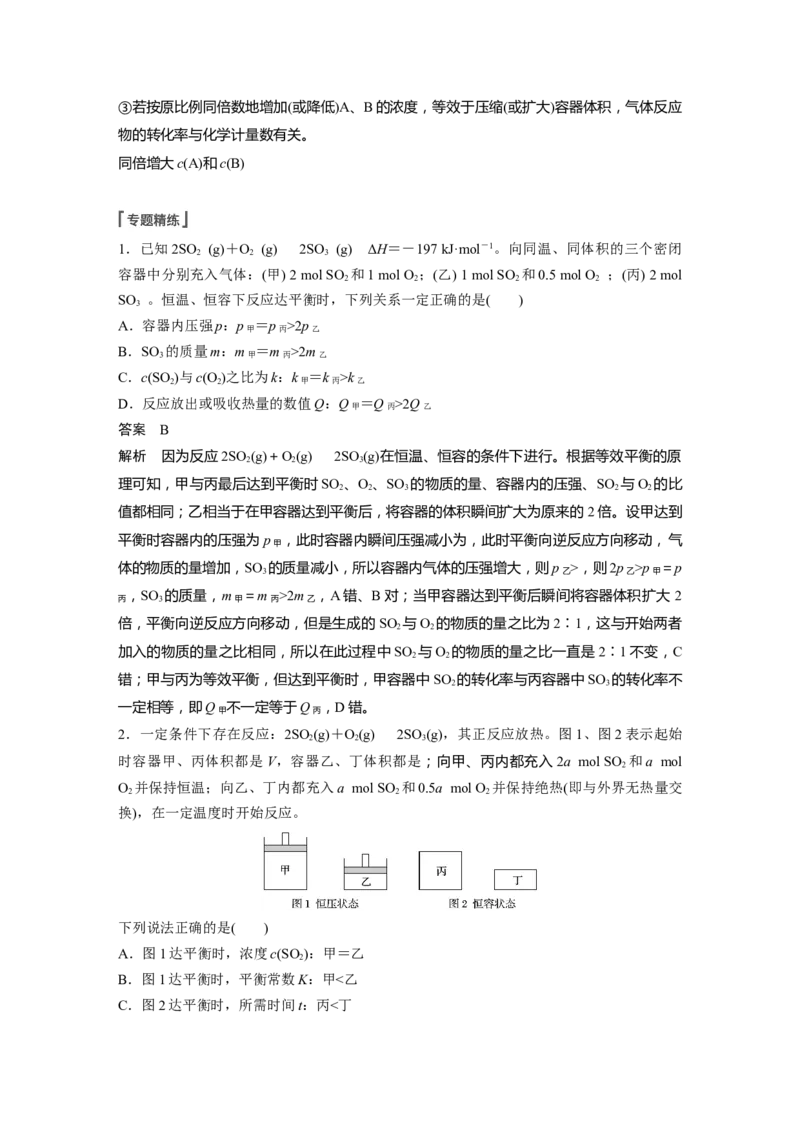
2.一定条件下存在反应:2SO (g)+O(g)2SO (g),其正反应放热。图1、图2表示起始
2 2 3
时容器甲、丙体积都是V,容器乙、丁体积都是;向甲、丙内都充入2a mol SO 和a mol
2
O 并保持恒温;向乙、丁内都充入a mol SO 和0.5a mol O 并保持绝热(即与外界无热量交
2 2 2
换),在一定温度时开始反应。
下列说法正确的是( )
A.图1达平衡时,浓度c(SO ):甲=乙
2
B.图1达平衡时,平衡常数K:甲<乙
C.图2达平衡时,所需时间t:丙<丁D.图2达平衡时,体积分数φ(SO ):丙>丁
3
答案 D
解析 甲和乙若都是恒温恒压,则两者等效,但乙为绝热恒压,又该反应正反应为放热反应,
则温度:甲<乙,温度升高平衡向逆反应方向移动,浓度c(SO ):甲<乙,平衡常数K:甲>
2
乙,故A、B项错误;丙和丁若都是恒温恒容,则两者等效,但丁为绝热恒容,则温度:丙
<丁,温度越高,反应速率越快,到达平衡的时间越短,所用的时间:丙>丁,C项错误;温
度升高平衡向逆反应方向移动,体积分数φ(SO ):丙>丁,D项正确。
3
3.Ⅰ.恒温、恒压下,在一可变容积的容器中发生如下反应:
A(g)+B(g)C(g)。
(1)若开始时放入1 mol A和1 mol B,达到平衡后,生成a mol C,这时A的物质的量为
________mol。
(2)若开始时放入3 mol A和3 mol B,达到平衡后,生成C的物质的量为________mol。
(3)若开始时放入x mol A、2 mol B和1 mol C,达到平衡后,A和C的物质的量分别是y
mol和3a mol,则x=________mol,y=________mol。平衡时,B的物质的量________(填
字母)。
A.大于2 mol
B.等于2 mol
C.小于2 mol
D.可能大于、等于或小于2 mol
作出此判断的理由是_________________________________________________________。
(4)若在(3)的平衡混合物中再加入 3 mol C,待再次达到平衡后,C 的物质的量分数是
________。
Ⅱ.若维持温度不变,在一个与(1)反应前起始体积相同且容积固定的容器中发生上述反应。
(5)开始时放入1 mol A和1 mol B达到平衡后生成b mol C,将b与(1)小题中的a进行比较:
________(选填一个编号)。
甲:ab
丙:a=b 丁:不能比较
作出此判断理由是________________________________________________________。
答案 (1)(1-a) (2)3a (3)2 (3-3a) D 若3a>1,B的物质的量小于2 mol;若3a=1,
B的物质的量等于2 mol;若3a<1,B的物质的量大于2 mol (4) (5)乙 因为(5)小题中容
器的容积不变,而(1)小题中容器的容积缩小,所以随着反应进行,(5)小题的容器中的压强
小于(1)小题容器中的压强,有利于平衡逆向移动,故反应达到平衡后a>b
解析 (1)由反应A(g)+B(g)C(g)可知,生成a mol C必消耗a mol A,则n(A)=(1-
a)mol。(2)因(2)与(1)为恒温恒压条件下的等效平衡,且(2)开始时A和B的物质的量为(1)开
始时A和B物质的量的3倍,则达到平衡后(2)生成C的物质的量为(1)生成C的物质的量的3倍,故生成C的物质的量为3a mol。(3)因(3)与(2)为恒温恒压条件下的等效平衡,若 1
mol C全部生成A和B,则可得到1 mol A和1 mol B,则x mol+1 mol=3 mol,解得x=
2。
A(g)+B(g)C(g)
开始物质的量mol 2 2 1
转化物质的量mol 3a-1 3a-1 3a-1
平衡物质的量mol 3-3a 3-3a 3a
从而可得y=3-3a,n(B) =(3-3a)mol。
平
由此可知,若3a>1,则B的物质的量小于2 mol;若3a=1,则B的物质的量等于2 mol;
若3a<1,则B的物质的量大于2 mol。(4)因(4)与(1)和(2)均为等效平衡,则(4)与(1)和(2)中C
的物质的量分数均相等,故C的物质的量分数为=或=。(5)因为容器的容积不变,而(1)小
题中容器的容积缩小,所以随着反应进行,(5)小题的容器中的压强小于(1)小题容器中的压
强,有利于平衡逆向移动,故反应达到平衡后a>b。