文档内容
专项特训 7 滴定过程的曲线分析
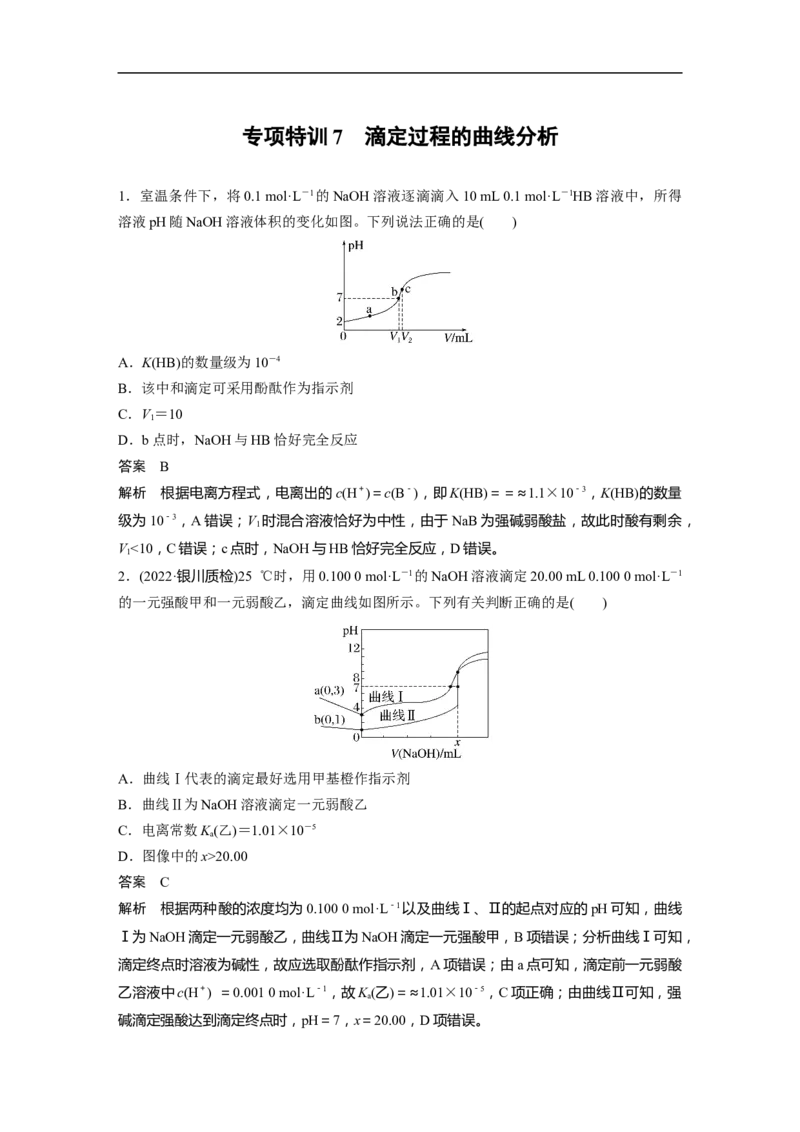
1.室温条件下,将0.1 mol·L-1的NaOH溶液逐滴滴入10 mL 0.1 mol·L-1HB溶液中,所得
溶液pH随NaOH溶液体积的变化如图。下列说法正确的是( )
A.K(HB)的数量级为10-4
B.该中和滴定可采用酚酞作为指示剂
C.V=10
1
D.b点时,NaOH与HB恰好完全反应
答案 B
解析 根据电离方程式,电离出的c(H+)=c(B-),即K(HB)==≈1.1×10-3,K(HB)的数量
级为10-3,A错误;V 时混合溶液恰好为中性,由于NaB为强碱弱酸盐,故此时酸有剩余,
1
V<10,C错误;c点时,NaOH与HB恰好完全反应,D错误。
1
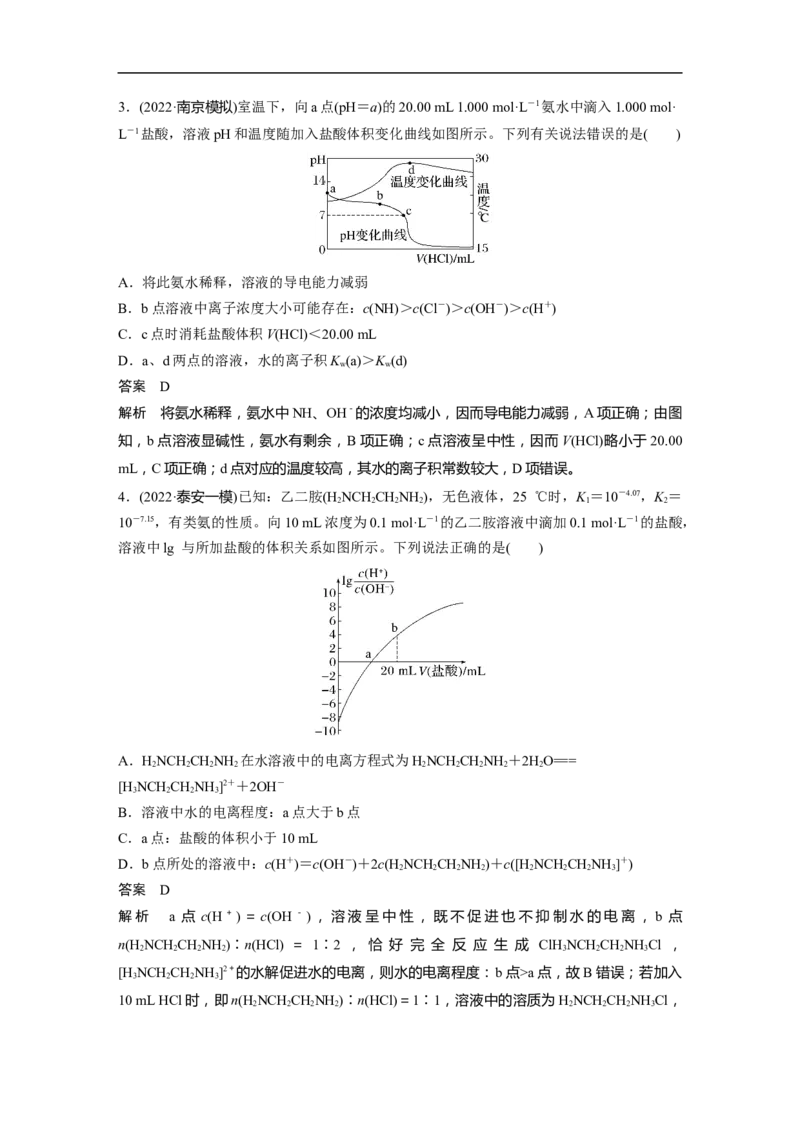
2.(2022·银川质检)25 ℃时,用0.100 0 mol·L-1的NaOH溶液滴定20.00 mL 0.100 0 mol·L-1
的一元强酸甲和一元弱酸乙,滴定曲线如图所示。下列有关判断正确的是( )
A.曲线Ⅰ代表的滴定最好选用甲基橙作指示剂
B.曲线Ⅱ为NaOH溶液滴定一元弱酸乙
C.电离常数K(乙)=1.01×10-5
a
D.图像中的x>20.00
答案 C
解析 根据两种酸的浓度均为0.100 0 mol·L-1以及曲线Ⅰ、Ⅱ的起点对应的pH可知,曲线
Ⅰ为NaOH滴定一元弱酸乙,曲线Ⅱ为NaOH滴定一元强酸甲,B项错误;分析曲线Ⅰ可知,
滴定终点时溶液为碱性,故应选取酚酞作指示剂,A项错误;由a点可知,滴定前一元弱酸
乙溶液中c(H+) =0.001 0 mol·L-1,故K(乙)=≈1.01×10-5,C项正确;由曲线Ⅱ可知,强
a
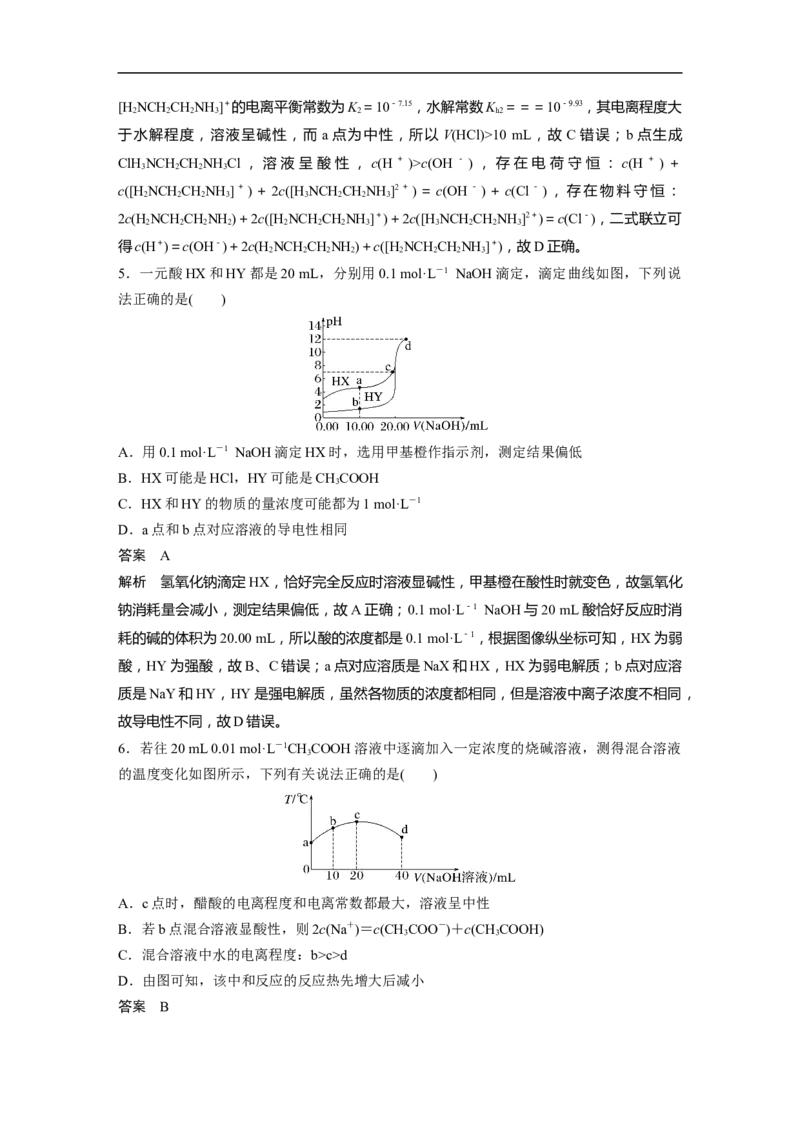
碱滴定强酸达到滴定终点时,pH=7,x=20.00,D项错误。3.(2022·南京模拟)室温下,向a点(pH=a)的20.00 mL 1.000 mol·L-1氨水中滴入1.000 mol·
L-1盐酸,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法错误的是( )
A.将此氨水稀释,溶液的导电能力减弱
B.b点溶液中离子浓度大小可能存在:c(NH)>c(Cl-)>c(OH-)>c(H+)
C.c点时消耗盐酸体积V(HCl)<20.00 mL
D.a、d两点的溶液,水的离子积K (a)>K (d)
w w
答案 D
解析 将氨水稀释,氨水中NH、OH-的浓度均减小,因而导电能力减弱,A项正确;由图
知,b点溶液显碱性,氨水有剩余,B项正确;c点溶液呈中性,因而V(HCl)略小于20.00
mL,C项正确;d点对应的温度较高,其水的离子积常数较大,D项错误。
4.(2022·泰安一模)已知:乙二胺(H NCH CHNH ),无色液体,25 ℃时,K =10-4.07,K =
2 2 2 2 1 2
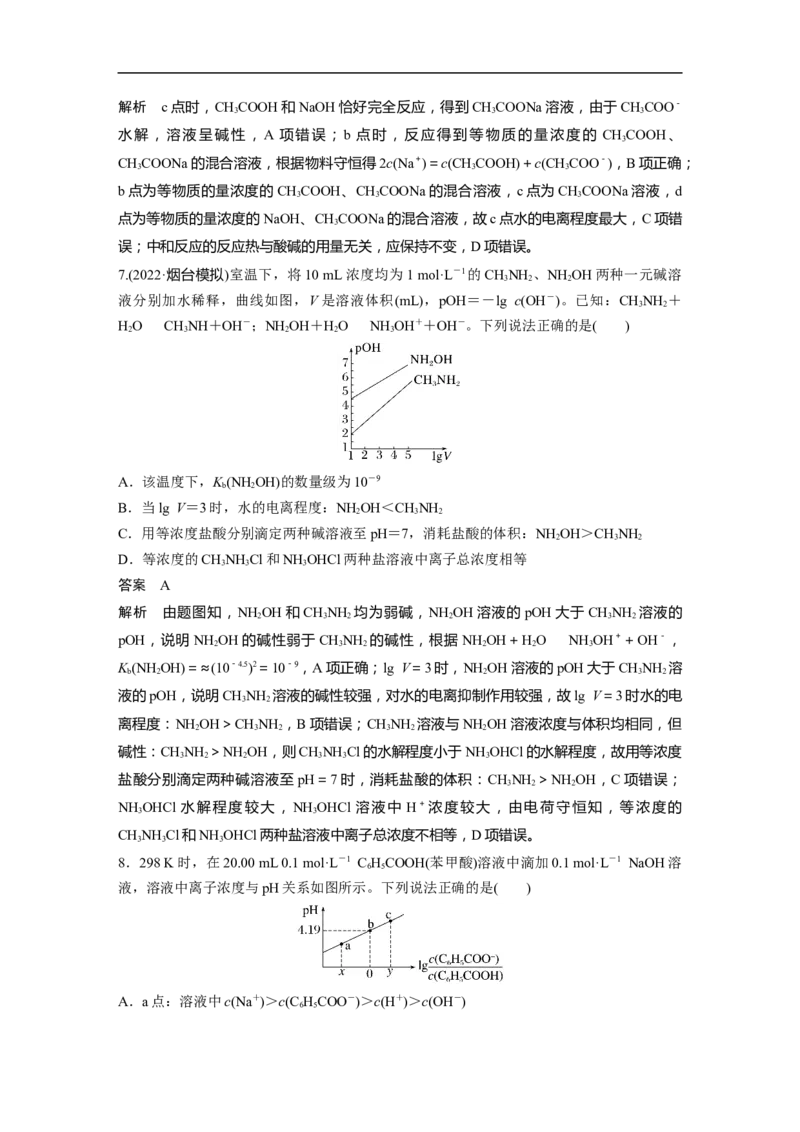
10-7.15,有类氨的性质。向10 mL浓度为0.1 mol·L-1的乙二胺溶液中滴加0.1 mol·L-1的盐酸,
溶液中lg 与所加盐酸的体积关系如图所示。下列说法正确的是( )
A.HNCH CHNH 在水溶液中的电离方程式为HNCH CHNH +2HO===
2 2 2 2 2 2 2 2 2
[H NCH CHNH ]2++2OH-
3 2 2 3
B.溶液中水的电离程度:a点大于b点
C.a点:盐酸的体积小于10 mL
D.b点所处的溶液中:c(H+)=c(OH-)+2c(H NCH CHNH )+c([H NCH CHNH ]+)
2 2 2 2 2 2 2 3
答案 D
解析 a 点 c(H+)=c(OH-),溶液呈中性,既不促进也不抑制水的电离,b 点
n(H NCH CHNH )∶n(HCl) = 1∶2 , 恰 好 完 全 反 应 生 成 ClH NCH CHNH Cl ,
2 2 2 2 3 2 2 3
[H NCH CHNH ]2+的水解促进水的电离,则水的电离程度:b点>a点,故B错误;若加入
3 2 2 3
10 mL HCl时,即n(H NCH CHNH )∶n(HCl)=1∶1,溶液中的溶质为HNCH CHNH Cl,
2 2 2 2 2 2 2 3[H NCH CHNH ]+的电离平衡常数为K =10-7.15,水解常数K ===10-9.93,其电离程度大
2 2 2 3 2 h2
于水解程度,溶液呈碱性,而 a 点为中性,所以 V(HCl)>10 mL,故 C 错误;b 点生成
ClH NCH CHNH Cl,溶液呈酸性, c(H+)>c(OH-),存在电荷守恒: c(H+)+
3 2 2 3
c([H NCH CHNH ]+)+2c([H NCH CHNH ]2+)=c(OH-)+c(Cl-),存在物料守恒:
2 2 2 3 3 2 2 3
2c(H NCH CHNH )+2c([H NCH CHNH ]+)+2c([H NCH CHNH ]2+)=c(Cl-),二式联立可
2 2 2 2 2 2 2 3 3 2 2 3
得c(H+)=c(OH-)+2c(H NCH CHNH )+c([H NCH CHNH ]+),故D正确。
2 2 2 2 2 2 2 3
5.一元酸HX和HY都是20 mL,分别用0.1 mol·L-1 NaOH滴定,滴定曲线如图,下列说
法正确的是( )
A.用0.1 mol·L-1 NaOH滴定HX时,选用甲基橙作指示剂,测定结果偏低
B.HX可能是HCl,HY可能是CHCOOH
3
C.HX和HY的物质的量浓度可能都为1 mol·L-1
D.a点和b点对应溶液的导电性相同
答案 A
解析 氢氧化钠滴定HX,恰好完全反应时溶液显碱性,甲基橙在酸性时就变色,故氢氧化
钠消耗量会减小,测定结果偏低,故A正确;0.1 mol·L-1 NaOH与20 mL酸恰好反应时消
耗的碱的体积为20.00 mL,所以酸的浓度都是0.1 mol·L-1,根据图像纵坐标可知,HX为弱
酸,HY为强酸,故B、C错误;a点对应溶质是NaX和HX,HX为弱电解质;b点对应溶
质是NaY和HY,HY是强电解质,虽然各物质的浓度都相同,但是溶液中离子浓度不相同,
故导电性不同,故D错误。
6.若往20 mL 0.01 mol·L-1CHCOOH溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液
3
的温度变化如图所示,下列有关说法正确的是( )
A.c点时,醋酸的电离程度和电离常数都最大,溶液呈中性
B.若b点混合溶液显酸性,则2c(Na+)=c(CHCOO-)+c(CHCOOH)
3 3
C.混合溶液中水的电离程度:b>c>d
D.由图可知,该中和反应的反应热先增大后减小
答案 B解析 c点时,CHCOOH和NaOH恰好完全反应,得到CHCOONa溶液,由于CHCOO-
3 3 3
水解,溶液呈碱性,A 项错误;b 点时,反应得到等物质的量浓度的 CHCOOH、
3
CHCOONa的混合溶液,根据物料守恒得2c(Na+)=c(CHCOOH)+c(CHCOO-),B项正确;
3 3 3
b点为等物质的量浓度的CHCOOH、CHCOONa的混合溶液,c点为CHCOONa溶液,d
3 3 3
点为等物质的量浓度的NaOH、CHCOONa的混合溶液,故c点水的电离程度最大,C项错
3
误;中和反应的反应热与酸碱的用量无关,应保持不变,D项错误。
7.(2022·烟台模拟)室温下,将10 mL浓度均为1 mol·L-1的CHNH 、NH OH两种一元碱溶
3 2 2
液分别加水稀释,曲线如图,V是溶液体积(mL),pOH=-lg c(OH-)。已知:CHNH +
3 2
HOCHNH+OH-;NH OH+HONH OH++OH-。下列说法正确的是( )
2 3 2 2 3
A.该温度下,K (NH OH)的数量级为10-9
b 2
B.当lg V=3时,水的电离程度:NH OH<CHNH
2 3 2
C.用等浓度盐酸分别滴定两种碱溶液至pH=7,消耗盐酸的体积:NH OH>CHNH
2 3 2
D.等浓度的CHNH Cl和NH OHCl两种盐溶液中离子总浓度相等
3 3 3
答案 A
解析 由题图知,NH OH和CHNH 均为弱碱,NH OH溶液的pOH大于CHNH 溶液的
2 3 2 2 3 2
pOH,说明NH OH的碱性弱于CHNH 的碱性,根据NH OH+HONH OH++OH-,
2 3 2 2 2 3
K (NH OH)=≈(10-4.5)2=10-9,A项正确;lg V=3时,NH OH溶液的pOH大于CHNH 溶
b 2 2 3 2
液的pOH,说明CHNH 溶液的碱性较强,对水的电离抑制作用较强,故lg V=3时水的电
3 2
离程度:NH OH>CHNH ,B项错误;CHNH 溶液与NH OH溶液浓度与体积均相同,但
2 3 2 3 2 2
碱性:CHNH >NH OH,则CHNH Cl的水解程度小于NH OHCl的水解程度,故用等浓度
3 2 2 3 3 3
盐酸分别滴定两种碱溶液至pH=7时,消耗盐酸的体积:CHNH >NH OH,C项错误;
3 2 2
NH OHCl 水解程度较大,NH OHCl 溶液中 H+浓度较大,由电荷守恒知,等浓度的
3 3
CHNH Cl和NH OHCl两种盐溶液中离子总浓度不相等,D项错误。
3 3 3
8.298 K时,在20.00 mL 0.1 mol·L-1 C HCOOH(苯甲酸)溶液中滴加0.1 mol·L-1 NaOH溶
6 5
液,溶液中离子浓度与pH关系如图所示。下列说法正确的是( )
A.a点:溶液中c(Na+)>c(C HCOO-)>c(H+)>c(OH-)
6 5B.b点:对应的NaOH溶液体积为10 mL
C.对b点溶液加热(不考虑挥发),实现曲线由b点向c点的变化
D.298 K时,C HCOOH的电离常数为1×10-4.19
6 5
答案 D
解析 由题图知,a点溶液呈酸性,根据电荷守恒可知 c(C HCOO-)>c(Na+)>c(H+)>c(OH
6 5
-),A错误;加10 mL NaOH溶液时,苯甲酸反应一半,此时溶液呈酸性,C HCOOH的电
6 5
离程度大于C HCOO-的水解程度,c(C HCOO-)>c(C HCOOH),而b点溶液中c(C HCOO
6 5 6 5 6 5 6 5
-)=c(C HCOOH),B错误;对b点溶液加热,C HCOOH的电离程度增大,溶液的pH降
6 5 6 5
低,C错误;选b点计算电离常数,K=c(H+)=1×10-4.19,D正确。
a
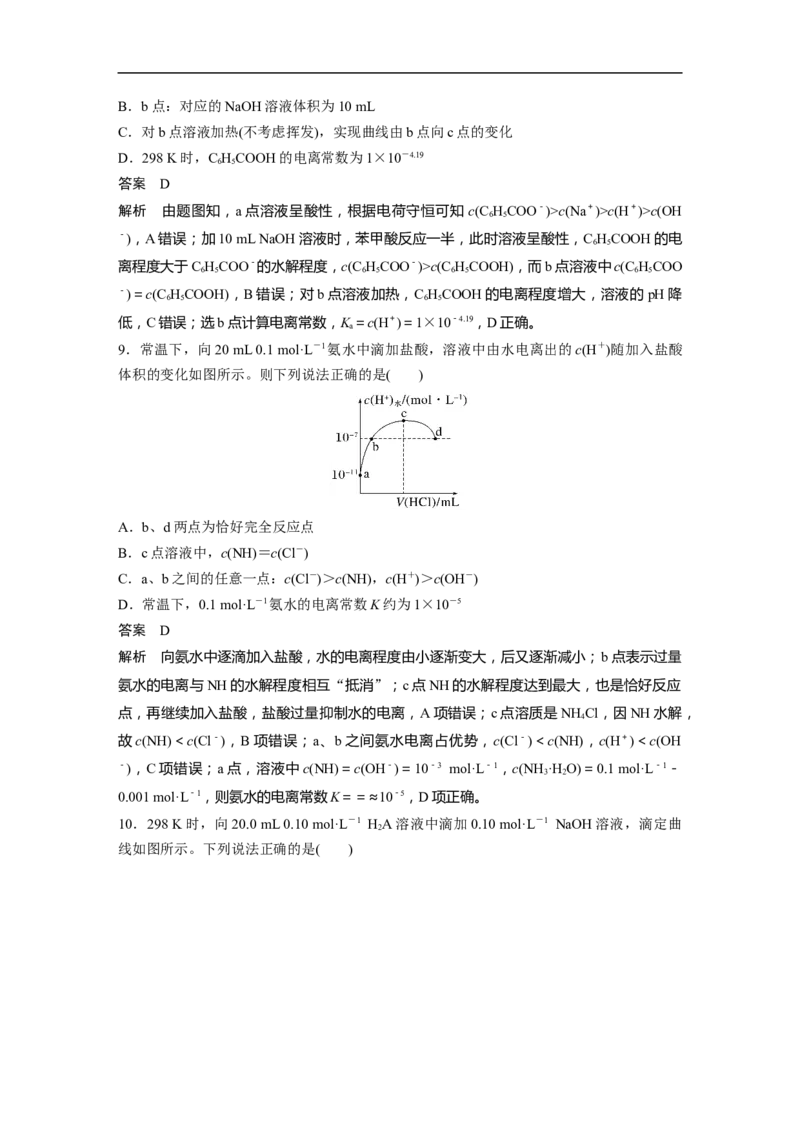
9.常温下,向20 mL 0.1 mol·L-1氨水中滴加盐酸,溶液中由水电离出的c(H+)随加入盐酸
体积的变化如图所示。则下列说法正确的是( )
A.b、d两点为恰好完全反应点
B.c点溶液中,c(NH)=c(Cl-)
C.a、b之间的任意一点:c(Cl-)>c(NH),c(H+)>c(OH-)
D.常温下,0.1 mol·L-1氨水的电离常数K约为1×10-5
答案 D
解析 向氨水中逐滴加入盐酸,水的电离程度由小逐渐变大,后又逐渐减小;b点表示过量
氨水的电离与NH的水解程度相互“抵消”;c点NH的水解程度达到最大,也是恰好反应
点,再继续加入盐酸,盐酸过量抑制水的电离,A项错误;c点溶质是NH Cl,因NH水解,
4
故c(NH)<c(Cl-),B项错误;a、b之间氨水电离占优势,c(Cl-)<c(NH),c(H+)<c(OH
-),C项错误;a点,溶液中c(NH)=c(OH-)=10-3 mol·L-1,c(NH ·H O)=0.1 mol·L-1-
3 2
0.001 mol·L-1,则氨水的电离常数K==≈10-5,D项正确。
10.298 K时,向20.0 mL 0.10 mol·L-1 HA溶液中滴加0.10 mol·L-1 NaOH溶液,滴定曲
2
线如图所示。下列说法正确的是( )A.该滴定过程应该选择石蕊溶液作指示剂
B.W点到X点发生的主要反应的离子方程式为
HA+2OH-===A2-+2HO
2 2
C.Y点对应的溶液中c(Na+)+c(H+)=c(OH-)+2c(A2-)
D.反应HA+A2-2HA-的平衡常数K=1.0×107.4
2
答案 D
解析 石蕊不能用作酸碱中和滴定的指示剂,根据图示滴定终点的pH可知,第二反应终点
应用酚酞作指示剂,A项错误;X点对应的溶液中溶质主要是NaHA,W点到X点发生的主
要反应的离子方程式为HA+OH-===HA-+HO,B项错误;根据电荷守恒:c(Na+)+c(H
2 2
+)=c(OH-)+c(HA-)+2c(A2-),因为Y点对应的溶液中c(HA-)=c(A2-),所以c(Na+)+
c(H+)=c(OH-)+3c(A2-),C项错误;HAHA-+H+,K =,由于W点对应的溶液中
2 a1
c(HA-)=c(H A),故K =c(H+)=1.0×10-2.3;HA-A2-+H+,K =,由于Y点对应的溶
2 a1 a2
液中c(HA-)=c(A2-),故K =c(H+)=1.0×10-9.7;HA+A2-2HA-的平衡常数K===
a2 2
1.0×107.4,D项正确。