文档内容
[复习目标] 1.理解电离常数、水解常数、溶度积常数的概念及影响因素。2.掌握电离常数、
水解常数、溶度积常数的相关计算。
1.电离常数(K )与电离度(α)的关系(以一元弱酸HA为例)
电离
HA H+ + A-
起始浓度: c 0 0
酸
平衡浓度: c ·(1-α) c ·α c ·α
酸 酸 酸
K ==。
电离
若α很小,可认为1-α≈1,则K =c ·α2(或α=)。
电离 酸
2.电离常数与水解常数的关系
(1)对于一元弱酸HA,K 与K 的关系
a h
HAH++A-,K(HA)=;A-+HOHA+OH-,K (A-)=。则K·K =c(H+)·c(OH-)=
a 2 h a h
K ,故K =。
w h
常温时K·K =K =1.0×10-14,K =。
a h w h
(2)对于二元弱酸HB,K (H B)、K (H B)与K (HB-)、K (B2-)的关系
2 a1 2 a2 2 h h
HB-+HOHB+OH-,K (HB-)===。
2 2 h
B2-+HOHB-+OH-,K (B2-)===。
2 h
考向拓展 常温时,对于一元弱酸HA,当K>1.0×10-7时,K <1.0×10-7,此时将等物质
a h
的量浓度的HA溶液与NaA溶液等体积混合,HA的电离程度大于A-的水解程度,溶液呈
酸性;同理,当K<1.0×10-7时,K >1.0×10-7,A-的水解程度大于HA的电离程度,溶液
a h
呈碱性。对于多元弱酸,K =,K 是其阴离子结合一个H+所形成的粒子的电离常数。
h a
[实例]
按要求回答下列问题。
(1)已知在25 ℃时,碳酸和亚硫酸的电离平衡常数如表所示:
电解质 碳酸 亚硫酸
K =4.30×10-7 K =1.00×10-2
a1 a1
电离常数
K =5.61×10-11 K =1.02×10-7
a2 a2
①NaHSO 水解反应的平衡常数K =_______________________________________。
3 h②HSO 溶液和NaHCO 溶液反应的主要离子方程式为__________________________
2 3 3
________________________________________________________________________。
答案 ①1.00×10-12 ②HSO +HCO===HSO+CO↑+HO
2 3 2 2
解 析 ① NaHSO 水 解 反 应 的 平 衡 常 数 K = = = 1.00×10 - 12 。 ② 酸 性 :
3 h
HSO >H CO>HSO,则 HSO 溶液和 NaHCO 溶液反应的主要离子方程式为 HSO +
2 3 2 3 2 3 3 2 3
HCO===HSO+CO↑+HO。
2 2
(2)已知HNO 的电离常数K=7.1×10-4;NH ·H O的电离常数K =1.7×10-5;则0.1 mol·L-1
2 a 3 2 b
NH NO 溶液中离子浓度由大到小的顺序是_____________________________________。
4 2
常温下NO水解反应的平衡常数K =______(结果保留两位有效数字)。
h
答案 c(NO)>c(NH)>c(H+)>c(OH-) 1.4×10-11
解析 依据NO+HOHNO+OH-,水解平衡常数表达式K ==×==≈1.4×10-11。
2 2 h
3.溶度积常数(K )的相关计算
sp
(1)M(OH) 悬浊液中K 、K 、pH间的关系
n sp w
M(OH) (s)Mn+(aq)+nOH-(aq)
n
K =c(Mn+)·cn(OH-)=·cn(OH-)==()n+1。
sp
(2)K 与溶解度(S)之间的计算关系
sp
对于AB型物质,其K =2。
sp
如60 ℃时溴酸银(AgBrO )的溶解度为0.6 g,则K 约等于________________。
3 sp
答案 6.5×10-4
解析 60 ℃时,其K =c(Ag+)·c(BrO)=2=2≈6.5×10-4。
sp
(3)K 与沉淀转化平衡常数K的计算关系
sp
建立K 与K的关系,一般是在K的表达式分子分母中同乘以某个离子的浓度,将分子分母
sp
转化为不同物质的K 。
sp
如在1.0 L Na CO 溶液中溶解0.01 mol BaSO ,列式计算,NaCO 溶液的最初浓度不得低于
2 3 4 2 3
______ mol·L-1[忽略溶液体积变化,已知:K (BaSO)=1.1×10-10、K (BaCO)=5.1×10-
sp 4 sp 3
9]。
答案 0.46
解析 沉淀转化的离子方程式为 CO(aq)+BaSO(s)BaCO (s)+SO(aq),K====
4 3
≈0.022。c(CO)== mol·L-1≈0.45 mol·
L-1,NaCO 溶液的最初浓度:c(Na CO)≥(0.01+0.45)mol·L-1=0.46 mol·L-1。
2 3 2 3
(4)K 与电离常数K 的计算关系
sp a
根据电离常数计算出各离子浓度,进而计算K 。
sp
如汽车尾气中的SO 可用石灰水吸收,生成亚硫酸钙浊液。常温下,测得 CaSO 与水形成的
2 3
浊液pH为9,忽略SO的第二步水解,则K (CaSO)=________(结果保留3位有效数字)。
sp 3
[已知:K (H SO )=1.54×10-2,K (H SO )=1.02×10-7]
a1 2 3 a2 2 3答案 1.05×10-6
解析 pH=9,c(OH-)=1×10-5mol·L-1,由SO+HOHSO+OH-知,c(HSO)=c(OH-)
2
=1×10-5mol·L-1。K (SO)==,则=,c(SO)=1.02×10-3mol·L-1。由元素质量守恒知:
h
c(Ca2+)=c(SO)+c(HSO)=1.02×10-3mol·
L-1+1×10-5mol·L-1=1.03×10-3mol·L-1。则K (CaSO)=c(Ca2+)·c(SO)≈1.05×10-6。
sp 3
(5)判断沉淀转化能否进行
已知:常温下,ZnS和CuS的K 分别为1.6×10-24和6.4×10-36,判断常温下反应ZnS+
sp
CuSO ===CuS+ZnSO 能否进行。
4 4
该反应的平衡常数
K==
==
=2.5×1010>105,故该反应能完全转化。
若计算沉淀转化的平衡常数K<10-5,则转化反应不能进行,若10-5K,所以在“浸取”时,上述平衡逆向移动,得到CaSO 而不是CaC O
4 2 4
5.钨是熔点最高的金属,是重要的战略物资。自然界中黑钨矿的主要成分是 FeWO 、
4
MnWO ,还含有少量Si、P、As的化合物。由黑钨矿制备WO 的工艺流程如下:
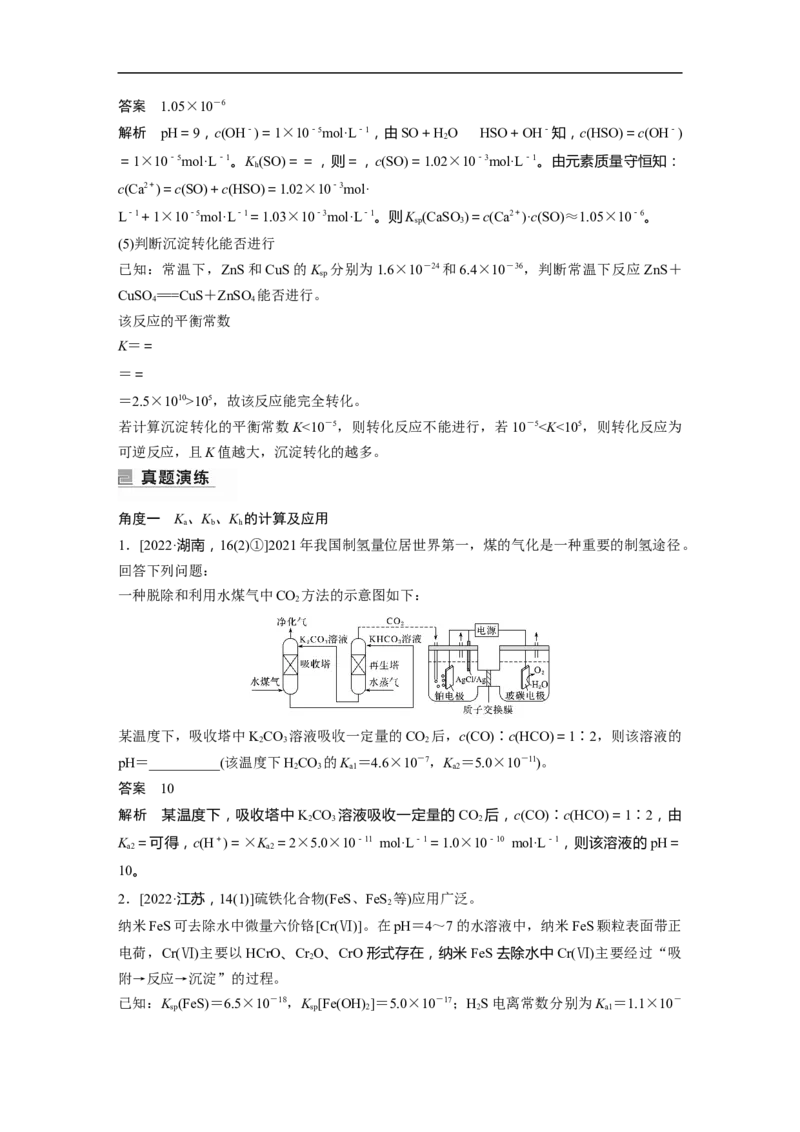
4 3浸出液中的溶质有NaWO 、NaSiO 、NaPO 、NaAsO ,加入MgSO 、HSO 将溶液的pH
2 4 2 3 3 4 3 4 4 2 4
调至9时,溶液中=____。(已知K [Mg (PO )]=2.0×10-24、K [Mg (AsO)]=2.0×10-20)
sp 3 4 2 sp 3 4 2
答案 10-2
解析 已知K [Mg (PO )]=c3(Mg2+)·c2(PO)=2.0×10-24、K [Mg (AsO)]=c3(Mg2+)·
sp 3 4 2 sp 3 4 2
c2(AsO)=2.0×10-20,将溶液的pH调至9时,溶液中===10-2。
专题强化练
1.已知常温下,NaCO 溶液的水解常数K =2×10-4,则当溶液中c(HCO)∶c(CO)=2∶1
2 3 h
时,试求该溶液的pH=________。
答案 10
解析 K ==2×10-4,又c(HCO)∶c(CO)=2∶1,则c(OH-)=10-4 mol·L-1,结合K =
h w
1.0×10-14,可得c(H+)=10-10 mol·L-1。
2.已知:常温下,K (H CrO)=0.18,K (H CrO)=3.2×10-7。试推测常温下,KHCrO 溶
a1 2 4 a2 2 4 4
液呈______(填“酸性”“碱性”或“中性”),其原因是_______________________
________________________________________________________________________
________________________________________________________________________(用必要
的文字说明)。
答案 酸性 KHCrO 在溶液中可发生水解,其水解常数K ==≈5.56×10-14,KHCrO 在溶
4 h 4
液中也可以发生电离,K (H CrO)=3.2×10-7>K ,即HCrO的水解程度小于其电离程度,
a2 2 4 h
溶液呈酸性
3.常温下,用NaOH溶液吸收SO 得到pH=9的NaSO 溶液,吸收过程中水的电离平衡
2 2 3
________(填“向左”“向右”或“不”)移动。试计算所得溶液中=__________。(常温下,
HSO 的电离常数K =1.0×10-2,K =6.0×10-8)
2 3 a1 a2
答案 向右 60
解析 NaOH电离出的OH-抑制水的电离,NaSO 电离出的SO因水解而促进水的电离。
2 3
K (SO)===,所以==60。
h
4.磷酸是三元弱酸,常温下三级电离常数分别是 K =7.1×10-3、K =6.2×10-8、K =
a1 a2 a34.5×
10-13。
常温下同浓度①NaPO 、②NaHPO 、③NaH PO 的pH由小到大的顺序是__________(填
3 4 2 4 2 4
序号);常温下,NaHPO 的水溶液呈__________(填“酸”“碱”或“中”)性,用K 与K
2 4 a h
的相对大小,说明判断理由:__________________________________________________
________________________________________________________________________。
答案 ③<②<① 碱 溶液中 HPO 的 K <K ,HPO 的水解程度大于其电离程度,
a3 h
NaHPO 溶液呈碱性
2 4
解析 磷酸是三元弱酸,磷酸钠在溶液中分步水解,一级水解抑制二级水解,一级和二级水
解抑制三级水解。酸根离子的水解程度越大,溶液的碱性越强,pH越大,则三种盐溶液中
酸根离子水解程度由小到大的顺序为③<②<①,则溶液pH由小到大的顺序为③<②<①;
NaHPO 的水解常数K ===≈1.61×10-7>K =4.5×10-13,HPO的水解程度大于其电离程
2 4 h a3
度,NaHPO 溶液呈碱性。
2 4
5.Zn2+(aq)+HS(aq)ZnS(s)+2H+(aq)的平衡常数 K=________。[已知:常温下,
2
K (ZnS)=3.0×10-25,HS的电离常数K =9.0×10-8、K =1.0×10-15]
sp 2 a1 a2
答案 300
解析 平衡常数K=====300。
6.从废旧LiFePO 电极中可回收锂元素。用硝酸充分溶浸废旧LiFePO 电极,测得浸取液
4 4
中c(Li+)=4 mol·L-1,加入等体积的碳酸钠溶液将Li+转化为LiCO 沉淀,若沉淀中的锂元
2 3
素占浸取液中锂元素总量的 90%,则加入碳酸钠溶液的浓度为________ mol·L-1。[已知
K (Li CO)=1.6×10-3,假设反应后溶液体积为反应前两溶液之和]
sp 2 3
答案 1.88
解析 浸取液中c(Li+)=4 mol·L-1,加入等体积的碳酸钠溶液将Li+转化为LiCO 沉淀,若
2 3
沉淀中的锂元素占浸取液中锂元素总量的 90%,设浸取液的体积为V L,则可知沉淀后的
c(Li+)= mol·L-1=0.2 mol·L-1,K (Li CO)=c2(Li+)·c(CO)=1.6×10-3,则0.2×0.2×c(CO)
sp 2 3
=1.6×10-3,故剩余c(CO)=0.04 mol·L-1,沉淀的c(CO)=×
mol·L-1=0.9 mol·L-1,总c(CO)=0.94 mol·L-1,由于此时体积为原体积的2倍,故加入碳
酸钠溶液的浓度为1.88 mol·L-1。
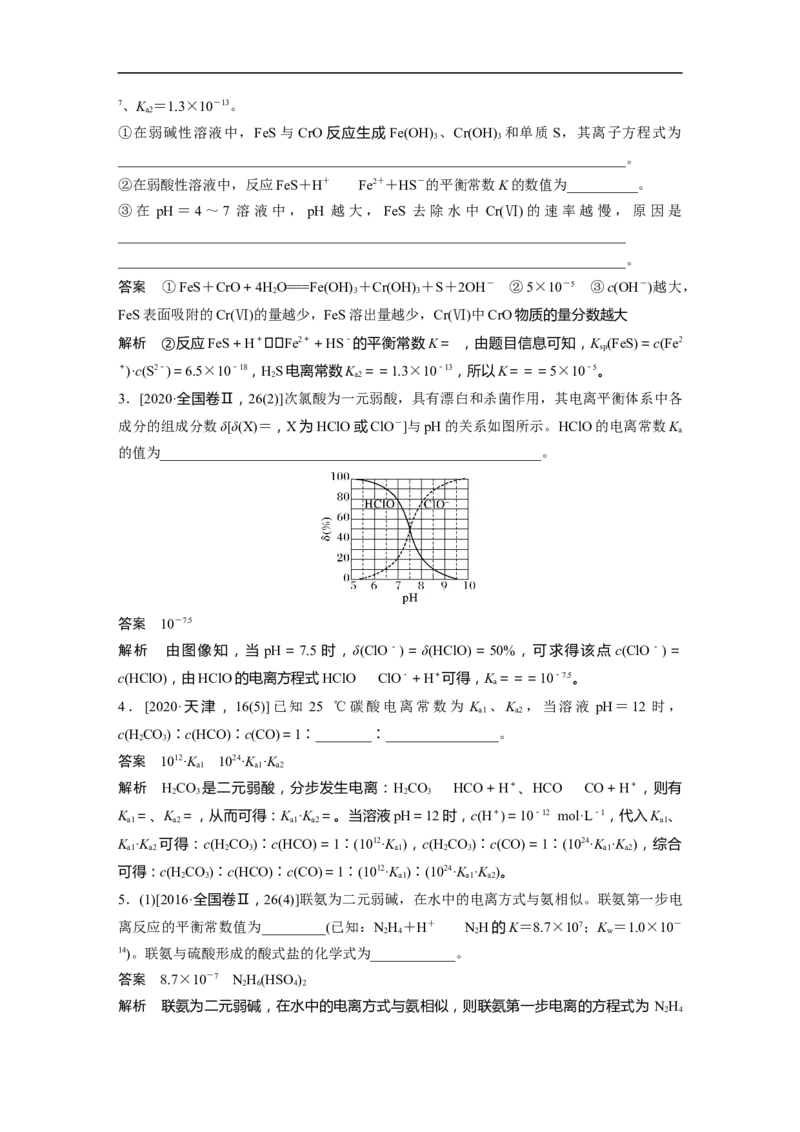
7.常温下,用0.100 0 mol·L-1的NaOH溶液滴定某浓度的二元弱酸(H X)溶液,所得溶液中
2
各种含X的微粒的物质的量分数(δ)与pH的变化曲线如图所示。则:HX的电离常数K =__________,X2-的水解常数K =__________。
2 a1 h
答案 10-1.2 10-9.8
解析 HX的电离常数K =,pH=1.2时,c(H X)=c(HX-),代入计算,可得K =10-1.2;
2 a1 2 a1
X2-的水解常数K =,pH=4.2时,c(X2-)=c(HX-),代入计算,可得K =104.2-14=10-9.8。
h h
8.镍、钴及其化合物在工业上有广泛的应用。工业上用红土镍矿(主要成分为NiO,含
CoO、FeO、Fe O、Al O、MgO、CaO和SiO)制备NiSO ·6H O和钴的工艺流程如图所示。
2 3 2 3 2 4 2
滤渣3的成分为MgF 和CaF 。若滤液1中c(Ca2+)=1.0×10-3 mol·L-1,当滤液2中c(Mg2+)
2 2
=1.5×10-6 mol·L-1时,除钙率为________(忽略沉淀前后溶液体积变化)。[已知:K (CaF )
sp 2
=1.5×10-10、K (MgF )=7.5×10-11]
sp 2
答案 99.7%
解析 当滤液2中c(Mg2+)=1.5×10-6 mol·L-1时,c2(F-)== mol2·L-2=5×10-5 mol2·L-
2,此时溶液中c(Ca2+)== mol·L-1=3×10-6 mol·L-1,除钙率为×100%=99.7%。
9.目前市面上的新能源汽车部分采用的是磷酸铁锂电池,其电极材料以硫铁矿(主要成分为
FeS,含少量Al O、SiO 和Fe O)为原料制备,工业流程如图所示。
2 2 3 2 3 4
已知几种金属离子沉淀的pH如表所示:
金属氢氧化物 Fe(OH) Fe(OH) Al(OH)
3 2 3
开始沉淀的pH 2.3 7.5 4.0
完全沉淀的pH 4.1 9.7 5.2
为了使Al3+完全沉淀,加入FeO调节pH最低为5.2(分析化学认为当溶液中离子浓度小于
1×10-5 mol·L-1时,该离子完全沉淀),计算K [Al(OH) ]=________。
sp 3
答案 10-31.4
解析 为了使Al3+完全沉淀,加入FeO调节pH最低为5.2,则氢氧根离子浓度为c(OH-)=
105.2-14 mol·L-1=10-8.8 mol·L-1,故K [Al(OH) ]=10-5×(10-8.8)3=10-31.4。
sp 3
10.五氧化二钒(V O)广泛用于冶金、化工等行业,用作合金添加剂、生产硫酸或石油精炼
2 5用的催化剂等。从废钒催化剂(含有KSO 、VO 、VO 、SiO 、Fe O 、NiO等)中回收钒,
2 4 2 5 2 4 2 2 3
既能避免污染环境,又能节约宝贵的资源,回收工艺流程如图:
加入HO 的目的是将过量的Fe2+转化为Fe3+。“氧化1”后,溶液中的金属阳离子主要有
2 2
Fe3+、Ni2+、VO2+,调节pH使离子沉淀,若溶液中c(Ni2+)=0.2 mol·L-1,则调节溶液的
pH最小值为__________可使Fe3+沉淀完全(离子浓度≤1.0×10-5 mol·L-1时沉淀完全),此
时________(填“有”或“无”)Ni(OH) 沉淀生成。{假设溶液体积不变,lg 6≈0.8,
2
K [Fe(OH) ]=2.16×10-39,K [Ni(OH) ]=2×10-15}
sp 3 sp 2
答案 2.8 无
解析 当c(Fe3+)=1.0×10-5 mol·L-1时,根据 K 的公式可知,溶液中的 c3(OH-)==
sp
mol3·L-3=2.16×10-34 mol3·L-3,c(OH-)=6×10-12 mol·L-1,计算可得 pH≈2.8,
Q[Ni(OH) ]=c(Ni2+)·c2(OH-)=0.2×(6.0×10-12)2=7.2×10-24,因为 Q[Ni(OH) ]<
2 2
K [Ni(OH) ],所以无Ni(OH) 沉淀生成。
sp 2 2