文档内容
(一)溶液中粒子浓度关系
1.单一溶液
(1)Na S溶液
2
水解方程式:________________________________________________________________;
离子浓度大小关系:__________________________________________________________;
电荷守恒:__________________________________________________________________;
元素质量守恒:______________________________________________________________;
质子守恒:__________________________________________________________________。
答案 S2-+HOHS-+OH-、HS-+HOHS+OH-
2 2 2
c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-)
c(Na+)=2[c(S2-)+c(HS-)+c(H S)]
2
c(OH-)=c(H+)+c(HS-)+2c(H S)
2
(2)NaHS溶液
水解方程式:_______________________________________________________________;
离子浓度大小关系:_________________________________________________________;
电荷守恒:_________________________________________________________________;
元素质量守恒:_____________________________________________________________;
质子守恒:_________________________________________________________________。
答案 HS-+HOHS+OH-
2 2
c(Na+)>c(HS-)>c(OH-)>c(H+)>c(S2-)
c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-)
c(Na+)=c(S2-)+c(HS-)+c(H S)
2
c(OH-)=c(H+)+c(H S)-c(S2-)
2
解析 NaHS既能发生水解又能发生电离,水溶液呈碱性:
HS-+HOHS+OH-(主要);
2 2
HS-H++S2-(次要)。
2.混合溶液
(1)1∶1的CHCOOH、CHCOONa溶液
3 3
水解方程式:_______________________________________________________________;
离子浓度大小关系:_________________________________________________________;电荷守恒:_________________________________________________________________;
元素质量守恒:_____________________________________________________________;
质子守恒:_________________________________________________________________。
答案 CHCOO-+HOCHCOOH+OH-
3 2 3
c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3
c(Na+)+c(H+)=c(CHCOO-)+c(OH-)
3
2c(Na+)=c(CHCOO-)+c(CHCOOH)
3 3
c(CHCOO-)+2c(OH-)=c(CHCOOH)+2c(H+)
3 3
解析 CHCOOHCHCOO-+H+(主要),CHCOO-+HOCHCOOH+OH-(次要),
3 3 3 2 3
水溶液呈酸性。
(2)CH COOH、CHCOONa混合呈中性溶液
3 3
离子浓度大小关系:________________________________________________________;
电荷守恒:________________________________________________________________;
元素质量守恒:____________________________________________________________。
答案 c(CHCOO-)=c(Na+)>c(H+)=c(OH-)
3
c(Na+)+c(H+)=c(CHCOO-)+c(OH-)
3
c(Na+)=c(CHCOO-)
3
解析 CHCOOHCHCOO-+H+
3 3
CHCOO-+HOCHCOOH+OH-
3 2 3
若溶液呈中性,则电离和水解相互抵消。
(3)常温下pH=2的CHCOOH与pH=12的NaOH等体积混合的溶液
3
离子浓度大小关系:________________________________________________________;
电荷守恒:________________________________________________________________。
答案 c(CHCOO-)>c(Na+)>c(H+)>c(OH-) c(Na+)+c(H+)=c(CHCOO-)+c(OH-)
3 3
解析 由于CHCOOH是弱酸,所以当完全反应后,CHCOOH仍过量许多,溶液呈酸性。
3 3
(二)滴定曲线的分析与应用
1.巧抓“四点”,突破溶液中的粒子浓度关系
(1)抓反应“一半”点,判断是什么溶质的等量混合。
(2)抓“恰好”反应点,生成的溶质是什么?判断溶液的酸碱性。
(3)抓溶液的“中性”点,生成什么溶质,哪种物质过量或不足。
(4)抓反应的“过量”点,溶液中的溶质是什么?判断哪种物质过量。
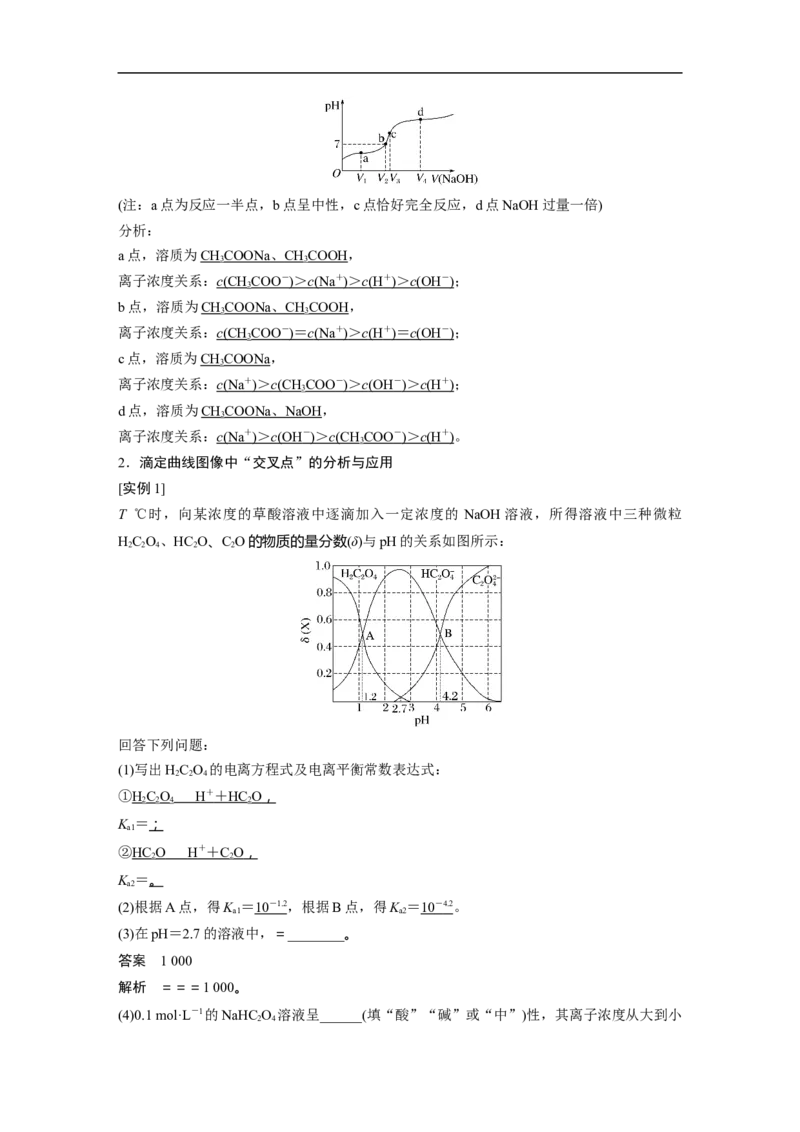
实例分析:向CHCOOH溶液中逐滴加入NaOH溶液,溶液pH与加入NaOH溶液的关系如
3
图所示:(注:a点为反应一半点,b点呈中性,c点恰好完全反应,d点NaOH过量一倍)
分析:
a点,溶质为CH COONa 、 CH COOH,
3 3
离子浓度关系: c (CH COO - ) > c (Na + ) > c (H + ) > c (OH - ) ;
3
b点,溶质为CH COONa 、 CH COOH,
3 3
离子浓度关系: c (CH COO - ) = c (Na + ) > c (H + ) = c (OH - ) ;
3
c点,溶质为CHCOONa,
3
离子浓度关系: c (Na + ) > c (CH COO - ) > c (OH - ) > c (H + ) ;
3
d点,溶质为CH COONa 、 NaOH ,
3
离子浓度关系: c (Na + ) > c (OH - ) > c (CH COO - ) > c (H + ) 。
3
2.滴定曲线图像中“交叉点”的分析与应用
[实例1]
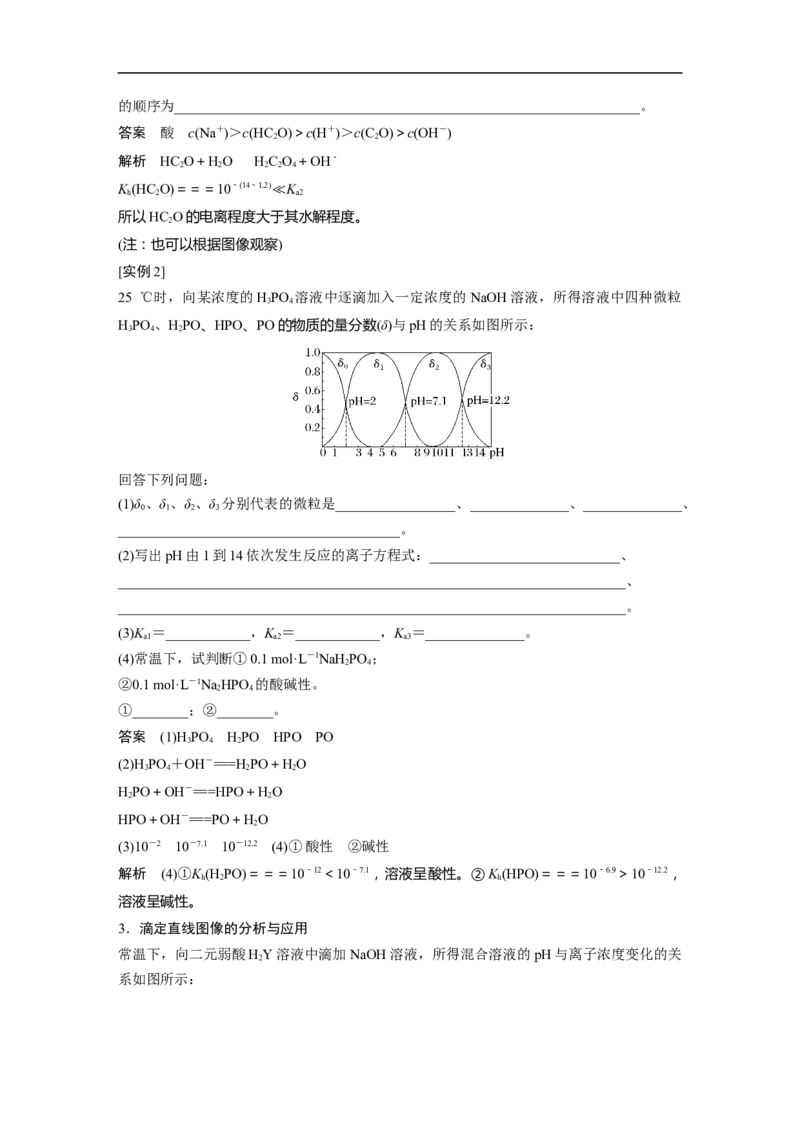
T ℃时,向某浓度的草酸溶液中逐滴加入一定浓度的 NaOH溶液,所得溶液中三种微粒
HC O、HC O、C O的物质的量分数(δ)与pH的关系如图所示:
2 2 4 2 2
回答下列问题:
(1)写出HC O 的电离方程式及电离平衡常数表达式:
2 2 4
①HC O H + + HC O ,
2 2 4 2
K =;
a1
②HC O H + + C O ,
2 2
K =。
a2
(2)根据A点,得K = 10 - 1.2 ,根据B点,得K = 10 - 4.2 。
a1 a2
(3)在pH=2.7的溶液中,=________。
答案 1 000
解析 ===1 000。
(4)0.1 mol·L-1的NaHC O 溶液呈______(填“酸”“碱”或“中”)性,其离子浓度从大到小
2 4的顺序为__________________________________________________________________。
答案 酸 c(Na+)>c(HC O)>c(H+)>c(C O)>c(OH-)
2 2
解析 HC O+HOHC O+OH-
2 2 2 2 4
K (HC O)===10-(14-1.2)≪K
h 2 a2
所以HC O的电离程度大于其水解程度。
2
(注:也可以根据图像观察)
[实例2]
25 ℃时,向某浓度的HPO 溶液中逐滴加入一定浓度的NaOH溶液,所得溶液中四种微粒
3 4
HPO 、HPO、HPO、PO的物质的量分数(δ)与pH的关系如图所示:
3 4 2
回答下列问题:
(1)δ 、δ 、δ 、δ 分别代表的微粒是_________________、______________、______________、
0 1 2 3
________________________________________。
(2)写出pH由1到14依次发生反应的离子方程式:___________________________、
________________________________________________________________________、
________________________________________________________________________。
(3)K =____________,K =____________,K =______________。
a1 a2 a3
(4)常温下,试判断①0.1 mol·L-1NaH PO ;
2 4
②0.1 mol·L-1NaHPO 的酸碱性。
2 4
①________;②________。
答案 (1)H PO HPO HPO PO
3 4 2
(2)H PO +OH-===HPO+HO
3 4 2 2
HPO+OH-===HPO+HO
2 2
HPO+OH-===PO+HO
2
(3)10-2 10-7.1 10-12.2 (4)①酸性 ②碱性
解析 (4)①K (H PO)===10-12<10-7.1,溶液呈酸性。②K (HPO)===10-6.9>10-12.2,
h 2 h
溶液呈碱性。
3.滴定直线图像的分析与应用
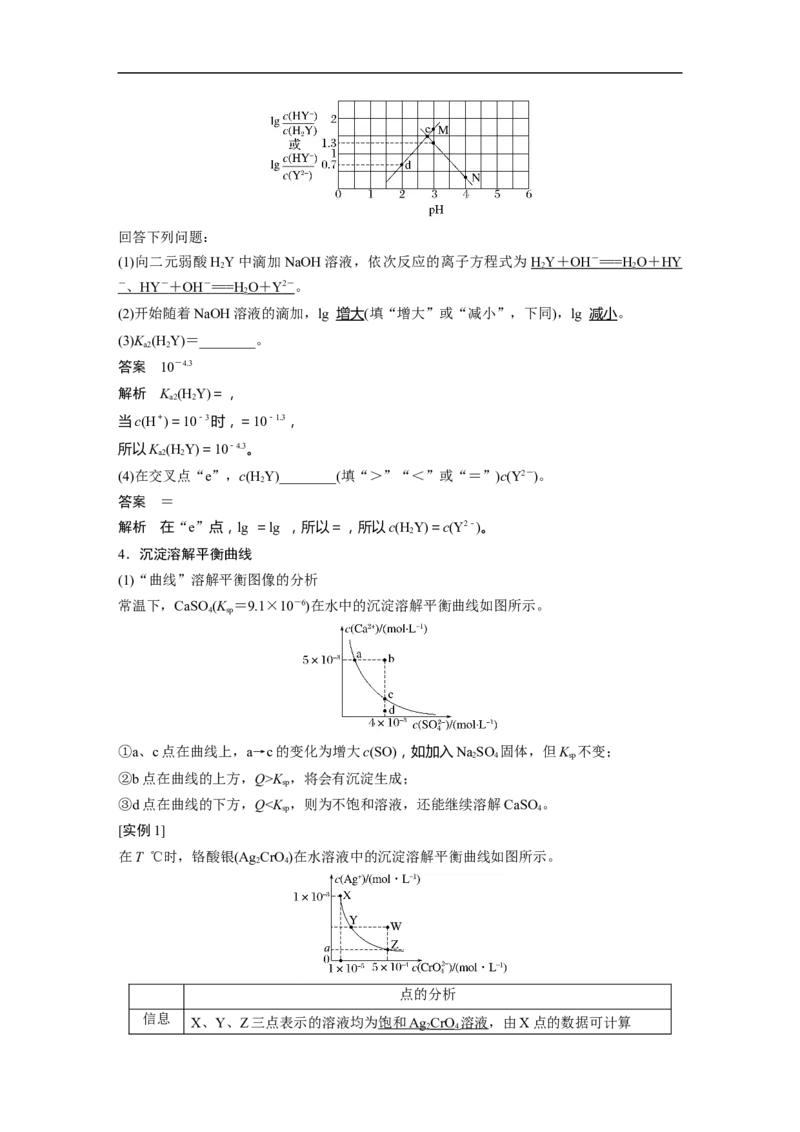
常温下,向二元弱酸HY溶液中滴加NaOH溶液,所得混合溶液的pH与离子浓度变化的关
2
系如图所示:回答下列问题:
(1)向二元弱酸HY中滴加NaOH溶液,依次反应的离子方程式为H Y + OH - == = H O + HY
2 2 2
- 、 HY - + OH - == = H O + Y 2 - 。
2
(2)开始随着NaOH溶液的滴加,lg 增大(填“增大”或“减小”,下同),lg 减小。
(3)K (H Y)=________。
a2 2
答案 10-4.3
解析 K (H Y)=,
a2 2
当c(H+)=10-3时,=10-1.3,
所以K (H Y)=10-4.3。
a2 2
(4)在交叉点“e”,c(H Y)________(填“>”“<”或“=”)c(Y2-)。
2
答案 =
解析 在“e”点,lg =lg ,所以=,所以c(H Y)=c(Y2-)。
2
4.沉淀溶解平衡曲线
(1)“曲线”溶解平衡图像的分析
常温下,CaSO(K =9.1×10-6)在水中的沉淀溶解平衡曲线如图所示。
4 sp
①a、c点在曲线上,a→c的变化为增大c(SO),如加入NaSO 固体,但K 不变;
2 4 sp
②b点在曲线的上方,Q>K ,将会有沉淀生成;
sp
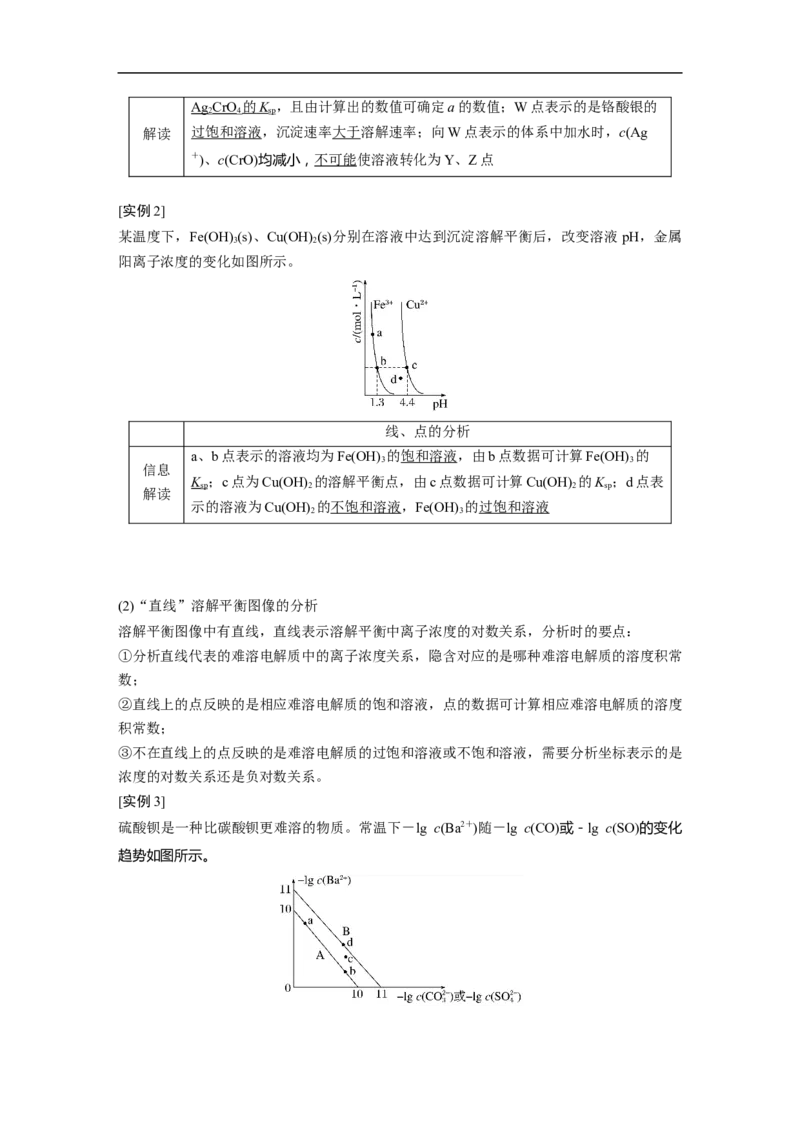
③d点在曲线的下方,QK (BaSO),所以离子浓度的
sp 3 sp 4
负对数的值:BaCO K ,所以
a 3 a1 a a1
[As(OH) T]-的酸性比As(OH) 的强,B正确;由图可知As(OH) 的浓度为左坐标,浓度的数
2 3 3
量级为10-3mol·L-1,[As(OH) T]-的浓度为右坐标,浓度的数量级为10-6mol·L-1,所以pH
2
=3.1时,As(OH) 的浓度比[As(OH) T]-的高,C正确;由已知条件,酒石酸(H T,lgK =
3 2 2 a1
-3.04,lgK =-4.37),As(OH) 的lgK 为-9.1,即酒石酸的第一步电离常数远大于亚砷酸
a2 3 a1
的第一步电离常数,所以酒石酸的酸性远强于 As(OH) ,另外总As的浓度也小于总T的浓
3
度,所以当pH=7.0时,溶液中浓度最高的物种不是As(OH) ,D错误。
32.(2022·辽宁,15)甘氨酸(NH CHCOOH)是人体必需氨基酸之一。在 25 ℃时,
2 2
NHCHCOOH、NHCHCOO-和NH CHCOO-的分布分数[如δ(A2-)=]与溶液pH关系如图。
2 2 2 2
下列说法错误的是( )
A.甘氨酸具有两性
B.曲线c代表NH CHCOO-
2 2
C.NHCHCOO-+HONHCHCOOH+OH-的平衡常数K=10-11.65
2 2 2
D.c2(NHCHCOO-)
2
c(NHCH COOH)·c(NH CH COO-),故D错误。
2 2 2
3.(2022·海南,14 改编)某元素 M 的氢氧化物 M(OH) (s)在水中的溶解反应为:
2
M(OH) (s)
2
M2+(aq)+2OH-(aq)、M(OH) (s)+2OH-(aq)M(OH)(aq),25 ℃,-lgc与pH的关系如图
2
所示,c为M2+或M(OH)浓度的值。下列说法错误的是( )
A.曲线①代表-lg c(M2+)与pH的关系B.M(OH) 的K 约为1×10-17
2 sp
C.向c(M2+)=0.1 mol·L-1的溶液中加入 NaOH溶液至pH=9.0,体系中元素 M主要以
M(OH) (s)存在
2
D.向c[M(OH)]=0.1 mol·L-1的溶液中加入等体积0.4 mol·L-1的HCl后,体系中元素M主
要以M2+存在
答案 D
解析 由题干信息,M(OH) (s)M2+(aq)+2OH-(aq),M(OH) (s)+2OH-(aq)M(OH)
2 2
(aq),随着pH增大,c(OH-)增大,则c(M2+)减小,c[M(OH)]增大,即-lg c(M2+)增大,-
lg c[M(OH)]减小,因此曲线①代表-lg c(M2+)与pH的关系,曲线②代表-lg c[M(OH)]与
pH的关系,据此分析解答。由分析可知,曲线①代表-lg c(M2+)与pH的关系,A正确;
由图像可知,pH=7.0时,-lg c(M2+)=3.0,则M(OH) 的K =c(M2+)·c2(OH-)=1×10-
2 sp
17,B正确;向c(M2+)=0.1 mol·L-1的溶液中加入NaOH溶液至pH=9.0,根据图像可知,
pH=9.0时,c(M2+)、c[M(OH)]均极小,则体系中元素M主要以M(OH) (s)存在,C正确;
2
由曲线②可知,c[M(OH)]=0.1 mol·L-1时pH≈14.5,则c(OH-)=100.5 mol·L-1>3 mol·L-
1,因此加入等体积 0.4 mol·L-1 的 HCl 后,c(OH-)减小,平衡 M(OH)s)+2OH-
(
(aq)[M(OH)](aq)逆向移动,因HCl的量不能使M(OH) 溶解,所以体系中M不可能主要
2
以M2+存在,D错误。
4.(2022·山东,14)工业上以SrSO (s)为原料生产SrCO (s),对其工艺条件进行研究。现有
4 3
含SrCO (s)的0.1 mol·L-1、1.0 mol·L-1 Na CO 溶液,含SrSO (s)的0.1 mol·L-1、1.0 mol·L-
3 2 3 4
1 Na SO 溶液。在一定pH范围内,四种溶液中lg [c(Sr2+)/mol·L-1]随pH的变化关系如图所
2 4
示。下列说法错误的是( )
A.反应SrSO (s)+CO(aq)SrCO (s)+SO(aq)的平衡常数K=
4 3
B.a=-6.5
C.曲线④代表含SrCO (s)的1.0 mol·L-1 Na CO 溶液的变化曲线
3 2 3
D.对含SrSO (s)且NaSO 和NaCO 初始浓度均为1.0 mol·L-1的混合溶液,pH ≥7.7时才
4 2 4 2 3
发生沉淀转化
答案 D
解析 硫酸是强酸,随着溶液pH变化,溶液中硫酸根离子浓度几乎不变,则含硫酸锶固体
的硫酸钠溶液中锶离子的浓度几乎不变,pH相同时,溶液中硫酸根离子浓度越大,锶离子浓度越小,所以曲线①代表含硫酸锶固体的0.1 mol·L-1硫酸钠溶液的变化曲线,曲线②代
表含硫酸锶固体的1.0 mol·L-1硫酸钠溶液的变化曲线;碳酸是弱酸,溶液pH越小,溶液中
碳酸根离子浓度越小,锶离子浓度越大,pH相同时,1.0 mol·L-1碳酸钠溶液中碳酸根离子
浓度大于0.1 mol·L-1碳酸钠溶液,则曲线③表示含碳酸锶固体的0.1 mol·L-1碳酸钠溶液的
变化曲线,曲线④表示含碳酸锶固体的1.0 mol·L-1碳酸钠溶液的变化曲线,故C正确;反
应SrSO (s)+CO(aq)SrCO (s)+SO(aq)的平衡常数K===,故A正确;曲线①代表含硫
4 3
酸锶固体的0.1 mol·L-1硫酸钠溶液的变化曲线,则硫酸锶的溶度积K (SrSO )=10-5.5×0.1
sp 4
=10-6.5,温度不变,溶度积不变,则溶液pH为7.7时,锶离子的浓度为 mol·L-1=10-6.5
mol·L-1,则 a为-6.5,故 B 正确;对含 SrSO (s)且NaSO 和NaCO 初始浓度均为 1.0
4 2 4 2 3
mol·L-1的混合溶液中锶离子浓度为10-6.5 mol·L-1,根据图示,pH≥6.9时锶离子浓度降低
所以pH≥6.9时发生沉淀转化,故D错误。
5.(2022·湖南,10)室温时,用0.100 mol·L-1的标准AgNO 溶液滴定15.00 mL浓度相等的
3
Cl-、Br-和I-混合溶液,通过电位滴定法获得lg c(Ag+)与V(AgNO)的关系曲线如图所示
3
(忽略沉淀对离子的吸附作用。若溶液中离子浓度小于1.0×10-5 mol·L-1时,认为该离子沉
淀完全。K (AgCl)=1.8×10-10,K (AgBr)=5.4×10-13,K (AgI)=8.5×10-17)。下列说法正
sp sp sp
确的是( )
A.a点:有白色沉淀生成
B.原溶液中I-的浓度为0.100 mol·L-1
C.当Br-沉淀完全时,已经有部分Cl-沉淀
D.b点:c(Cl-)>c(Br-)>c(I-)>c(Ag+)
答案 C
解析 向含浓度相等的Cl-、Br-和I-混合溶液中滴加硝酸银溶液,根据三种沉淀的溶度积
常数,三种离子沉淀的先后顺序为I-、Br-、Cl-,根据滴定图示,当滴入4.50 mL硝酸银溶
液时,Cl-恰好沉淀完全,此时共消耗硝酸银的物质的量为 4.50×10-3 L×0.100 mol·L-1=
4.5×10-4 mol,所以Cl-、Br-和I-均为1.5×10-4 mol。I-先沉淀,AgI是黄色的,所以a
点有黄色沉淀AgI生成,故A错误;原溶液中I-的物质的量为1.5×10-4 mol,则I-的浓度
为=0.010 0 mol·L-1,故B错误;当Br-沉淀完全时(Br-浓度为1.0×10-5 mol·L-1),溶液中
的c(Ag+)== mol·L-1=5.4×10-8 mol·L-1,若Cl-已经开始沉淀,则此时溶液中的c(Cl-)
== mol·L-1≈3.3×10-3 mol·L-1,原溶液中的c(Cl-)=c(I-)=0.010 0 mol·L-1,则已经有
部分Cl-沉淀,故C正确;b点加入了过量的硝酸银溶液,Ag+浓度最大,则b点各离子浓度为c(Ag+)>c(Cl-)>c(Br-)>c(I-),故D错误。
6.(2021·山东,15改编)赖氨酸[H N+(CH)CH(NH)COO-,用HR表示]是人体必需氨基酸,
3 2 4 2
其盐酸盐(H RCl )在水溶液中存在如下平衡:HR2+HR+HRR-。向一定
3 2 3 2
浓度的HRCl 溶液中滴加NaOH溶液,溶液中HR2+、HR+、HR和R-的分布系数δ(X)随
3 2 3 2
pH变化如图所示。已知δ(X)=,下列表述正确的是( )
A.>
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2
C.O点,pH=
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
答案 D
解析 M点c(H R2+)=c(H R+),由此可知K ≈10-2.2,同理K ≈10-9.1,K ≈10-10.8,==10
3 2 1 2 3
-6.9,==10-1.7,因此<,故A错误;M点存在电荷守恒:c(R-)+c(OH-)+c(Cl-)=2c(H R2
3
+)+c(H R+)+c(H+)+c(Na+),此时c(H R2+)=c(H R+),因此c(R-)+c(OH-)+c(Cl-)=
2 3 2
3c(H R+)+c(H+)+c(Na+),故B错误;O点c(H R+)=c(R-),因此=1,即==1,因此c(H
2 2
+)=,溶液pH=-lg c(H+)=,故C错误;P点溶质为NaCl、HR、NaR,此时溶液呈碱性,
因此 c(OH-)>c(H+),溶质浓度大于水解和电离所产生的微粒浓度,因此 c(Na+)>c(Cl
-)>c(OH-)>c(H+),故D正确。
考向一 滴定曲线的分析应用
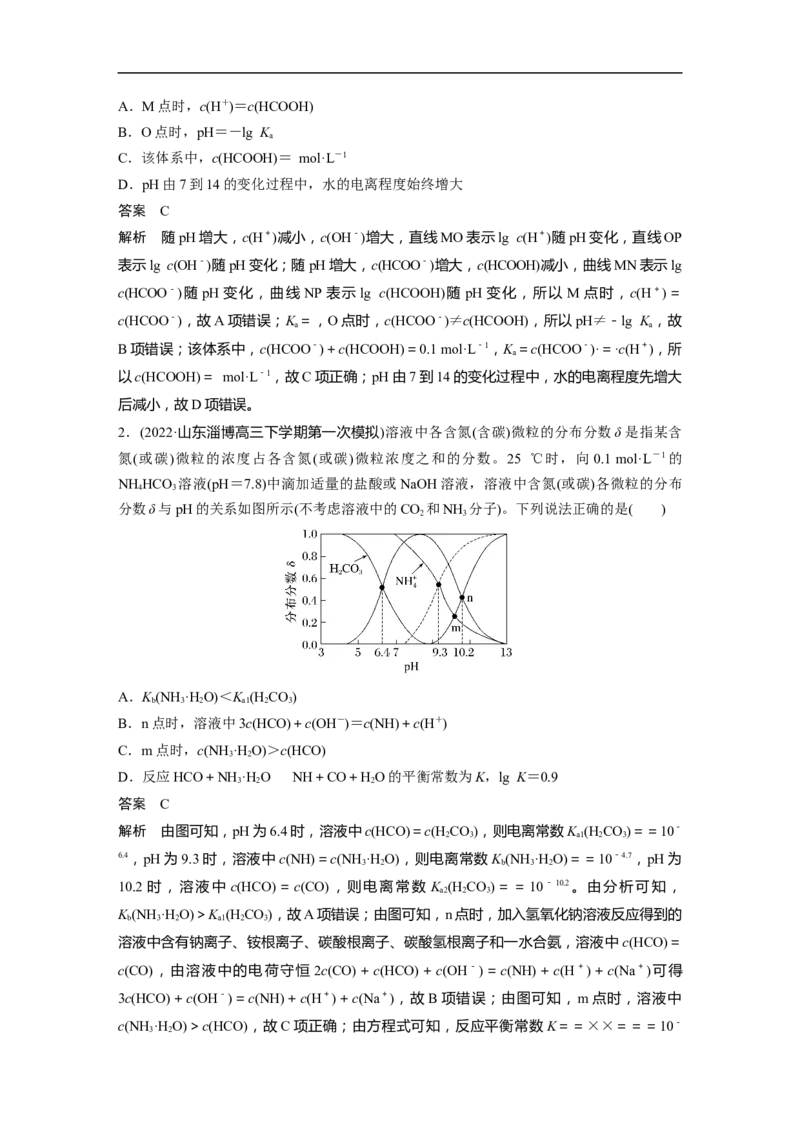
1.(2022·唐山高三下学期第一次模拟)25 ℃时,某混合溶液中c(HCOO-)+c(HCOOH)=0.1
mol·
L-1,lg c(HCOOH)、lg c(HCOO-)、lg c(H+)和lg c(OH-)随pH变化的关系如图所示。K
a
为HCOOH的电离常数,下列说法正确的是( )A.M点时,c(H+)=c(HCOOH)
B.O点时,pH=-lg K
a
C.该体系中,c(HCOOH)= mol·L-1
D.pH由7到14的变化过程中,水的电离程度始终增大
答案 C
解析 随pH增大,c(H+)减小,c(OH-)增大,直线MO表示lg c(H+)随pH变化,直线OP
表示lg c(OH-)随pH变化;随pH增大,c(HCOO-)增大,c(HCOOH)减小,曲线MN表示lg
c(HCOO-)随 pH 变化,曲线 NP 表示 lg c(HCOOH)随 pH 变化,所以 M 点时,c(H+)=
c(HCOO-),故A项错误;K=,O点时,c(HCOO-)≠c(HCOOH),所以pH≠-lg K,故
a a
B项错误;该体系中,c(HCOO-)+c(HCOOH)=0.1 mol·L-1,K=c(HCOO-)·=·c(H+),所
a
以c(HCOOH)= mol·L-1,故C项正确;pH由7到14的变化过程中,水的电离程度先增大
后减小,故D项错误。
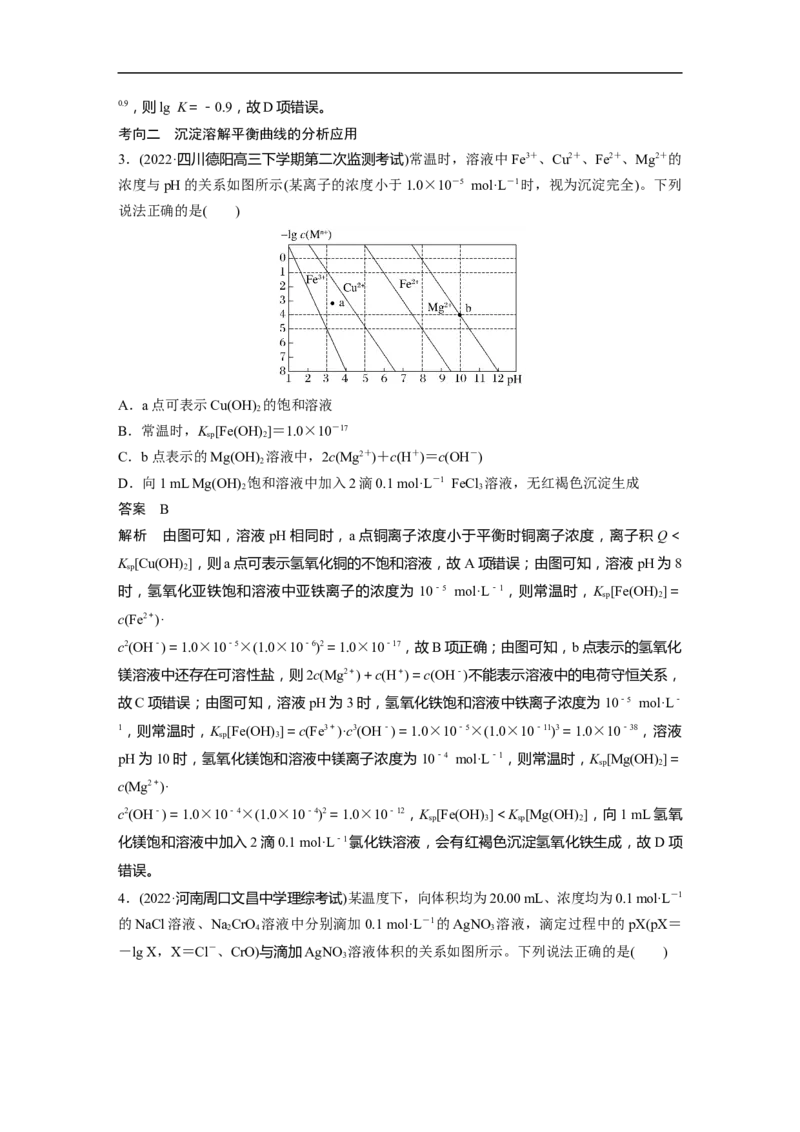
2.(2022·山东淄博高三下学期第一次模拟)溶液中各含氮(含碳)微粒的分布分数δ是指某含
氮(或碳)微粒的浓度占各含氮(或碳)微粒浓度之和的分数。25 ℃时,向0.1 mol·L-1的
NH HCO 溶液(pH=7.8)中滴加适量的盐酸或NaOH溶液,溶液中含氮(或碳)各微粒的分布
4 3
分数δ与pH的关系如图所示(不考虑溶液中的CO 和NH 分子)。下列说法正确的是( )
2 3
A.K (NH ·H O)<K (H CO)
b 3 2 a1 2 3
B.n点时,溶液中3c(HCO)+c(OH-)=c(NH)+c(H+)
C.m点时,c(NH ·H O)>c(HCO)
3 2
D.反应HCO+NH ·H ONH+CO+HO的平衡常数为K,lg K=0.9
3 2 2
答案 C
解析 由图可知,pH为6.4时,溶液中c(HCO)=c(H CO),则电离常数K (H CO)==10-
2 3 a1 2 3
6.4,pH为9.3时,溶液中c(NH)=c(NH ·H O),则电离常数K (NH ·H O)==10-4.7,pH为
3 2 b 3 2
10.2 时,溶液中 c(HCO)=c(CO),则电离常数 K (H CO)==10-10.2。由分析可知,
a2 2 3
K (NH ·H O)>K (H CO),故A项错误;由图可知,n点时,加入氢氧化钠溶液反应得到的
b 3 2 a1 2 3
溶液中含有钠离子、铵根离子、碳酸根离子、碳酸氢根离子和一水合氨,溶液中 c(HCO)=
c(CO),由溶液中的电荷守恒 2c(CO)+c(HCO)+c(OH-)=c(NH)+c(H+)+c(Na+)可得
3c(HCO)+c(OH-)=c(NH)+c(H+)+c(Na+),故B项错误;由图可知,m点时,溶液中
c(NH ·H O)>c(HCO),故C项正确;由方程式可知,反应平衡常数K==××===10-
3 20.9,则lg K=-0.9,故D项错误。
考向二 沉淀溶解平衡曲线的分析应用
3.(2022·四川德阳高三下学期第二次监测考试)常温时,溶液中Fe3+、Cu2+、Fe2+、Mg2+的
浓度与pH的关系如图所示(某离子的浓度小于1.0×10-5 mol·L-1时,视为沉淀完全)。下列
说法正确的是( )
A.a点可表示Cu(OH) 的饱和溶液
2
B.常温时,K [Fe(OH) ]=1.0×10-17
sp 2
C.b点表示的Mg(OH) 溶液中,2c(Mg2+)+c(H+)=c(OH-)
2
D.向1 mL Mg(OH) 饱和溶液中加入2滴0.1 mol·L-1 FeCl 溶液,无红褐色沉淀生成
2 3
答案 B
解析 由图可知,溶液pH相同时,a点铜离子浓度小于平衡时铜离子浓度,离子积Q<
K [Cu(OH)],则a点可表示氢氧化铜的不饱和溶液,故 A项错误;由图可知,溶液pH为8
sp 2
时,氢氧化亚铁饱和溶液中亚铁离子的浓度为 10-5 mol·L-1,则常温时,K [Fe(OH) ]=
sp 2
c(Fe2+)·
c2(OH-)=1.0×10-5×(1.0×10-6)2=1.0×10-17,故B项正确;由图可知,b点表示的氢氧化
镁溶液中还存在可溶性盐,则2c(Mg2+)+c(H+)=c(OH-)不能表示溶液中的电荷守恒关系,
故C项错误;由图可知,溶液pH为3时,氢氧化铁饱和溶液中铁离子浓度为10-5 mol·L-
1,则常温时,K [Fe(OH) ]=c(Fe3+)·c3(OH-)=1.0×10-5×(1.0×10-11)3=1.0×10-38,溶液
sp 3
pH为10时,氢氧化镁饱和溶液中镁离子浓度为10-4 mol·L-1,则常温时,K [Mg(OH) ]=
sp 2
c(Mg2+)·
c2(OH-)=1.0×10-4×(1.0×10-4)2=1.0×10-12,K [Fe(OH) ]<K [Mg(OH) ],向1 mL氢氧
sp 3 sp 2
化镁饱和溶液中加入2滴0.1 mol·L-1氯化铁溶液,会有红褐色沉淀氢氧化铁生成,故D项
错误。
4.(2022·河南周口文昌中学理综考试)某温度下,向体积均为20.00 mL、浓度均为0.1 mol·L-1
的NaCl溶液、NaCrO 溶液中分别滴加0.1 mol·L-1的AgNO 溶液,滴定过程中的pX(pX=
2 4 3
-lg X,X=Cl-、CrO)与滴加AgNO 溶液体积的关系如图所示。下列说法正确的是( )
3A.曲线 Ⅱ 表示AgNO 溶液滴定NaCl溶液的过程
3
B.K (Ag CrO)=10-2b
sp 2 4
C.其他条件不变,如果NaCl溶液的浓度改为0.05 mol·L-1,则滴定终点向上移动
D.若a=5,b=4,则用AgNO 标准液滴定NaCl时可用KCrO 溶液做指示剂
3 2 4
答案 D
解析 由图可知,pX=a或b时反应完全,并且二者的起始浓度、体积均相同,即二者溶质
的 起 始 物 质 的 量 相 同 , 反 应 为 NaCl + AgNO===AgCl↓ + NaNO 、 NaCrO +
3 3 2 4
2AgNO===Ag CrO↓+2NaNO ,完全反应时NaCrO 消耗AgNO 溶液的体积是NaCl的2
3 2 4 3 2 4 3
倍,所以曲线 Ⅰ 表示滴定NaCl溶液、曲线 Ⅱ 表示滴定NaCrO 溶液,A选项错误;曲
2 4
线Ⅱ表示滴定 NaCrO 溶液,达到滴定终点时 pX=b,即 c(CrO)=10-b mol·L-1,
2 4
Ag CrO(s)2Ag+(aq)+CrO(aq),则c(Ag+)=2c(CrO)=2.0×10-b mol·L-1,K (Ag CrO)
2 4 sp 2 4
=c2(Ag+)·c(CrO)=(2.0×10-b)2×10-b=4.0×10-3b,B选项错误;温度不变,氯化银的溶度
积不变,若将NaCl溶液的浓度改为0.05 mol·L-1,需要的硝酸银溶液的体积变成原来的一
半,因此滴定终点会向左平移,C 选项错误;由数据可得出,K (AgCl)=10-10,
sp
K (Ag CrO)=4×10-12,当溶液中同时存在Cl-和CrO时,Cl-沉淀需要的Ag+少,先沉淀,
sp 2 4
用AgNO 标准溶液滴定NaCl时,可用KCrO 溶液做指示剂,滴定至终点时,会生成砖红
3 2 4
色的Ag CrO,D选项正确。
2 4