文档内容
[复习目标] 1.掌握配制一定物质的量浓度溶液的方法。2.掌握中和滴定的实验操作、误差
分析及有关计算。3.掌握氧化还原反应、沉淀反应在滴定法中的应用。
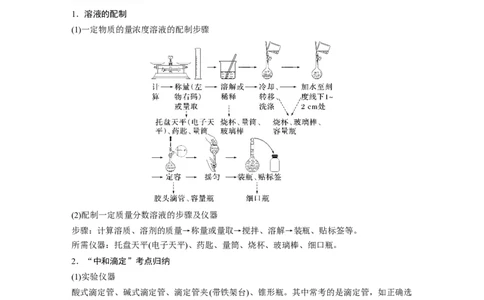
1.溶液的配制
(1)一定物质的量浓度溶液的配制步骤
(2)配制一定质量分数溶液的步骤及仪器
步骤:计算溶质、溶剂的质量→称量或量取→搅拌、溶解→装瓶、贴标签等。
所需仪器:托盘天平(电子天平)、药匙、量筒、烧杯、玻璃棒、细口瓶。
2.“中和滴定”考点归纳
(1)实验仪器
酸式滴定管、碱式滴定管、滴定管夹(带铁架台)、锥形瓶。其中常考的是滴定管,如正确选
择滴定管(包括量程),滴定管的检漏、洗涤和润洗,滴定管的正确读数方法等。
(2)操作步骤
①滴定前的准备:查漏、洗涤、润洗、充液(赶气泡)、调液面、读数;②滴定:移液、滴加
指示剂、滴定至终点、读数;③计算。
(3)指示剂的选择
类型 滴定过程 指示剂 终点颜色变化溶液由黄色变
强酸滴定强碱(或弱碱) 甲基橙
酸碱中 为橙色
和反应 溶液由无色变
强碱滴定强酸(或弱酸) 酚酞
为浅红色
NaSO 溶液滴定未知 淀粉 溶液由蓝色变
2 2 3
氧化还 浓度的碘水 溶液 为无色
原反应 酸性KMnO 溶液滴定 溶液由无色变
4
不需要指示剂
HO(或HC O)溶液 为浅红色
2 2 2 2 4
出现淡红色沉
沉淀 AgNO 溶液滴定含Cl-
3
KCrO 溶液 淀(Ag CrO 为
2 4 2 4
反应 的溶液
砖红色沉淀)
(4)误差分析
写出计算式,分析操作对V 的影响,由计算式得出对最终测定结果的影响,切忌死记硬背
标
结论。此外对读数视线问题要学会画图分析。
(5)数据处理
正确“取舍”数据,计算“平均”体积,根据反应式确定标准液与待测液浓度和体积的关系,
从而列出公式进行计算。
3.滴定终点规范描述
(1)用a mol·L-1的盐酸滴定未知浓度的NaOH溶液,用酚酞作指示剂,达到滴定终点的现象
是________________________________________________________________________
________________________________________________________________________;
若用甲基橙作指示剂,达到滴定终点的现象是
________________________________________________________________________
________________________________________________________________________。
答案 当滴入最后半滴盐酸,溶液由红色变为无色,且半分钟内不恢复红色 当滴入最后半
滴盐酸,溶液由黄色变为橙色,且半分钟内不恢复黄色
(2)用标准碘溶液滴定溶有SO 的水溶液,以测定水中SO 的含量,应选用____________作指
2 2
示剂,达到滴定终点的现象是__________________________________________________。
答案 淀粉溶液 当滴入最后半滴标准碘溶液,溶液由无色变为蓝色,且半分钟内不褪色
(3)用标准酸性KMnO 溶液滴定溶有SO 的水溶液,以测定水中SO 的含量,________(填
4 2 2
“是”或“否”)需要选用指示剂,达到滴定终点的现象是________________________
________________________________________________________________________。
答案 否 当滴入最后半滴标准酸性KMnO 溶液,溶液由无色变为浅红色,且半分钟内不
4
褪色
(4)用氧化还原滴定法测定TiO 的质量分数:一定条件下,将TiO 溶解并还原为Ti3+,再用
2 2
KSCN溶液作指示剂,用NH Fe(SO ) 标准溶液滴定Ti3+至全部生成Ti4+,滴定Ti3+时发生
4 4 2反应的离子方程式为________________________________________________________
________________________________________________________________________,
达到滴定终点的现象是______________________________________________________
________________________________________________________________________。
答案 Ti3++Fe3+===Ti4++Fe2+ 当滴入最后半滴NH Fe(SO ) 标准溶液,溶液变成浅红色,
4 4 2
且半分钟内不褪色
(5)用标准KI溶液滴定含有Fe3+的溶液,应选用________作指示剂,达到滴定终点的现象是
________________________________________________________________________。
答案 KSCN溶液 当滴入最后半滴标准KI溶液,溶液红色褪去,且半分钟内不恢复红色
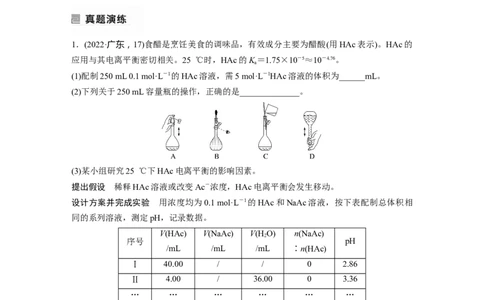
1.(2022·广东,17)食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。HAc的
应用与其电离平衡密切相关。25 ℃时,HAc的K=1.75×10-5≈10-4.76。
a
(1)配制250 mL 0.1 mol·L-1的HAc溶液,需5 mol·L-1HAc溶液的体积为______mL。
(2)下列关于250 mL容量瓶的操作,正确的是______________。
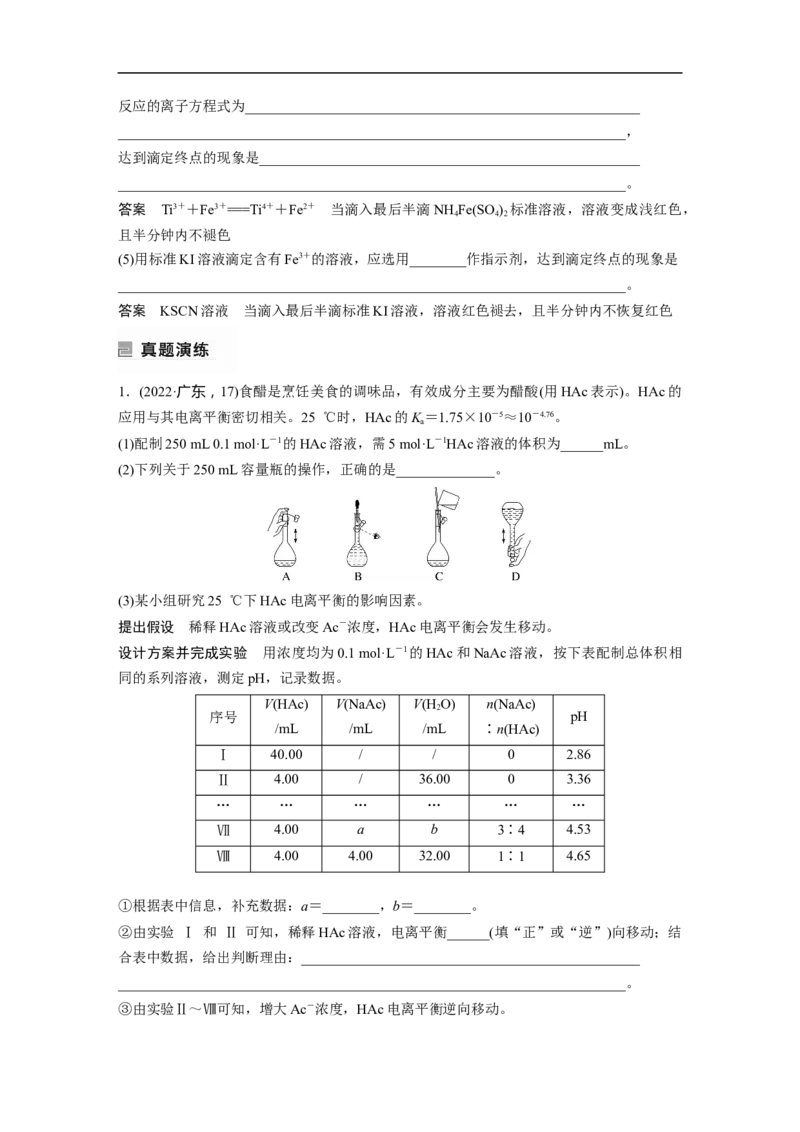
(3)某小组研究25 ℃下HAc电离平衡的影响因素。
提出假设 稀释HAc溶液或改变Ac-浓度,HAc电离平衡会发生移动。
设计方案并完成实验 用浓度均为0.1 mol·L-1的HAc和NaAc溶液,按下表配制总体积相
同的系列溶液,测定pH,记录数据。
V(HAc) V(NaAc) V(H O) n(NaAc)
2
序号 pH
/mL /mL /mL ∶n(HAc)
Ⅰ 40.00 / / 0 2.86
Ⅱ 4.00 / 36.00 0 3.36
… … … … … …
Ⅶ 4.00 a b 3∶4 4.53
Ⅷ 4.00 4.00 32.00 1∶1 4.65
①根据表中信息,补充数据:a=________,b=________。
②由实验 Ⅰ 和 Ⅱ 可知,稀释HAc溶液,电离平衡______(填“正”或“逆”)向移动;结
合表中数据,给出判断理由:________________________________________________
________________________________________________________________________。
③由实验Ⅱ~Ⅷ可知,增大Ac-浓度,HAc电离平衡逆向移动。实验结论 假设成立。
(4)小组分析上表数据发现:随着的增加,c(H+)的值逐渐接近HAc的K。
a
查阅资料获悉:一定条件下,按=1配制的溶液中,c(H+)的值等于HAc的K。
a
对比数据发现,实验Ⅷ中pH=4.65与资料数据K=10-4.76存在一定差异;推测可能由物质
a
浓度准确程度不够引起,故先准确测定HAc溶液的浓度再验证。
①移取20.00 mL HAc溶液,加入2滴酚酞溶液,用0.100 0 mol·L-1NaOH溶液滴定至终点,
消耗体积为22.08 mL,则该HAc溶液的浓度为__________ mol·L-1。画出上述过程的滴定曲
线示意图并标注滴定终点。
②用上述HAc溶液和0.100 0 mol·L-1NaOH溶液,配制等物质的量的HAc与NaAc混合溶液,
测定pH,结果与资料数据相符。
(5)小组进一步提出:如果只有浓度均约为0.1 mol·L-1的HAc和NaOH溶液,如何准确测定
HAc的K?小组同学设计方案并进行实验。请完成下表中Ⅱ的内容。
a
Ⅰ 移取20.00 mL HAc溶液,用NaOH溶液滴定至终点,消耗NaOH溶液V mL
1
Ⅱ __________,测得溶液的pH为4.76
实验总结 得到的结果与资料数据相符,方案可行。
(6)根据K 可以判断弱酸的酸性强弱。写出一种无机弱酸及其用途:______________。
a
答案 (1)5.0 (2)C (3)①3.00 33.00
②正 实验Ⅱ相较于实验Ⅰ,醋酸溶液稀释了10倍,而实验Ⅱ的pH增大值小于1
(4)①0.110 4
(5)向滴定后的混合液中加入20 mL HAc溶液 (6)HClO:漂白剂和消毒液(或HSO :还原剂、
2 3
防腐剂或HPO :食品添加剂、制药、生产肥料)
3 4
解析 (1)溶液稀释过程中,溶质的物质的量不变,因此 250×10-3 L×0.1 mol·L-1=V×5
mol·
L-1,解得V=5×10-3 L=5.0 mL。(2)振荡时应用瓶塞塞住容量瓶口,不可用手指压住容量
瓶口,故A错误;定容时,视线、溶液凹液面和刻度线应“三线相切”,不能仰视或俯视,
且胶头滴管不能插入到容量瓶中,故B错误;向容量瓶中转移液体,需用玻璃棒引流,玻
璃棒下端位于刻度线以下,同时玻璃棒不能接触容量瓶瓶口,故C正确;定容完成后,盖
上瓶塞,左手食指抵住瓶塞,右手扶住容量瓶底部,将容量瓶反复上下颠倒,摇匀,故D
错误。(3)①实验Ⅶ的溶液中n(NaAc)∶n(HAc)=3∶4,V(HAc)=4.00 mL,因此V(NaAc)=
3.00 mL,即a=3.00,由实验Ⅰ可知,溶液总体积为40.00 mL,因此V(H O)=40.00 mL-
24.00 mL-3.00 mL=33.00 mL,即b=33.00。②实验Ⅰ所得溶液的pH=2.86,实验Ⅱ的溶液
中c(HAc)为实验Ⅰ的,稀释过程中,若不考虑电离平衡移动,则实验Ⅱ所得溶液的pH=
2.86+1=3.86,但实际溶液的pH=3.36<3.86,说明稀释过程中,溶液中n(H+)增大,即电
离平衡正向移动。(4)①滴定过程中发生反应:HAc+NaOH===NaAc+HO,由反应方程式
2
可知,滴定至终点时,n(HAc)=n(NaOH),因此 22.08 mL×0.100 0 mol·L-1=20.00
mL×c(HAc),解得c(HAc)=0.110 4 mol·
L-1。滴定过程中,当V(NaOH)=0时,c(H+)=≈ mol·L-1=10-2.88 mol·
L-1,溶液的pH=2.88,当V(NaOH)=11.04 mL时,n(NaAc)=n(HAc),溶液的pH=4.76,
当V(NaOH)=22.08 mL时,达到滴定终点,溶液中溶质为NaAc,Ac-发生水解,溶液呈弱
碱性,当NaOH溶液过量较多时,c(NaOH)无限接近0.1 mol·L-1,溶液pH接近13,因此滴
定曲线如图:
。
(5)向20.00 mLHAc溶液中加入V mL NaOH溶液达到滴定终点,滴定终点的溶液中溶质为
1
NaAc,当=1时,溶液中c(H+)的值等于HAc的K,因此可再向溶液中加入20.00 mL HAc
a
溶液,使溶液中n(NaAc)=n(HAc)。(6)不同的无机弱酸在生活中应用广泛,如HClO具有强
氧化性,在生活中可用于漂白和消毒;HSO 具有还原性,可用作还原剂,在葡萄酒中添加
2 3
适量HSO 可用作防腐剂;HPO 是中强酸,可用作食品添加剂,同时在制药、生产肥料等
2 3 3 4
行业有广泛用途。
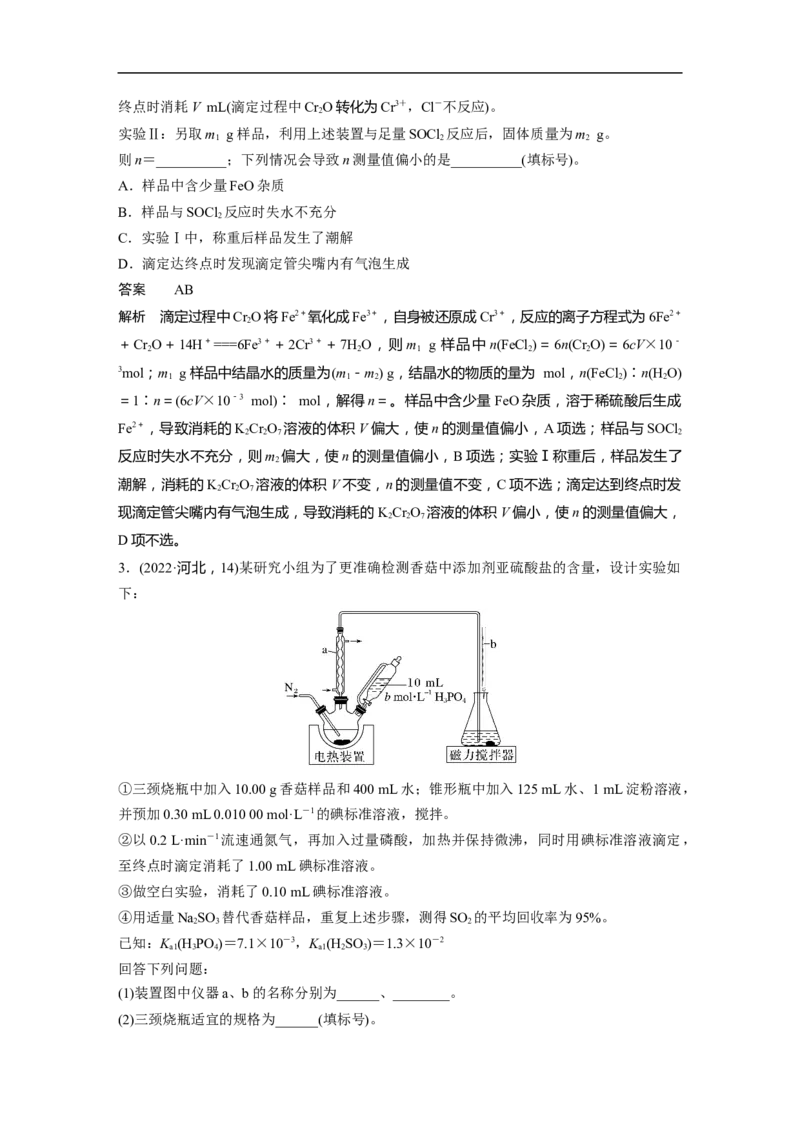
2.[2022·山东,18(2)]实验室利用FeCl ·4H O和亚硫酰氯(SOCl )制备无水FeCl 的装置如图
2 2 2 2
所示(加热及夹持装置略)。已知SOCl 沸点为76 ℃,遇水极易反应生成两种酸性气体。回
2
答下列问题:
现有含少量杂质的FeCl ·nHO,为测定n值进行如下实验:
2 2
实验Ⅰ:称取m g样品,用足量稀硫酸溶解后,用c mol·L-1KCr O 标准溶液滴定Fe2+达
1 2 2 7终点时消耗V mL(滴定过程中Cr O转化为Cr3+,Cl-不反应)。
2
实验Ⅱ:另取m g样品,利用上述装置与足量SOCl 反应后,固体质量为m g。
1 2 2
则n=__________;下列情况会导致n测量值偏小的是__________(填标号)。
A.样品中含少量FeO杂质
B.样品与SOCl 反应时失水不充分
2
C.实验Ⅰ中,称重后样品发生了潮解
D.滴定达终点时发现滴定管尖嘴内有气泡生成
答案 AB
解析 滴定过程中CrO将Fe2+氧化成Fe3+,自身被还原成Cr3+,反应的离子方程式为6Fe2+
2
+CrO+14H+===6Fe3++2Cr3++7HO,则 m g 样品中 n(FeCl)=6n(CrO)=6cV×10-
2 2 1 2 2
3mol;m g样品中结晶水的质量为(m -m) g,结晶水的物质的量为 mol,n(FeCl )∶n(H O)
1 1 2 2 2
=1∶n=(6cV×10-3 mol)∶ mol,解得n=。样品中含少量FeO杂质,溶于稀硫酸后生成
Fe2+,导致消耗的KCr O 溶液的体积V偏大,使n的测量值偏小,A项选;样品与SOCl
2 2 7 2
反应时失水不充分,则m 偏大,使n的测量值偏小,B项选;实验Ⅰ称重后,样品发生了
2
潮解,消耗的KCr O 溶液的体积V不变,n的测量值不变,C项不选;滴定达到终点时发
2 2 7
现滴定管尖嘴内有气泡生成,导致消耗的KCr O 溶液的体积V偏小,使n的测量值偏大,
2 2 7
D项不选。
3.(2022·河北,14)某研究小组为了更准确检测香菇中添加剂亚硫酸盐的含量,设计实验如
下:
①三颈烧瓶中加入10.00 g香菇样品和400 mL水;锥形瓶中加入125 mL水、1 mL淀粉溶液,
并预加0.30 mL 0.010 00 mol·L-1的碘标准溶液,搅拌。
②以0.2 L·min-1流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,
至终点时滴定消耗了1.00 mL碘标准溶液。
③做空白实验,消耗了0.10 mL碘标准溶液。
④用适量NaSO 替代香菇样品,重复上述步骤,测得SO 的平均回收率为95%。
2 3 2
已知:K (H PO )=7.1×10-3,K (H SO )=1.3×10-2
a1 3 4 a1 2 3
回答下列问题:
(1)装置图中仪器a、b的名称分别为______、________。
(2)三颈烧瓶适宜的规格为______(填标号)。A.250 mL B.500 mL C.1 000 mL
(3)解释加入HPO ,能够生成SO 的原因:
3 4 2
________________________________________________________________________
________________________________________________________________________。
(4)滴定管在使用前需要__________、洗涤、润洗;滴定终点时溶液的颜色为____________;
滴定反应的离子方程式为____________________________________________________
________________________________________________________________________。
(5)若先加磷酸再通氮气,会使测定结果__________(填“偏高”“偏低”或“无影响”)。
(6)该样品中亚硫酸盐含量为____________ mg·kg-1(以SO 计,结果保留三位有效数字)。
2
答案 (1)球形冷凝管 酸式滴定管 (2)C
(3)加入HPO 后,溶液中存在化学平衡HSO SO +HO,SO 的溶解度随着温度升高而
3 4 2 3 2 2 2
减小,SO 逸出后,促进了化学平衡HSO SO +HO向右移动 (4)检漏 蓝色 I +SO
2 2 3 2 2 2 2
+2HO===2I-+4H++SO
2
(5)偏低 (6)80.8
解析 由题中信息可知,检测香菇中添加剂亚硫酸盐的含量的原理是用过量的磷酸与其中的
亚硫酸盐反应生成SO ,用氮气将SO 排入到锥形瓶中被水吸收,最后用碘标准溶液滴定,
2 2
测出样品中亚硫酸盐含量。(2)三颈烧瓶中加入10.00 g香菇样品和400 mL水,向其中加入
HPO 的体积不超过10 mL。在加热时,三颈烧瓶中的液体不能超过其容积的,因此,三颈
3 4
烧瓶适宜的规格为1 000 mL,选C。(3)虽然K (H PO )=7.1×10-3<K (H SO )=1.3×10-
a1 3 4 a1 2 3
2,但是HPO 为难挥发性的酸,而HSO 易分解为SO 和水,SO 的溶解度随着温度升高而
3 4 2 3 2 2
减小,SO 逸出后,促进了化学平衡HSO SO +HO向右移动。(4)滴定管在使用前需要
2 2 3 2 2
检漏、洗涤、润洗;滴定前,溶液中的碘被SO 还原为碘离子,溶液的颜色为无色,滴定终
2
点时,过量的半滴碘标准溶液使淀粉溶液变为蓝色且半分钟之内不变色,因此,滴定终点时
溶液为蓝色;滴定反应的离子方程式为I+SO +2HO===2I-+4H++SO。(5)若先加磷酸再
2 2 2
通氮气,则不能将装置中的空气及时排出,有部分亚硫酸盐和 SO 被装置中的氧气氧化,碘
2
标准溶液的消耗量将减少,因此会使测定结果偏低。(6)实验中SO 消耗的碘标准溶液的体
2
积为0.30 mL+1.00 mL=1.30 mL,减去空白实验消耗的0.10 mL,则实际消耗碘标准溶液的
体积为1.20 mL,根据反应I +SO +2HO===2I-+4H++SO可以计算出n(SO )=n(I)=1.20
2 2 2 2 2
mL
×10-3 L·mL-1×0.010 00 mol·L-1=1.20×10-5 mol,由于SO 的平均回收率为95%,则实
2
际生成的n(SO )=≈1.263×10-5 mol,则根据S元素守恒可知,该样品中亚硫酸盐含量为
2
≈80.8 mg·kg-1。
4.(2021·湖南,15)碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料
制备碳酸钠,并测定产品中少量碳酸氢钠的含量,过程如下:
步骤Ⅰ.Na CO 的制备
2 3步骤Ⅱ.产品中NaHCO 含量测定
3
①称取产品2.500 g,用蒸馏水溶解,定容于250 mL容量瓶中;
②移取25.00 mL上述溶液于锥形瓶中,加入2滴指示剂M,用0.100 0 mol·L-1盐酸标准溶
液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸V mL;
1
③在上述锥形瓶中再加入2滴指示剂N,继续用0.100 0 mol·L-1盐酸标准溶液滴定至终点
(第二滴定终点),又消耗盐酸V mL;
2
④平行测定三次,V 平均值为22.45,V 平均值为23.51。
1 2
已知:(i)当温度超过35 ℃时,NH HCO 开始分解。
4 3
(ii)相关盐在不同温度下的溶解度表(g/100 g HO)
2
温度/℃ 0 10 20 30 40 50 60
NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3
NH HCO 11.9 15.8 21.0 27.0
4 3
NaHCO 6.9 8.2 9.6 11.1 12.7 14.5 16.4
3
NH Cl 29.4 33.3 37.2 41.4 45.8 50.4 55.2
4
回答下列问题:
(1) 步 骤 Ⅰ 中 晶 体 A 的 化 学 式 为 __________ , 晶 体 A 能 够 析 出 的 原 因 是
________________________________________________________________________。
(2)步骤Ⅰ中“300 ℃加热”所选用的仪器是________(填标号)。
(3)指示剂N为______________,描述第二滴定终点前后颜色变化:__________________
______________________________________________________。
(4)产品中NaHCO 的质量分数为__________(保留三位有效数字)。
3
(5)第一滴定终点时,某同学俯视读数,其他操作均正确,则 NaHCO 质量分数的计算结果
3
________(填“偏大”“偏小”或“无影响”)。
答案 (1)NaHCO 在相同温度下,NaHCO 的溶解度较小,故NaHCO 晶体能够析出(答案
3 3 3
合理即可) (2)D (3)甲基橙 溶液由黄色变橙色 (4)3.56% (5)偏大
解析 (1)根据题给信息中盐在不同温度下的溶解度不难看出,控制温度在 30~35 ℃,目的
是为了使NH HCO 不发生分解,同时析出NaHCO 固体,得到晶体A,因为在相同温度下,
4 3 3NaHCO 的溶解度较小。
3
(2)300 ℃加热抽干后的NaHCO 固体,需用坩埚、泥三角、三脚架等进行操作,所以符合
3
题意的为D项。
(3)分析可知,第二次滴定时,使用的指示剂N为甲基橙,滴定到终点前溶液的溶质为碳酸
氢钠和氯化钠,滴定达到终点后溶液的溶质为氯化钠,所以溶液的颜色变化为由黄色变为橙
色。
(4)第一滴定发生的反应是NaCO+HCl===NaHCO +NaCl,则n(Na CO)=n (NaHCO )=
2 3 3 2 3 生成 3
n(HCl)=0.100 0 mol·L-1×22.45×10-3L=2.245×10-3 mol,第二滴定消耗的盐酸的体积V
2
=23.51,则根据化学方程式:NaHCO +HCl===NaCl+HO+CO↑可知,消耗的NaHCO
3 2 2 3
的物质的量n (NaHCO )=0.100 0 mol·L-1×23.51×10-3L=2.351×10-3mol,则原溶液中的
总 3
NaHCO 的物质的量 n(NaHCO )=n (NaHCO )-n (NaHCO )= 2.351×10-3mol-
3 3 总 3 生成 3
2.245×10-3mol=1.06×10-4mol,则原产品中 NaHCO 的物质的量为×1.06×10-4mol=
3
1.06×10-3mol,故产品中NaHCO 的质量分数为×100%=
3
3.561 6%≈3.56%。
(5)第一滴定时,其他操作均正确的情况下,俯视读数,则会使标准液盐酸的体积偏小,即
测得V 偏小,所以原产品中NaHCO 的物质的量会偏大,最终导致其质量分数偏大。
1 3
考向一 溶液的配制与滴定
1.(2022·广东省普通高中学业水平合格性考试)用 NaOH 固体配制 100 mL 0.1 mol·L-1
NaOH溶液,下列说法错误的是( )
A.选用100 mL容量瓶
B.用玻璃棒搅拌或引流
C.容量瓶使用前需查验是否漏水
D.需加入100 mL水
答案 D
解析 题目要求配制100 mL溶液,就要选择100 mL容量瓶,A项正确;固体在烧杯中溶解,
用玻璃棒搅拌,冷却后用玻璃棒引流,B项正确;容量瓶使用前需查验是否漏水,C项正确;
加入100 mL水,会使溶液体积大于100 mL,溶液浓度小于0.1 mol·L-1,D项错误。
2.测定某草酸晶体样品的纯度的主要操作包括:
①称取一定质量的草酸晶体,加水使其完全溶解;
②转移定容待测液;
③移取20.00 mL待测液,用0.100 0 mol·L-1的KMnO 溶液滴定。
4
上述操作中,不需要用到的仪器为( )答案 D
解析 由题意可知,称取一定质量的草酸晶体时需要用到的仪器为托盘天平,转移定容待测
液时需要用到的仪器为容量瓶,用0.100 0 mol·L-1的高锰酸钾溶液滴定时用到的仪器为酸式
滴定管和锥形瓶,则实验时不需要用到的仪器为碱式滴定管。
考向二 氧化还原滴定
3.测定过硫酸钠(Na SO)产品纯度:称取0.250 0 g样品,用蒸馏水溶解,加入过量KI,充
2 2 8
分反应后,再滴加几滴指示剂,用 0.100 0 mol·L-1NaSO 标准溶液滴定,达到滴定终点时,
2 2 3
消耗标准溶液的体积为19.50 mL。(已知:I+2SO===SO+2I-)
2 2 4
(1)选用的指示剂是______________,达到滴定终点的现象是_________________________
___________________________________________________________________________。
(2)样品的纯度为__________%。
答案 (1)淀粉溶液 滴入最后半滴标准溶液,溶液的蓝色褪去,且半分钟内不恢复蓝色
(2)92.82
解析 (1)根据淀粉遇I 变蓝色,可选用淀粉溶液作指示剂,若达到滴定终点,会看到溶液
2
由蓝色变为无色,且半分钟内不再变为蓝色。
(2)Na SO 作氧化剂,与KI反应的离子方程式为SO+2I-===2SO+I ,I 与NaSO 反应的
2 2 8 2 2 2 2 2 3
离子方程式为I +2SO===SO+2I-,可得关系式:NaSO ~I ~2NaSO ,n(Na SO)=
2 2 4 2 2 8 2 2 2 3 2 2 3
0.100 0 mol·L-1×19.50×10-3 L=1.95×10-3 mol,则n(Na SO)=n(Na SO)=9.75×
2 2 8 2 2 3
10-4 mol,m(Na SO)=9.75×10-4 mol×238 g·mol-1=0.232 05 g,则该样品的纯度为
2 2 8
×100%=92.82%。
4.过氧乙酸(含有少量HO 杂质)的含量测定流程如图。
2 2
―→―→―→―→
(1)判断HO 恰好除尽的实验现象是___________________________________________
2 2
________________________________________________________________________。
(2)过氧乙酸被Fe2+还原,还原产物之一为乙酸,其离子方程式为________________。(3)若样品体积为V mL,加入c mol·L-1 FeSO 溶液V mL,消耗c mol·L-1 KCrO 溶液
0 1 4 1 2 2 2 7
V mL。则过氧乙酸的含量为__________ g·L-1。
2
答案 (1)当滴入最后半滴高锰酸钾溶液时,溶液由无色变为浅红色,且半分钟内不褪色
(2)CH COOOH+ 2Fe2++2H+===CHCOOH+2Fe3++HO (3)
3 3 2
解析 (1)高锰酸钾溶液为紫红色,过氧化氢没除尽之前,加高锰酸钾,溶液紫红色会褪去,
若过氧化氢已除尽,再滴入高锰酸钾溶液,溶液将变为浅红色。(3)Fe2+总物质的量为cV×
1 1
10-3mol,n(K Cr O)=cV×10-3mol。根据得失电子守恒有:KCr O ~2Cr3+~6e-~6Fe2+
2 2 7 2 2 2 2 7
~6Fe3+,即每1 mol K Cr O 与6 mol Fe2+恰好完全反应,所以与cV×10-3mol KCr O 反
2 2 7 2 2 2 2 7
应的Fe2+的物质的量为6cV×10-3mol,则与过氧乙酸反应的Fe2+的物质的量为cV×10-
2 2 1 1
3mol-6cV×10-3mol,根据CHCOOOH+2Fe2++2H+===CHCOOH+2Fe3++HO可得,
2 2 3 3 2
CHCOOOH的物质的量为,CHCOOOH的质量为×76 g·mol-1=38(cV×10-3-6cV×10-
3 3 1 1 2 2
3) g,则过氧乙酸的含量为= g·L-1。
考向三 沉淀滴定
5.沉淀滴定法是测定粒子浓度的方法之一,为了测定某废水中SCN-的浓度,可用标准
AgNO 溶液滴定待测液。已知:
3
物质 AgCl AgI AgCN Ag CrO AgSCN
2 4
颜色 白 黄 白 砖红 白
K 1.8×10-10 8.3×10-17 1.2×10-16 3.5×10-11 1.0×10-12
sp
(1)滴定时可选为滴定指示剂的是_________________________________________(填字母)。
A.NaCl溶液 B.KCrO 溶液
2 4
C.KI溶液 D.NaCN溶液
(2)如何确定该滴定过程的终点:______________________________________________
________________________________________________________________________。
答案 (1)B (2)当滴入最后半滴标准液时,出现浅红色沉淀,且半分钟内沉淀颜色不改变
解析 (1)指示剂选择原则为颜色变化明显、溶解度微大于 AgSCN,根据表中数据可知选
KCrO 溶液作为指示剂。
2 4
6.已知:ClNO与HO反应生成HNO 和HCl。通过以下实验测定ClNO样品的纯度。取m g
2 2
ClNO样品溶于水,配制成250 mL溶液;取出25.00 mL样品于锥形瓶中,以KCrO 溶液作
2 4
为指示剂,用c mol·L-1 AgNO 标准溶液滴定至终点,消耗标准溶液的体积为20.00 mL。
3
达到滴定终点的现象是____________________________________________________________
________________________________________________________________________,
亚硝酰氯(ClNO)的质量分数为______________________________________________。
[已知:Ag CrO 为砖红色固体;K (AgCl)=1.8×10-10,K (Ag CrO)=3.5×10-11]
2 4 sp sp 2 4
答案 滴入最后半滴标准溶液,溶液中生成浅红色沉淀,且半分钟内沉淀颜色不改变 %
解析 根据 ClNO~HCl~AgNO 关系式,得到 25.00 mL 样品溶液中 ClNO 物质的量
3n(ClNO)=n(AgNO)=c mol·L-1×0.02 L=0.02c mol,亚硝酰氯(ClNO)的质量分数为
3
×100%=%。
专题强化练
1.二氯异氰尿酸钠[(CNO) ClNa]是常用的杀菌消毒剂,常温下为白色固体,难溶于冷水。
3 2
某同学利用高浓度的NaClO溶液和(CNO) H 固体,在10 ℃时反应制备二氯异氰尿酸钠。
3 3
某实验小组通过下列实验测定二氯异氰尿酸钠样品中有效氯的含量。
反应原理:[(CNO) Cl]-+H++2HO===(CNO) H +2HClO,HClO+2I-+H+===I +Cl-+
3 2 2 3 3 2
HO,I+2SO===SO+2I-
2 2 2 4
实验步骤:准确称取m g样品,用容量瓶配制成250 mL溶液;取25.00 mL上述溶液于碘量
瓶中,加入适量稀硫酸和过量KI溶液,充分反应后,用c mol·L-1 Na SO 标准溶液滴定至
2 2 3
溶液呈微黄色。加入淀粉指示剂继续滴定至终点,消耗NaSO 溶液平均为V mL。
2 2 3
(1)滴定终点的颜色变化为____________。
(2)该样品的有效氯含量表达式为_________________________________________________
________________________________________________________________________(化为最
简式)。(该样品的有效氯=×100%)
答案 (1)恰好由蓝色变成无色
(2)%
解析 (1)该反应用淀粉作指示剂,淀粉遇碘变蓝色,因此滴定终点的现象为滴入最后半滴
标准液时,溶液恰好由蓝色变成无色,且半分钟内不恢复。
(2)根据题目所给反应可得关系式:HClO~I ~2S O,则n(HClO)=×n(S O)=×
2 2 2
c mol·L-1×V×10-3 L=5×10-4cV mol,故样品中有效氯含量为
×100%=%。
2.摩尔盐[(NH )Fe(SO )·6H O]是一种常见的复盐。某实验小组用下列方法测定摩尔盐中Fe2
4 2 4 2 2
+的含量,取30.00 g固体于小烧杯中,加入适量稀硫酸,溶解后在 250 mL容量瓶中定容。
取25.00 mL上述溶液于锥形瓶中,用0.1 mol·L-1的KMnO 溶液滴定至终点。平行操作三次,
4
消耗KMnO 溶液的平均体积为16.00 mL。此样品中Fe2+的含量为________%(结果保留小数
4
点后1位)。导致该测定结果与理论值有偏差的可能原因是_____________________(填字母)。
A.配制溶液定容时俯视刻度线
B.取摩尔盐溶液的滴定管没有润洗
C.取待测液的锥形瓶洗净后未干燥
D.摩尔盐的结晶水数量不足
答案 14.9 AD
解析 根据转移电子守恒可知滴定过程中存在数量关系n(Fe2+)=5n(KMnO),所以25.00
4mL待测液中n(Fe2+)=5×0.1 mol·L-1×0.016 L=0.008 mol,则250 mL待测液中n(Fe2+)=
0.08 mol , 则 样 品 中 Fe2 + 的 含 量 为 ×100%≈14.9% ; 理 论 上 Fe2 + 的 含 量 应 为
×100%≈14.3%,测定结果偏大;配制溶液定容时俯视刻度线,导致所配待测液浓度偏大,
25.00 mL待测液消耗的高锰酸钾溶液偏多,测定结果偏大,A项符合题意;取摩尔盐溶液
的滴定管没有润洗,导致摩尔盐被稀释,25.00 mL待测液消耗的高锰酸钾溶液偏少,测定
结果应偏小,B项不符合题意;取待测液的锥形瓶洗净后未干燥对测定结果无影响,C项不
符合题意;摩尔盐的结晶水数量不足导致30.00 g固体中所含Fe2+偏多,测定结果偏大,D
项符合题意。
3.硫代硫酸钠(Na SO)广泛用于电镀、鞣制皮革、棉织品漂白后的脱氯剂等。某实验小组
2 2 3
的同学用下列方法测定NaSO·5H O的质量分数,准确称取5.00 g硫代硫酸钠样品,溶于
2 2 3 2
蒸馏水配制成100 mL溶液,取25.00 mL注入锥形瓶中,以淀粉作指示剂,用0.100 0 mol·L-1
标准碘溶液滴定。已知:2SO(aq)+I(aq)===SO(aq)(无色)+2I-(aq)。
2 2 4
(1)滴定终点的现象是______________。
(2)第一次滴定开始和结束时,滴定管中的液面如图,则消耗标准碘溶液的体积为
________mL。
(3)重复上述操作三次,记录另两次数据如表中所示,则产品中 NaSO·5H O的质量分数为
2 2 3 2
________%(结果保留两位小数)。
滴定次数 初读数/mL 末读数/mL
第二次 1.24 23.36
第三次 0.24 24.45
答案 (1)当滴加最后半滴标准溶液时,溶液由无色变为蓝色,且半分钟内不褪色 (2)22.10
(3)87.73
解析 (1)当达到滴定终点时,标准碘溶液过量,淀粉遇碘变蓝,所以滴定终点的现象为当
滴加最后半滴标准溶液时,溶液由无色变为蓝色,且半分钟内不褪色。(2)由图可知,起始
读数为0.00 mL,终点读数为22.10 mL,故第一次滴定消耗碘标准溶液的体积为22.10 mL。
(3)第二次滴定消耗碘标准溶液的体积为23.36 mL-1.24 mL=22.12 mL,第三次滴定消耗碘
标准溶液的体积为24.45 mL-0.24 mL=24.21 mL,第三次数据误差较大应舍去,所以消耗
标准液的平均体积为=22.11 mL,根据反应可得关系式:2NaSO·5H O~I ,所以
2 2 3 2 2
n(Na SO·5H O)=2n(I)=2×0.100 0 mol·L-1×22.11×10-3 L,所以产品中2NaSO·5H O
2 2 3 2 2 2 2 3 2
的含量为×100%≈87.73%。4.草酸(HOOC—COOH,弱酸)及其化合物在工业中有重要作用。草酸具有较强的还原性,
与氧化剂作用易被氧化成二氧化碳和水,故实验室可利用草酸测定次氯酸钠溶液的浓度。实
验步骤如下:取20.00 mL 0.5 mol·L-1草酸溶液于锥形瓶中,用次氯酸钠溶液滴定,至终点
时消耗次氯酸钠溶液为25.00 mL。
(1)次氯酸钠与草酸反应的离子方程式为________________________________________。
(2)次氯酸钠溶液物质的量浓度为____mol·L-1。
答案 (1)H C O+ClO-===Cl-+2CO↑+HO (2)0.4
2 2 4 2 2
解析 根据题中信息知草酸具有较强的还原性,与氧化剂作用易被氧化成二氧化碳和水,可
知碳的化合价由+3价升高为+4价,次氯酸钠具有强氧化性,Cl的化合价由+1价降低为
-1价,根据化合价升降守恒、原子守恒和电荷守恒,可得反应的离子方程式为 HC O +
2 2 4
ClO-===Cl-+2CO↑+HO;根据上述离子方程式可知HC O ~ClO-,可得次氯酸钠溶液
2 2 2 2 4
物质的量浓度c== mol·L-1=0.4 mol·L-1。
5.钛白(TiO)是重要的化工原料,呈白色粉末,不溶于水。某实验小组用硫酸法制备钛白。
2
在70~80 ℃条件下,不断通入空气并搅拌,钛铁矿同浓硫酸反应制得可溶性硫酸盐。TiO2
+称为钛酰离子,易水解生成钛酸,进而制得钛白。在制取钛白的过程中,需要测定钛液中
Ti(Ⅳ)的含量。首先用铝片将Ti(Ⅳ)还原为Ti3+,再用0.020 0 mol·L-1 Fe (SO ) 标准溶液滴
2 4 3
定(反应原理为Ti3++Fe3+===Ti4++Fe2+)。
滴定 待测溶液 标准溶液的体积/mL
次数 的体积/mL 滴定前刻度 滴定后刻度
1 25.00 0.11 8.61
2 25.00 7.51 15.00
3 25.00 0.30 7.81
滴定时可选用的指示剂为____________,滴定终点溶液的颜色变化为__________,钛液中
Ti(Ⅳ)的浓度为________ g·L-1(以TiOSO 计)。
4
答案 KSCN溶液 无色变红色 1.92
解析 标准溶液为Fe (SO ) 溶液,达到滴定终点时Fe3+稍过量,所以可以用KSCN溶液作
2 4 3
指示剂;达到滴定终点时溶液会由无色变为红色;三次滴定所用标准溶液的体积分别为 8.50
mL、7.49 mL、7.51 mL,因为第一组数据与其他数据相差较大,需要舍去,根据第二组和
第三组数据得标准液的平均体积为7.50 mL,则所用Fe3+物质的量为0.007 5 L×0.020 0 mol·L
-1×2=0.000 3 mol,根据反应原理可知待测液中Ti3+的物质的量与Fe3+的物质的量相等,即
0.000 3 mol。待测液体积为25.00 mL,根据原子守恒可得钛液中Ti(Ⅳ)的浓度为=1.92 g·L-
1。
6.二氯异氰尿酸钠(C NOClNa)为白色固体,难溶于冷水,是氧化性消毒剂中最为广谱、
3 3 3 2
高效、安全的消毒剂。某实验小组用下列方法测定粗产品中二氯异氰尿酸钠的纯度。将m g
粗产品溶于无氧蒸馏水中配制成100 mL溶液,取20.00 mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5 min。用c mol·L-1的NaSO 标准溶液进行滴
2 2 3
定,加入指示剂,滴定至终点时,消耗V mL Na SO 标准溶液。(已知:杂质不与KI反应,
2 2 3
涉及的反应为C NOCl+3H++4I-===C HNO+2I+2Cl-、I+2SO===2I-+SO)
3 3 3 3 3 3 3 2 2 2 4
(1)加入的指示剂是__________(填名称)。
(2)C NOClNa的百分含量为________%(用含m、c、V的代数式表示)。
3 3 3 2
(3)下列操作会导致粗产品中二氯异氰尿酸钠的纯度偏低的是________(填字母)。
a.盛装NaSO 标准溶液的滴定管未润洗
2 2 3
b.滴定管在滴定前有气泡,滴定后无气泡
c.碘量瓶中加入的稀硫酸偏少
答案 (1)淀粉溶液 (2) (3)c
解析 (1)淀粉遇I 会变为蓝色,当滴定结束时I 消耗完全,溶液蓝色褪去,故滴定时应选
2 2
择淀粉溶液作指示剂。(2)由涉及的反应的化学方程式可得转化关系式:C NOCl~2I ~
3 3 3 2
4SO,由滴定消耗c mol·L-1 Na SO 溶液V mL可知,m g粗产品中二氯异氰尿酸钠的物
2 2 2 3
质的量为n(C NOClNa)=n(Na SO)×=c mol·L-1×V×10-3 L××=×10-3 mol,则粗产
3 3 3 2 2 2 3
品的纯度为×100%=%。(3)盛装NaSO 标准溶液的滴定管未润洗,会导致NaSO 标准溶
2 2 3 2 2 3
液的浓度偏低,消耗的NaSO 的量偏多,最终导致物质的纯度偏高,a不符合题意;滴定
2 2 3
管在滴定前有气泡,滴定后无气泡,则消耗的标准溶液的体积偏大,由此计算的物质的纯度
偏高,b不符合题意;如果硫酸的用量过少,则导致反应不能充分进行,产生的 I 的量偏低,
2
最终导致消耗的NaSO 标准溶液的体积偏少,由此计算出的物质的纯度偏低,c符合题意。
2 2 3
7.叠氮化钠(NaN )是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气
3
囊中的药剂。实验室用滴定法测定叠氮化钠样品中NaN 的质量分数:
3
①将2.500 g试样配成500 mL溶液。
②取50.00 mL上述溶液置于锥形瓶中,加入50.00 mL 0.100 0 mol·L-1(NH )Ce(NO ) 溶液。
4 2 3 6
发生反应:2(NH )Ce(NO )+2NaN ===4NH NO +2Ce(NO )+2NaNO +3N↑。
4 2 3 6 3 4 3 3 3 3 2
③充分反应后,将溶液稀释,向溶液中加入 8 mL浓硫酸,滴入3滴邻菲罗琳指示液,用
0.050 0 mol·L-1(NH )Fe(SO ) 标准溶液滴定过量的Ce4+,消耗溶液体积为34.00 mL。发生
4 2 4 2
反应:Ce4++Fe2+===Ce3++Fe3+。
试样中NaN 的质量分数为__________(结果保留四位有效数字)。
3
答案 85.80%
解析 消耗的(NH )Fe(SO ) 的物质的量为 0.050 0 mol·L-1×0.034 L=0.001 7 mol,加入
4 2 4 2
(NH )Ce(NO ) 的物质的量为0.100 0 mol·L-1×0.05 L=0.005 mol,根据Ce4++Fe2+===Ce3+
4 2 3 6
+Fe3+可知,与NaN 反应的(NH )Ce(NO ) 的物质的量为 0.005 mol-0.001 7 mol=0.003 3
3 4 2 3 6
mol,依据2(NH )Ce(NO ) +2NaN ===4NH NO +2Ce(NO ) +2NaNO +3N↑可知,50.00
4 2 3 6 3 4 3 3 3 3 2
mL溶液中含有的NaN 的物质的量为0.003 3 mol,则试样中NaN 的质量分数为×100%=
3 3
85.80%。8.硫氰化钾(KSCN)是中学化学实验室的常见药品。某实验小组测定制备的晶体中KSCN的
含量:称取10.00 g样品,配成1 000 mL溶液,取25.00 mL溶液于锥形瓶中,加入适量稀硝
酸,再加入几滴Fe(NO ) 溶液作指示剂,用0.100 0 mol·L-1 AgNO 标准溶液滴定,滴定时
3 3 3
发生反应:SCN-+Ag+===AgSCN↓(白色),平均消耗AgNO 标准溶液24.50 mL。
3
(1)刚好沉淀完时,锥形瓶中溶液的颜色变化是__________。
(2)晶体中KSCN的质量分数为______________。
答案 (1)溶液由红色变为无色(或浅黄色或黄色)
(2)95.06%
解析 (1)滴定时发生的离子反应为SCN-+Ag+===AgSCN↓,则刚好沉淀完时,溶液中的
SCN-反应完全,红色褪去,只存在少量Fe3+的颜色,故锥形瓶中溶液的颜色变化是由红色
褪为无色或浅黄色或黄色。(2)由反应 SCN-+Ag+===AgSCN↓,可得出 n(KSCN)=
n(AgNO)=0.100 0 mol·L-1×24.50×10-3 L=2.45×10-3 mol,晶体中KSCN的质量分数为
3
×100%=95.06%。
9.某化学兴趣小组利用0.200 0 mol·L-1的AgNO 溶液测定某NaCl、KCl混合溶液中Cl-的
3
物质的量浓度。
Ⅰ.配制250 mL 0.200 0 mol·L-1的AgNO 溶液。配制过程:计算所需AgNO 固体的质量→
3 3
称量→溶解→转移、洗涤→定容、摇匀→装瓶、贴标签。
(1)配制该溶液需要的玻璃仪器:烧杯、量筒、玻璃棒、胶头滴管、__________。
(2)用托盘天平称取________ g AgNO 固体。
3
(3)定容时若仰视刻度线,造成的后果应如何补救?
________________________________________________________________________。
Ⅱ.已知25 ℃时,以下五种物质的K 如下表所示:
sp
物质 AgCl Ag CrO AgBr AgⅠ Ag S
2 4 2
2× 2× 5.4× 8.3× 6.3×
K
sp
10-10 10-12 10-13 10-16 10-50
颜色 白色 砖红色 浅黄色 黄色 黑色
(4)现以所配制的 AgNO 溶液测定某溶液中 c(Cl-),适宜作滴定指示剂的物质是
3
__________(填字母)。
A.KCrO 溶液 B.KBr溶液
2 4
C.KI溶液 D.KS溶液
2
滴定过程中,用标准AgNO 溶液滴定待测液时,眼睛应注视________,滴定终点的实验现
3
象为____________。
(5)下列操作中可导致测定的Cl-浓度偏低的是________(填字母)。
A.取标准AgNO 溶液的滴定管,未经润洗就直接注入溶液,进行滴定实验
3
B.盛装标准液的滴定管在滴定前有气泡,滴定后气泡消失C.读取AgNO 溶液体积时,开始时仰视读数,滴定结束时俯视读数
3
D.锥形瓶内有少量蒸馏水
(6)实验数据记录如下表所示:
标准AgNO 溶液体积
3
滴定 待测溶液
滴定前的 滴定后的
次数 体积/mL
刻度/mL 刻度/mL
第一次 50.00 0.00 25.05
第二次 50.00 4.10 29.10
第三次 50.00 0.40 25.35
则该待测液中,c(Cl-)的物质的量浓度为________ mol·L-1。(结果保留四位有效数字)
答案 (1)250 mL棕色容量瓶 (2)8.5 (3)重新配制溶液 (4)A 锥形瓶中沉淀颜色的变化
当滴入最后半滴硝酸银溶液时,出现砖红色沉淀,且30秒内沉淀颜色不变 (5)C (6)0.100
0
解 析 Ⅰ .(2) 配 制 250 mL 0.200 0 mol·L - 1 的 AgNO 溶 液 。 则 m(AgNO) =
3 3
n(AgNO)×M(AgNO)=0.250 L×0.200 0 mol·L-1×170 g·mol-1=8.5 g,故用托盘天平称取
3 3
8.5 g AgNO 固体。Ⅱ.(4)只有当滴定剂和被滴定物的生成物的溶解度比滴定剂和指示剂的生
3
成物的溶解度小时,完全反应后,继续滴加滴定剂,滴定剂和指示剂反应生成沉淀,保证滴
定剂和被滴定物完全反应。此题中,只有氯化银沉淀完全后,银离子才能与滴定剂的离子反
应生成其他有色沉淀。则:
K (Ag CrO)=c2(Ag+)·c(CrO)=2×10-12,可知CrO开始沉淀时c(CrO)==,银离子浓度相
sp 2 4
同时,CrO开始沉淀时浓度大于氯离子浓度,即CrO开始沉淀时,氯离子已经完全沉淀,A
符合;氯化银、溴化银、碘化银的组成都是1∶1型,依据K 可知溶解性:氯化银>溴化银
sp
>碘化银,氯离子未沉淀完全时,碘离子、溴离子即开始沉淀,B、C不符合;K (Ag S)=
sp 2
c2(Ag+)·c(S2-)=6.3×10-50,可知S2-开始沉淀时浓度c(S2-)==;K (AgCl)=c(Ag+)·c(Cl-)
sp
=2×10-10,可知Cl-开始沉淀时c(Cl-)==,银离子浓度相同时,硫离子开始沉淀时浓度
远远小于氯离子浓度,即硫离子沉淀时,氯离子未完全沉淀,D不符合。滴定过程中,用标
准AgNO 溶液滴定待测液时,眼睛应注视锥形瓶中沉淀颜色的变化。(5)取标准AgNO 溶液
3 3
的滴定管,未经润洗就直接注入溶液,导致标准液体积偏大,测定结果偏高,A项不符合;
盛装标准液的滴定管在滴定前有气泡,滴定后气泡消失,导致标准液体积偏大,测定结果偏
高,B项不符合;读取AgNO 溶液体积时,开始时仰视读数,滴定结束时俯视读数,导致
3
标准液体积偏小,测定结果偏低,C项符合;滴定过程中会加少量蒸馏水,锥形瓶内有少量
蒸馏水,不影响滴定结果,D项不符合。(6)消耗标准AgNO 溶液的体积依次为25.05 mL、
3
25.00 mL和24.95 mL,根据数据的有效性,3组数据均有效,则c(Cl-)==0.100 2 mol·L-
1
1,c(Cl-)==0.100 0 mol·L-1,
2
c(Cl-)==0.099 8 mol·L-1,
3
则c(Cl-)===0.100 0 mol·L-1。