文档内容
特色练 12 电解质溶液中的曲线分析
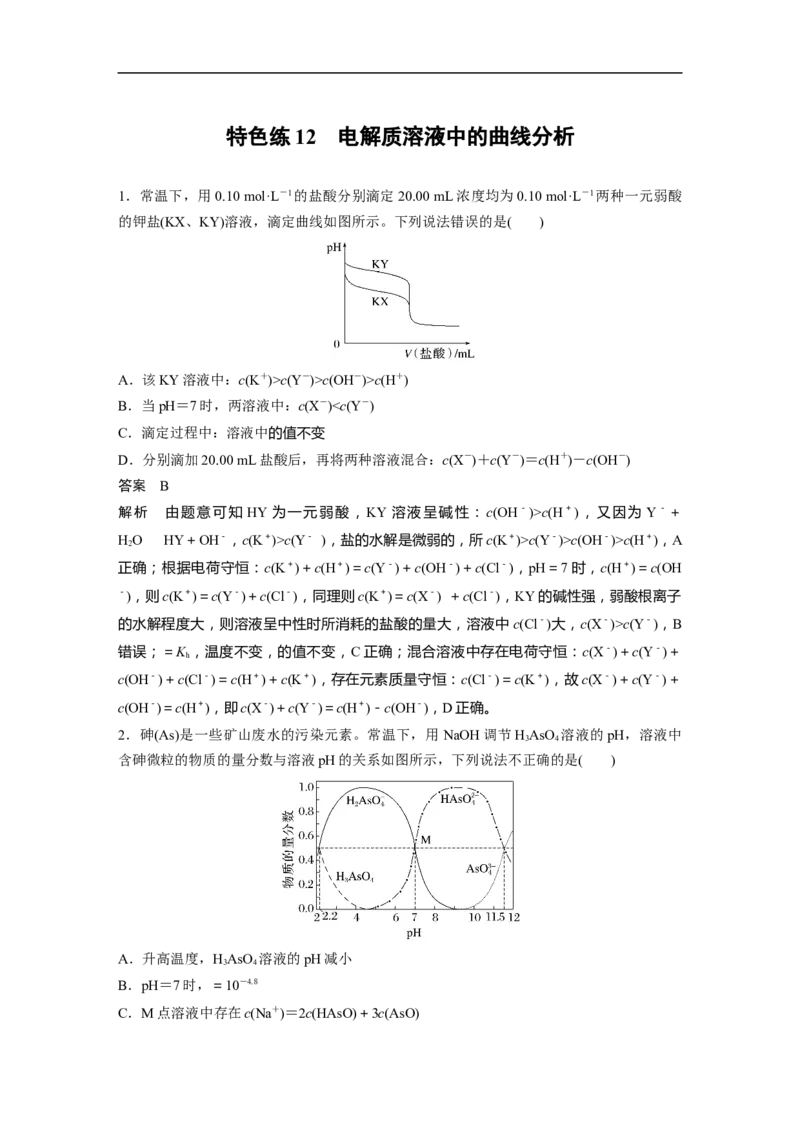
1.常温下,用0.10 mol·L-1的盐酸分别滴定20.00 mL浓度均为0.10 mol·L-1两种一元弱酸
的钾盐(KX、KY)溶液,滴定曲线如图所示。下列说法错误的是( )
A.该KY溶液中:c(K+)>c(Y-)>c(OH-)>c(H+)
B.当pH=7时,两溶液中:c(X-)c(H+),又因为 Y-+
HOHY+OH-,c(K+)>c(Y- ),盐的水解是微弱的,所c(K+)>c(Y-)>c(OH-)>c(H+),A
2
正确;根据电荷守恒:c(K+)+c(H+)=c(Y-)+c(OH-)+c(Cl-),pH=7时,c(H+)=c(OH
-),则c(K+)=c(Y-)+c(Cl-),同理则c(K+)=c(X-) +c(Cl-),KY的碱性强,弱酸根离子
的水解程度大,则溶液呈中性时所消耗的盐酸的量大,溶液中 c(Cl-)大,c(X-)>c(Y-),B
错误;=K ,温度不变,的值不变,C正确;混合溶液中存在电荷守恒:c(X-)+c(Y-)+
h
c(OH-)+c(Cl-)=c(H+)+c(K+),存在元素质量守恒:c(Cl-)=c(K+),故c(X-)+c(Y-)+
c(OH-)=c(H+),即c(X-)+c(Y-)=c(H+)-c(OH-),D正确。
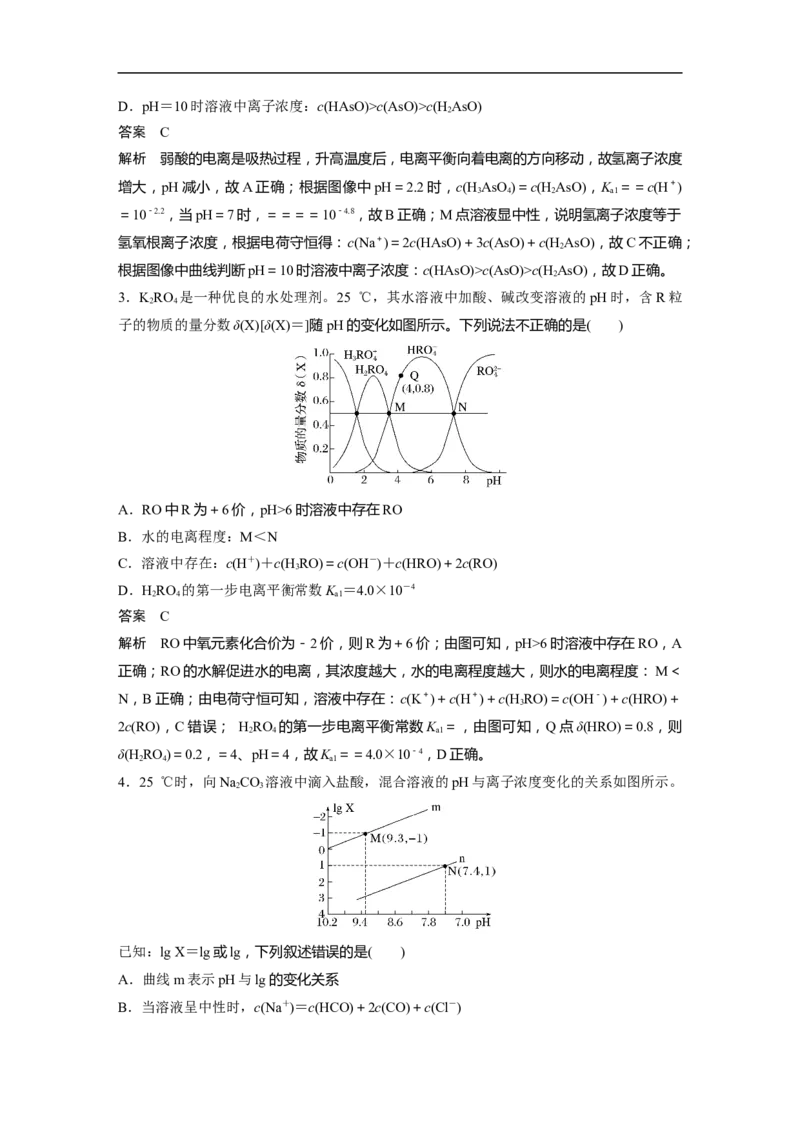
2.砷(As)是一些矿山废水的污染元素。常温下,用NaOH调节HAsO 溶液的pH,溶液中
3 4
含砷微粒的物质的量分数与溶液pH的关系如图所示,下列说法不正确的是( )
A.升高温度,HAsO 溶液的pH减小
3 4
B.pH=7时,=10-4.8
C.M点溶液中存在c(Na+)=2c(HAsO)+3c(AsO)D.pH=10时溶液中离子浓度:c(HAsO)>c(AsO)>c(H AsO)
2
答案 C
解析 弱酸的电离是吸热过程,升高温度后,电离平衡向着电离的方向移动,故氢离子浓度
增大,pH减小,故A正确;根据图像中pH=2.2时,c(H AsO )=c(H AsO),K ==c(H+)
3 4 2 a1
=10-2.2,当pH=7时,====10-4.8,故B正确;M点溶液显中性,说明氢离子浓度等于
氢氧根离子浓度,根据电荷守恒得:c(Na+)=2c(HAsO)+3c(AsO)+c(H AsO),故C不正确;
2
根据图像中曲线判断pH=10时溶液中离子浓度:c(HAsO)>c(AsO)>c(H AsO),故D正确。
2
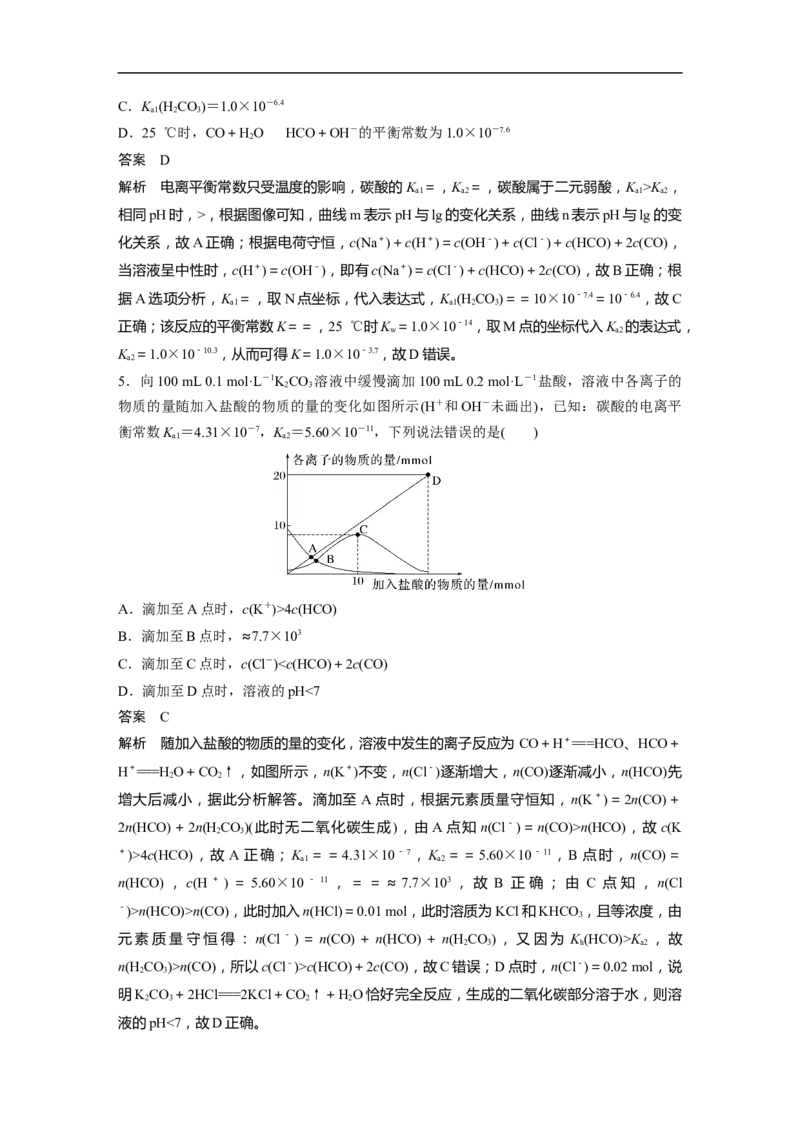
3.KRO 是一种优良的水处理剂。25 ℃,其水溶液中加酸、碱改变溶液的pH时,含R粒
2 4
子的物质的量分数δ(X)[δ(X)=]随pH的变化如图所示。下列说法不正确的是( )
A.RO中R为+6价,pH>6时溶液中存在RO
B.水的电离程度:M<N
C.溶液中存在:c(H+)+c(H RO)=c(OH-)+c(HRO)+2c(RO)
3
D.HRO 的第一步电离平衡常数K =4.0×10-4
2 4 a1
答案 C
解析 RO中氧元素化合价为-2价,则R为+6价;由图可知,pH>6时溶液中存在RO,A
正确;RO的水解促进水的电离,其浓度越大,水的电离程度越大,则水的电离程度:M<
N,B正确;由电荷守恒可知,溶液中存在:c(K+)+c(H+)+c(H RO)=c(OH-)+c(HRO)+
3
2c(RO),C错误; HRO 的第一步电离平衡常数K =,由图可知,Q点δ(HRO)=0.8,则
2 4 a1
δ(H RO)=0.2,=4、pH=4,故K ==4.0×10-4,D正确。
2 4 a1
4.25 ℃时,向NaCO 溶液中滴入盐酸,混合溶液的pH与离子浓度变化的关系如图所示。
2 3
已知:lg X=lg或lg,下列叙述错误的是( )
A.曲线m表示pH与lg的变化关系
B.当溶液呈中性时,c(Na+)=c(HCO)+2c(CO)+c(Cl-)C.K (H CO)=1.0×10-6.4
a1 2 3
D.25 ℃时,CO+HOHCO+OH-的平衡常数为1.0×10-7.6
2
答案 D
解析 电离平衡常数只受温度的影响,碳酸的K =,K =,碳酸属于二元弱酸,K >K ,
a1 a2 a1 a2
相同pH时,>,根据图像可知,曲线m表示pH与lg的变化关系,曲线n表示pH与lg的变
化关系,故A正确;根据电荷守恒,c(Na+)+c(H+)=c(OH-)+c(Cl-)+c(HCO)+2c(CO),
当溶液呈中性时,c(H+)=c(OH-),即有c(Na+)=c(Cl-)+c(HCO)+2c(CO),故B正确;根
据A选项分析,K =,取N点坐标,代入表达式,K (H CO)==10×10-7.4=10-6.4,故C
a1 a1 2 3
正确;该反应的平衡常数K==,25 ℃时K =1.0×10-14,取M点的坐标代入K 的表达式,
w a2
K =1.0×10-10.3,从而可得K=1.0×10-3.7,故D错误。
a2
5.向100 mL 0.1 mol·L-1KCO 溶液中缓慢滴加100 mL 0.2 mol·L-1盐酸,溶液中各离子的
2 3
物质的量随加入盐酸的物质的量的变化如图所示(H+和OH-未画出),已知:碳酸的电离平
衡常数K =4.31×10-7,K =5.60×10-11,下列说法错误的是( )
a1 a2
A.滴加至A点时,c(K+)>4c(HCO)
B.滴加至B点时,≈7.7×103
C.滴加至C点时,c(Cl-)n(HCO),故 c(K
2 3
+)>4c(HCO),故 A 正确;K ==4.31×10-7,K ==5.60×10-11,B 点时,n(CO)=
a1 a2
n(HCO) , c(H +) = 5.60×10 -11 , = = ≈ 7.7×103, 故 B 正 确 ; 由 C 点 知 , n(Cl
-)>n(HCO)>n(CO),此时加入n(HCl)=0.01 mol,此时溶质为KCl和KHCO ,且等浓度,由
3
元素质量守恒得:n(Cl-)=n(CO)+n(HCO)+n(H CO),又因为 K (HCO)>K ,故
2 3 h a2
n(H CO)>n(CO),所以c(Cl-)>c(HCO)+2c(CO),故C错误;D点时,n(Cl-)=0.02 mol,说
2 3
明KCO +2HCl===2KCl+CO↑+HO恰好完全反应,生成的二氧化碳部分溶于水,则溶
2 3 2 2
液的pH<7,故D正确。