文档内容
衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷 第 14 套 2.BiOCl是一种具有珠光泽的材料,利用金属Bi制备BiOCl的工艺流程如图:
组编人:于洪强
做题时间:2022 年__月___日,__:__—__:__ 校对人: 汪志新
审核人:
实际得分:____家长签字(严禁代签):______
下列说法错误的是
励志格言:如果在胜利前却步,往往只会拥抱失败;如果在困难时坚持,常常会获得新的
成功。 A. 酸浸工序中分次加入稀HNO 可降低反应剧烈程度
3
本套亮点:汇集工艺流程各地最新模拟题,有基础考查题,也有新颖且有思维量的题目,
充分利用,定能查漏补缺,收获满满。 B. 转化工序中加入稀HCl可抑制生成BiONO 3
注意事项:
C. 水解工序中加入少量CH COONa(s)可提高Bi3+水解程度
3
1, 本套密卷满分100分,做题所需时间75分钟;
2, 请一律用0.5或以上的黑色中性签字笔在规定的答题纸上做答,注意书写规范; D. 水解工序中加入少量NH NO (s)有利于BiOCl的生成
4 3
3,做题不改错,等于没有做!做完之后,要求依照答案用红笔自判所有主客观题,并算
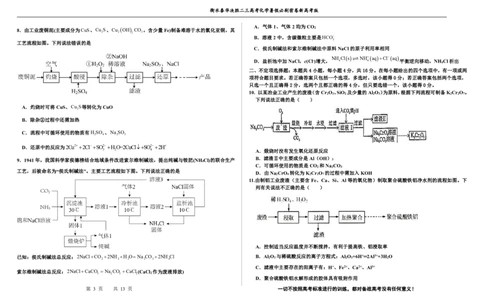
出总得分,请家长签字确认,并在积累本进行认真的错题整改反思,并把本套题的主要收 3.工业上以SO 和纯碱为原料制备无水NaHSO 的主要流程如下,下列说法错误的是
2 3
获、主要不足和反思写到每套题所附的反思纸上,开学上交。
一、单项选择题本题共9小题,每小题3分,共27分。在每小题给出的四个选项中,只有一项是符合 SO 2 吸收 结晶 湿料 气流干燥 NaHSO 3
题目要求的。
中和
母液
1. 一种工业制备无水氯化镁的工艺流程如下: (pH=8)
纯碱、水
A.吸收过程中有气体生成
B.结晶后母液中含有NaHCO
3
下列说法错误的是
A. 物质X常选用生石灰 C.气流干燥湿料时温度不宜过高
B. 工业上常用电解熔融MgCl 制备金属镁
2 D.中和后溶液中含有Na SO 和NaHCO
2 3 3
高温
C. “氯化”过程中发生的反应为MgO+C+Cl MgCl +CO
2 2
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水MgCl
2
第 1 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
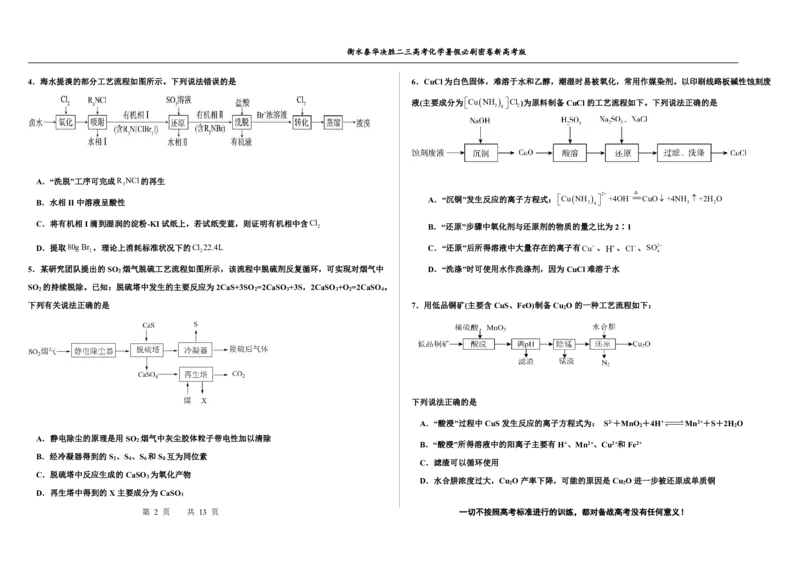
4.海水提溴的部分工艺流程如图所示。下列说法错误的是 6.CuCl为白色固体,难溶于水和乙醇,潮湿时易被氧化,常用作媒染剂。以印刷线路板碱性蚀刻废
液(主要成分为
CuNH
3
4
Cl
2
)为原料制备CuCl的工艺流程如下。下列说法正确的是
A.“洗脱”工序可完成R NCl的再生
3
B.水相II中溶液呈酸性
A.“沉铜”发生反应的离子方程式:
CuNH
3
4
2+ +4OH- CuO+4NH
3
+2H
2
O
C.将有机相I滴到湿润的淀粉-KI试纸上,若试纸变蓝,则证明有机相中含Cl
2 B.“还原”步骤中氧化剂与还原剂的物质的量之比为2∶1
D.提取80g Br ,理论上消耗标准状况下的Cl 22.4L C.“还原”后所得溶液中大量存在的离子有Cu、H、Cl、SO2
2 2 4
5.某研究团队提出的SO 烟气脱硫工艺流程如图所示,该流程中脱硫剂反复循环,可实现对烟气中 D.“洗涤”时可使用水作洗涤剂,因为CuCl难溶于水
2
SO 的持续脱除。已知:脱硫塔中发生的主要反应为2CaS+3SO =2CaSO +3S,2CaSO +O =2CaSO 。
2 2 3 3 2 4
下列有关说法正确的是 7.用低品铜矿(主要含CuS、FeO)制备Cu O的一种工艺流程如下:
2
下列说法正确的是
A.“酸浸”过程中CuS发生反应的离子方程式为: S2-+MnO
2
+4H+Mn2++S+2H
2
O
A.静电除尘的原理是用SO 烟气中灰尘胶体粒子带电性加以清除
2 B.“酸浸”所得溶液中的阳离子主要有H+、Mn2+、Cu2+和Fe2+
B.经冷凝器得到的S 、S 、S 和S 互为同位素
2 4 6 8 C.滤渣可以循环使用
C.脱硫塔中反应生成的CaSO 为氧化产物
3 D.水合肼浓度过大,Cu O产率下降,可能的原因是Cu O进一步被还原成单质铜
2 2
D.再生塔中得到的X主要成分为CaSO
3
第 2 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
A.气体1、气体2均为CO
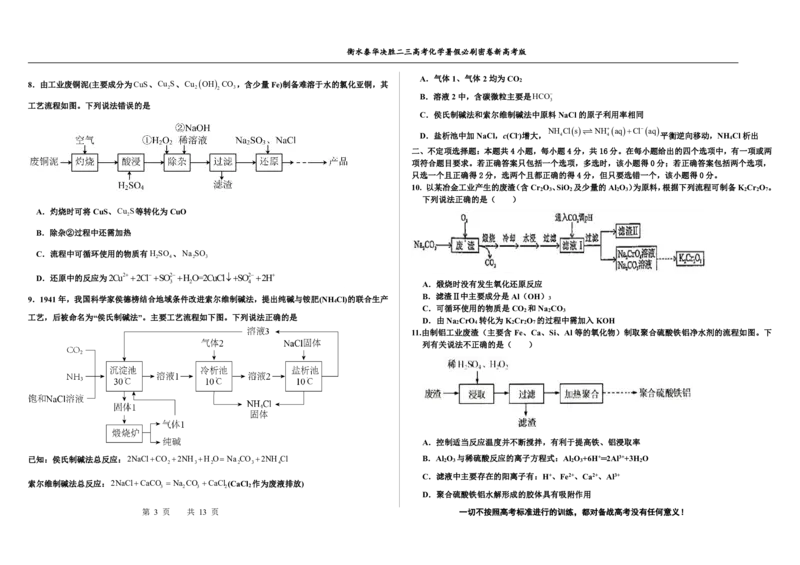
8.由工业废铜泥(主要成分为CuS、Cu S、Cu OH CO ,含少量Fe)制备难溶于水的氯化亚铜,其 2
2 2 2 3
B.溶液2中,含碳微粒主要是HCO
3
工艺流程如图。下列说法错误的是
C.侯氏制碱法和索尔维制碱法中原料NaCl的原子利用率相同
NH Cls NHaqClaq
D.盐析池中加NaCl,c(Cl-)增大, 4 4 平衡逆向移动,NH Cl析出
4
二、不定项选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,有一项或两
项符合题目要求。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,
只选一个且正确得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
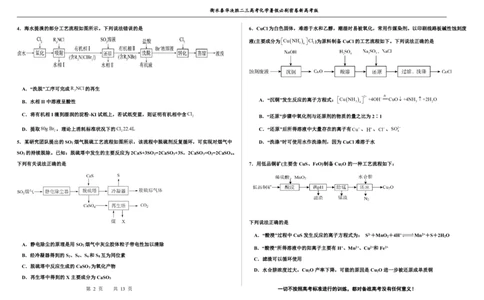
10. 以某冶金工业产生的废渣(含Cr O 、SiO 及少量的Al O )为原料,根据下列流程可制备K Cr O 。
2 3 2 2 3 2 2 7
下列说法正确的是( )
A.灼烧时可将CuS、Cu S等转化为CuO
2
B.除杂②过程中还需加热
C.流程中可循环使用的物质有H SO 、Na SO
2 4 2 3
D.还原中的反应为2Cu22ClSO2HO=2CuClSO22H
3 2 4 A.煅烧时没有发生氧化还原反应
9.1941年,我国科学家侯德榜结合地域条件改进索尔维制碱法,提出纯碱与铵肥(NH Cl)的联合生产
B.滤渣Ⅱ中主要成分是Al(OH)
3
4
C.可循环使用的物质是CO 和Na CO
2 2 3
工艺,后被命名为“侯氏制碱法”。主要工艺流程如下图。下列说法正确的是
D.由Na CrO 转化为K Cr O 的过程中需加入KOH
2 4 2 2 7
11.由制铝工业废渣(主要含Fe、Ca、Si、Al等的氧化物)制取聚合硫酸铁铝净水剂的流程如图。下
列有关说法不正确的是( )
A.控制适当反应温度并不断搅拌,有利于提高铁、铝浸取率
已知:侯氏制碱法总反应:2NaClCO 2 2NH 3 H 2 O Na 2 CO 3 2NH 4 Cl B.Al 2 O 3 与稀硫酸反应的离子方程式:Al 2 O 3 +6H+═2Al3++3H 2 O
C.滤液中主要存在的阳离子有:H+、Fe2+、Ca2+、Al3+
索尔维制碱法总反应:2NaClCaCO Na CO CaCl(CaCl 作为废液排放)
3 2 3 2 2
D.聚合硫酸铁铝水解形成的胶体具有吸附作用
第 3 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
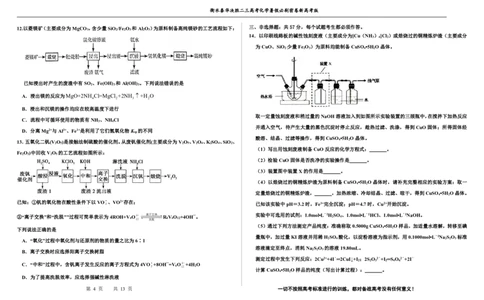
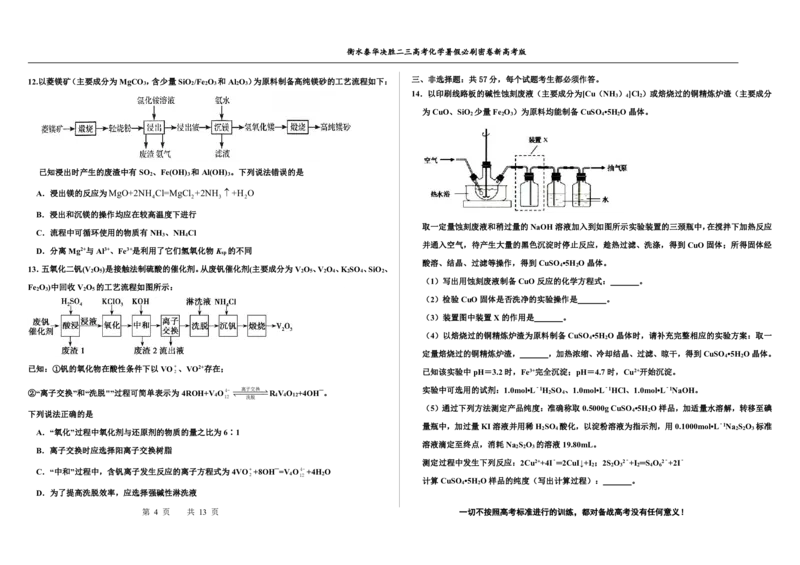
12.以菱镁矿(主要成分为MgCO ,含少量SiO /Fe O 和Al O )为原料制备高纯镁砂的工艺流程如下: 三、非选择题:共57分,每个试题考生都必须作答。
3 2 2 3 2 3
14.以印刷线路板的碱性蚀刻废液(主要成分为[Cu(NH )]Cl )或焙烧过的铜精炼炉渣(主要成分
3 4 2
为CuO、SiO 少量Fe O )为原料均能制备CuSO •5H O晶体。
2 2 3 4 2
已知浸出时产生的废渣中有SO 、Fe(OH) 和Al(OH) 。下列说法错误的是
2 3 3
A.浸出镁的反应为MgO+2NH Cl=MgCl +2NH +H O
4 2 3 2
B.浸出和沉镁的操作均应在较高温度下进行
取一定量蚀刻废液和稍过量的NaOH溶液加入到如图所示实验装置的三颈瓶中,在搅拌下加热反应
C.流程中可循环使用的物质有NH 、NH Cl
3 4
并通入空气,待产生大量的黑色沉淀时停止反应,趁热过滤、洗涤,得到CuO固体;所得固体经
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物K 的不同
sp
酸溶、结晶、过滤等操作,得到CuSO •5H O晶体。
13.五氧化二钒(V O )是接触法制硫酸的催化剂。从废钒催化剂(主要成分为V O 、V O 、K SO 、SiO 、 4 2
2 5 2 5 2 4 2 4 2
(1)写出用蚀刻废液制备CuO反应的化学方程式: 。
Fe O )中回收V O 的工艺流程如图所示:
2 3 2 5
(2)检验CuO固体是否洗净的实验操作是 。
(3)装置图中装置X的作用是 。
(4)以焙烧过的铜精炼炉渣为原料制备CuSO •5H O晶体时,请补充完整相应的实验方案:取一
4 2
定量焙烧过的铜精炼炉渣, ,加热浓缩、冷却结晶、过滤、晾干,得到CuSO •5H O晶体。
4 2
已知:①钒的氧化物在酸性条件下以VO
2
、VO2+存在;
已知该实验中pH=3.2时,Fe3+完全沉淀;pH=4.7时,Cu2+开始沉淀。
②“离子交换”和“洗脱"”过程可简单表示为4ROH+V 4 O 1 4 2 - 离 子 洗 交 脱 换 R 4 V 4 O 12 +4OH—。 实验中可选用的试剂:1.0mol•L﹣1H 2 SO 4 、1.0mol•L﹣1HCl、1.0mol•L﹣1NaOH。
(5)通过下列方法测定产品纯度:准确称取0.5000gCuSO •5H O样品,加适量水溶解,转移至碘
下列说法正确的是 4 2
量瓶中,加过量KI溶液并用稀H SO 酸化,以淀粉溶液为指示剂,用0.1000mol•L﹣1Na S O 标准
A.“氧化”过程中氧化剂与还原剂的物质的量之比为6∶1 2 4 2 2 3
溶液滴定至终点,消耗Na S O 的溶液19.80mL。
B.离子交换时应选择阳离子交换树脂 2 2 3
测定过程中发生下列反应:2Cu2++4I﹣═2CuI↓+I ;2S O 2﹣+I ═S O 2﹣+2I﹣
2 2 3 2 4 6
C.“中和”过程中,含钒离子发生反应的离子方程式为4VO+8OH—=V O4-+4H O
2 4 12 2
计算CuSO •5H O样品的纯度(写出计算过程): 。
4 2
D.为了提高洗脱效率,应选择强碱性淋洗液
第 4 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
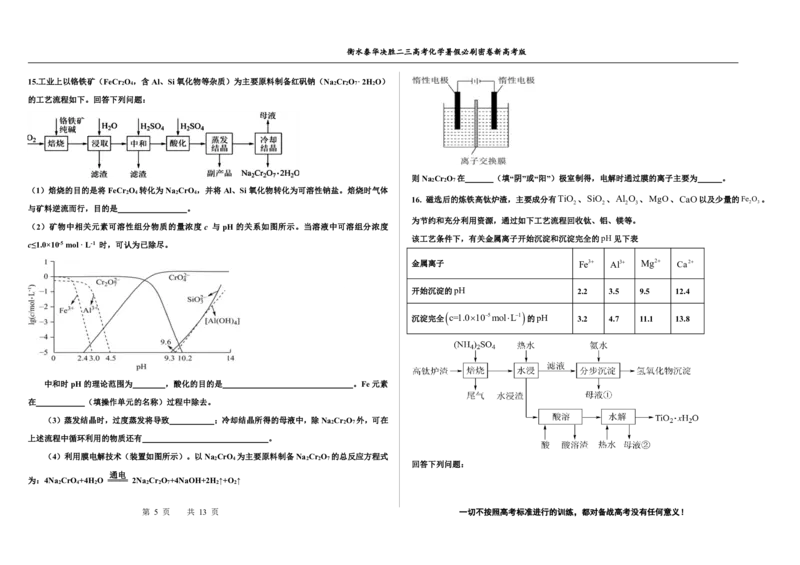
15.工业上以铬铁矿(FeCr O ,含Al、Si氧化物等杂质)为主要原料制备红矾钠(Na Cr O ·2H O)
2 4 2 2 7 2
的工艺流程如下。回答下列问题:
则Na Cr O 在 (填“阴”或“阳”)极室制得,电解时通过膜的离子主要为 。
2 2 7
(1)焙烧的目的是将FeCr O 转化为Na CrO ,并将Al、Si氧化物转化为可溶性钠盐。焙烧时气体
2 4 2 4
16. 磁选后的炼铁高钛炉渣,主要成分有TiO 、SiO 、Al O 、MgO、CaO以及少量的Fe O 。
2 2 2 3 2 3
与矿料逆流而行,目的是 。
为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
(2)矿物中相关元素可溶性组分物质的量浓度 c 与 pH 的关系如图所示。当溶液中可溶组分浓度
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
c≤1.0×10-5mol·L-1 时,可认为已除尽。
金属离子 Fe3 Al3 Mg2 Ca2
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全 c=1.0105molL1 的pH 3.2 4.7 11.1 13.8
中和时pH的理论范围为 ,酸化的目的是 。Fe元素
在 (填操作单元的名称)过程中除去。
(3)蒸发结晶时,过度蒸发将导致 ;冷却结晶所得的母液中,除Na Cr O 外,可在
2 2 7
上述流程中循环利用的物质还有 。
(4)利用膜电解技术(装置如图所示)。以Na CrO 为主要原料制备Na Cr O 的总反应方程式
2 4 2 2 7
回答下列问题:
通电
为:4Na CrO +4H O ===== 2Na Cr O +4NaOH+2H ↑+O ↑
2 4 2 2 2 7 2 2
第 5 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
(1)“焙烧”中,TiO 、SiO 几乎不发生反应,Al O 、MgO、CaO、Fe O 转化为相应的硫酸盐,
(2)“滤液②”中含有的金属离子是______________。
2 2 2 3 2 3
(3)“转化”中可替代H O 的物质是______________。若工艺流程改为先“调pH”后“转化”,即
2 2
写出Al O 转化为NH Al SO 的化学方程式_______。
2 3 4 4 2
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,依次析出的金属离子
是___。
,“滤液③”中可能含有的杂质离子为______________。
(3)“母液①"中Mg2+浓度为_______molL-1。
(4)“水浸渣”在160℃“酸溶”最适合的酸是_______。“酸溶渣”的成分是_______、_______。 (4)利用上述表格数据,计算Ni(OH) 的K =______________(列出计算式)。如果“转化”后的
2 sp
(5)“酸溶”后,将溶液适当稀释并加热,TiO2水解析出TiO xH O沉淀,该反应的离子方程式是 溶液中Ni2+浓度为1.0mol·L−1,则“调pH”应控制的pH范围是______________。
2 2
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该
_______。
反应的离子方程式______________。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得_______,循环利用。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是______________。
17.某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。
采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO ·7H O):
4 2
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ni2+ Al3+ Fe3+ Fe2+
开始沉淀时(c=0.01mol·L−1)的pH 7.2 3.7 2.2 7.5
沉淀完全时(c=1.0×10−5mol·L−1)的pH 8.7 4.7 3.2 9.0
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是______________。为回收金属,用稀硫酸将“滤液①”调
为中性,生成沉淀。写出该反应的离子方程式______________。
第 6 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
化学假期作业(十四)答题纸 (3)
(总分 57 分,除标注外,其余每空 2 分) (4)
姓名 学号 得分
(5)
14、(11分)
17、 (18分)
(1)
(1)
(2)
(2)
(3)
(3)
(4)
(4)
(5)
(5) (6)
(3分)
15、(14分)
(1)
(2)
(3)
(4)
16、(14分)
(1)
(2)
第 7 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷第十四套化学参考答案 B项,结晶后母液中主要成分为NaHSO ,不可能有NaHCO ,否则会发生反应NaHSO +NaHCO
3 3 3 3
=Na SO +CO +H O,错误;
1.答案:D 2 3 2 2
C项,气流干燥时,温度过高会使NaHSO 分解,正确;
解析:本题主要考查海水制备无水氯化镁的无机工艺流程。D项,煅烧后的产物中主要为MgO, 3
D项,中和时发生反应NaHSO +Na CO =NaHCO +Na SO ,正确。
MgO中加入稀盐酸后得到MgCl 溶液,但将MgCl 溶液加热蒸发后所得的产物为Mg(OH) ,不是无 3 2 3 3 2 3
2 2 2
4、【答案】C
水MgCl ,故D项错误;A项,苦卤水中加入物质X主要是将溶液中的镁元素转化为Mg(OH) 沉淀,
2 2
故物质X溶于水后应该显碱性,生石灰价格便宜且溶于水显碱性,故物质X常选用生石灰,故A项
A.用盐酸“洗脱”R
3
NBr生成HBr和R
3
NCl,R
3
NCl再生,继续用干“吸附”阶段反应,A正确;
正确;B项,镁的金属性强于铝,故选用电解法进行冶炼,制备镁可选用电解熔融MgCl
2
的方法,故
B.卤水“氧化”时Cl 与卤水反应置换出Br ,同时Cl 与H O反应生成HCl进入水相Ⅰ,“还原”时SO
2 2 2 2 2
B项正确;C项,煅烧后的产物中主要为MgO,氯化过程加入了碳与氯气反应后生成了MgCl 与CO,
2 与R N ClBr 反应生成H SO 、HBr、R NCl、R NCl再与HBr反应生成HCl和R NBr,故水相Ⅱ
3 2 2 4 3 3 3
高温
发生的反应为MgCCl MgCl CO
2 2 含HCl与H SO ,溶液呈酸性,B正确;
2 4
2.答案:D C.有机相Ⅰ中的R N ClBr 可氧化KI,进而使淀粉-KI试纸变蓝,C错误;
3 2
解析: D.在流程的“氧化”和“转化”阶段,两次都用到Cl ,制得80g即0.5mol Br 理论上消耗标准状况下的
2 2
Cl 22.4L,D正确;
2
故答案为:C。
5【答案】A
A.静电除尘的原理是使灰尘带电后在电场力的作用下奔向电极并吸附于电极上,可利用SO 烟气中
2
灰尘胶体粒子带电性加以清除,选项A正确;
B.S 、S 、S 和S 都为硫的不同单质,互为同素异形体,选项B错误;
2 4 6 8
C.脱硫塔中发生反应2CaS+3SO =2CaSO +3S, 则S为氧化产物和还原产物,CaSO 既不是氧化产
3.B 2 3 3
【解析】
物也不是还原产物,选项C错误;
A项,吸收过程中发生反应2SO +Na CO +H O=2NaHSO +CO ,所以吸收过程中有CO 气体
D.“再生塔”中C与CaSO
4
反应生成CO
2
和X,根据原子守恒、电子守恒规律及脱硫剂反复循环的信
2 2 3 2 3 2 2
生成,正确;
息,可判断X为CaS,选项D错误;
第 8 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
答案选A。 C.滤渣主要成分是硫单质,不能循环使用,故C错误;
6、【答案】B D.若水合肼浓度过大,水合肼与溶液中的铜离子反应生成铜,会导致氧化亚铜的产率降低,故D正
A.选项中的离子方程式没有配平,正确的离子方程式为: 确;
故选D。
CuNH
3
4
2+ +2OH- CuO+4NH
3
+H
2
O,故A错误;
8、【答案】C
B.“还原”步骤中Cu2+做氧化剂,和还原剂Na SO 反应,铜的化合价从+2价降低到+1价,S的化合 【分析】
2 3
价从+4价升高到+6价,发生反应的离子方程式为:2Cu2++SO2-+2Cl-+H O=2CuCl↓+SO2-+2H+,氧化 废铜泥灼烧后将金属元素转化为可溶液硫酸的氧化物,酸浸后先加H 2 O 2 氧化Fe2+,再加NaOH稀溶
3 2 4
液,过滤除去Fe(OH) ,往滤液中加入Na SO 、NaCl还原后经系列操作得到氯化亚铜产品。
剂与还原剂的物质的量之比为2∶1,故B正确; 3 2 3
【详解】
C.根据B选项中的离子方程式可知,反应后的溶液中存在大量的H+和SO2-,但不能存在大量的Cu+
4
A.根据流程信息,灼烧的目的是使含铜物质尽可能溶解在硫酸溶液中,所以是将CuS、Cu S等转化
2
和Cl-,故C错误;
为CuO,A正确;
D.CuCl虽然难溶于水,但潮湿时易被氧化,所以不能用水做洗涤剂,应该用乙醇洗涤,故D错误;
故选B。
B.除杂的目的是使铁元素转化成FeOH
3
而转化成滤渣,①H
2
O
2
目的是将Fe2转化成Fe3,②加
7、【答案】D NaOH稀溶液,调节溶液的pH,使Fe3转化成FeOH 沉淀,但只加入NaOH稀溶液容易形成FeOH
3 3
【分析】
胶体更难除杂,所以还应加热,B正确;
由题给流程可知,低品铜矿用稀硫酸、二氧化锰酸浸时,硫化铜与稀硫酸和二氧化锰反应生成硫酸铜、
C.还原反应同时生成H SO ,酸浸又消耗H SO ,所以H SO 可循环使用,但Na SO 没有参与循环,
2 4 2 4 2 4 2 3
硫酸锰、硫和水,氧化亚铁与与稀硫酸和二氧化锰反应生成硫酸铁、硫酸锰、硫和水,向反应后的溶
C错误
液中加入合适的试剂调节溶液pH,将铁离子转化为氢氧化铁沉淀,过滤得到含有硫、氢氧化铁的滤渣
和含有锰离子和铜离子的滤液;向滤液中加入合适的试剂将锰离子转化为沉淀,过滤得到锰渣和含有
D.还原中Cu2+被还原得到氯化亚铜,反应为2Cu2 2ClSO
3
2H
2
O=2CuCl SO2
4
2H,D正
铜离子的滤液;向滤液中加入水合肼将铜离子转化为氧化亚铜。 确;
【详解】 故选C。
A.酸浸过程中硫化铜发生的反应为硫化铜与稀硫酸和二氧化锰反应生成硫酸铜、硫酸锰、硫和水, 9、【答案】D
反应的离子方程式为CuS+MnO +4H+=Cu2++Mn2++S+2H O,故A错误; 【分析】
2 2
B.由分析可知,酸浸所得溶液中的阳离子主要有H+、Mn2+、Cu2+和Fe3+,故B错误; 在饱和NaCl溶液中先通入NH ,然后通入CO 气体,发生反应:
3 2
第 9 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
NaCl+H O+NH +CO =NaHCO ↓+NH Cl,过滤分离得到的固体1是NaHCO ,将固体1在煅烧炉中
2 3 2 3 4 3
Δ
加热,发生分解反应:2NaHCO Na CO +CO ↑+H O,得到纯碱和气体1是CO 气体;溶液1
3 2 3 2 2 2
中含有NaCl、NaHCO 、NH Cl;在冷却池中通入NH ,使溶液显碱性,同时增大了溶液中c(NH),
3 4 3 4
NH Cls NHaqClaq逆向移动;析出NH Cl固体可作氮肥;溶液2含有NaCl、Na CO 、
4 4 4 2 3
(NH ) CO 、NH Cl。在盐析池中加入NaCl,c(Cl-)增大,NH Cls NHaqClaq的平衡逆向
4 2 3 4 4 4
移动,NH Cl析出,析出盐后的溶液3循环回转到沉淀池中,再用于制取纯碱。
4
【详解】
A.根据上述分析可知气体1为CO ,气体2为NH ,A错误;
2 3
B.向冷析池中通入NH ,增大溶液中c(NH),便于析出盐NH Cl,此时溶液显碱性,因此溶液2中,
3 4 4
含碳微粒主要是CO2,B错误;
3
C.侯氏制碱法中Na+用于制取纯碱Na CO ,Cl-用于制取NH Cl,NH Cl可作氮肥,也可用于金属加
2 3 4 4
工除锈等,原子利用率较高;而索尔维法制取纯碱时,反应产生的CaCl 作为废液排出,原子利用率
2
大大降低,故侯氏制碱法中原料NaCl的原子利用率比索尔维制碱法中原料NaCl的原子利用率高,C
错误;
D.盐析池中加入NaCl固体,增大了溶液中c(Cl-)增大,使盐NH Cl的溶解结晶平衡
4
11
NH Cls NHaqClaq逆向移动,从而使NH Cl结晶析出,D正确;
4 4 4 12
故合理选项是D。
10
第 10 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
换树脂,故B错误;
C.“中和”过程中,将铁离子沉淀,而含钒离子发生反应的离子方程式为4VO+8OH-=V O4-+4H O,
2 4 12 2
故C正确;
D.根据4ROH+V 4 O 1 4 2 - 离 子 洗 交 脱 换 R 4 V 4 O 12 +4OH-,为了提高洗脱效率,应选择强碱性淋洗液,故D
正确。
综上所述,答案为CD。
14、
13、【答案】CD
【分析】
废钒催化剂(主要成分为V O 、V O 、K SO 、SiO 、Fe O )加入稀硫酸,二氧化硅不反应,V O 、
2 5 2 4 2 4 2 2 3 2 5
V O 、Fe O 和稀硫酸反应,生成VOSO ,加入氯酸钾,VO2+被氧化,再加入KOH将铁离子沉淀,
2 4 2 3 4
VO 2 变为V 4 O 1 4 2 -,根据信息用离子交换膜交换得到R 4 V 4 O 12 ,再洗脱得到V 4 O 1 4 2 -,再加入氯化铵沉淀 15. 【答案】
煅烧,最终得到V O 。 (1) 为使气体和铬铁矿充分混合,反应物充分反应。
2 5
【详解】 (2)4.5 到 9.3;将铬元素由 CrO 2-转变成目标产物红矾钠的 Cr O 2-。(或将 Na CrO 转变成
4 2 7 2 4
A.“氧化”过程中主要是VO2+和ClO发生氧化还原反应,ClO化合价降低到Cl-,降低6个,VO2+ Na 2 Cr 2 O 7 。);浸取
3 3
(3)目标产物红矾钠失去结晶水;硫酸
化合价升高到VO,升高1个,因此氧化剂与还原剂的物质的量之比为1∶6;故A错误;
2
(4)阳极;Na+
B.根据离子交换表示为4ROH+V 4 O 1 4 2 - 离 子 洗 交 脱 换 R 4 V 4 O 12 +4OH-,因此离子交换时应选择阴离子交 【解析】
第 11 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
工业生产为了使原料充分利用,采用的方法之一是逆流原理,其目的就是使得反应物之间充分混 (1)由题意可知,“烧培”中加入NH SO ,Al O 转化为 NH AlSO ,故其化学方程式为
4 2 4 2 3 4 4 2
合,反应充分。所以焙烧时气体与矿料逆流而行,目的是为使气体和铬铁矿充分混合,反应物充分反
焙烧
Al O 4NH SO NH AlSO 6NH 3H O。
应。 2 3 4 2 4 4 4 2 3 2
中和时时的目的是为了将Al、Si的可溶性盐转变成沉淀,且Al元素不以铝离子形式再次溶解,
(2)由题意知,焙烧”中,TiO 、SiO 几乎不发生反应,Al O 、MgO、CaO、Fe O 转化为相应的硫
2 2 2 3 2 3
所以中和时pH的理论范围为4.5到9.3。
酸盐,即水浸后滤液含Fe3、Al3、Mg2、Ca2,其pH约为2.0;故根据沉淀表格可知,在“分步沉淀”
焙烧的目的是将FeCr O 转化为Na CrO ,而目标产物红矾钠是Na Cr O ,所以酸化的目的是将
2 4 2 4 2 2 7
铬元素由CrO 2-转变成目标产物红矾钠的Cr O 2-。(或将Na CrO 转变成Na Cr O 。)
时用氨水逐步调节pH至11.6,依次析出的金属离子是Fe3、Al3、Mg2 。
4 2 7 2 4 2 2 7
铁元素再加入纯碱焙烧时,铁的氧化物难溶于水,在浸取中以滤渣形式分离出去。 (3)pH=11时,Mg2恰好完全沉淀,Mg(OH) 的K c Mg2 c2 OH 1105 102.92 1010.8,
2 sp
蒸发结晶得到的是红矾钠(Na Cr O ·2H O),晶体中含结晶水。如果过度蒸发,晶体受热失去
2 2 7 2
结晶水。生产过程中加入的硫酸与Na 2 CrO 4 ,Al、Si的可溶性钠盐反应时,得到副产物硫酸盐(硫酸 第(2)问中调节后的pH=11.6,此时c Mg2 c2 K O s H p 1 1 0 0 2 1 . 0 4 .8 2 106 。
钠)。之后硫酸酸化,所以母液中的硫酸为可循环利用的物质。
(4)“水浸渣”为CaSO 、SiO 、TiO ,而最后的水解产物只含TiO xH O,故在160℃“酸溶”只溶解
4 2 2 2 2
电解时阳极氢氧根放电,产生氧气,阳极区剩余的氢离子使CrO 2-转变成Cr O 2-,所以重铬酸钠
4 2 7 了TiO ,则最适合的酸是H SO ;CaSO 、SiO 不溶于H SO ,故“酸溶渣”的成分是CaSO 、SiO 。
2 2 4 4 2 2 4 4 2
在阳极产生。阴极区氢离子放电得到H ,溶液中存在OH-离子。Na+通过离子交换膜,转移到阴极区
2 (5)“酸溶”后,将溶液适当稀释并加热,TiO2水解析出TiO xH O沉淀,该反应的离子方程式是:
2 2
得到产物氢氧化钠。
TiO2 (x1)H OTiO xH O2H 。
2 2 2
16.答案:(1)Al O 4NH SO 2NH AlSO 3H O6NH
2 3 4 4 4 4 2 2 3
(6)由流程图可知,母液①为NH SO ,母液②为H SO ,将“母液①”和“母液②”混合,吸收尾
4 2 4 2 4
(2)Fe3、Al3+、Mg3
气NH ,经处理得NH SO ,因此可以循环利用的为NH SO 。
3 4 2 4 4 2 4
(3)106
17.
(4)H SO ;SiO ;CaSO
2 4 2 4
△ (1)除去油脂,溶解铝及其氧化物 Al(OH) 4 +H+=Al(OH) 3 ↓+H 2 O
(5)TiO2 (x1)H O TiO xH O2H
2 2 2
(2)Ni2+、Fe2+、Fe3+
(6)NH SO (3)O 2 或空气 Fe3+
4 2 4
(4)0.01×(107.2−14)2[或10−5×(108.7−14)2] 3.2~6.2
解析:本题主要考查常见无机物的制备。
(5)2Ni2++ClO−+4OH−=2NiOOH↓+Cl−+H O
2
第 12 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
(6)提高镍回收率
第( )套化学暑假必刷密卷专用反思表
填表时间:2022 年__月___日,__:__;反思人:___________家长签字:_____________
本套暴露的主要问题
板块 该板块失分 对每一分失分的原因反思
单项选 总分 27 分
择题 丢了( )分
双选题 总分 16 分
丢了( )分
主观题 总分 57 分
丢了( )分
本套题的主要收获
知识上
的收获
技巧上
的收获
本套题的综合反思
做题状
态
做题结
果
自我提
醒
第 13 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!