文档内容
衡水泰华决胜二三高考化学暑假必刷密卷新高考版
B.W的简单离子半径一定大于X的简单离子半径
衡水泰华中学决胜高考化学暑假必刷密卷
第16套
C.W的最高正价和最低负价的代数和为0 D.Z的单质的水溶液具有漂白性
组编人:汪志新
做题时间:2022年 月 日, : —— :
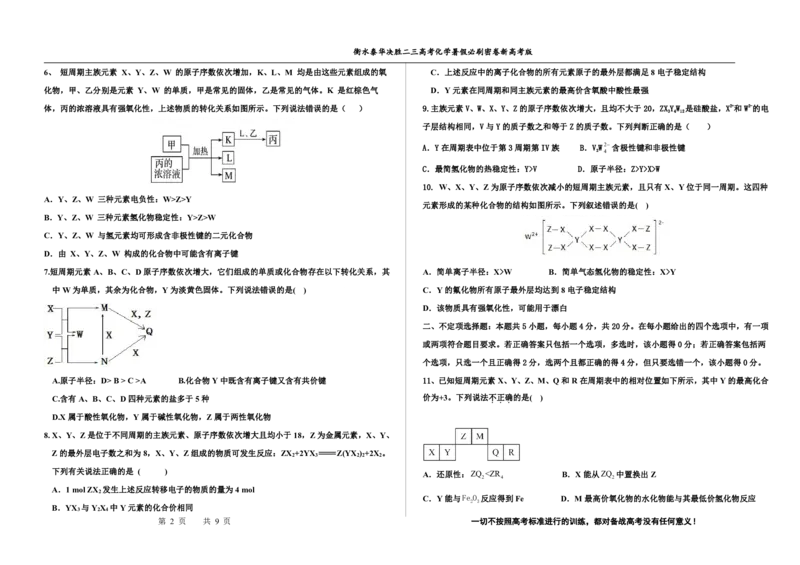
3.《Nature》杂志评选出的2019年世界十大科技进展之一是我国科研人员发现用于“点击化学”的
校对人:于洪强
实际得分: 家长签字(严禁代签):
审核人: 一种新化合物(如图所示),W、X、Y、Z为短周期主族元素且原子序数依次增大,Y原子的最
外层电子数与W原子的核外电子总数相等,X、Z同主族。下列说法正确的是( )
励志格言:现在的每一滴汗水、每一份付出,都会交织成那绚丽的双翼,在六月破茧 A. 原子半径:Z>X>Y
而出,在梦想的舞台上绽放异彩。
B. 四种元素中,最高价含氧酸酸性最强的为Y
本套亮点:汇集元素周期律、周期表、化学键各地最新模拟题,有基础考查题,也有
新颖且有思维量的题目,充分利用,定能查漏补缺,收获满满。 C. 最简单氢化物的沸点:W>X
注意事项: D. 最简单氢化物的稳定性:W>X>Y
1、本套密卷满分 100 分,做题所需时间75分钟; 4. 四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X
2、请一律用 0.5 或以上的黑色中性签字笔在规定的答题纸上做答,注意书写规范;
3、做题不改错,等于没有做!做完之后,要求依照答案用红笔自判所有主客观题,
的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y
并算出总得分,请家长签字确认,并在积累本进行认真的错题整改反思,并把本套题 同族,Z与X形成的离子化合物的水溶液呈中性。下列说法正确的是( )
的主要收获、主要不足和反思写到每套题所附的反思纸上,开学上交。
A.简单离子半径:WZ
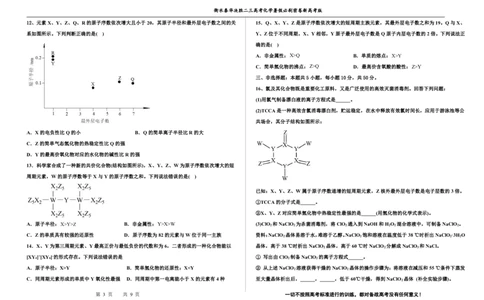
1.短周期元素X、Y、Z、W在元素周期表中的相对位置如右图所示,其中W原子的质子数是其
最外层电子数的三倍。下列说法不正确的是( ) 5.X、Y、Z、W为原子序数依次增大的短周期主族元素,只有W为金属元素。甲、乙、丙分别为
A.原子半径:W>Z>Y>X X、Z、W三种元素所对应的单质。A、B、C、D均为由X、Y、Z三种元素组成的化合物,化
B.最高价氧化物对应水化物的酸性:X>W>Z 合物B的稀溶液常用于保存动物标本。它们的转化关系如图所示。下列说法错误的是( )
C.最简单气态氢化物的热稳定性:Y>X>W>Z
D.元素X、Z、W的最高化合价分别与其主族序数相等
2.短周期主族元素W、X、Y、Z的原子序数依次增大,W、X同主族。Y原子的最外层电子数
等于X原子的电子总数,Z原子的电子总数等于W、X、Y三种原子的电子数之和,Z的最高
价氧化物对应水化物的化学式为H ZO 。W、X、Y三种元素形成的一种化合物的结构如图所
n 2n+2
示。下列说法错误的是( )
A.X与Z可组成非极性分子 B.原子半径大小关系是:r(X)<r(Z)<r(Y)<r(W)
C.四种化合物中B的沸点最低 D.四种化合物中Y原子的杂化方式有2种
A.Y的最高价氧化物对应的水化物属于弱碱
第 1 页 共 9 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
6、 短周期主族元素 X、Y、Z、W 的原子序数依次增加,K、L、M 均是由这些元素组成的氧 C.上述反应中的离子化合物的所有元素原子的最外层都满足8电子稳定结构
化物,甲、乙分别是元素 Y、W 的单质,甲是常见的固体,乙是常见的气体。K 是红棕色气 D.Y元素在同周期和同主族元素的最高价含氧酸中酸性最强
体,丙的浓溶液具有强氧化性,上述物质的转化关系如图所示。下列说法错误的是( ) 9.主族元素V、W、X、Y、Z的原子序数依次增大,且均不大于20,ZXYW 是硅酸盐,X2+和W2-的电
3 4 12
子层结构相同,V与Y的质子数之和等于Z的质子数。下列判断正确的是( )
A.Y在周期表中位于第3周期第IV族 B.VW2含极性键和非极性键
2 4
C.最简氢化物的热稳定性:Y>V D.原子半径:Z>Y>X>W
10. W、X、Y、Z为原子序数依次减小的短周期主族元素,且只有X、Y位于同一周期。这四种
A.Y、Z、W 三种元素电负性:W>Z>Y
元素形成的某种化合物的结构如图所示。下列叙述错误的是( )
B.Y、Z、W 三种元素氢化物稳定性:Y>Z>W
C.Y、Z、W 与氢元素均可形成含非极性键的二元化合物
D.由 X、Y、Z、W 构成的化合物中可能含有离子键
7.短周期元素A、B、C、D原子序数依次增大,它们组成的单质或化合物存在以下转化关系,其 A.简单离子半径:X>W B.简单气态氢化物的稳定性:X>Y
中W为单质,其余为化合物,Y为淡黄色固体。下列说法错误的是( ) C.Y的氟化物所有原子最外层均达到8电子稳定结构
D.该物质具有强氧化性,可能用于漂白
二、不定项选择题:本题共5小题,每小题4分,共20分。在每小题给出的四个选项中,有一项
或两项符合题目要求。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两
个选项,只选一个且正确得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
A.原子半径:D>B>C>A B.化合物Y中既含有离子键又含有共价键 11、已知短周期元素X、Y、Z、M、Q和R在周期表中的相对位置如下所示,其中Y的最高化合
C.含有A、B、C、D四种元素的盐多于5种 价为+3。下列说法不 . 正 . 确 . 的是( )
D.X属于酸性氧化物,Y属于碱性氧化物,Z属于两性氧化物
8.X、Y、Z是位于不同周期的主族元素、原子序数依次增大且均小于18,Z为金属元素,X、Y、
Z的最外层电子数之和为8,X、Y、Z组成的物质可发生反应:ZX +2YX Z(YX ) +2X 。
2 3 2 2 2
下列有关说法正确的是 ( ) A.还原性:ZQ Q B.单质的熔点:X>Y
C.简单氢化物的沸点:Z>Q D.最高价含氧酸的酸性:Z>Y
三、非选择题:本题共5小题,每小题10分,共50分。
16、氯及其化合物既是重要化工原料,又是广泛使用的高效灭菌消毒剂。回答下列问题:
(1)用氯气制备漂白液的离子方程式是______。
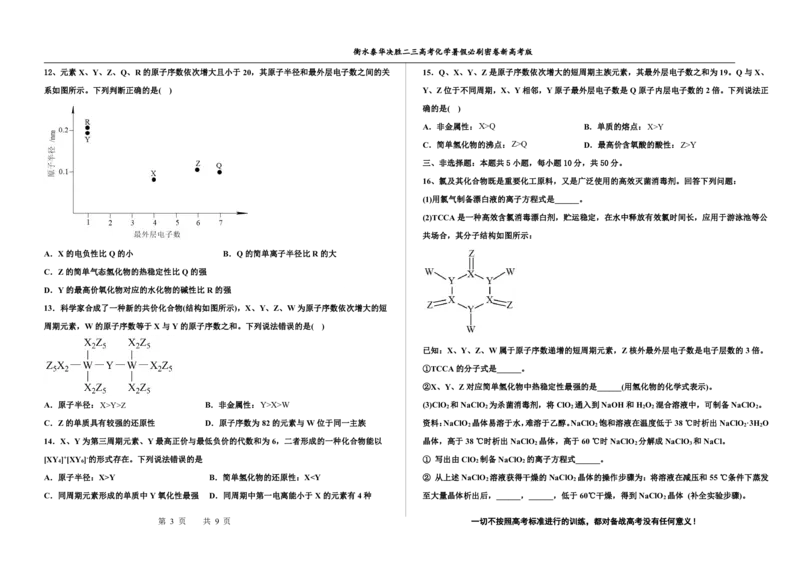
(2)TCCA是一种高效含氯消毒漂白剂,贮运稳定,在水中释放有效氯时间长,应用于游泳池等公
共场合,其分子结构如图所示:
A.X的电负性比Q的小 B.Q的简单离子半径比R的大
C.Z的简单气态氢化物的热稳定性比Q的强
D.Y的最高价氧化物对应的水化物的碱性比R的强
13.科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数依次增大的短
周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是( )
已知:X、Y、Z、W属于原子序数递增的短周期元素,Z核外最外层电子数是电子层数的3倍。
①TCCA的分子式是______。
②X、Y、Z对应简单氢化物中热稳定性最强的是______(用氢化物的化学式表示)。
A.原子半径:X>Y>Z B.非金属性:Y>X>W (3)ClO 和NaClO 为杀菌消毒剂,将ClO 通入到NaOH和H O 混合溶液中,可制备NaClO 。
2 2 2 2 2 2
C.Z的单质具有较强的还原性 D.原子序数为82的元素与W位于同一主族 资料:NaClO 晶体易溶于水,难溶于乙醇。NaClO 饱和溶液在温度低于38℃时析出NaClO ·3H O
2 2 2 2
14.X、Y为第三周期元素、Y最高正价与最低负价的代数和为6,二者形成的一种化合物能以 晶体,高于38℃时析出NaClO 晶体,高于60℃时NaClO 分解成NaClO 和NaCl。
2 2 3
[XY ]+[XY ]-的形式存在。下列说法错误的是 ① 写出由ClO 制备NaClO 的离子方程式______。
4 6 2 2
A.原子半径:X>Y B.简单氢化物的还原性:X_______(填化学式)。
期,A、D同主族,A为短周期原子半径最小的元素,M原子最外层电子数为次外层的3倍,A、 (5)由下列元素形成的化合物中含有离子键的是_______。
M常温下能形成两种液态化合物A M和A M ,E元素的周期数与主族序数相等。请用化学用语 A.①③ B.②③ C.①④ D.⑥⑨
2 2 2
回答下列问题: (6)写出⑤在空气中燃烧产物的电子式_______。
(1)B元素在周期表中的位置为_________;由A、M、D三种元素组成的化合物中含有的化学键为
_________;A M分子的空间结构为_________;
2
(2)用电子式表示D M的形成过程_________
2
第 4 页 共 9 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
20.铋元素位于第六周期VA族,常用于治疗胃病的药物中,也广泛用于合金制造、冶金工业、半
导体工业、核工业中。
(1)画出铋元素最外层电子的电子排布式_______,该元素的原子核外共有_______个未成对电子。
(2)铅铋合金被用于核反应堆的导热剂,判断:该合金的熔点_______金属铋的熔点(填“大于”、“小
于”、“等于”、“无法确定”)。
(3)请尝试画出BiH 的电子式_______。推测以下说法正确的是_______。
3
A.BiH 是非极性分子 B.热稳定性:NH >BiH
3 3 3
C.酸性HBiO >HNO D.原子半径r(Bi)______(1分)。
②______(1分),______(1分)。 (5)_______(1分)。
17、 (6)_______(1分)。
(1)___________(1分)。 20、
(2)___________(1分)。 (1)_______(1分),_______(1分)
(3)___________(2分)。 (2)_______(1分)
(4)___________(1分)。 (3)_______(1分)。_______(2分)。
(5)___________(2分): ___________(1分)。 (4)_____________________________________(2分)。
(6)________________________________________________(2分)。 (5)_______BiO+_______Mn+_______H+→_______Bi3++_______MnO+______(2分)
3 4
18、
(1)_________(1分); __________________(1分); _________(1分);
(2)______________________________________(2分)。
(3)____________(1分) 。
(4)___________________________________(2分)。
(5)___________(2分)。
第 6 页 共 9 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷第 16 套参考答案 解析:
11、根据短周期元素X、Y、Z、M、Q和R在周期表中的相对位置,以及Y的最高化合价为+3,
一、单项选择题 1——5 ABABA 6——10 BDDBC
可推知,X为:Mg,Y为:Al,Z为:C,M为:N,Q为:S,R为:Cl,据此分析答题。
二、不定项选择题 11——15 A AB C BD D A.ZQ 为:CS ,ZR 为:CCl ,CS 中硫的还原性强于CCl 中的氯元素,A错误;
2 2 4 4 2 4
点燃
16、Cl 2 +2OH-=Cl-+ClO-+H 2 O C 3 N 3 O 3 Cl 3 H 2 O 2ClO 2 +H 2 O 2 +2OH- =2ClO 2 +O 2 +
B.Mg和CO
2
发生下述反应:
2Mg+CO 2 = 2MgO+C
,B正确;
2H 2 O 趁热过滤(或高于38℃过滤) 乙醇洗涤 C.Al和Fe 2 O 3 发生铝热反应如下: 2Al+Fe O 高 = 温 Al O +2Fe ,C正确;
2 3 2 3
17、 (1)Ar (2)KOH (3)K+>Ca2+>Mg2+
D.M为:N,N的最高价氧化物的水化物为:HNO ,最低价氢化物为:NH ,二者发生如下反
3 3
(4)H O或者H O (5) 黄色 (6)Al O +2OH-=2AlO-+H O
2 2 2 2 3 2 2
应:HNO NH NH NO ,D正确;
3 3 4 3
18、
12、X、Y、Z、Q、R的原子序数依次增大且小于20,由图像中最外层电子数和原子半径的关系
(1) 第二周期第IVA族 离子键、(极性)共价键 V形(或写角形)
可知,X为C、Y为Na、Z为S、Q为Cl、R为K。
(2) (3)O2-> Na+> Al3+
A.C的电负性比Cl的小,故A正确;
(4)Cu+2H++H 2 O 2 =Cu2++2H 2 O (5)5.6 B.核外电子数相同时质子数越大半径越小,故Q的简单离子半径比R的大,故B正确;
19、(1) 硫 第三周期第ⅥA族
C.同周期元素,原子序数越大非金属性越强,则简单氢化物更稳定,则Z的简单气态氢化物的
(2) Na 2Na O +2CO =2Na CO +O 、2Na O +2H O=4NaOH+O 热稳定性比Q的弱,故C错误;
2 2 2 2 3 2 2 2 2 2
D.同主族元素,原子序数越大金属性越强,则最高价氧化物对应水化物的碱性越强,则Y的最
(3)NaOH (4) HF HCl (5)D (6)
高价氧化物对应的水化物的碱性比R的弱,故D错误;
13、由共价化合物的结构可知,X、W形成4个共价键,Y形成2个共价键,Z形成1个共价键,
20、(1) 6s26p3 3 (2)小于 (3) B
X、Y、Z、W是原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和,
(4)BiF 为离子晶体,熔化破坏离子键,BrCl 为分子晶体,熔化破坏分子间作用力,离子键强于分
则X为C元素、Y为O元素、Z为F元素、W为Si元素。
3 3
子间力,因此BiF 的熔点高于BrCl
A.同周期元素,从左到右原子半径依次减小,则C、O、F的原子半径大小顺序为C>O>F;
3 3
B.同周期元素,从左到右元素的非金属性依次增强,同主族元素,从上到下元素的非金属性依次
(5) 减弱,则C、O、Si的非金属性强弱顺序为O>C>Si,故B正确;
C.位于元素周期表右上角的氟元素的非金属性最强,单质具有很强的氧化性,故C错误;
第 7 页 共 9 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
D.原子序数为82的元素为铅元素,与硅元素都位于元素周期表ⅣA族,故D正确; Z为Cl或S或P,其简单氢化物为HCl或H S或PH ,由于前者物质中存在分子间氢键,而后者
2 3
14、Y位于第三周期,且最高正价与最低负价的代数和为6,则Y是Cl元素,由X、Y形成的阴 物质中不存在,故沸点Q>Z,C错误;
离子和阳离子知,X与Y容易形成共价键,根据化合物的形式知X是P元素。 D.元素的非金属性越强,其最高价含氧酸的酸性越强,P、S、Cl的非金属性均强于Si,因此最
A.P与Cl在同一周期,则P半径大,即X>Y,A项符合题意; 高价含氧酸酸性:Z>Y,D正确;
B.两者对应的简单氢化物分别是PH 和HCl,半径是P3->Cl-,所以PH 的失电子能力强,还原 16、根据TCCA分子结构,X、Y、Z、W属于原子序数递增的短周期元素,根据结构得到X为C,
3 3
性强,即X>Y,B项不符合题意; Y为N,Z核外最外层电子数是电子层数的3倍,则Z为O,W为Cl
C.同周期元素从左往右,金属性减弱, (1)用氯气制备漂白液是氯气通入到NaOH溶液中生成NaCl、NaClO和H O,其离子方程式是
2
非金属性增强,各元素对应的金属单质还原性减弱,非金属单质的氧化性增强,所以Cl 的氧化性 Cl +2OH-=Cl-+ClO-+H O。
2 2 2
最强,C项不符合题意; (2)①根据图中结构和前面分析得到TCCA的分子式是C N O Cl ;故答案为:C N O Cl 。
3 3 3 3 3 3 3 3
D.同一周期,从左到右,第一电离能呈现增大的趋势,第VA族元素的第一电离能大于相邻元素 ②根据前面分析及同周期从左到右非金属性逐渐增强,其简单气态氢化物稳定性逐渐增强,因此X、
的第一电离能;所以第三周期第一电离能从小到大依次为Na、Al、Mg、Si、S、P、Cl,所以有5 Y、Z对应简单氢化物中热稳定性最强的是H O;
2
种,D项符合题意; (3)①将ClO 通入到NaOH和H O 混合溶液中,可制备NaClO ,因此ClO 制备NaClO 的离子
2 2 2 2 2 2
15、Q、X、Y、Z为原子序数依次增大的短周期主族元素,Q与X、Y、Z不在同一周期,Y原子 方程式2ClO +H O +2OH- =2ClO+O +2H O;
2 2 2 2 2 2
最外层电子数为Q元原子内层电子数的2倍,则Q应为第二周期元素,X、Y、Z位于第三周期,
②根据题意,由于NaClO 饱和溶液在温度低于38℃时析出NaClO ·3H O晶体,高于38℃时析
2 2 2
Y的最外层电子数为4,则Y为Si元素,X、Y相邻,且X的原子序数小于Y,则X为Al元素,
出NaClO 晶体,高于60℃时NaClO 分解成NaClO 和NaCl,NaClO 晶体易溶于水,难溶于乙
2 2 3 2
Q、X、Y、Z的最外层电子数之和为19,则Q、Z的最外层电子数之和为19-3-4=12,主族元素的
醇;因此需在温度高于38℃过滤,用乙醇洗涤,低于60℃干燥,得到NaClO 晶体;
2
最外层电子数最多为7,若Q的最外层电子数为7,为F元素,Z的最外层电子数为5,为P元素,
17、由题干元素周期表的部分结构可知,①②③④⑤⑥⑦⑧⑨⑩分别为Na、K、Mg、Ca、Al、C、
若Q的最外层电子数为6,为O元素,则Z的最外层电子数为6,为S元素,若Q的最外层电子
O、Cl、Br和Ar等十种元素,据此分析解题。
数为5,为N元素,Z的最外层电子数为7,为Cl元素;综上所述,Q为N或O或F,X为Al,
(1)由分析可知,10种元素中,化学性质最不活泼的是Ar;
Y为Si,Z为Cl或S或P,据此分析解题。
(2)已知元素最高价氧化物对应的水化物的碱性与其金属性一致,故元素对应的最高价氧化物水化
A.X为Al,Q为N或O或F,同一周期从左往右元素非金属性依次增强,同一主族从上往下依
物中碱性最强的是KOH;
次减弱,故非金属性:Q>X,A错误;
(3)由分析可知,②③④三种元素分别为:K、Mg、Ca,故形成的离子中,离子半径由大到小的顺
B.由分析可知,X为Al属于金属晶体,Y为Si属于原子晶体或共价晶体,故单质熔点Si>Al,
序是K+>Ca2+>Mg2+;
即Y>X,B错误;
(4)由分析可知,元素⑦为O,故其的氢化物的化学式为H O或者H O ,故答案为:H O或者H O ;
2 2 2 2 2 2
C.含有氢键的物质沸点升高,由分析可知Q为N或O或F,其简单氢化物为H O或NH 或HF,
2 3
第 8 页 共 9 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
(5)由分析可知,①和⑨两元素分别为Na、Br,故其形成化合物的电子式为: ,该
(3)元素金属性越强,其最高价氧化物的水化物碱性越强,同周期元素随着核电荷数增大金属性减
弱,则⑤⑥⑦三种元素所形成的最高价氧化物对应的水化物碱性最强的是NaOH;
化合物中含有Na元素,Na的焰色反应是黄色,故答案为: ;黄色;
(4)非金属性F大于Cl,④与⑨的气态氢化物的稳定性为HF>HCl;
(6)由分析可知,⑤为Al,故反应的离子方程式为:Al 2 O 3 +2OH-=2AlO- 2 +H 2 O。 (5)A.①和③可形成HCl,只含共价键,A错误;
18、A为短周期原子半径最小的元素,A为H;M原子最外层电子数为次外层的3倍,则M为O; B.②和③可形成碳的氧化物,只含共价键,B错误;
常温下A、M能形成两种液态化合物A M和A M ,该液态化合物分别为H O和H O ;A、D同 C.①和④可形成HF,只含共价键,C错误; D.⑥和⑨可形成氯化镁,只含离子键,D正确;
2 2 2 2 2 2
主族,则D为Na元素;E元素的周期序数与主族序数相等,且E的原子序数最大,E应为第三
(6)钠在空气中燃烧生成过氧化钠,电子式为: 。
周期第ⅢA族元素,故E为Al元素;A、B、C、D、E为短周期元素,且原子序数依次增大,质
20、(1) 铋元素位于第六周期VA族,第6层有5个电子,铋元素最外层电子的电子排布式为6s26p3,
子数之和为39,设B的原子序数为x,则有1+x+8+11+13=39,x=6,所以B为碳元素;
(1)B元素的原子序数为6,K、L层依次排有2、4个电子,则在周期表中的位置为第二周期ⅣA
价电子轨道表示式为 ,该元素的原子核外共有3个未成对电子。
族;A、M、D三种元素组成的化合物为NaOH,钠离子与氢氧根间以离子键结合,氢氧根中氧原
(2)合金熔点低于成分金属的熔点,铅铋合金被用于核反应堆的导热剂。
子和氢原子以极性共价键结合;H O分子的空间结构为V形。
2
(2)D 2 M为Na 2 O,Na 2 O为离子化合物,用电子式表示其形成过程为: (3) BiH 是共价化合物,BiH 的电子式 。
3 3
。
A.BiH 中Bi价电子对数是4,有1个孤电子对,空间构型为三角锥形,是极性分子,故A错误;
(3)Na+、Al3+、O2-电子层结构相同,质子数越多,离子半径越小,所以离子半径从大到小的顺序为: 3
B.同主族元素从上到下,非金属性减弱,气态氢化物稳定性减弱,热稳定性:NH >BiH 。
O2-> Na+> Al3+。 3 3
C.同主族元素从上到下,非金属性减弱,最高价含氧酸的酸性减弱,酸性HBiO r(P),故D错误;
(5)根据反应NaH+H O=NaOH+H ↑,0.1molNaH与水反应生成NaOH、H 物质的量都为0.1mol,
2 2 2
(4)BiF 为离子晶体,熔化破坏离子键,BrCl 为分子晶体,熔化破坏分子间作用力,离子键强于
根据反应2NaOH+2Al+2H O=2NaAlO +3H ↑,0.1molNaOH与0.1molAl恰好完全反应生成 3 3
2 2 2
分子间力,因此BiF 的熔点高于BrCl ;
0.15molH ,则n(H )=0.1mol+0.15mol=0.25mol, V(H )=0.25mol×22.4L/mol=5.6L。 3 3
2 2 2
19、元素在周期表的位置可知,①~⑨分别为H、C、O、F、Na、Mg、Al、S、Cl,以分析答题。
(5)电荷守恒,配平离子方程式为7BiO
3
+2Mn+26H+→7Bi3++2MnO
4
+13H
2
O,并用单线桥标出电
(1)⑧所对应的元素名称为硫,其在周期表中的位置为第三周期第ⅥA族;
子转移的方向和数目为 。
(2)在①—⑨元素中,原子半径最大的是Na;其某种氧化物可用于呼吸面具中氧气来源,则该氧化
物为过氧化钠,反应的化学方程式为:2Na O +2CO =2Na CO +O 、2Na O +2H O=4NaOH+O ;
2 2 2 2 3 2 2 2 2 2
第 9 页 共 9 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!