文档内容
衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷 第 5 套 Ba2++2OH-+2H++SO2
=BaSO ↓+2H O
4 4 2
组编人:张莹莹
做题时间:2022 年__月___日,__:__—__:__ 校对人: 张云暖 3.(2022·全国乙卷)某白色粉末样品,可能含有Na SO 、Na SO 、Na S O 和Na CO 。取少量样
2 4 2 3 2 2 3 2 3
审核人:王立明
实际得分:____家长签字(严禁代签):______ 品进行如下实验:
①溶于水,得到无色透明溶液
励志格言:人生的旅途,前途很远,也很暗。然而不要怕,不怕的人的面前才有路。
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
——鲁迅
本套亮点:汇集非金属元素各地最新模拟题,考察了离子共存,方程式书写,离子浓度计
③取②的上层清液,向其中滴加BaCl 溶液有沉淀生成。
2
算等高考常见知识点。
注意事项: 该样品中确定存在的是
1, 本套密卷满分100分,做题所需时间75分钟;
2, 请一律用0.5或以上的黑色中性签字笔在规定的答题纸上做答,注意书写规范; A.Na SO、Na S O B.Na SO、Na S O
2 4 2 2 3 2 3 2 2 3
3,做题不改错,等于没有做!做完之后,要求依照答案用红笔自判所有主客观题,并算
C.Na SO 、Na CO D.Na SO、Na CO
出总得分,请家长签字确认,并在积累本进行认真的错题整改反思,并把本套题的主要收 2 4 2 3 2 3 2 3
获、主要不足和反思写到每套题所附的反思纸上,开学上交。 4、(2021山东卷) 下列由实验现象所得结论错误的是
一、单项选择题本题共9小题,每小题3分,共27分。在每小题给出的四个选项中,只有一项是符合
题目要求的。 A. 向NaHSO 3 溶液中滴加氢硫酸,产生淡黄色沉淀,证明HSO 3 具有氧化性
1、(2019江苏)室温下,下列各组离子在指定溶液中能大量共存的是( ) B. 向酸性KMnO 溶液中加入Fe O 粉末,紫色褪去,证明Fe O 中含Fe(Ⅱ)
4 3 4 3 4
A.0.1mol·L-1NaOH溶液:Na+、K+、CO2
3
-、AlO-
2 C. 向浓HNO 中插入红热的炭,产生红棕色气体,证明炭可与浓HNO 反应生成NO
3 3 2
B.0.1mol·L-1FeCl
2
溶液:K+、Mg2+、SO2
4
-、MnO-
4 D. 向NaClO溶液中滴加酚酞试剂,先变红后褪色,证明NaClO在溶液中发生了水解反应
C.0.1mol·L-1K
2
CO
3
溶液:Na+、Ba2+、Cl-、OH- 5、(2021全国乙卷). 下列过程中的化学反应,相应的离子方程式正确的是
D.0.1mol·L-1H 2 SO 4 溶液:K+、NH+ 4 、NO- 3 、HSO- 3 A. 用碳酸钠溶液处理水垢中的硫酸钙:CO 3 2 CaSO 4 CaCO 3 SO2 4
2、(2022·全国甲卷)能正确表示下列反应的离子方程式为
B. 过量铁粉加入稀硝酸中:Fe4H NO Fe3 NO2H O
3 2
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
C 硫酸铝溶液中滴加少量氢氧化钾溶液:Al3 4OH AlO 2H O
. 2 2
B.明矾溶液与过量氨水混合:Al3++4NH +2H O=AlO+4NH
3 2 2 4
D. 氯化铜溶液中通入硫化氢:Cu2 S2 CuS
C.硅酸钠溶液中通入二氧化碳:SiO2 +CO +H O=HSiO+HCO
3 2 2 3 3
6.(2020新课标Ⅲ)对于下列实验,能正确描述其反应的离子方程式是
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:
2 4 4
A.用Na SO 溶液吸收少量Cl :3SO2- +Cl +H O=2HSO- +2Cl-+SO2-
2 3 2 3 2 2 3 4
第 1 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
B.向CaCl 溶液中通入CO :Ca2++H O+CO =CaCO ↓+2H+ A.该溶液中肯定不含Ba2+
2 2 2 2 3
C.向H O 溶液中滴加少量FeCl :2Fe3++H O =O ↑+2H++2Fe2+ B.若向该溶液中加入过量的稀硫酸,溶液中的阴离子会减少一种
2 2 3 2 2 2
D.同浓度同体积NH HSO 溶液与NaOH溶液混合:NH+ +OH-=NH ·H O C.若向该溶液中加入足量NaOH溶液,滤出沉淀,洗净灼烧后最多能得8.0g固体
4 4 4 3 2
D.该溶液中除水电离出的OH-、H+之外所含离子是Na+、Fe2+、SO2-、NO-
7.(2021湖南).对下列粒子组在溶液中能否大量共存的判断和分析均正确的是 4 3
二、不定项选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,有一项或两
粒子组 判断和分析 项符合题目要求。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,
只选一个且正确得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
不能大量共存,因发生反应:
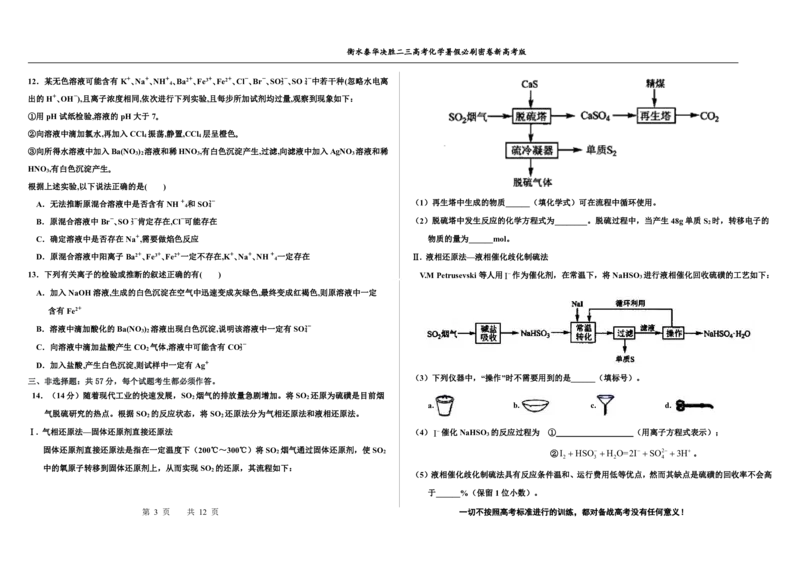
10、在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。
A Na、Al3、Cl、NH H O
3 2 Al3 4NH H O=AlO 4NH 2H O
3 2 2 4 2
不能大量共存,因发生反应:
B H、K、S
2
O
3
2、SO2
4
2H S O2=SSO H O
2 3 2 2
C Na、Fe3、SO2、H O 能大量共存,粒子间不反应
4 2 2
下列条件关于离子共存说法中正确的是( )
D H、Na、Cl、MnO 能大量共存,粒子间不反应
4 A.a点对应的溶液中不能大量存在:Fe3+、Na+、Cl-、SO2-
4
A.A B.B C.C D.D B.b点对应的溶液中大量存在:NH+ 4 、Ba2+、OH-、I-
8.有一无色溶液,可能含有Fe3+、K+、Al3+、Mg2+、NH+ 、Cl-、SO2-、HCO- 、MnO- 中的几种。为确定其
C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、HCO-
3
4 4 3 4
D.d点对应的溶液中大量存在:Na+、K+、SO2-、Cl-
3
成分,做如下实验:①取部分溶液,加入适量的Na O 固体,产生无色无味的气体和白色沉淀,再加入足量
2 2
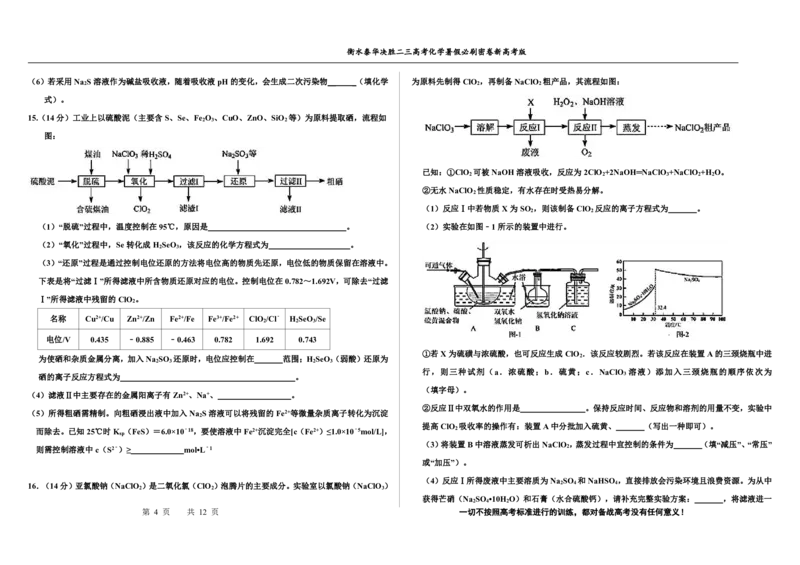
11、(2021山东卷) 实验室中利用固体KMnO 进行如图实验,下列说法错误的是
4
的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO 酸化的Ba(NO ) 溶液,有白色沉淀产
3 3 2
生。下列推断正确的是( )
A.肯定有Al3+、Mg2+、NH+ 、Cl- B.肯定有Al3+、Mg2+、HCO-
4 3
C.肯定有K+、HCO- 、MnO- D.肯定有Al3+、Mg2+、SO2-
3 4 4
9.某溶液中除水电离出的OH-、H+之外含Na+、Fe2+、Al3+、Ba2+、SO2-、NO- 、Cl-中的4 种,这4种离
4 3
A.G与H均为氧化产物 B. 实验中KMnO 只作氧化剂
4
子的物质的量均为0.1mol。若向该溶液中加入少量稀硫酸,无沉淀生成但有气泡产生。下列说法错误的
C.Mn元素至少参与了3个氧化还原反应 D.G与H的物质的量之和可能为0.25mol
是( )
第 2 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
12.某无色溶液可能含有K+、Na+、NH+ 、Ba2+、Fe3+、Fe2+、Cl-、Br-、SO2-、SO2-中若干种(忽略水电离
4 3 4
出的H+、OH-),且离子浓度相同,依次进行下列实验,且每步所加试剂均过量,观察到现象如下:
①用pH试纸检验,溶液的pH大于7。
②向溶液中滴加氯水,再加入CCl 振荡,静置,CCl 层呈橙色。
4 4
③向所得水溶液中加入Ba(NO ) 溶液和稀HNO ,有白色沉淀产生,过滤,向滤液中加入AgNO 溶液和稀
3 2 3 3
HNO ,有白色沉淀产生。
3
根据上述实验,以下说法正确的是( )
A.无法推断原混合溶液中是否含有NH+ 和SO2- (1)再生塔中生成的物质______(填化学式)可在流程中循环使用。
4 4
B.原混合溶液中Br-、SO2
3
-肯定存在,Cl-可能存在 (2)脱硫塔中发生反应的化学方程式为________。脱硫过程中,当产生48g单质S
2
时,转移电子的
C.确定溶液中是否存在Na+,需要做焰色反应 物质的量为______mol。
D.原混合溶液中阳离子Ba2+、Fe3+、Fe2+一定不存在,K+、Na+、NH+
4
一定存在 Ⅱ. 液相还原法—液相催化歧化制硫法
13.下列有关离子的检验或推断的叙述正确的有( ) V.MPetrusevski等人用I作为催化剂,在常温下,将NaHSO
3
进行液相催化回收硫磺的工艺如下:
A.加入NaOH溶液,生成的白色沉淀在空气中迅速变成灰绿色,最终变成红褐色,则原溶液中一定
含有Fe2+
B.溶液中滴加酸化的Ba(NO ) 溶液出现白色沉淀,说明该溶液中一定有SO2-
3 2 4
C.向溶液中滴加盐酸产生CO 气体,溶液中可能含有CO2-
2 3
D.加入盐酸,产生白色沉淀,则试样中一定有Ag+
三、非选择题:共57分,每个试题考生都必须作答。
(3)下列仪器中,“操作”时不需要用到的是______(填标号)。
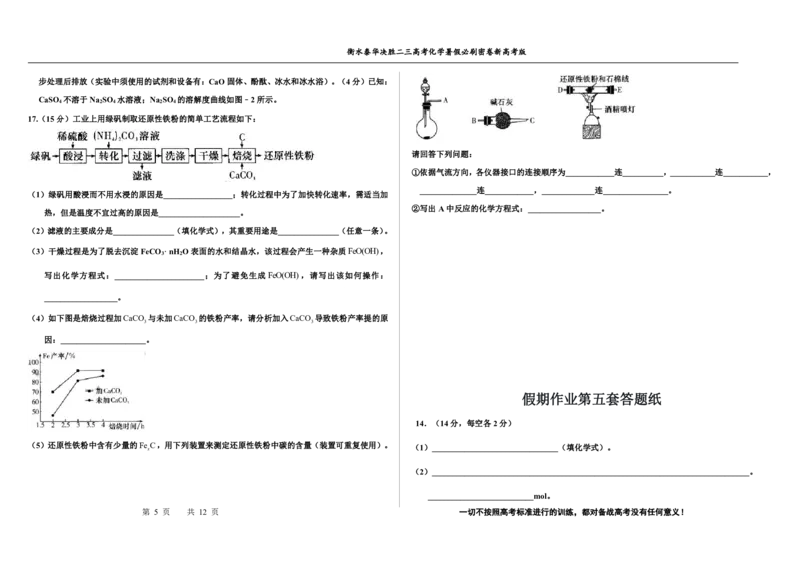
14.(14分)随着现代工业的快速发展,SO 烟气的排放量急剧增加。将SO 还原为硫磺是目前烟
2 2
a. b. c. d.
气脱硫研究的热点。根据SO 的反应状态,将SO 还原法分为气相还原法和液相还原法。
2 2
Ⅰ. 气相还原法—固体还原剂直接还原法 (4)I催化NaHSO
3
的反应过程为 ① (用离子方程式表示);
固体还原剂直接还原法是指在一定温度下(200℃~300℃)将SO 2 烟气通过固体还原剂,使SO 2 ②I HSO H O=2I SO2 3H。
2 3 2 4
中的氧原子转移到固体还原剂上,从而实现SO 的还原,其流程如下:
2
(5)液相催化歧化制硫法具有反应条件温和、运行费用低等优点,然而其缺点是硫磺的回收率不会高
于______%(保留1位小数)。
第 3 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
(6)若采用Na S溶液作为碱盐吸收液,随着吸收液pH的变化,会生成二次污染物__ _(填化学 为原料先制得ClO ,再制备NaClO 粗产品,其流程如图:
2 2 2
式)。
15.(14分)工业上以硫酸泥(主要含S、Se、Fe O 、CuO、ZnO、SiO 等)为原料提取硒,流程如
2 3 2
图:
已知:①ClO 可被NaOH溶液吸收,反应为2ClO +2NaOH═NaClO +NaClO +H O。
2 2 3 2 2
②无水NaClO 性质稳定,有水存在时受热易分解。
2
(1)反应Ⅰ中若物质X为SO ,则该制备ClO 反应的离子方程式为 。
2 2
(1)“脱硫”过程中,温度控制在95℃,原因是 。 (2)实验在如图﹣1所示的装置中进行。
(2)“氧化”过程中,Se转化成H SeO ,该反应的化学方程式为 。
2 3
(3)“还原”过程是通过控制电位还原的方法将电位高的物质先还原,电位低的物质保留在溶液中。
下表是将“过滤Ⅰ”所得滤液中所含物质还原对应的电位。控制电位在0.782~1.692V,可除去“过滤
Ⅰ”所得滤液中残留的ClO 。
2
名称 Cu2+/Cu Zn2+/Zn Fe2+/Fe Fe3+/Fe2+ ClO /Cl﹣ H SeO /Se
2 2 3
电位/V 0.435 ﹣0.885 ﹣0.463 0.782 1.692 0.743
①若X为硫磺与浓硫酸,也可反应生成ClO .该反应较剧烈。若该反应在装置A的三颈烧瓶中进
为使硒和杂质金属分离,加入Na SO 还原时,电位应控制在 范围;H SeO(弱酸)还原为 2
2 3 2 3
行,则三种试剂(a.浓硫酸;b.硫黄;c.NaClO 溶液)添加入三颈烧瓶的顺序依次为
硒的离子反应方程式为 。 3
(填字母)。
(4)滤液Ⅱ中主要存在的金属阳离子有Zn2+、Na+、 。
②反应Ⅱ中双氧水的作用是 。保持反应时间、反应物和溶剂的用量不变,实验中
(5)所得粗硒需精制。向粗硒浸出液中加入Na S溶液可以将残留的Fe2+等微量杂质离子转化为沉淀
2
提高ClO 吸收率的操作有:装置A中分批加入硫黄、 (写出一种即可)。
而除去。已知25℃时K (FeS)=6.0×10﹣18,要使溶液中Fe2+沉淀完全[c(Fe2+)≤1.0×10﹣5mol/L], 2
sp
(3)将装置B中溶液蒸发可析出NaClO ,蒸发过程中宜控制的条件为 (填“减压”、“常压”
则需控制溶液中c(S2﹣)≥ mol•L﹣1 2
或“加压”)。
(4)反应Ⅰ所得废液中主要溶质为Na SO 和NaHSO ,直接排放会污染环境且浪费资源。为从中
16.(14分)亚氯酸钠(NaClO )是二氧化氯(ClO )泡腾片的主要成分。实验室以氯酸钠(NaClO ) 2 4 4
2 2 3
获得芒硝(Na SO •10H O)和石膏(水合硫酸钙),请补充完整实验方案: ,将滤液进一
2 4 2
第 4 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
步处理后排放(实验中须使用的试剂和设备有:CaO固体、酚酞、冰水和冰水浴)。(4分)已知:
CaSO 不溶于Na SO 水溶液;Na SO 的溶解度曲线如图﹣2所示。
4 2 4 2 4
17.(15分)工业上用绿矾制取还原性铁粉的简单工艺流程如下:
请回答下列问题:
①依据气流方向,各仪器接口的连接顺序为____________连__________,___________连___________,
______________连____________,_____________连________________。
(1)绿矾用酸浸而不用水浸的原因是_________________;转化过程中为了加快转化速率,需适当加
②写出A中反应的化学方程式:__________________。
热,但是温度不宜过高的原因是____________________。
(2)滤液的主要成分是_______________(填化学式),其重要用途是_______________(任意一条)。
(3)干燥过程是为了脱去沉淀FeCO ·nH O表面的水和结晶水,该过程会产生一种杂质FeO(OH),
3 2
写出化学方程式:______________________;为了避免生成FeO(OH),请写出该如何操作:
__________________。
(4)如下图是焙烧过程加CaCO 与未加CaCO 的铁粉产率,请分析加入CaCO 导致铁粉产率提的原
3 3 3
因:_____________________。
假期作业第五套答题纸
14.(14分,每空各2分)
(5)还原性铁粉中含有少量的Fe
x
C,用下列装置来测定还原性铁粉中碳的含量(装置可重复使用)。 (1)_______________________________(填化学式)。
(2)______________________________________________________________________________。
__________________________mol。
第 5 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
(3)_____________________(填标号)。 17.(15分,除标注外,各2分)
(4) ①___________________________________________________________________________; (1)__________________________________________________________________________________;
(5)__________________________%。 ___________________________________________________________________________________。
(6)______________________________(填化学式)。 (2)_______________(填化学式)(2分),____________________________(任意一条)。(1分)
15.(14分,除标注外,各2分) (3)________________________________________;________________________________。(各1分)
(1)__________________________________________________________________________。(3分) (4)___________________________________________________________________________________。
(2)_________________________________________________________________________。(3分) (5)
(3)____________________;_______________________________________________________。 ①____________连__________,___________连___________,______________连____________,
(4)_________________________。 _____________连________________。
(5)_________________________mol•L﹣1 ②
16.(14分,除标注外,各2分) ______________________________________________________________________________________。
(1)__________________________________________________。(3分)
(2) 衡水泰华中学决胜高考化学暑假必刷密卷第五套化学参考答案
1.答案:A
①_______________________________________(填字母)。
解析:在NaOH溶液中,Na+、K+、CO2-、AlO-相互之间不发生化学反应,可以大量共存,A项正确。Fe2+
3 2
②_____________________________________________。______________________(写出一种即可)。
具有还原性,MnO-具有氧化性,两者之间可发生氧化还原反应,不能共存,故B项错误。CO2-和Ba2+
4 3
(3)____________________。 可以结合成BaCO 沉淀,不能大量共存,故C项错误。在酸性条件下,NO-可将HSO-氧化,不能大量
3 3 3
共存,故D项错误。
(4)__________________________________________________________________________。(3分)
第 6 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
2、答案:D 4、【答案】C
【解析】A.硝酸具有强氧化性,可以将S2-氧化为S单质,自身根据其浓度大小还原为NO或NO 2 , 解析A.淡黄色沉淀是S,在反应过程中硫元素由NaHSO 中的+4价降低到0价,发生还原反应,HSO-
3 3
反应的离子方程式为4H++2NO+S2-=S↓+2NO ↑+2H O(浓)或8H++2NO+3S2-=3S↓+2NO↑+4H O(稀),
3 2 2 3 2 体现氧化性,A项不符合题意;
A错误;
B.酸性高锰酸钾溶液具有强氧化性,与还原性物质反应紫色才会褪去,所以可以证明Fe O 中有还原
3 4
B.明矾在水中可以电离出Al3+,可以与氨水中电离出的OH-发生反应生成Al(OH) ,但由于氨水的碱
3 性物质,即Fe(Ⅱ),B项不符合题意;
性较弱,生成的Al(OH) 不能继续与弱碱发生反应,故反应的离子方程式为
3 C.在该反应中浓硝酸体现氧化性,N元素化合价降低,生成的产物可能是NO或者NO ,NO暴露于
2
Al3++3NH 3 ·H 2 O=Al(OH) 3 ↓+3NH 4 ,B错误; 空气中也会迅速产生红棕色气体,无法证明反应产物,C项符合题意;
C.硅酸的酸性小于碳酸,向硅酸钠溶液中通入二氧化碳时,生成硅酸沉淀,二氧化碳则根据其通入
D.先变红说明溶液显碱性,证明NaClO在溶液中发生了水解, ,
的量的多少反应为碳酸根或碳酸氢根,反应的离子方程式为SiO 3 2 +H 2 O+CO 2 =H 2 SiO 3 ↓+CO 3 2 (CO 2 少 后来褪色,是因为水解产生了漂白性物质HClO,D项不符合题意;
量)或SiO2 +2H O+2CO =H SiO ↓+2HCO(CO 过量),C错误; 5、答案A
3 2 2 2 3 3 2
解析 A.硫酸钙微溶,用碳酸钠溶液处理水垢中的硫酸钙转化为难溶的碳酸钙,离子方程式为:
D.将等物质的量浓度的Ba(OH) 与NH HSO 溶液以体积比1:2混合,Ba(OH) 电离出的OH-与
2 4 4 2
,故A正确;
NH HSO 电离出的H+反应生成水,Ba(OH) 电离出的Ba2+与NH HSO 电离出的SO2反应生成BaSO
4 4 2 4 4 4 4
B.过量的铁粉与稀硝酸反应生成硝酸亚铁、一氧化氮和水,离子方程式应为:
沉淀,反应的离子方程为为Ba2++2OH-+2H++SO2 =BaSO ↓+2H O,D正确;
4 4 2
3Fe+8H++2NO-=3Fe2++2NO↑+4H O,故B错误;
3 2
故答案选D。
C.硫酸铝溶液与少量氢氧化钾溶液反应生成氢氧化铝沉淀和硫酸钾,离子方程式应为:
3.答案:A
Al3++3OH-=Al(OH) ↓,故C错误;
3
【解析】由题意可知,①取少量样品溶于水得到无色透明溶液,说明固体溶于水且相互之间能共存,
D.硫化氢为弱电解质,书写离子方程式时不拆,离子方程式应为:Cu2++H S=CuS↓+2H+,故D错误;
2
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体放出,说明固体中存在Na S O ,发生反
2 2 3 6.答案A
应S 2 O 3 2-+2H+=S↓+H 2 O+SO 2 ↑,离心分离,③取②的上层清液,向其中滴加BaCl 2 溶液,有沉淀生成, 解析A.用Na 2 SO 3 溶液吸收少量的Cl 2 ,Cl 2 具有强氧化性,可将部分 氧化为 ,同时产生的氢
则沉淀为BaSO 4 ,说明固体中存在Na 2 SO 4 ,不能确定是否有Na 2 SO 3 和Na 2 CO 3 ,Na 2 SO 3 与过量盐酸 离子与剩余部分 结合生成 ,Cl 被还原为Cl-,反应的离子反应方程式为:
2
反应生成二氧化硫,Na CO 与过量盐酸反应生成二氧化碳,而这些现象可以被Na S O 与过量盐酸反
2 3 2 2 3 3 +Cl +H O=2 +2Cl-+ ,A选项正确;
2 2
应的现象覆盖掉,综上分析,该样品中确定存在的是:Na SO 、Na S O ,
2 4 2 2 3 B.向CaCl 溶液中通入CO ,H CO 是弱酸,HCl是强酸,弱酸不能制强酸,故不发生反应,B选
2 2 2 3
答案选A。
第 7 页 共 12 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
项错误; 子,所以溶液中存在的阴离子为硫酸根离子,再根据溶液电中性可知,正电荷物质的量为0.1mol×2=0.2
C.向H O 中滴加少量的FeCl ,Fe3+的氧化性弱于H O ,不能氧化H O ,但Fe3+能催化H O 的分 mol,负电荷物质的量为0.1mol×2+0.1mol=0.3mol,溶液中一定还存在0.1mol正电荷,该离子的物质
2 2 3 2 2 2 2 2 2
解,正确的离子方程式应为2H O 2H O+O ↑,C选项错误;
的量为0.1mol,所以该离子为钠离子。根据以上分析可知,溶液中一定不存在钡离子,故A项正确,不符合
2 2 2 2
题意。溶液中氢氧根离子、硫酸根离子不会消失;根据反应方程式NO- +3Fe2++4H+===NO↑+3Fe3+
D.NH HSO 电离出的H+优先和NaOH溶液反应,同浓度同体积的NH HSO 溶液与NaOH溶液混 3
4 4 4 4
+2H O可知,亚铁离子不足,加入足量的稀硫酸后,硝酸根离子不会消失,故B项错误,符合题意。若向该
合,氢离子和氢氧根恰好完全反应,正确的离子反应方程式应为:H++OHˉ=H O,D选项错误; 2
2
溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体为氧化铁,根据铁离子守恒,
7答案B。
生成氧化铁的物质的量为0.05mol,质量为0.05mol×160g·mol-1=8.0g,故C项正确,不符合题意。根据
解析A.Al3+和NH H O生成Al(OH) 沉淀而不是生成AlO,故A错误;
3 2 3 2
分析可知,该溶液中除H+、OH-之外所含离子是Fe2+、Na+、NO- 、SO2-,故D项正确,不符合题意。
3 4
B.S 2 O 3 2和H+反应生成单质硫、二氧化硫和水,离子方程式为:2H++S 2 O 3 2 =S↓+SO 2 ↑+H 2 O,故B 二、不定项选择题(每个小题有1-2个正确选项,共5小题,每题4分,部分分2分,共20分)
正确; 10、答案:AD
C.Fe3+能催化H O 的分解,Fe3+与H O 不能大量共存,故C错误; 解析:水的离子积为K =c(H+)×c(OH-),由图可知,a、b均在25 ℃,离子积相同;而c、d均在T ℃,离子
2 2 2 2 w
D.在酸性条件下MnO能将Cl-氧化为Cl ,不能大量共存,故D错误; 积相同。Fe3+水解显酸性,而a点对应的溶液显中性,离子不能大量共存,故A项错误。NH+ 4 与OH-反应生
4 2
成一水合氨,离子不能大量共存,故B项错误。HCO-水解显碱性,而c点对应的溶液显中性,HCO-离子
8.答案:D 3 3
不能大量共存,故C 项错误。d点时c(H+)