文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题17
1.水体中的局部氮循环如下图所示,其中含氮物质转化方向与水深有关。下列说法正确的是
A. 若氨态氮与亚硝态氮反应生成1molN ,转移6mole-
2
B. 反硝化过程中,含N物质都被还原
C. 图中涉及的反应有部分反应没有发生电子转移
D. 不同水深含氮物质转化方向不同,一定与水压有关
答案:B
解析:A.氨态氮与亚硝态氮可以转化为氮气,根据得失电子守恒,反应方程式是NH+ NO
=
N↑+2H O,N元素由-3价上升到0价,又由+3价下降到0价,生成1molN ,转移3mole-,故A
2 2 2
错误;
B.由图中转化关系可知,反硝化过程中含N物质化合价均降低,被还原,故B正确;
C.由图中转化关系可知,图中涉及的反应,元素化合价都发生了变化,故均为氧化还原反应,
都发生了电子的转移,故C错误;
D.表层水中氧气浓度大,含氮物质转化以硝化过程为主,发生氧化反应;底层水中氧气浓度
小,含氮物质转化以反硝化过程为主,发生还原反应,所以不同水深含氮物质转化方向不同,可能
与溶氧量有关,和水压无关,故D错误;
2.对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
粒子组 判断和分析
A Fe2+、NH、SO、 [Fe(CN) ]3- 能大量共存,粒子间不反应
6
B H+、Na+、Cl-、MnO 能大量共存,粒子间不反应
不能大量共存,因发生反应:Al3++
C Na+、Al3+、Cl-、NH ∙HO
3 2 4NH ∙HO=AlO+4NH+2HO
3 2 2
不能大量共存,因发生反应:2H++SO S↓
D H+、K+、SO 2 =
2 、SO +SO ↑+HO
2 2
答案:D
解析:A.Fe2+与[Fe(CN) ]3-反应产生蓝色沉淀,不能大量共存,故A错误。
6
B.Cl-被酸性MnO B错误。
氧化生成氯气,不能大量共存,故
C.Al3+与NH ∙HO反应生成的Al(OH) 不能溶于氨水,故C错误。
3 2 3
D.H=与SO 2H++SO S↓+SO ↑+HO,故D正确。
2 反应方程式为 2 = 2 23.某溶液中可能存在K+、Al3+、Fe2+、NH、NO CO SO中的几种离子,且存在的各离子的物
、 、
质的量相等,某同学对该溶液进行如下实验:
下列判断正确的是
A.原溶液中一定不存在K+
B.白色沉淀可能是Al(OH)
3
C.气体A一定是CO,气体B一定是NH
2 3
D.原溶液中一定存在Al3+、Fe2+、NO NH
、
答案:A
解析:溶液与过量稀盐酸反应生成气体A,则溶液中可能含有HCO Fe2+、NOHCO Fe2+不能
或 ( 与
共存);溶液Ⅰ与过量氢氧化钡反应生成气体B和有色沉淀,则原溶液中一定含Fe2+、NH、NO
,一定
HCO Ⅱ与适量二氧化碳反应生成白色沉淀,则该白色沉淀可能为碳酸钡和氢氧化铝中的一种
不含 ;溶液
或两种,由存在的各离子的物质的量相等及电荷守恒可知,原溶液中一定不含K+、Al3+、一定含
SO。由上述分析可知,原溶液中一定含Fe2+、NH、NO SO,一定不含K+、Al3+、HCO
、 ,白色沉淀为碳酸钡,
A为NO,气体B为氨气,有色沉淀为Fe(OH) ,故A正确。
气体 3
4.用酸性KMnO 溶液处理硫化亚铜(Cu S)和二硫化亚铁(FeS )的混合物时,发生反应:
4 2 2
Ⅰ:MnO Cu S+H+→Cu2++SO+Mn2++HO (未配平)
+ 2 2
Ⅱ:MnO FeS+H+→Fe3++SO+Mn2++HO (未配平)
+ 2 2
下列说法正确的是
A.反应Ⅰ中Cu S既是氧化剂又是还原剂
2
B.反应Ⅰ中每生成1mol SO,转移电子的物质的量为10 mol
C.反应Ⅱ中氧化剂与还原剂的物质的量之比为1∶3
D.若反应Ⅰ和反应Ⅱ中消耗的KMnO 的物质的量相同,则反应Ⅰ和反应Ⅱ中消耗的还原剂的
4
物质的量之比为2∶3
答案:B
解析:A.反应Ⅰ中Cu S中Cu的化合价从+1升高到+2价,S的化合价从-2升高到+6,
2
Cu S只是还原剂,故A错误。
2
B.反应Ⅰ中每生成1 mol SO,2 molCu2+失去2 mol 电子,1 molS2-失去8 mol 电子,总共转
移电子的物质的量为10 mol 电子,故B正确。
C.根据电子守恒由反应Ⅱ得出,氧化剂与还原剂的物质的量之比为3∶1,故C错误。
D.若反应Ⅰ和反应Ⅱ中消耗的KMnO 的物质的量相同,则反应Ⅰ和反应Ⅱ中消耗的还原剂的
4
物质的量之比为3∶2,故D错误。
5.下列离子方程式不正确的是A.锂离子电池的负极反应:LiC -xe-=xLi++C
x y y
B.向CuCl 溶液中滴加过量氨水:Cu2++2NH·H O=Cu(OH) ↓+2NH
2 3 2 2
C.1.5mol·L-1100mL的FeBr 溶液中通入3.36L(标况)Cl :2Fe2++2Br-+2Cl=2Fe3++4Cl-+
2 2 2
Br
2
D.调节pH=5(常温),向ZnSO 溶液中加入适量KMnO 溶液(还原产物MnO )除去少量杂质
4 4 2
Fe2+:3Fe2++MnO O=3Fe(OH) ↓+MnO↓+5H+。
+7H2 3 2
答案:B
解析:A.原电池负极发生氧化反应,失电子,故锂离子电池的负极反应: Li Cy-xe-=xLi+
x
+Cy, A正确;
B.向CuCl 溶液中滴加过量氨水反应生成[Cu(NH )]2+;故为Cu2++4NH∙HO=[Cu(NH )]2+
2 3 4 3 2 3 4
+4HO,B错误;
2
C.用K [Fe(CN)6]溶液检验Fe2+反应生成KFe[Fe(CN) ],故为K++Fe2++[Fe(CN) ]3-=
3 6 6
KFe[Fe(CN) ]↓,C正确;
6
D.KMnO 溶液(还原产物MnO )将Fe2+氧化成Fe3+转化成Fe(OH) ,故为3Fe2++MnO O=
4 2 3 +7H2
3Fe(OH) ↓+MnO↓+5H+,D正确。
3 2
6.下列离子方程式书写正确的是
A.铜与稀硝酸反应:Cu+4H++2NO Cu2++2NO ↑+2HO
= 2 2
B.NaSO 溶液和稀硫酸混合:SO 2H+=S↓+SO ↑+HO
2 2 3 2 + 2 2
C.向饱和碳酸钠溶液中通入过量CO:CO CO+HO=2HCO
2 + 2 2
D.将NaOH溶液和HC O 溶液等体积等浓度混合:2OH-+HC O=C O HO
2 2 4 2 2 4 2 +2 2
答案:B
解析:A.铜与稀硝酸反应生成NO,离子方程式为3Cu+8H++2NO 2++2NO↑+4HO,A错误;
=3Cu 2
B.NaSO 溶液和稀硫酸反应生成二氧化硫、硫单质和水,离子方程式为SO 2H+=S↓+SO ↑
2 2 3 2 + 2
+HO,B正确;
2
C.向饱和碳酸钠溶液中通入过量CO 生成碳酸氢钠,碳酸氢钠溶解度小析出,离子方程式为
2
2Na++CO +H O=2NaHCO ↓,C错误;
+CO2 2 3
D.草酸是二元弱酸,将NaOH溶液和HC O 溶液等体积等浓度混合生成OH−+HC O=
2 2 4 2 2 4
HC O+HO,D错误;
2 2
7.将“84”消毒液和洁厕灵同时使用会发生反应:Na37ClO+2H35Cl=NaCl+Cl↑+HO。下列
2 2
有关说法中正确的是
A. 该反应生成Cl 的摩尔质量为70g∙mol-1
2
B. 35Cl和37Cl所含中子数之比为35∶37
C. 该反应中,体现了HCl的酸性和氧化性
D. 该反应涉及的物质中有4种物质含共价键
答案:D解析:A.反应中次氯酸钠中氯元素化合价降低、HCl中部分氯元素化合价升高,两者反应生
成氯气,则该反应生成Cl 的摩尔质量为72g∙mol-1,A错误;
2
B.核素的表示方法为:元素符号左下角为质子数,左上角为质量数;35Cl和37Cl所含中子数
之比为(35-17)∶(37-17)=9∶10,B错误;
C.反应HCl中部分氯元素化合价升高,体现出还原性,C错误;
D.该反应涉及的物质中次氯酸钠、氯化氢、氯气、水,共4种物质含共价键,D正确;
8.常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 0.1 mol·L-1KNO 溶液中:Cu2+、NH、Cl-、SO
3
B. 澄清透明的溶液中:Fe3+、Mg2+、SCN-、Br-
C. 使酚酞变红色的溶液中:Ba2+、A13+、ClO、Cl-
D. 水电离的c(H+)=1×10-12mol·L-1的溶液中:Na+、K+、I-、NO
答案:A
解析:A.各离子间互不反应,可以大量共存,故A正确;
B.Fe3+、SCN-离子之间结合生成络离子,不能大量共存,故B错误;
C.使酚酞变红色的溶液,显碱性,A13+与OH-不能大量共存,故C错误;
D.水电离的c(H+)=1×10-12mol·L-1的溶液,水的电离被抑制,溶液可能是强酸性或强碱性,当
溶液为强酸性时,I-、NO +发生氧化还原反应,不能大量共存,故D错误;
和H
9.秋冬季节是雾霾的高发时间,某实验小组收集了所在地区的雾霾,经处理后得试样溶液,
溶液中可能含有的离子有Na+、NH、Mg2+、Al3+、SO、NO Cl-。某同学设计了如下实验:
、
步骤 实验操作 实验现象
取试样溶液于锥形瓶中,滴加过量的Ba(OH) 溶 有无色气体a、白色沉淀
① 2
液,微热,充分反应后过滤 b生成
② 将上述无色气体a通过湿润的红色石蕊试纸 试纸变蓝
③ 往白色沉淀b上滴加稀盐酸 沉淀部分溶解
④ 取步骤①过滤后的滤液,通入CO 有白色沉淀生成
2
根据以上实验操作与现象,该同学得出的结论错误的是
A.通过步骤①③可确定试样溶液中肯定存在Mg2+、SO
B.上述实验中不能确定的阴离子有NO Cl-
、
C.可通过焰色反应鉴别试样溶液中是否存在Na+
D.步骤④的实验说明试样溶液中还含有Al3+
答案:D
解析:根据实验①滴加过量的Ba(OH) 溶液,微热,充分反应后过滤,有无色气体a、白色沉
2
淀b生成,实验②将上述无色气体a通过湿润的红色石蕊试纸,试纸变蓝,说明有NH;实验①产
生白色沉淀可能是Mg(OH) ,也可能是BaSO,实验③往白色沉淀b上滴加稀盐酸,沉淀部分溶解,
2 4
说明沉淀是Mg(OH) 和BaSO,故有Mg2+和SO ,实验①加入过量的Ba(OH)
2 4 。④取步骤①过滤后的滤液,通入CO2 2溶液,白色沉淀一定含有BaCO ,可能含有Al(OH) ,故原溶液中可能有Al3+;
3 3
A.根据分析可知实验①产生白色沉淀可能是Mg(OH) ,也可能是BaSO,实验③往白色沉淀
2 4
b上滴加稀盐酸,沉淀部分溶解,说明沉淀是Mg(OH) 和BaSO,故有Mg2+和SO,故A正确;
2 4
B.上述实验肯定存在的有Mg2+、SO、NH、Al3+,不能确定是否有阴离子NO Cl-,故B正确;
、
C.Na+的焰色反应产生黄色火焰,可通过焰色反应鉴别试样溶液中是否存在Na+,故C正确;
D.取步骤①过滤后的滤液,通入CO,实验①加入过量的Ba(OH) 溶液,白色沉淀一定含有
2 2
BaCO ,可能含有Al(OH) ,故原溶液中可能有Al3+,故D错误;
3 3
10.下列条件下的化学反应,相应的离子方程式一定正确的是
A.将2.24LCO 通入500mL0.3mol·L-1的NaOH溶液中:2CO+3OH-=CO HCO HO
2 2 + + 2
B.向NH Fe(SO ) 溶液中加入少量NaOH溶液:NH+OH-=NH ∙HO
4 4 2 3 2
C.1L1mol·L-1FeBr 溶液与一定量氯气反应转移的电子数为2×6.02×1023时,反应的离子方程
2
式为2Fe2++2Br-+2Cl=2Fe3++Br +4Cl-
2 2
D.向Ca(ClO) 溶液通入少量SO :Ca2++2ClO-+SO +HO=CaSO↓+2HClO
2 2 2 2 3
答案:C
解析:A.没有明确是否为标准状况,2.24LCO 的物质的量不一定是0.1mol,A错误;
2
B.向NH Fe(SO ) 溶液中加入少量NaOH溶液,OH-先与Fe3+反应,反应的离子方程式为
4 4 2
Fe3++3OH-=Fe(OH) ↓,B错误;
3
C.1L1mol·L-1FeBr 溶液与一定量氯气反应转移的电子数为2×6.02×1023时,说明消耗的氯气
2
为1mol,还原性Fe2+>Br-,1molFe2+、1molBr-被氧化,反应的离子方程式为2Fe2++2Br-+2Cl=
2
2Fe3++Br +4Cl-,C正确;
2
D.次氯酸具有强氧化性,会将亚硫酸钙氧化为硫酸钙,两者不能同时生成,D错误;
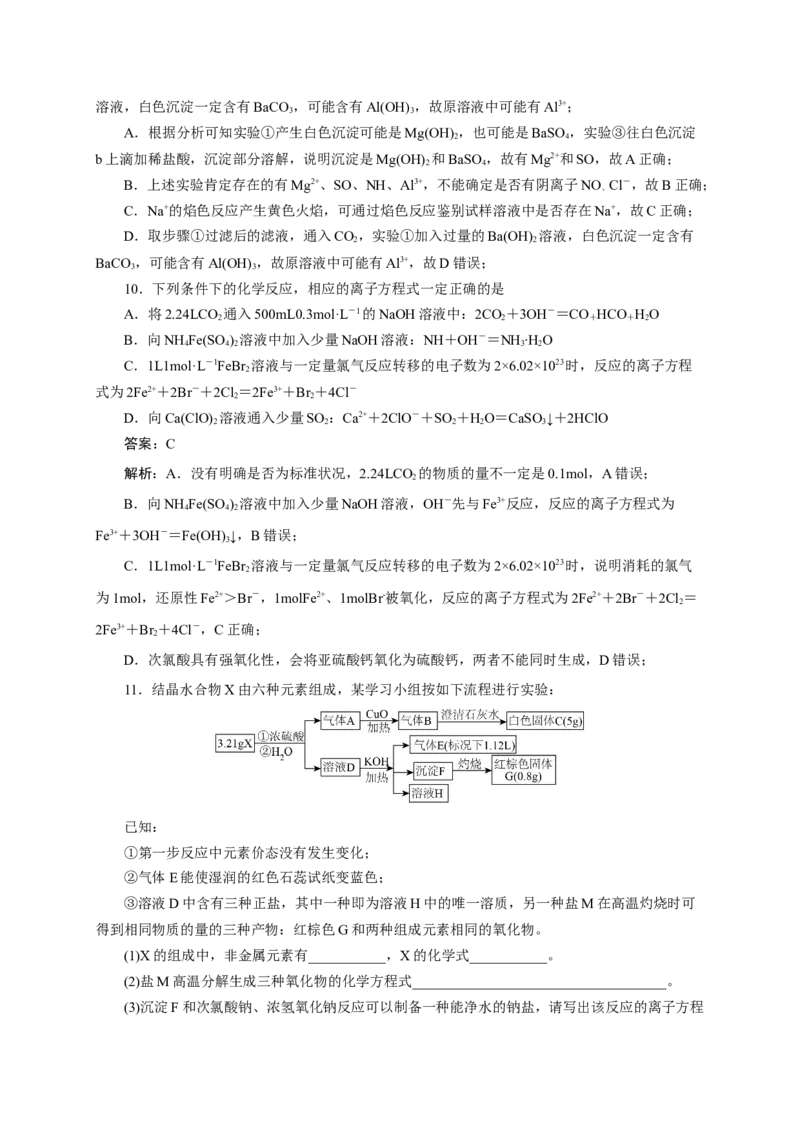
11.结晶水合物X由六种元素组成,某学习小组按如下流程进行实验:
已知:
①第一步反应中元素价态没有发生变化;
②气体E能使湿润的红色石蕊试纸变蓝色;
③溶液D中含有三种正盐,其中一种即为溶液H中的唯一溶质,另一种盐M在高温灼烧时可
得到相同物质的量的三种产物:红棕色G和两种组成元素相同的氧化物。
(1)X的组成中,非金属元素有___________,X的化学式___________。
(2)盐M高温分解生成三种氧化物的化学方程式____________________________________。
(3)沉淀F和次氯酸钠、浓氢氧化钠反应可以制备一种能净水的钠盐,请写出该反应的离子方程式_________________________________________________。
(4)溶液D在空气中敞口放置一段时间后,请设计实验检验溶液D中可能存在的金属阳离子:
___________。
答案:(1)C、H、O、N K Fe(CN) ∙HO (2)2FeSO ===Fe2O+SO ↑+SO ↑
3 5 2 4 3 2 3
(3)Fe(OH) +2ClO-+2OH-=FeO+2Cl-+2HO
2 2
(4)检验钾离子:用铂丝蘸取少量样品在酒精灯火焰上灼烧,透过蓝色钴玻璃片观察到紫色火焰
则有钾离子;检验亚铁离子:取少量样品于试管中,滴加酸性高锰酸钾溶液,若紫色褪去,或加铁
氰化钾出现蓝色沉淀则含有亚铁离子检验三价铁离子:取少量样品于试管中,滴少量KSCN溶液,
若溶液出现血红色,则含有三价铁离子
解析:气体A和CuO反应生成气体B能使澄清石灰水变浑浊,则气体A是CO,气体B是
CO,白色固体C是CaCO ,则n(C元素)=n(CO)=n(CO)==0.05mol;红棕色固体G是沉淀F经
2 3 2
灼烧得到,则G是Fe O,其物质的量n(Fe O)==0.005mol,n(Fe元素)=2×=0.01mol,气体E能
2 3 2 3
使湿润的红色石蕊试纸变蓝,E为氨气,物质的量n(N元素)= n(NH )==0.05mol;第一步反应中元
3
素价态没有发生变化,且溶液D中含有三种正盐,则D中含有SO,D能与KOH反应生成氨气,
则D中含有NH,其中一种即为溶液H中的唯一溶质,则H为含KSO , D中另一种盐M在高温
2 4
灼烧时可得到相同物质的量的Fe O 和两种组成元素相同的氧化物应为SO 、SO ,n(Fe元素):n(S
2 3 2 3
元素)=1∶1,则正盐M为FeSO ,则F是Fe(OH) ,所以D中的三种正盐分别是:KSO 、
4 2 2 4
(NH )SO 、FeSO ;结晶水合物X由六种元素组成,则X中含有H、O、K、Fe、N、C元素,且
4 2 4 4
n(C元素)∶n(Fe元素)∶n(N元素)=0.05mol∶0.01mol∶0.05mol=5∶1∶5,则为Fe(CN)离子,则n(K元
素)=0.03mol, m(HO)=3.21g-m(C元素)-m(Fe元素)-m(N元素)-m(K元素)=3.21g-0.6g-
2
0.56g-0.7g-1.17g=0.18g,n(H O)=0.01mol,所以X的化学式为KFe(CN) ∙HO。据此作答。
2 3 5 2
(1)根据分析,X中含有H、O、K、Fe、N、C元素,非金属元素有H、O、N、C;X的化学式
为KFe(CN) ∙HO;
3 5 2
(2)根据分析,M是FeSO ,受热分解可得到相同物质的量的三种产物,方程式为:
4
2FeSO ===Fe2O+SO ↑+SO ↑;
4 3 2 3
(3)根据分析,沉淀F为Fe(OH) ,与次氯酸钠、浓氢氧化钠反应可以制备一种能净水的钠盐为
2
高铁酸钠,反应的离子方程式为:Fe(OH) +2ClO-+2OH-=FeO+2Cl-+2HO;
2 2
(4)根据分析,溶液D 中的三种正盐分别是:KSO 、(NH )SO 、FeSO ,在空气中敞口放置一
2 4 4 2 4 4
段时间后,Fe2+可能会部分或全部被氧化为Fe3+。检验钾离子:用铂丝蘸取少量样品在酒精灯火焰
上灼烧,透过蓝色钴玻璃片观察到紫色火焰则有钾离子;检验亚铁离子:取少量样品于试管中,滴
加酸性高锰酸钾溶液,若紫色褪去,或加铁氰化钾出现蓝色沉淀则含有亚铁离子;检验三价铁离子:
取少量样品于试管中,滴少量KSCN溶液,若溶液出现血红色,则含有三价铁离子。
12.铝酸铋[Bi(AlO)]主要用作抗酸药及抗溃疡药,具有中和胃酸和收敛作用。以辉铋矿(主要
2 3
成分为BiS,含有SiO、Cu S、FeS 杂质)为原料制备铝酸铋的一种工艺流程如图所示:
2 3 2 2 2已知:①常温下,Cu(OH) 、Fe(OH) 、Fe(OH) 和Bi(OH) 的K 分别为2.0×10-20、4.0×10-
2 2 3 3 sp
16、.4.0×10-38和8.0×10-31,lg2=0.3。
②Cu(OH) 能溶于氨水生成[Cu(NH )]2+。
2 3 4
③Sn2+和Sn4+在碱性溶液中分别以[Sn(OH) ]2-和[Sn(OH) ]2-的形式存在。
4 6
请回答下列问题:
(1)铋与氮同主族,铋元素在元素周期表中的位置是___________。
(2)滤渣1中除了硫单质,还含另一种物质,30g该物质中含共价键的数目是_______,FeCl 与
3
Cu S反应中氧化剂与还原剂的物质的量之比为________。
2
(3)“还原”时,加入铋的目的是___________________________。
(4)“沉淀”前,若滤液中Cu2+浓度为0.005mol·L-1,Fe2+浓度为0.01mol·L-1,则“沉淀”时调pH
的最大值应小于___________。
(5)在碱性溶液中,可用[Sn(OH) ]2-鉴定Bi3+存在,Bi3+被还原为Bi写出该反应的离子方程式:
4
_______________________________________。
(6)在氢氧化钠溶液中,次氯酸钠能将Bi(OH) 氧化为NaBiO,写出该反应的化学方程式:____
3 3
____________________________________。
答案:(1)第六周期VA族 (2)2N 4∶1
A
(3)将Fe3+还原为Fe2+,防止沉铋时有Fe(OH) 生成 (4)7.3
3
(5)2Bi3++3[Sn(OH) ]2-+6OH-=2Bi↓+3[Sn(OH) ]2-
4 6
(6)Bi(OH) +NaOH+NaClO=NaBiO+NaCl+2HO
3 3 2
解析:由题给流程可知,辉铋矿中加入氯化铁和盐酸的混合溶液浸取时,金属硫化物转化为硫
和可溶性金属氯化物,二氧化硅与混合溶液不反应,过滤得到含有硫、二氧化硅的滤渣和滤液;向
滤液中加入铋,将溶液中的铁离子还原为亚铁离子,过滤得到滤液;调节滤液的pH,将铋离子、
铜离子转化为氢氧化铋、氢氧化铜沉淀,过滤得到含有亚铁离子的滤液和滤渣;向滤渣中加入氨水,
将氢氧化铜周围四氨合铜离子,过滤得到含有四氨合铜离子的滤液和氢氧化铋;氢氧化铋溶于稀硝
酸得到硝酸铋溶液,硝酸铋溶液与偏铝酸钠溶液反应制得铝酸铋。
(1)原子序数为83的铋元素与氮元素同主族,则铋元素位于元素周期表第六周期VA族,故答
案为:第六周期VA族;
(2)由分析可知,滤渣1的主要成分是硫和二氧化硅,二氧化硅中每个硅原子与4个氧原子形成
4个硅氧键,则30g二氧化硅中含共价键的数目为×4×N mol—1=2N ;氯化铁溶液与氯化亚铜反应生
A A
成氯化亚铁、氯化铜和硫沉淀,反应的化学方程式为4FeCl +Cu S=4FeCl +2CuCl +S,则反应中氧
3 2 2 2
化剂氯化铁与还原剂硫化亚铜的物质的量之比为,故答案为:2N ;4∶1;
A
(3)由分析可知,“还原”时,加入铋的目的是将溶液中的铁离子还原为亚铁离子,防止沉铋时有氢氧化铁沉淀生成,故答案为:将Fe3+还原为Fe2+,防止沉铋时有Fe(OH) 生成;
3
(4)由溶度积可知,当亚铁离子开始沉淀时,溶液中的氢氧根离子浓度为=2.0×10-7mol/L,溶液
pH为7.3,则“沉淀”时调pH的最大值应小于7.3,故答案为:7.3;
(5)由题意可知,碱性溶液中 [Sn(OH) ]2-与Bi3+反应生成生成Bi和[Sn(OH) ]2-,反应的离子方程
4 6
式为2Bi3++3[Sn(OH) ]2-+6OH-=2Bi↓+3[Sn(OH) ]2-,故答案为:2Bi3++3[Sn(OH) ]2-+6OH-=2Bi↓+
4 6 4
3[Sn(OH) ]2-;
6
(6)由题意可知,在氢氧化钠溶液中,次氯酸钠溶液与Bi(OH) 反应生成NaBiO、氯化钠和水,
3 3
反应的化学方程式为Bi(OH) +NaOH+NaClO=NaBiO+NaCl+2HO,故答案为:Bi(OH) +NaOH+
3 3 2 3
NaClO=NaBiO+NaCl+2HO。
3 2