文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题22
1.关于反应4Cu2++8OH-+NH=2Cu O↓+N↑+6HO,下列说法正确的是
2 4 2 2 2
A. N 是还原产物 B. 氧化剂与还原剂的物质的量之比为1∶4
2
C. NH 既是氧化剂又是还原剂 D. 生成28gN,转移4mol电子
2 4 2
答案:D
解析:A. 分析方程式中的化合价可知,NH 中N元素的化合价为-2,N 中的N元素的化合价
2 4 2
为0,N元素的化合价升高,N 为氧化产物,故A错误;
2
B. 分析方程式中的化合价可知,Cu元素化合价降低,Cu2+为氧化剂,N元素化合价升高,
NH 为还原剂,氧化剂与还原剂的物质的量之比为4:1,故B错误;
2 4
C. NH 中有且只有N元素化合价升高,所以NH 仅为还原剂,故C错误;
2 4 2 4
D. 分析方程式可知,每生成1mol N,转移的电子数为4mol,28g N ,正好为1mol N,故D
2 2 2
正确;
2.对于下列实验,其离子方程式描述错误的是
A. 稀硝酸中加入少量铁粉:3Fe+2NO +=3Fe2++2NO↑+4HO
+8H 2
B. 将足量FeCl 溶液滴入Mg(OH) 浊液中:3Mg(OH) +2Fe3+=Fe(OH) +3Mg2+
3 2 2 3
C. Cl 通入冷的KOH溶液中:Cl+2OH-=ClO-+Cl-+HO
2 2 2
D. NHHSO 溶液中加入少量Ba(OH) 溶液:Ba2++2OH-+2H++SO=BaSO↓+2HO
4 4 2 4 2
答案:A
解析:A.稀硝酸中加入少量铁粉生成硝酸铁和一氧化氮气体,Fe+2NO +=Fe3++2NO↑+
+4H
2HO,A错误;
2
B.足量FeCl 溶液滴入Mg(OH) 浊液中,氢氧化镁浊液转化为氢氧化铁浊液:3Mg(OH) +
3 2 2
2Fe3+=Fe(OH) +3Mg2+,B正确;
3
C.Cl 通入冷的KOH溶液中生成氯化钾和次氯酸钾、水:Cl+2OH-=ClO-+Cl-+HO,C
2 2 2
正确;
D.NH HSO 溶液中加入少量Ba(OH) 溶液,钡离子和氢氧根离子完全反应生成硫酸钡沉淀和
4 4 2
水,Ba2++2OH-+2H++SO=BaSO↓+2HO,D正确;
4 2
3.从含镍催化剂(含NiO、Fe O、Al O 等物质)中回收金属资源的部分流程如下:
2 3 2 3下列说法错误的是
A.试剂X为NaOH溶液
B.“酸化”反应的离子方程式可能为CO+AlO+2HO=HCO Al(OH) ↓
2 2 + 3
C.该工艺回收的金属资源为Al O、Fe O、NiSO·7HO
2 3 2 3 4 2
D.若杂质中含有Fe2+,浓缩结晶所得产品中可能含FeSO ·7HO
4 2
答案:C
解析:A项,通过CO 的酸化可知,溶浸应为“碱浸”,正确;B项,“酸化”时,CO 过量
2 2
即得到碳酸氢根,正确;C项,红褐色固体为Fe(OH) ,错误;D项,杯酚与其它分子作用可形成
3
超分子,错误。
4.下列物质性质实验对应的离子方程式书写正确的是
A.漂白粉溶液吸收CO 后产生白色沉淀:Ca2++CO+HO=CaCO ↓+2H+
2 2 2 3
B.Fe(OH) 溶于氢碘酸:Fe(OH) +3H+=Fe3++3HO
3 3 2
C.用碳酸钠溶液处理锅炉水垢:CaSO(s)+CO CaCO (s)+SO
4 3
D.同浓度同体积NH HSO 溶液与NaOH溶液混合:NH+OH-=NH ∙HO
4 4 3 2
答案:C
解析:A. 漂白粉溶液吸收CO 后产生碳酸钙沉淀和次氯酸,反应的离子方程式是Ca2++2ClO-
2
+CO+HO=CaCO ↓+2HClO,故A错误;
2 2 3
B. Fe(OH) 溶于氢碘酸生成碘化亚铁、碘单质、水,反应的离子方程式是2Fe(OH) +2I-+
3 3
6H+=2Fe2++I+3HO,故B错误;
2 2
C. 用碳酸钠溶液处理锅炉水垢,沉淀硫酸钙转化为碳酸钙沉淀,反应的离子方程式是
CaSO(s)+CO CaCO (s)+SO,故C正确;
4 3
D. 同浓度同体积NH HSO 溶液与NaOH溶液混合,NH HSO 与NaOH等物质的量反应生成硫
4 4 4 4
酸铵、硫酸钠、水,反应的离子方程式是H++OH-=HO,故D错误。
2
5.下列物质属于电解质且溶于水为碱性的是
A. K CO B. H SO C. NH D. NH Cl
2 3 2 4 3 4
答案:A
解析:A.KCO 在水溶液和熔融状态下均能导电,是电解质,溶于水后碳酸根离子水解显碱
2 3
性,选项A正确;B.HSO 在水溶液中能导电,属于电解质,但溶液显酸性,选项B错误;
2 4
C.NH 于水反应生成电解质一水合氨,NH 属于非电解质,选项C错误;
3 3
D.NH Cl是盐,在水溶液中完全电离产生自由移动的离子,属于强电解质,但溶于水后因铵
4
根离子水解显酸性,选项D错误;
6.下列反应的方程式正确的是
A. 在高温加热下铁与水蒸气反应:2Fe+3HO(g)=====Fe O+3H
2 2 3 2
B. 用NaOH 溶液吸收过量SO :2OH-+SO =SO HO
2 2 + 2
C. 含1molFeBr 溶液中通入1mol Cl :2Fe2++2Br-+2Cl=2Fe3++Br +4Cl-
2 2 2 2
D. 将Mg(HCO ) 溶液与过量的NaOH溶液混合:2HCO Mg2++2OH-=MgCO +CO HO
3 2 + 3 +2 2
答案:C
解析:A.高温下铁与水蒸气反应生成四氧化三铁和氢气,化学方程式为3Fe+
4HO(g)=====Fe O+4H,故A错误;
2 3 4 2
B.当二氧化硫过量时,和NaOH溶液反应生成亚硫酸氢钠,因此离子方程式为OH-+SO =
2
HSO O,故B错误;
+H2
C.二价铁离子还原性强于溴离子,氯气少量先氧化亚铁离子,再氧化溴离子,故1mol Cl 先
2
将1molFeBr 中的1molFe3+全部氧化,剩余的氯气还能氧化1molBr-,即被氧化的Fe2+、Br-的物质
2
的量之比为1∶1,因此离子方程式为2Fe2++2Br-+2Cl=2Fe3++Br +4Cl-,故C正确;
2 2
D.将Mg(HCO ) 溶液与过量的NaOH溶液混合反应生成氢氧化镁和碳酸钠,离子方程式为:
3 2
2HCO Mg2++4OH-=Mg(OH) ↓+2CO HO,故D错误。
+ 2 +2 2
7.含共价键的强电解质的是
A. MgCl B. NaHSO C. NH D. CH COOH
2 4 3 3
答案:B
解析:强电解质:在水溶液中或熔融状态下能完全电离的化合物;弱电解质:在水溶液中不能
完全电离的化合物。相邻原子之间通过共用电子对形成的化学键为共价键,据此判断。
A.氯化镁只含离子键,A错误;
B.硫酸氢钠是在水溶液中或熔融状态下能完全电离的化合物,属于强电解质,钠离子与硫酸
氢根离子之间存在离子键,硫酸氢根离子内氧原子与硫原子、氢原子和氧原子之间存在共价键,B
正确;
C.氨气为非电解质,C错误;
D.醋酸在水溶液中只能部分电离,属于弱电解质,D错误;
8.下列指定反应的离子方程式正确的是A.向碘化亚铁溶液中滴加少量稀硝酸:NO 2++4H+=3Fe3++NO↑+2HO
+3Fe 2
B.久置的HS溶液变浑浊:2S2﹣+O +4H+=2S↓+2HO
2 2 2
C.NH HCO 溶液与足量NaOH溶液混合后加热:NH+OH﹣===NH ↑+H O
4 3 3 2
D.用氨水溶解氯化银沉淀:AgCl+2NH•H O=[Ag(NH)]++Cl﹣+2H O
3 2 3 2 2
答案:D
解析:A.向碘化亚铁溶液中滴加少量稀硝酸反应的离子方程式为:2NO -+8H+=3I+2NO↑
+6I 2
+4HO,故A错误;
2
B.久置的HS 溶液被氧气氧化生成S沉淀而变浑浊,离子方程式:2HS+O=2S↓+2HO,故
2 2 2 2
B错误;
C.氢氧化钠足量,铵根离子、碳酸氢根离子都参加反应.离子方程式:NH+HCO ﹣===CO
+2OH
NH ↑+2H O,故C错误;
+ 3 2
D.氨水与氯化银沉淀发生络合反应生成可溶性络合物,离子方程式:AgCl+2NH ·H O=
3 2
Ag(NH)+Cl-+2HO,故D正确;
3 2
9.下列各组离子能大量共存,且加入相应试剂后发生反应的离子方程式正确的是
选项 离子组 加入试剂 加入试剂后发生的离子反应
A II、NH、SO HO 溶液 2I-+2HO=I+2HO+O↑
2 2 2 2 2 2 2
B K+、HCO NO AlCl 溶液 Al3++3HCO Al(OH) +3CO↑
、 3 = 3 2
C Ag+、Ba2+、S2- HSO 溶液 2H++S2-=HS↑
2 4 2
D Fe3+、Cl-、SCN- NaOH溶液 Fe3++3OH-=Fe(OH) ↓
3
答案:B
解析:A.过氧化氢和碘离子反应生成碘单质和水,离子方程式为 2I-+2H++HO =I +
2 2 2
2HO,A错误;
2
B.铝离子和碳酸氢根离子双水解生成氢氧化铝沉淀和二氧化碳,B正确;
C.银离子和硫离子生成硫化银沉淀,不共存,C错误;
D.Fe3+和SCN-生成红色物质,不共存,D错误;
10.工业上以SO 和纯碱(Na CO)为原料制备无水NaHSO 的主要流程如图所示。下列说法错误
2 2 3 3
的是(已知:HSO 的K =1.5×10-2,K =1.0×10-7)
2 3 a1 a2
A. “吸收”反应的离子方程式为CO 2SO +HO=CO+2HSO
+ 2 2 2
B. “结晶”后的母液可循环使用
C. “干燥”时应在高温下通入SO 气体
2
D. “干燥”后的无水NaHSO 产品中可能混有NaSO
3 2 4
答案:C
解析:碳酸钠吸收二氧化硫生成亚硫酸氢钠,结晶在二氧化硫气流中烘干得到亚硫酸氢钠晶体;
A.已知:HSO 的K =1.5×10-2,K =1.0×10-7;吸收后溶液pH为4.1,溶液显酸性,则反应
2 3 a1 a2
生成亚硫酸氢钠,离子方程式为CO 2SO +HO=CO+2HSO
+ 2 2 2 ,A正确;
B.“结晶”后的母液后含有亚硫酸氢钠,可循环使用,B正确;
C.亚硫酸氢钠受热分解,故不能高温干燥,C错误;
D.亚硫酸氢钠容易被空气中氧气氧化为硫酸钠,故“干燥”后的无水NaHSO 产品中可能混
3
有NaSO ,D正确;
2 4
11.一种白色结晶状粉末化合物X由4种短周期元素构成,为探究其性质。完成了以下实验;
回答下列问题:
(1)X的组成元素是____________,X的化学式是____________。
(2)溶液Y在酸性条件下能使淀粉、KI溶液变蓝色,写出离子方程式:__________________。
(3)固体X的水溶液能使酸性高锰酸钾溶液褪色,写出化学方程式:__________________。
(4)请设计一个实验方案检验红棕色混合气体的组成。_______________。
答案:(1)氢、氮、氧、硫 NOHSO (2)2NO I-+4H+=I+2NO↑+2HO
4 +2 2 2
(3)2KMnO+5NOHSO +2HO=KSO +2MnSO +5HNO+2HSO
4 4 2 2 4 4 3 2 4
(4)将红棕色气体通过冷凝装置冷凝,若气体变为无色,说明含有二氧化氮气体;充分冷凝后的
气体通过排水法收集后得到的无色气体,遇到空气变为红棕色,说明存在一氧化氮气体
解析:白色结晶状粉末化合物X由4种短周期元素构成,生成红棕色气体被氢氧化钠吸收生成
Y,则气体中含有二氧化氮,得到溶液Y在酸性条件下能使淀粉、KI溶液变蓝色,则Y含有亚硝
酸钠,根据钠、氮元素关系可知,氮元素为0.2L×1.0mol/L=0.2mol;得到强酸和硝酸钡生成硫酸钡
沉淀26.6g,则硫酸根离子物质的量为26.6g÷233g/mol=0.2mol;X和水加热生成氮氧化合物和含硫
酸根离子的强酸,根据质量守恒可知,4种元素应该为氢、氮、氧、硫,硫酸根质量为0.2mol×96g/mol=19.2g、氮元素质量为0.2mol×14g/mol=2.8g,含有剩余氢氧质量为
25.4g-19.2g-2.8g=3.4g,则应该还有0.2mol的OH-,故X应该为NOHSO ;
4
(1)由分析可知,X的组成元素是氢、氮、氧、硫,X的化学式是NOHSO ;
4
(2)溶液Y在酸性条件下能使淀粉、KI溶液变蓝色,则反应为亚硝酸根离子在酸性条件下将碘
离子氧化为碘单质,反应为2NO I-+4H+=I+2NO↑+2HO;
+2 2 2
(3)固体X的水溶液能使酸性高锰酸钾溶液褪色,反应中锰元素化合价降低为+2价,则氮元素
化合价会生成得到硝酸,反应为高锰酸钾和NOHSO 发生氧化还原反应生产硫酸钾、硫酸锰、硝酸
4
和硫酸,出化学方程式:2KMnO +5NOHSO +2HO=KSO +2MnSO +5HNO+2HSO ;
4 4 2 2 4 4 3 2 4
(4)二氧化氮为红棕色气体,一氧化氮为无色气体但是容易和氧气生成红棕色二氧化氮气体,故
检验红棕色混合气体的组成方案可以为:将红棕色气体通过冷凝装置冷凝,若气体变为无色,说明
含有二氧化氮气体;充分冷凝后的气体通过排水法收集后得到的无色气体,遇到空气变为红棕色,
说明存在一氧化氮气体。
12.工业上以镍铁硫化矿(主要成分为NiS、FeS、SiO 等)为原料制备兰尼镍(一种带有多孔结
2
构的细 小晶粒组成的镍铝合金,具有优良的储氢性能) ,并获得副产品黄钠铁矾
[NaFe (SO )(OH) ]工艺流程 如下:
3 4 2 6
回答下列问题:
(1)“煆烧过程中NiS、FeS分别转化为Ni O、Fe O,写出NiS转化为Ni O 的化学方程式:
2 3 2 3 2 3
________________________________________________。
(2)已知Ni O 具有强氧化性,则滤渣1的主要成分为_______(填化学式,下同),气体2是
2 3
_______。
(3)滤渣2的主要成分为黄钠铁矾,写出生成黄钠铁矾和气体的离子方程式:_______________。
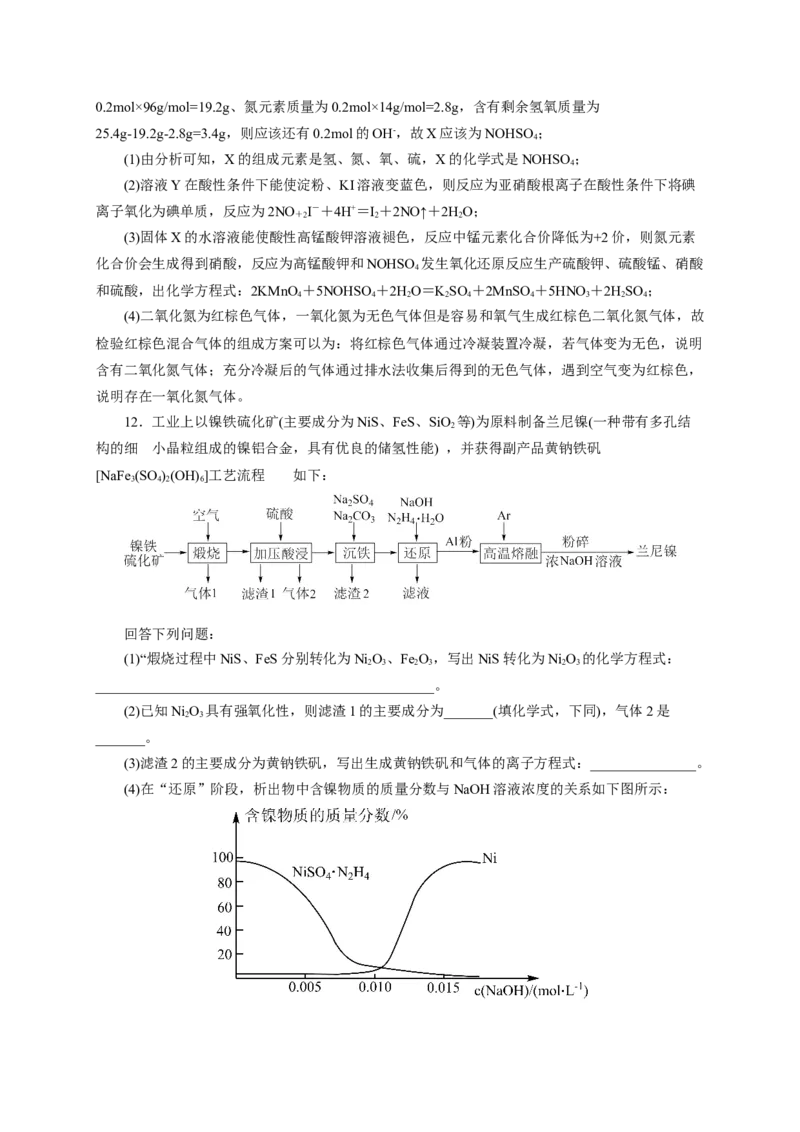
(4)在“还原”阶段,析出物中含镍物质的质量分数与NaOH溶液浓度的关系如下图所示:NaOH溶液浓度不同时,析出产物中Ni的质量分数不同,其原因可能为_________________。
(5)“高温熔融”阶段通入Ar的目的是___________________________________。
(6)“高温熔融”后加浓NaOH溶液的目的是使镍铝合金产生多孔结构,其反应原理为_________
______________________________(用离子方程式表示)。
(7)Ni(OH) 可用于制备镍钴锰三元电极材料。用NiSO 溶液制备Ni(OH) 时,若要使滤液中的
2 4 2
c(Ni2+)≤1.0 ×10-6 mol·L-1,则滤液的pH不小于_______{已知:K [Ni(OH) ] =2.0 ×10-15,lg2=0.3}。
sp 2
答案:(1)4NiS+7O=====2Ni O+4SO (2) SiO O
2 2 3 2 2 2
(3) Na++3Fe3++2SO+6H++6CO NaFe (SO )(OH) ↓+6CO↑
= 3 4 2 6 2
(4)碱性越强,NH 的还原性越强,析出的Ni越多 (5)防止镍、铝被空气中的氧气氧化
2 4
(6) 2Al+2OH-+2HO=2AlO+3H↑ (7)9.65
2 2
解析:由流程图知,镍铁硫化矿(主要成分为NiS、FeS、SiO 等)煅烧时,NiS、FeS与O 反应
2 2
生成Ni O、Fe O 和SO ,则气体1含有SO ,向煅烧后的固体加入硫酸酸浸,Ni O、Fe O 与硫酸
2 3 2 3 2 2 2 3 2 3
反应生成可溶性硫酸盐,发生的反应为2Ni O+4HSO =4NiSO +4HO+O↑、Fe O+3HSO =
2 3 2 4 4 2 2 2 3 2 4
Fe (SO )+4HO+O↑,SiO 不与硫酸反应,则滤渣1中含有SiO,气体2为O,再加入NaSO 和
2 4 3 2 2 2 2 2 2 4
NaCO 沉铁生成NaFe (SO )(OH) ,则滤渣2为NaFe (SO )(OH) ,然后加入NaOH、NH∙HO还
2 3 3 4 2 6 3 4 2 6 2 4 2
原Ni2+生成Ni,Ni与Al粉在Ar氛围中高温熔融生成镍铝合金,最后粉碎加入浓NaOH溶液,铝与
氢氧化钠溶液反应产生氢气使镍铝合金产生多孔的结构,得到兰尼镍。
(1)由题意知,NiS在通入空气煅烧的条件下生成Ni O 和一种气体,其化学方程式为4NiS+
2 3
7O=====2Ni O+4SO ;故答案为:4NiS+7O=====2Ni O+4SO ;
2 2 3 2 2 2 3 2
(2)据分析知,滤渣1的主要成分为SiO;气体2是O;故答案为:SiO;O;
2 2 2 2
(3)根据流程中所加入的试剂,以及生成物可知生成黄钠铁矾和气体的离子方程式为Na++
3Fe3++2SO+6H++6CO NaFe (SO )(OH) ↓+6CO↑;故答案为:Na++3Fe3++2SO+6H++6CO
= 3 4 2 6 2 =
NaFe (SO )(OH) ↓+6CO↑;
3 4 2 6 2
(4)从图中可以看出,镍单质的质量随着氢氧化钠的浓度的增大而增大,可能的原因为碱性越强,
NH 的还原性越强,析出的Ni越多;故答案为:碱性越强,NH 的还原性越强,析出的Ni越多;
2 4 2 4
(5)高温熔融通入Ar形成无氧环境,目的是防止镍、铝被空气中的氧气氧化;故答案为:防止
镍、铝被空气中的氧气氧化;
(6)据分析知,“高温熔融”后加浓NaOH溶液的目的是使镍铝合金产生多孔结构的原因是铝与
氢氧化钠反应产生氢气,其离子方程式为2Al+2OH-+2HO=2AlO+3H↑;故答案为:2Al+2OH
2 2
-+2HO=2AlO+3H↑;
2 2
(7)根据K [Ni(OH) ]=c(Ni2+)∙c2(OH-)=2.0×10-15,若要是溶液中c(Ni2+)≤1.0 ×10-6 mol·L-1,则
sp 2
c(OH-)≥≥×10-4.5mol·L-1,pOH=-lgc(OH-)≤4.5-0.15≤4.35,又pH+pOH=14,则pH≥9.65;故答
案为:9.65。