文档内容
2024 高考一轮复习收官卷
第 1 模拟
时间:100分钟 分值:100分
可能用到的相对原子质量:H 1 C 12 O16 Na 23 Mg24 S 32 Cl 35.5 Cu 64 As 75 Ag 108
一、选择题(每小题只有一个正确选项,共16×3分)
1.(2023·全国·校联考一模)“蓝天、碧水、净土”三大环保保卫战正加快生态环境治理和现代化建设。
下列说法错误的是
A.废旧电池必须回收处理,可以防止重金属污染
B.尽量少用或不用含磷洗涤剂,以防止水体富营养化
C.农田使用铵态氮肥要深施覆土,以防止氮肥被氧化
D.在燃油车上安装三元催化转化器,以降低污染气体的排放
2.(2023·湖南长沙·长郡中学校联考模拟预测)下列化学用语不正确的是
A.果糖、核糖的分子式:
B.甲醛中 键的电子云轮廓图:
C. 的VSEPR模型:
D.氨气分子中氮原子的杂化轨道表示式:
3.(2023·河北唐山·统考模拟预测)下列方案设计、现象和结论正确的是
选项 实验目的 实验方案 现象或结论
判断KCl的化学 将KCl固体溶于水, 溶液可导电,说明KCl中含有离子
A
键类型 进行导电性实验 键
向鸡蛋清溶液中滴加 溶液变浑浊,再加水浑浊消失说明
B 检验蛋白质性质
饱和(NH )SO 溶液 鸡蛋清溶液发生了盐析
4 2 4
检验溶液中是否 取少量该溶液于试管 有白色沉淀生成,说明该溶液中一
C
含有SO 中,滴加BaCl 溶液 定含有SO
2
探究不同价态硫 向NaS与NaSO 的混 溶液变浑浊,说明NaS与NaSO 之
2 2 3 2 2 3
D
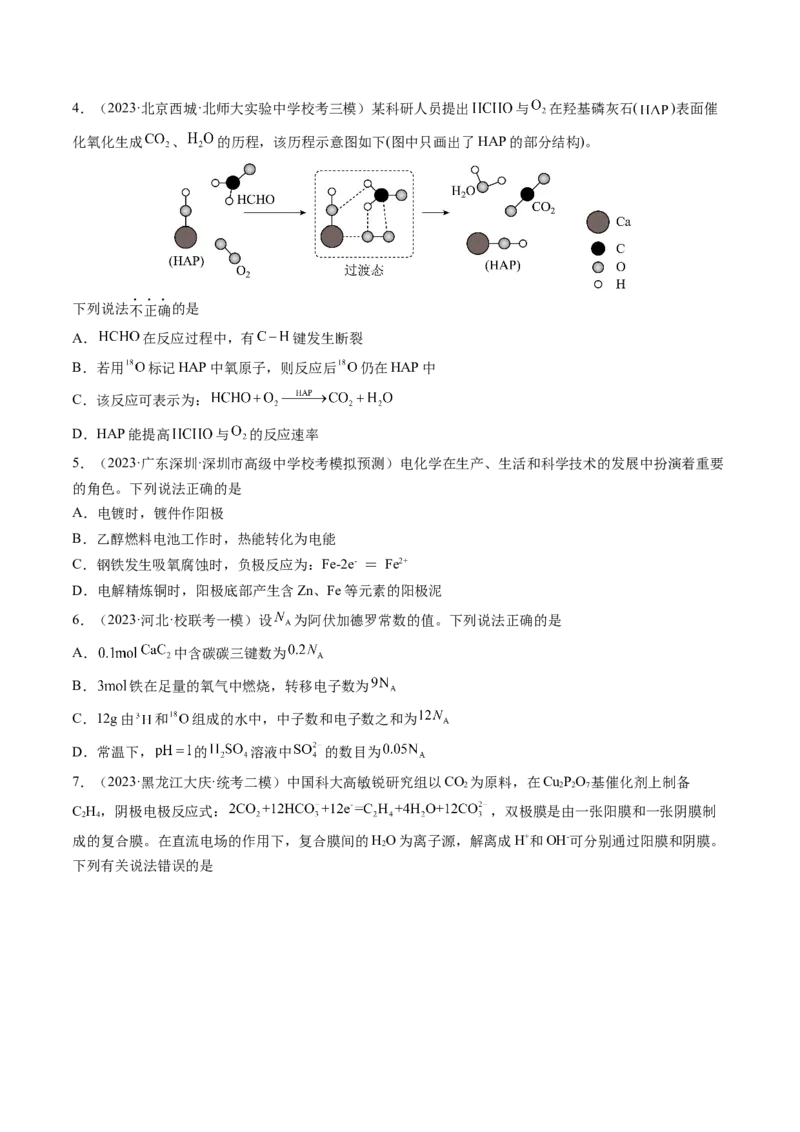
元素的转化 合溶液中加入硝酸 间发生了氧化还原反应4.(2023·北京西城·北师大实验中学校考三模)某科研人员提出 与 在羟基磷灰石( )表面催
化氧化生成 、 的历程,该历程示意图如下(图中只画出了HAP的部分结构)。
下列说法不正确的是
A. 在反应过程中,有 键发生断裂
B.若用 标记HAP中氧原子,则反应后 仍在HAP中
C.该反应可表示为:
D.HAP能提高 与 的反应速率
5.(2023·广东深圳·深圳市高级中学校考模拟预测)电化学在生产、生活和科学技术的发展中扮演着重要
的角色。下列说法正确的是
A.电镀时,镀件作阳极
B.乙醇燃料电池工作时,热能转化为电能
C.钢铁发生吸氧腐蚀时,负极反应为:Fe-2e- = Fe2+
D.电解精炼铜时,阳极底部产生含Zn、Fe等元素的阳极泥
6.(2023·河北·校联考一模)设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含碳碳三键数为
B. 铁在足量的氧气中燃烧,转移电子数为
C.12g由 和 组成的水中,中子数和电子数之和为
D.常温下, 的 溶液中 的数目为
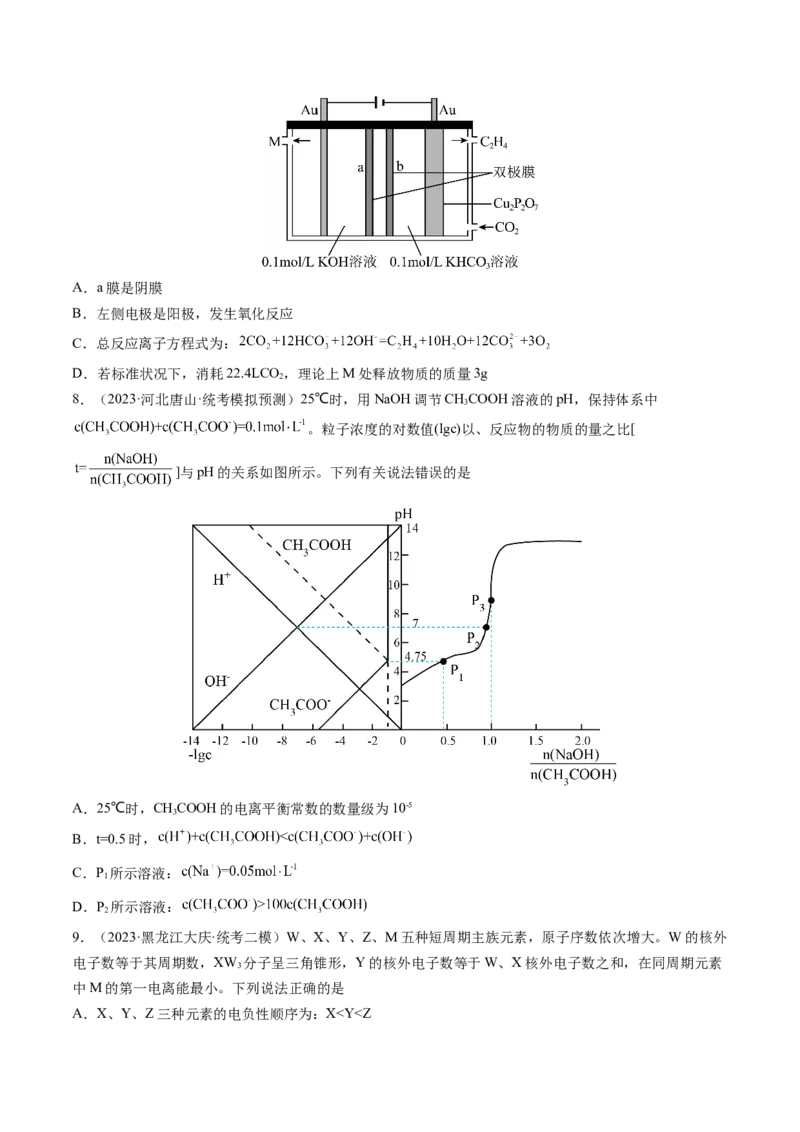
7.(2023·黑龙江大庆·统考二模)中国科大高敏锐研究组以CO 为原料,在Cu PO 基催化剂上制备
2 2 2 7
C H,阴极电极反应式: ,双极膜是由一张阳膜和一张阴膜制
2 4
成的复合膜。在直流电场的作用下,复合膜间的HO为离子源,解离成H+和OH-可分别通过阳膜和阴膜。
2
下列有关说法错误的是A.a膜是阴膜
B.左侧电极是阳极,发生氧化反应
C.总反应离子方程式为:
D.若标准状况下,消耗22.4LCO ,理论上M处释放物质的质量3g
2
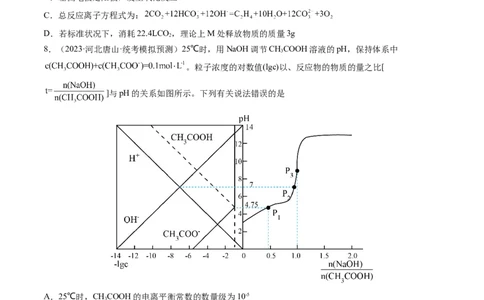
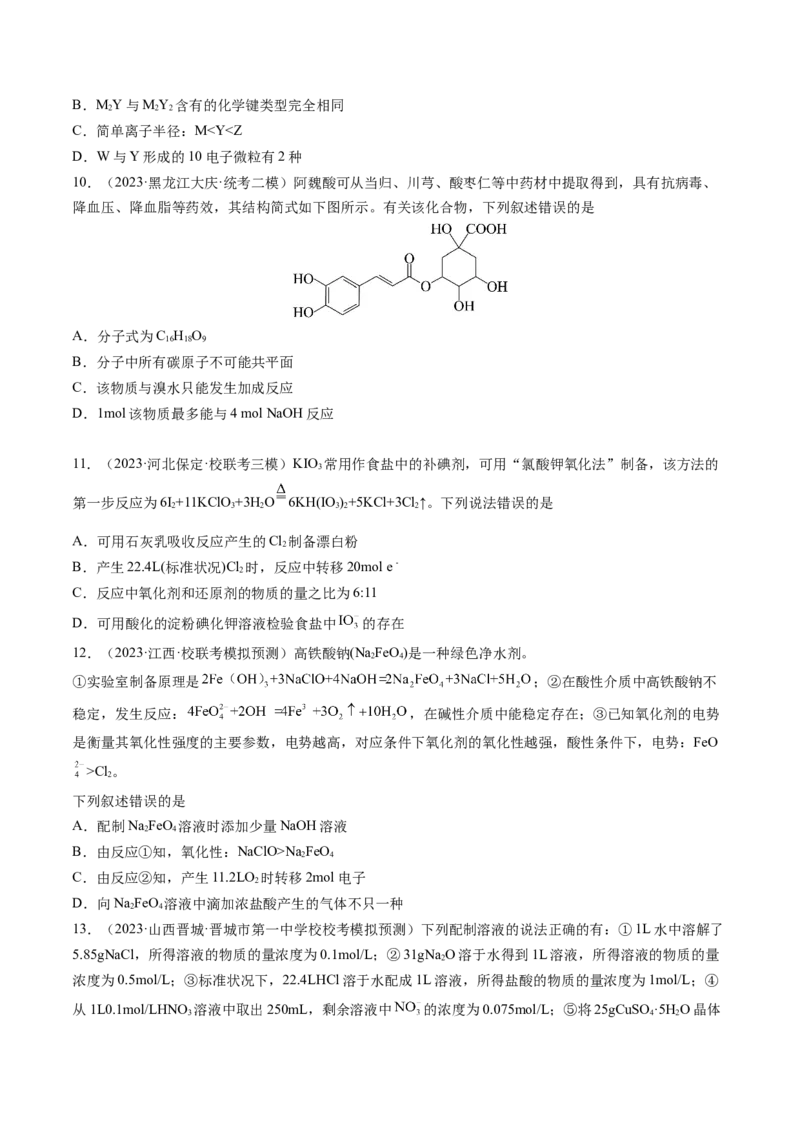
8.(2023·河北唐山·统考模拟预测)25℃时,用NaOH调节CHCOOH溶液的pH,保持体系中
3
。粒子浓度的对数值(lgc)以、反应物的物质的量之比[
]与pH的关系如图所示。下列有关说法错误的是
A.25℃时,CHCOOH的电离平衡常数的数量级为10-5
3
B.t=0.5时,
C.P 所示溶液:
1
D.P 所示溶液:
2
9.(2023·黑龙江大庆·统考二模)W、X、Y、Z、M五种短周期主族元素,原子序数依次增大。W的核外
电子数等于其周期数,XW 分子呈三角锥形,Y的核外电子数等于W、X核外电子数之和,在同周期元素
3
中M的第一电离能最小。下列说法正确的是
A.X、Y、Z三种元素的电负性顺序为:XCl。
2
下列叙述错误的是
A.配制NaFeO 溶液时添加少量NaOH溶液
2 4
B.由反应①知,氧化性:NaClO>Na FeO
2 4
C.由反应②知,产生11.2LO 时转移2mol电子
2
D.向NaFeO 溶液中滴加浓盐酸产生的气体不只一种
2 4
13.(2023·山西晋城·晋城市第一中学校校考模拟预测)下列配制溶液的说法正确的有:①1L水中溶解了
5.85gNaCl,所得溶液的物质的量浓度为0.1mol/L;②31gNaO溶于水得到1L溶液,所得溶液的物质的量
2
浓度为0.5mol/L;③标准状况下,22.4LHCl溶于水配成1L溶液,所得盐酸的物质的量浓度为1mol/L;④
从1L0.1mol/LHNO 溶液中取出250mL,剩余溶液中 的浓度为0.075mol/L;⑤将25gCuSO ·5H O晶体
3 4 2溶于75g水中所得溶质的质量分数为16%;⑥将一定量18.4mol/L的硫酸与水等质量混合,所得溶液的浓
度大于9.2mol/L
A.①③ B.④⑥ C.③⑤ D.⑤⑥
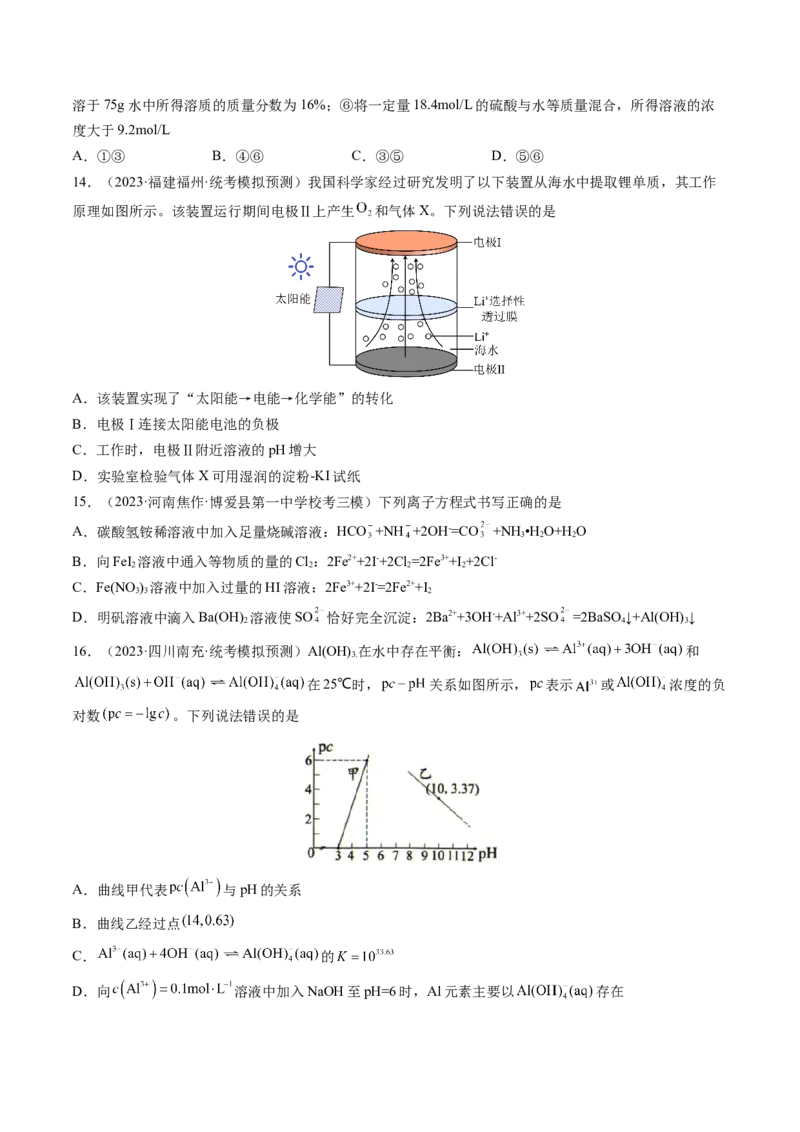
14.(2023·福建福州·统考模拟预测)我国科学家经过研究发明了以下装置从海水中提取锂单质,其工作
原理如图所示。该装置运行期间电极Ⅱ上产生 和气体X。下列说法错误的是
A.该装置实现了“太阳能→电能→化学能”的转化
B.电极Ⅰ连接太阳能电池的负极
C.工作时,电极Ⅱ附近溶液的pH增大
D.实验室检验气体X可用湿润的淀粉-KI试纸
15.(2023·河南焦作·博爱县第一中学校考三模)下列离子方程式书写正确的是
A.碳酸氢铵稀溶液中加入足量烧碱溶液:HCO +NH +2OH-=CO +NH•H O+HO
3 2 2
B.向FeI 溶液中通入等物质的量的Cl:2Fe2++2I-+2Cl=2Fe3++I +2Cl-
2 2 2 2
C.Fe(NO ) 溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I
3 3 2
D.明矾溶液中滴入Ba(OH) 溶液使SO 恰好完全沉淀:2Ba2++3OH-+Al3++2SO =2BaSO ↓+Al(OH) ↓
2 4 3
16.(2023·四川南充·统考模拟预测)Al(OH) 在水中存在平衡: 和
3.
在25℃时, 关系如图所示, 表示 或 浓度的负
对数 。下列说法错误的是
A.曲线甲代表 与pH的关系
B.曲线乙经过点
C. 的
D.向 溶液中加入NaOH至pH=6时,Al元素主要以 存在二、主观题(共5小题,共52分)
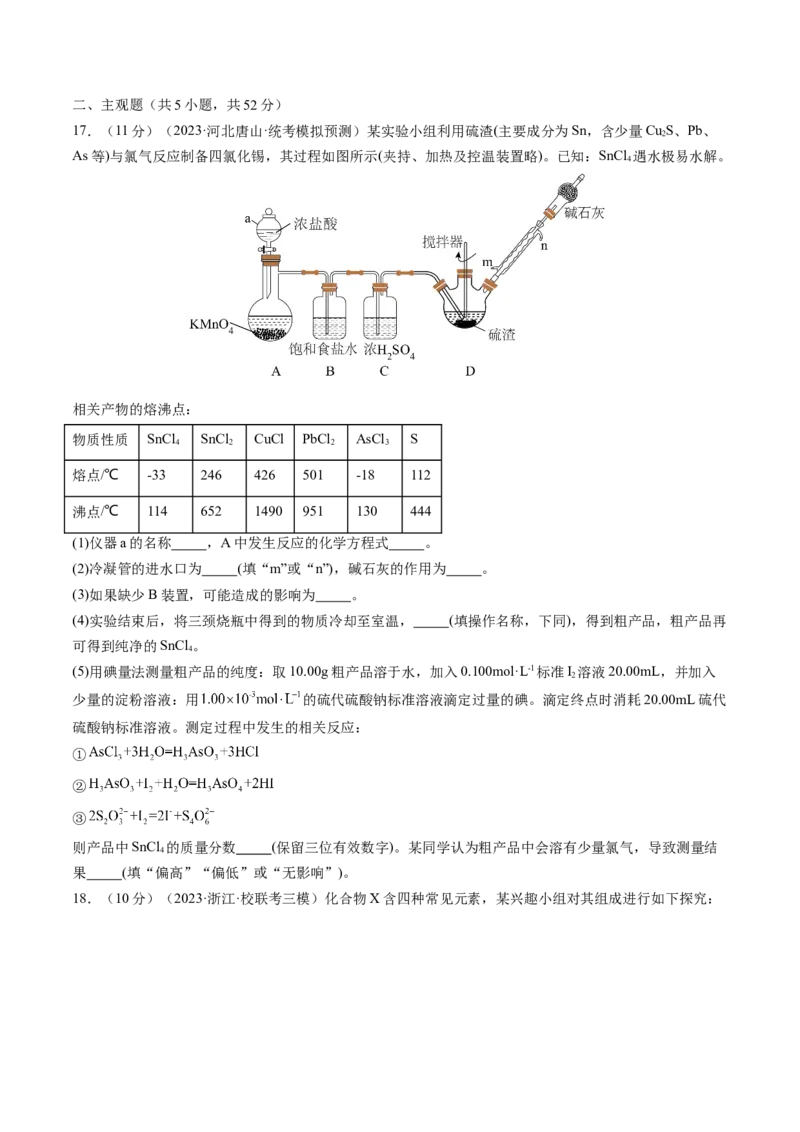
17.(11分)(2023·河北唐山·统考模拟预测)某实验小组利用硫渣(主要成分为Sn,含少量Cu S、Pb、
2
As等)与氯气反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。已知:SnCl 遇水极易水解。
4
相关产物的熔沸点:
物质性质 SnCl SnCl CuCl PbCl AsCl S
4 2 2 3
熔点/℃ -33 246 426 501 -18 112
沸点/℃ 114 652 1490 951 130 444
(1)仪器a的名称 ,A中发生反应的化学方程式 。
(2)冷凝管的进水口为 (填“m”或“n”),碱石灰的作用为 。
(3)如果缺少B装置,可能造成的影响为 。
(4)实验结束后,将三颈烧瓶中得到的物质冷却至室温, (填操作名称,下同),得到粗产品,粗产品再
可得到纯净的SnCl 。
4
(5)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol·L-1标准I 溶液20.00mL,并加入
2
少量的淀粉溶液:用 的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代
硫酸钠标准溶液。测定过程中发生的相关反应:
①
②
③
则产品中SnCl 的质量分数 (保留三位有效数字)。某同学认为粗产品中会溶有少量氯气,导致测量结
4
果 (填“偏高”“偏低”或“无影响”)。
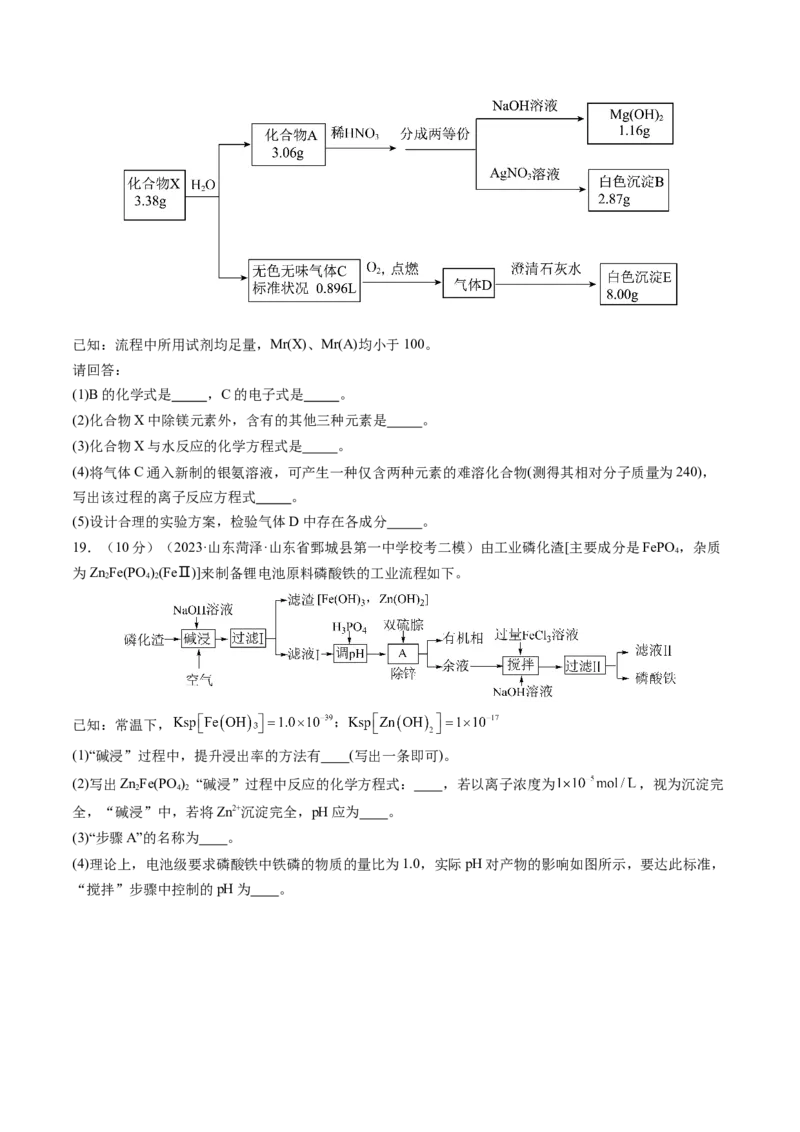
18.(10分)(2023·浙江·校联考三模)化合物X含四种常见元素,某兴趣小组对其组成进行如下探究:已知:流程中所用试剂均足量,Mr(X)、Mr(A)均小于100。
请回答:
(1)B的化学式是 ,C的电子式是 。
(2)化合物X中除镁元素外,含有的其他三种元素是 。
(3)化合物X与水反应的化学方程式是 。
(4)将气体C通入新制的银氨溶液,可产生一种仅含两种元素的难溶化合物(测得其相对分子质量为240),
写出该过程的离子反应方程式 。
(5)设计合理的实验方案,检验气体D中存在各成分 。
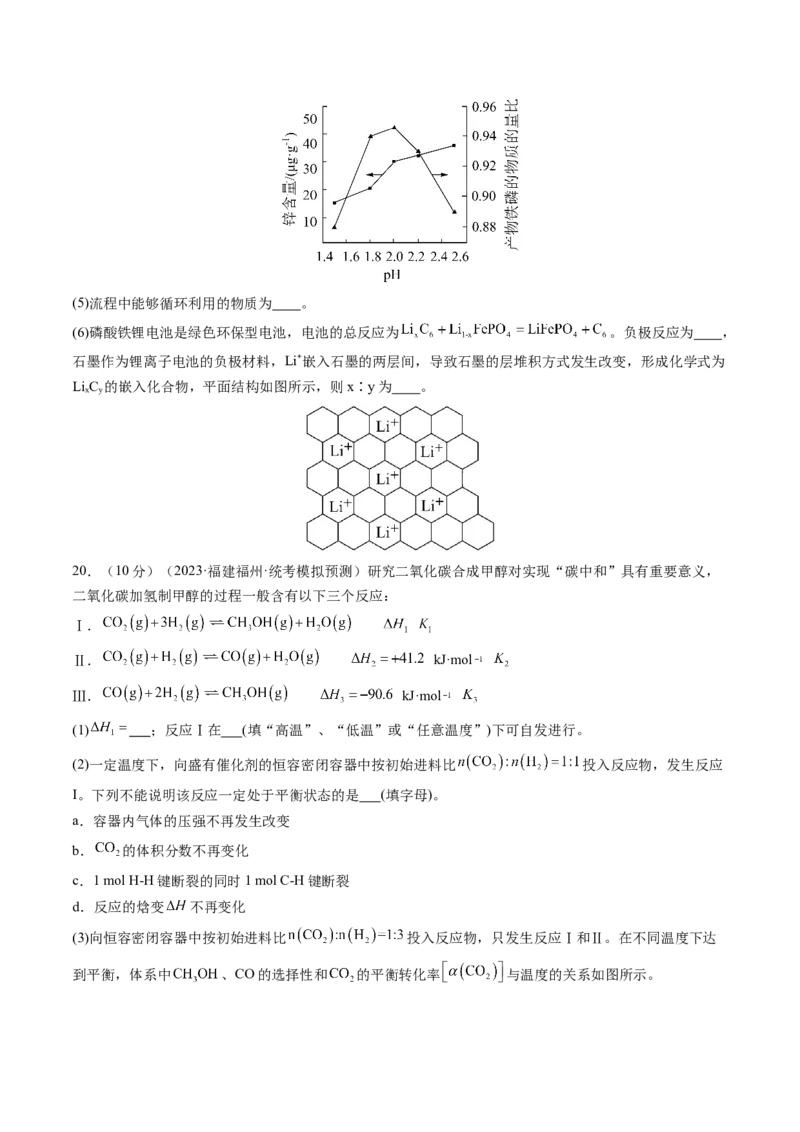
19.(10分)(2023·山东菏泽·山东省鄄城县第一中学校考二模)由工业磷化渣[主要成分是FePO ,杂质
4
为ZnFe(PO )(FeⅡ)]来制备锂电池原料磷酸铁的工业流程如下。
2 4 2
已知:常温下,
(1)“碱浸”过程中,提升浸出率的方法有 (写出一条即可)。
(2)写出ZnFe(PO ) “碱浸”过程中反应的化学方程式: ,若以离子浓度为 ,视为沉淀完
2 4 2
全,“碱浸”中,若将Zn2+沉淀完全,pH应为 。
(3)“步骤A”的名称为 。
(4)理论上,电池级要求磷酸铁中铁磷的物质的量比为1.0,实际pH对产物的影响如图所示,要达此标准,
“搅拌”步骤中控制的pH为 。(5)流程中能够循环利用的物质为 。
(6)磷酸铁锂电池是绿色环保型电池,电池的总反应为 。负极反应为 ,
石墨作为锂离子电池的负极材料,Li⁺嵌入石墨的两层间,导致石墨的层堆积方式发生改变,形成化学式为
LiC 的嵌入化合物,平面结构如图所示,则x∶y为 。
x y
20.(10分)(2023·福建福州·统考模拟预测)研究二氧化碳合成甲醇对实现“碳中和”具有重要意义,
二氧化碳加氢制甲醇的过程一般含有以下三个反应:
Ⅰ.
Ⅱ. kJ·mol
Ⅲ. kJ·mol
(1) ;反应Ⅰ在 (填“高温”、“低温”或“任意温度”)下可自发进行。
(2)一定温度下,向盛有催化剂的恒容密闭容器中按初始进料比 投入反应物,发生反应
I。下列不能说明该反应一定处于平衡状态的是 (填字母)。
a.容器内气体的压强不再发生改变
b. 的体积分数不再变化
c.1 mol H-H键断裂的同时1 mol C-H键断裂
d.反应的焓变 不再变化
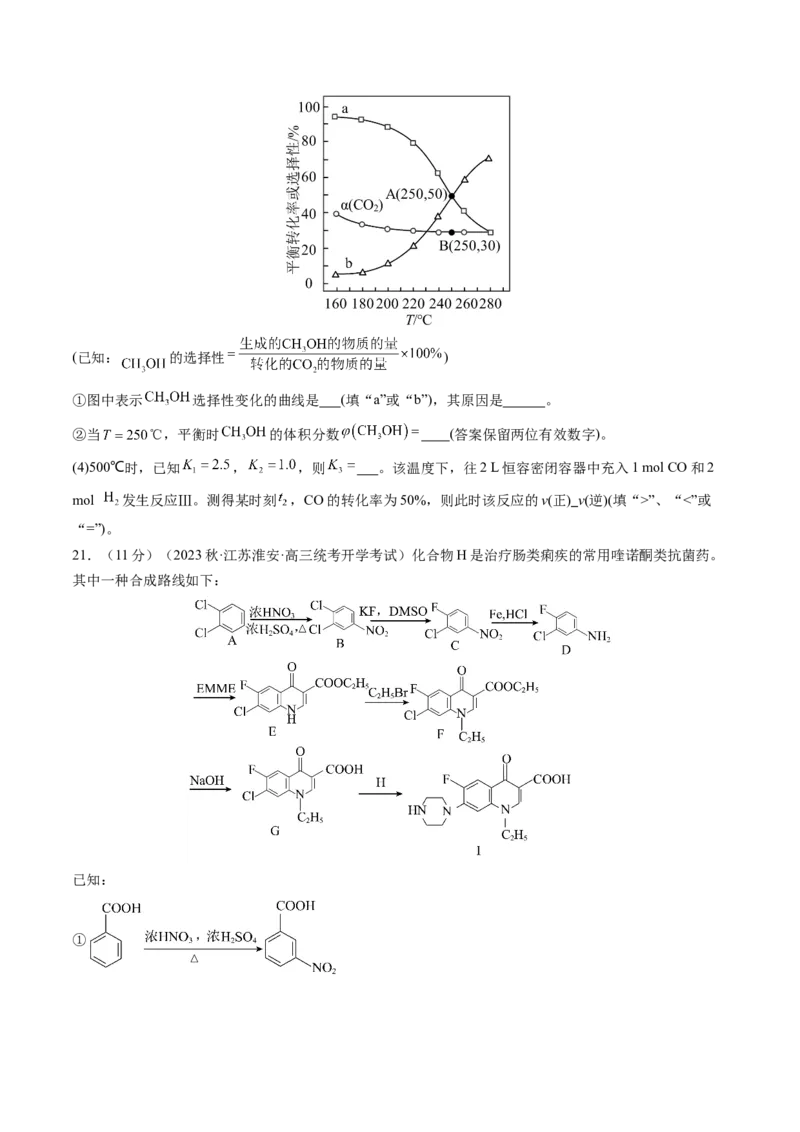
(3)向恒容密闭容器中按初始进料比 投入反应物,只发生反应Ⅰ和Ⅱ。在不同温度下达
到平衡,体系中 、CO的选择性和 的平衡转化率 与温度的关系如图所示。(已知: 的选择性 )
①图中表示 选择性变化的曲线是 (填“a”或“b”),其原因是 。
②当 ℃,平衡时 的体积分数 (答案保留两位有效数字)。
(4)500℃时,已知 , ,则 。该温度下,往2 L恒容密闭容器中充入1 mol CO和2
mol 发生反应Ⅲ。测得某时刻 ,CO的转化率为50%,则此时该反应的v(正) v(逆)(填“>”、“<”或
“=”)。
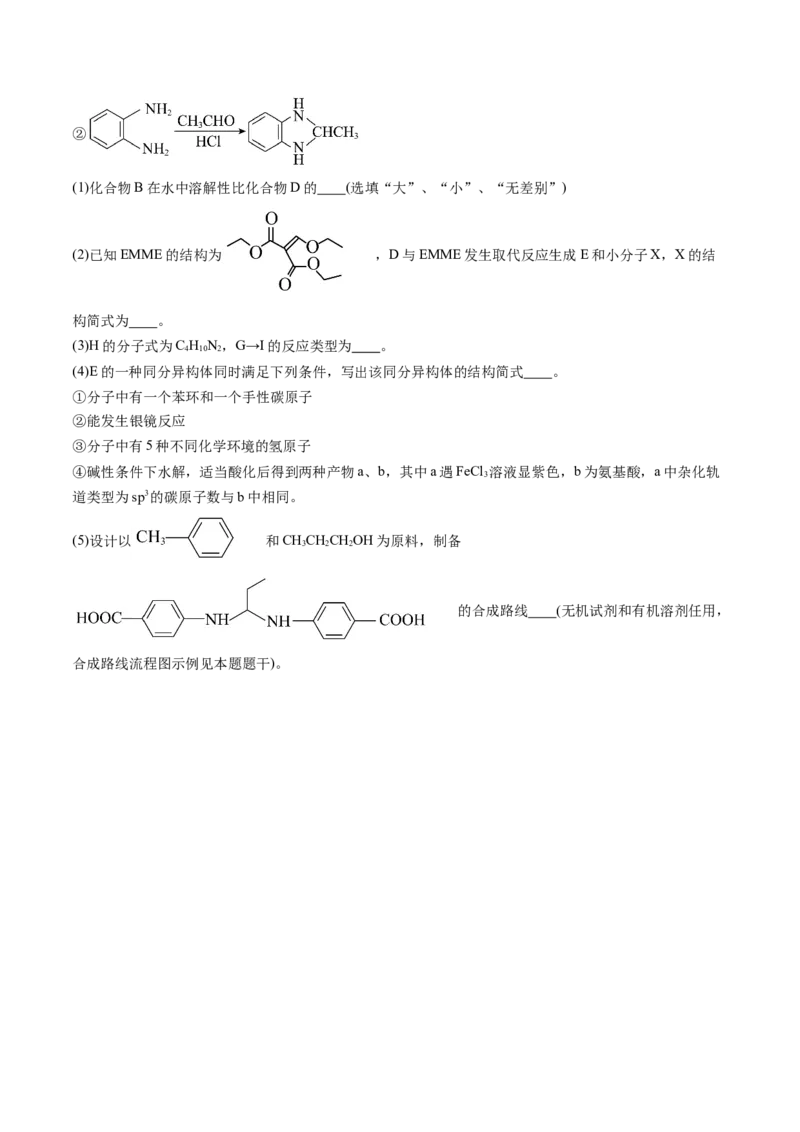
21.(11分)(2023秋·江苏淮安·高三统考开学考试)化合物H是治疗肠类痢疾的常用喹诺酮类抗菌药。
其中一种合成路线如下:
已知:
①②
(1)化合物B在水中溶解性比化合物D的 (选填“大”、“小”、“无差别”)
(2)已知EMME的结构为 ,D与EMME发生取代反应生成E和小分子X,X的结
构简式为 。
(3)H的分子式为C H N,G→I的反应类型为 。
4 10 2
(4)E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式 。
①分子中有一个苯环和一个手性碳原子
②能发生银镜反应
③分子中有5种不同化学环境的氢原子
④碱性条件下水解,适当酸化后得到两种产物a、b,其中a遇FeCl 溶液显紫色,b为氨基酸,a中杂化轨
3
道类型为sp3的碳原子数与b中相同。
(5)设计以 和CHCHCHOH为原料,制备
3 2 2
的合成路线 (无机试剂和有机溶剂任用,
合成路线流程图示例见本题题干)。