文档内容
2025届高三化学一轮专题复习讲义(20)
专题四 元素及其化合物
4-5 非金属及其化合物(三、氮及其重要化合物)(1课时,共3课时)
【复习目标】
1.了解氮元素单质及其重要化合物的制备方法,掌握其主要性质及应用。
2.了解氮及其化合物的转化关系。
3.了解氮的化合物对环境的影响。
【重点突破】
1.精准理解相关化学反应原理,掌握NO 对环境污染的治理应用。
x
2.掌握相关氮的化合物的结构、性质、制备、应用。
【真题再现】
例题1.(2018·江苏)NO(主要指NO和NO )是大气主要污染物之一。有效去除大气中的
x 2
NO 是环境保护的重要课题。
x
(1)用水吸收NO 的相关热化学方程式如下:
x
2NO (g)+HO(l)=== HNO (aq)+HNO (aq) ΔH=−116.1 kJ·mol−1
2 2 3 2
3HNO(aq) ===HNO(aq)+2NO(g)+HO(l) ΔH=75.9 kJ·mol−1
2 3 2
反应3NO (g)+HO(l) ===2HNO(aq)+NO(g)的ΔH= kJ·mol−1。
2 2 3
(2)用稀硝酸吸收NO ,得到HNO 和HNO 的混合溶液,电解该混合溶液可获得较浓的
x 3 2
硝酸。写出电解时阳极的电极反应式: 。
(3)用酸性(NH )CO水溶液吸收NO ,吸收过程中存在HNO 与(NH )CO生成N 和
2 2 x 2 2 2 2
CO 的反应。写出该反应的化学方程式: 。
2
(4)在有氧条件下,新型催化剂M能催化NH 与NO 反应生成N。
3 x 2
①NH 与NO 生成N 的反应中,当生成1 mol N 时,转移的电子数为
3 2 2 2
mol。
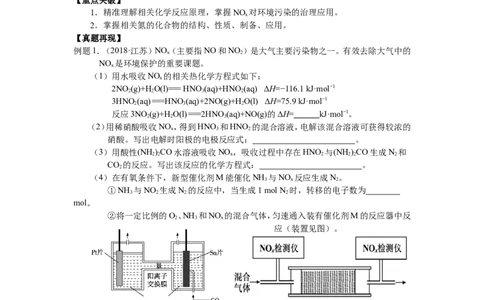
②将一定比例的O、NH 和NO 的混合气体,匀速通入装有催化剂M的反应器中反
2 3 x
应(装置见图)。
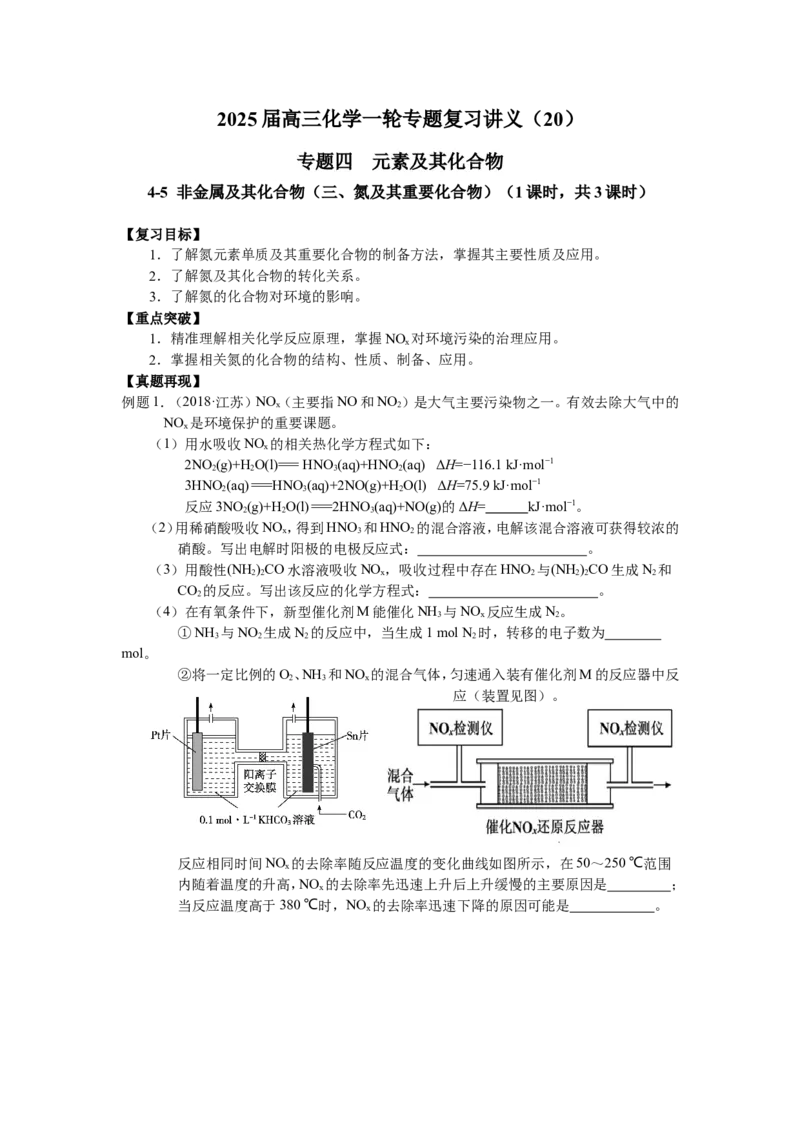
反应相同时间NO 的去除率随反应温度的变化曲线如图所示,在50~250 ℃范围
x
内随着温度的升高,NO 的去除率先迅速上升后上升缓慢的主要原因是 ;
x
当反应温度高于380 ℃时,NO 的去除率迅速下降的原因可能是 。
x。
解析:
(1)应用盖斯定律解答。
(2)根据电解原理,阳极发生失电子的氧化反应,阳极反应为HNO 失去电子生成
2
HNO。
3
(3)HNO 与(NH )CO反应生成N 和CO,根据得失电子守恒和原子守恒写出方程式。
2 2 2 2 2
(4)①NH 与NO 的反应为8NH +6NO 7N+12H O,该反应中NH 中-3价的N升
3 2 3 2 2 2 3
至0价,NO 中+4价的N降至0价,生成7molN 转移24mol电子。
2 2
②因为反应时间相同,所以低温时主要考虑温度和催化剂对化学反应速率的影响;
高温时NH 与O 发生催化氧化反应生成NO。
3 2
答案:(1) −136.2
(2)HNO−2e−+H O===3H++NO−
2 2 3
(3)2HNO+(NH)CO===2N↑+CO ↑+3H O
2 2 2 2 2 2
(4)24/7
(5)迅速上升段是催化剂活性随温度升高增大与温度升高共同使NO 去除反应速率迅
x
速增大;上升缓慢段主要是温度升高引起的NO 去除反应速率增大
x
(6)催化剂活性下降;NH 与O 反应生成了NO
3 2
小结:本题以有效去除NO 为载体,考查盖斯定律的应用、电解原理、指定情境下方程式的书
x
写,氧化还原反应中转移电子数的计算、图像的分析。主要体现的是对化学反应原理
的考查,对化学反应原理的准确理解是解题的关键。
例2.(2019江苏)NO、NO和NO 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后
2 2
才能排放。
(1)NO的处理。NO是硝酸生产中氨催化氧化的副产物,用特种催化剂能使NO分解。
2 2 2
NH 与O 在加热和催化剂作用下生成NO的化学方程式为 。
3 2 2
(2)NO和NO 的处理。已除去NO的硝酸尾气可用NaOH溶液吸收,主要反应为
2 2
NO+NO +2OH-=== 2NO -+H O
2 2 2
2NO +2OH-=== NO -+NO-+H O
2 2 3 2
①下列措施能提高尾气中NO和NO 去除率的有 (填字母)。
2
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO 晶体,所得晶体中的主要杂质是
2
(填化学式);吸收后排放的尾气中含量较高的氮氧化物是 (填化学式)。
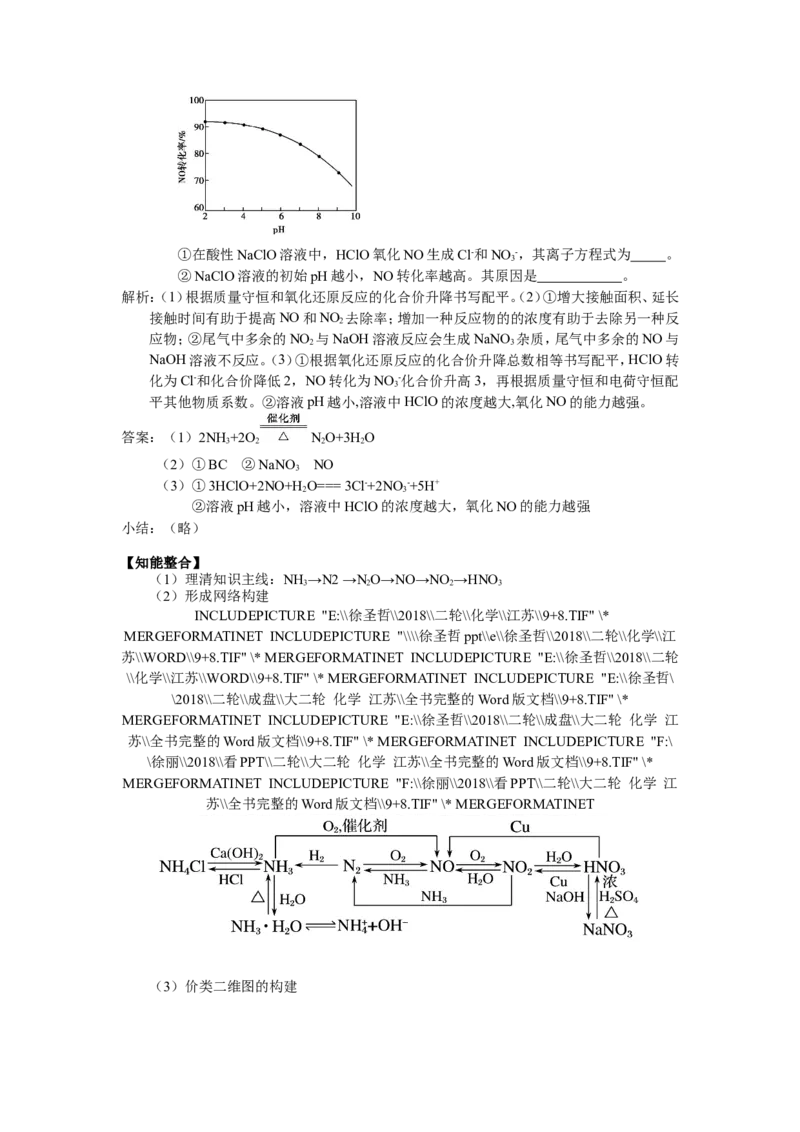
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条
件相同,NO转化为NO -的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如
3
图所示。①在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO -,其离子方程式为 。
3
②NaClO溶液的初始pH越小,NO转化率越高。其原因是 。
解析:(1)根据质量守恒和氧化还原反应的化合价升降书写配平。(2)①增大接触面积、延长
接触时间有助于提高NO和NO 去除率;增加一种反应物的的浓度有助于去除另一种反
2
应物;②尾气中多余的NO 与NaOH溶液反应会生成NaNO 杂质,尾气中多余的NO与
2 3
NaOH溶液不反应。(3)①根据氧化还原反应的化合价升降总数相等书写配平,HClO转
化为Cl-和化合价降低2,NO转化为NO -化合价升高3,再根据质量守恒和电荷守恒配
3
平其他物质系数。②溶液pH越小,溶液中HClO的浓度越大,氧化NO的能力越强。
答案:(1)2NH +2O N O+3HO
3 2 2 2
(2)①BC ②NaNO NO
3
(3)①3HClO+2NO+H O=== 3Cl-+2NO-+5H+
2 3
②溶液pH越小,溶液中HClO的浓度越大,氧化NO的能力越强
小结:(略)
【知能整合】
(1)理清知识主线:NH→N2 →NO→NO→NO→HNO
3 2 2 3
(2)形成网络构建
INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\化学\\江苏\\9+8.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "\\\\徐圣哲ppt\\e\\徐圣哲\\2018\\二轮\\化学\\江
苏\\WORD\\9+8.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮
\\化学\\江苏\\WORD\\9+8.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\
\2018\\二轮\\成盘\\大二轮 化学 江苏\\全书完整的Word版文档\\9+8.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\成盘\\大二轮 化学 江
苏\\全书完整的Word版文档\\9+8.TIF" \* MERGEFORMATINET INCLUDEPICTURE "F:\
\徐丽\\2018\\看PPT\\二轮\\大二轮 化学 江苏\\全书完整的Word版文档\\9+8.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "F:\\徐丽\\2018\\看PPT\\二轮\\大二轮 化学 江
苏\\全书完整的Word版文档\\9+8.TIF" \* MERGEFORMATINET
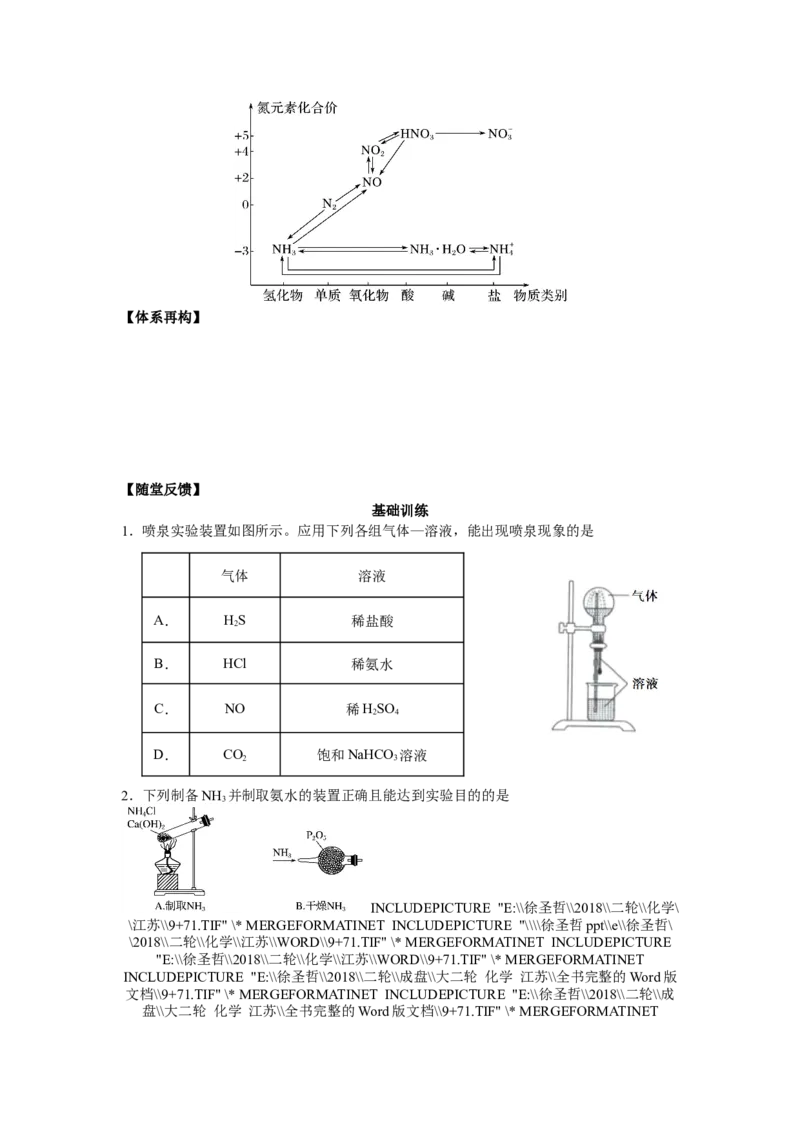
(3)价类二维图的构建【体系再构】
【随堂反馈】
基础训练
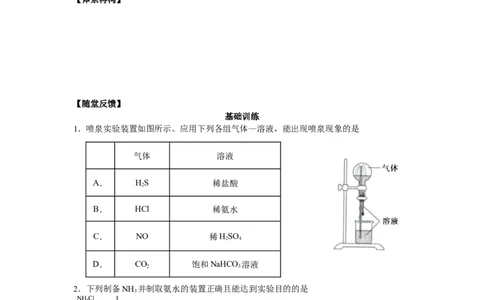
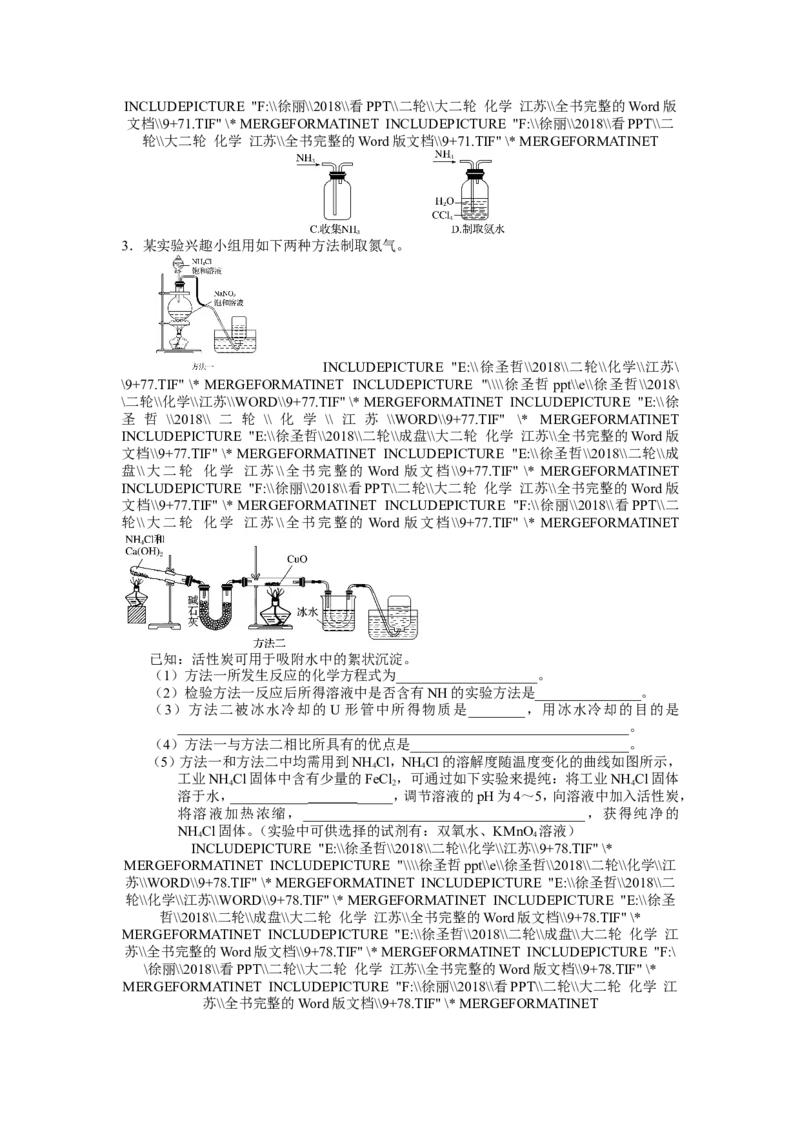
1.喷泉实验装置如图所示。应用下列各组气体—溶液,能出现喷泉现象的是
气体 溶液
A. HS 稀盐酸
2
B. HCl 稀氨水
C. NO 稀HSO
2 4
D. CO 饱和NaHCO 溶液
2 3
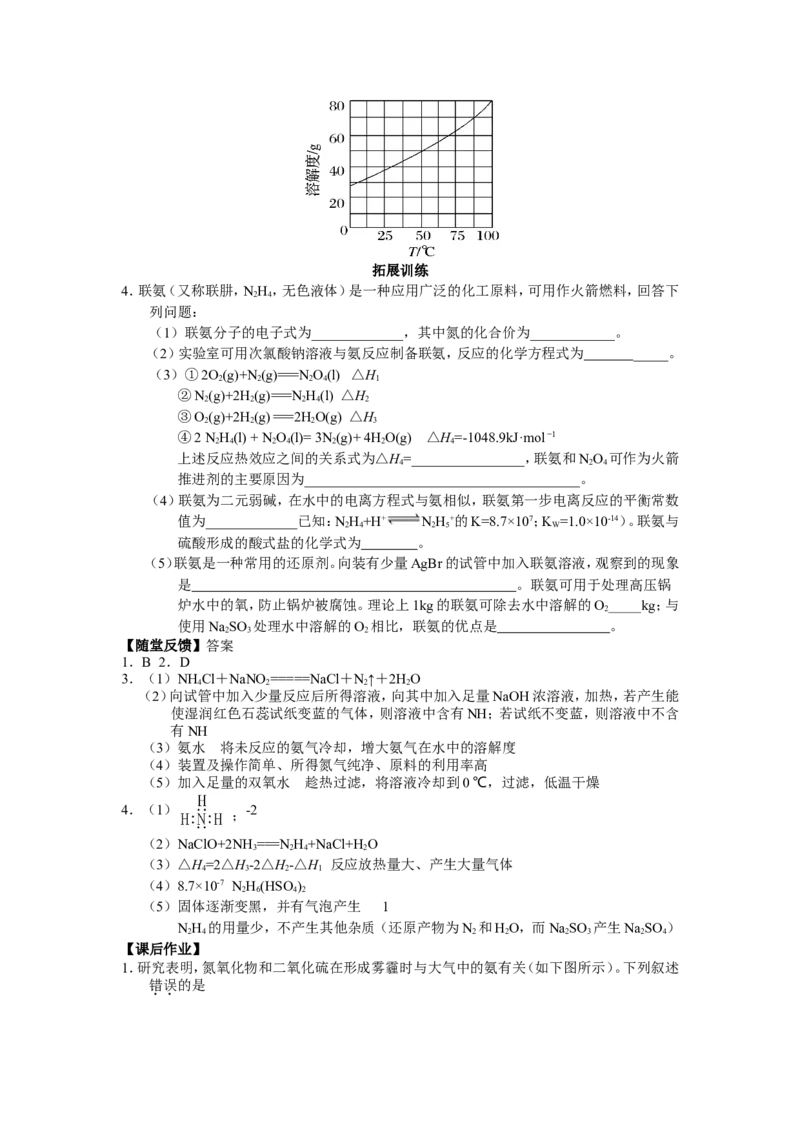
2.下列制备NH 并制取氨水的装置正确且能达到实验目的的是
3
INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\化学\
\江苏\\9+71.TIF" \* MERGEFORMATINET INCLUDEPICTURE "\\\\徐圣哲ppt\\e\\徐圣哲\
\2018\\二轮\\化学\\江苏\\WORD\\9+71.TIF" \* MERGEFORMATINET INCLUDEPICTURE
"E:\\徐圣哲\\2018\\二轮\\化学\\江苏\\WORD\\9+71.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\成盘\\大二轮 化学 江苏\\全书完整的Word版
文档\\9+71.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\成
盘\\大二轮 化学 江苏\\全书完整的Word版文档\\9+71.TIF" \* MERGEFORMATINETINCLUDEPICTURE "F:\\徐丽\\2018\\看PPT\\二轮\\大二轮 化学 江苏\\全书完整的Word版
文档\\9+71.TIF" \* MERGEFORMATINET INCLUDEPICTURE "F:\\徐丽\\2018\\看PPT\\二
轮\\大二轮 化学 江苏\\全书完整的Word版文档\\9+71.TIF" \* MERGEFORMATINET
3.某实验兴趣小组用如下两种方法制取氮气。
INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\化学\\江苏\
\9+77.TIF" \* MERGEFORMATINET INCLUDEPICTURE "\\\\徐圣哲ppt\\e\\徐圣哲\\2018\
\二轮\\化学\\江苏\\WORD\\9+77.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐
圣 哲 \\2018\\ 二 轮 \\ 化 学 \\ 江 苏 \\WORD\\9+77.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\成盘\\大二轮 化学 江苏\\全书完整的Word版
文档\\9+77.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\成
盘\\大二轮 化学 江苏\\全书完整的 Word 版文档\\9+77.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\徐丽\\2018\\看PPT\\二轮\\大二轮 化学 江苏\\全书完整的Word版
文档\\9+77.TIF" \* MERGEFORMATINET INCLUDEPICTURE "F:\\徐丽\\2018\\看PPT\\二
轮\\大二轮 化学 江苏\\全书完整的 Word 版文档\\9+77.TIF" \* MERGEFORMATINET
已知:活性炭可用于吸附水中的絮状沉淀。
(1)方法一所发生反应的化学方程式为____________________。
(2)检验方法一反应后所得溶液中是否含有NH的实验方法是_______________。
(3)方法二被冰水冷却的 U 形管中所得物质是________,用冰水冷却的目的是
________________________________________________________________。
(4)方法一与方法二相比所具有的优点是_______________________________。
(5)方法一和方法二中均需用到NH Cl,NH Cl的溶解度随温度变化的曲线如图所示,
4 4
工业NH Cl固体中含有少量的FeCl ,可通过如下实验来提纯:将工业NH Cl固体
4 2 4
溶于水,___________ _____,调节溶液的pH为4~5,向溶液中加入活性炭,
将溶液加热浓缩,________________________________________,获得纯净的
NH Cl固体。(实验中可供选择的试剂有:双氧水、KMnO 溶液)
4 4
INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\化学\\江苏\\9+78.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "\\\\徐圣哲ppt\\e\\徐圣哲\\2018\\二轮\\化学\\江
苏\\WORD\\9+78.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2018\\二
轮\\化学\\江苏\\WORD\\9+78.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣
哲\\2018\\二轮\\成盘\\大二轮 化学 江苏\\全书完整的Word版文档\\9+78.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\成盘\\大二轮 化学 江
苏\\全书完整的Word版文档\\9+78.TIF" \* MERGEFORMATINET INCLUDEPICTURE "F:\
\徐丽\\2018\\看PPT\\二轮\\大二轮 化学 江苏\\全书完整的Word版文档\\9+78.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "F:\\徐丽\\2018\\看PPT\\二轮\\大二轮 化学 江
苏\\全书完整的Word版文档\\9+78.TIF" \* MERGEFORMATINET拓展训练
4.联氨(又称联肼,NH,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下
2 4
列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为____________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为 _____。
(3)①2O(g)+N(g)===NO(l) △H
2 2 2 4 1
②N(g)+2H(g)===NH(l) △H
2 2 2 4 2
③O(g)+2H(g) ===2HO(g) △H
2 2 2 3
④2 N H(l) + N O(l)= 3N(g)+ 4H O(g) △H=-1048.9kJ·mol −1
2 4 2 4 2 2 4
上述反应热效应之间的关系式为△H=________________,联氨和NO 可作为火箭
4 2 4
推进剂的主要原因为_______________________________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数
值为_____________已知:NH+H+ NH+的K=8.7×107;K =1.0×10-14)。联氨与
2 4 2 5 W
硫酸形成的酸式盐的化学式为 。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象
是 。联氨可用于处理高压锅
炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O kg;与
2
使用NaSO 处理水中溶解的O 相比,联氨的优点是 。
2 3 2
【随堂反馈】答案
1.B 2.D
3.(1)NH Cl+NaNO =====NaCl+N↑+2HO
4 2 2 2
(2)向试管中加入少量反应后所得溶液,向其中加入足量NaOH浓溶液,加热,若产生能
使湿润红色石蕊试纸变蓝的气体,则溶液中含有NH;若试纸不变蓝,则溶液中不含
有NH
(3)氨水 将未反应的氨气冷却,增大氨气在水中的溶解度
(4)装置及操作简单、所得氮气纯净、原料的利用率高
(5)加入足量的双氧水 趁热过滤,将溶液冷却到0 ℃,过滤,低温干燥
4.(1) -2
;
(2)NaClO+2NH ===NH+NaCl+HO
3 2 4 2
(3)△H=2△H-2△H-△H 反应放热量大、产生大量气体
4 3 2 1
(4)8.7×10-7 NH(HSO )
2 6 4 2
(5)固体逐渐变黑,并有气泡产生 1
NH 的用量少,不产生其他杂质(还原产物为N 和HO,而NaSO 产生NaSO )
2 4 2 2 2 3 2 4
【课后作业】
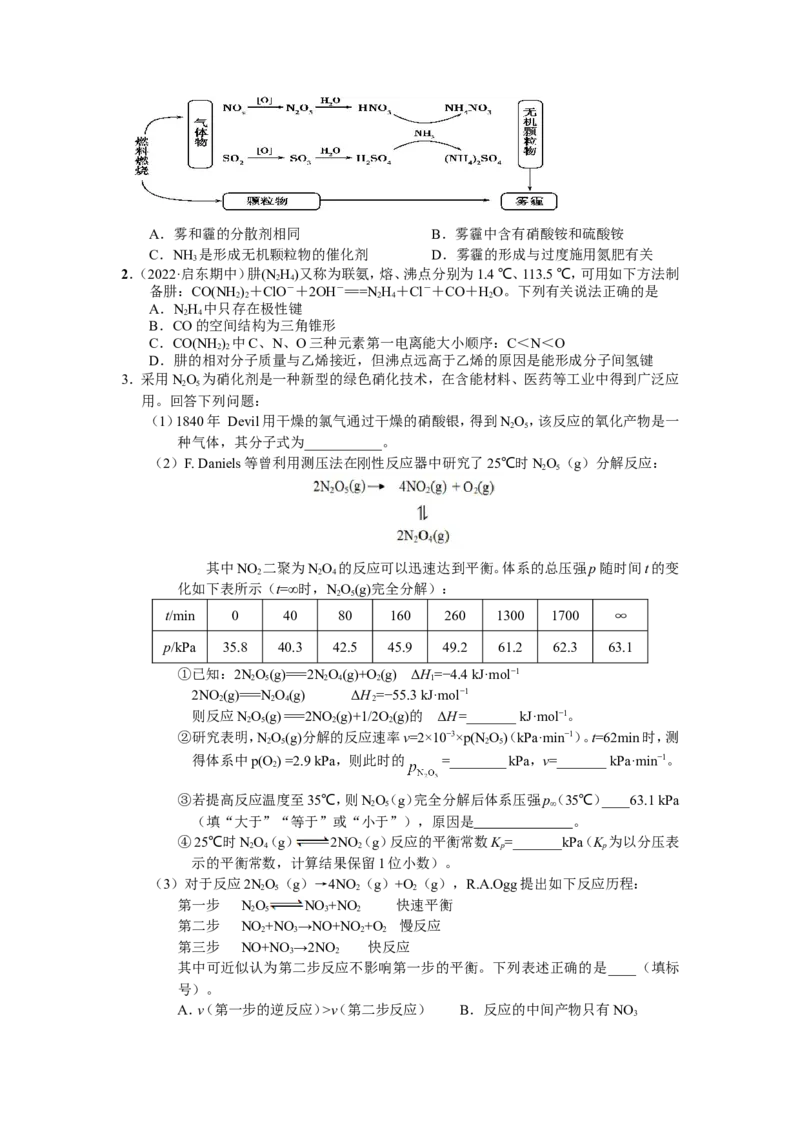
1.研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述
错误的是A.雾和霾的分散剂相同 B.雾霾中含有硝酸铵和硫酸铵
C.NH 是形成无机颗粒物的催化剂 D.雾霾的形成与过度施用氮肥有关
3
2.(2022·启东期中)肼(N H)又称为联氨,熔、沸点分别为1.4 ℃、113.5 ℃,可用如下方法制
2 4
备肼:CO(NH)+ClO-+2OH-===N H+Cl-+CO+HO。下列有关说法正确的是
2 2 2 4 2
A.NH 中只存在极性键
2 4
B.CO的空间结构为三角锥形
C.CO(NH) 中C、N、O三种元素第一电离能大小顺序:C<N<O
2 2
D.肼的相对分子质量与乙烯接近,但沸点远高于乙烯的原因是能形成分子间氢键
3.采用NO 为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应
2 5
用。回答下列问题:
(1)1840年 Devil用干燥的氯气通过干燥的硝酸银,得到NO,该反应的氧化产物是一
2 5
种气体,其分子式为___________。
(2)F. Daniels等曾利用测压法在刚性反应器中研究了25℃时NO(g)分解反应:
2 5
其中NO 二聚为NO 的反应可以迅速达到平衡。体系的总压强p随时间t的变
2 2 4
化如下表所示(t=∞时,NO(g)完全分解):
2 5
t/min 0 40 80 160 260 1300 1700 ∞
p/kPa 35.8 40.3 42.5 45.9 49.2 61.2 62.3 63.1
①已知:2NO(g)===2NO(g)+O (g) ΔH=−4.4 kJ·mol−1
2 5 2 4 2 1
2NO (g)===NO(g) ΔH =−55.3 kJ·mol−1
2 2 4 2
则反应NO(g) ===2NO (g)+1/2O (g)的 ΔH=_______ kJ·mol−1。
2 5 2 2
②研究表明,NO(g)分解的反应速率v=2×10−3×p(N O() kPa·min−1)。t=62min时,测
2 5 2 5
得体系中p(O ) =2.9 kPa,则此时的 =________kPa,v=_______ kPa·min−1。
2
③若提高反应温度至35℃,则NO(g)完全分解后体系压强p(35℃)____63.1 kPa
2 5 ∞
(填“大于”“等于”或“小于”),原因是 。
④25℃时NO(g) 2NO(g)反应的平衡常数K =_______kPa(K 为以分压表
2 4 2 p p
示的平衡常数,计算结果保留1位小数)。
(3)对于反应2NO(g)→4NO (g)+O (g),R.A.Ogg提出如下反应历程:
2 5 2 2
第一步 NO NO +NO 快速平衡
2 5 3 2
第二步 NO +NO→NO+NO +O 慢反应
2 3 2 2
第三步 NO+NO →2NO 快反应
3 2
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是____(填标
号)。
A.v(第一步的逆反应)>v(第二步反应) B.反应的中间产物只有NO
3C.第二步中NO 与NO 的碰撞仅部分有效 D.第三步反应活化能较高
2 3
4.(2022·常州期中)燃煤烟气中90%以上的NO 是NO,脱硝技术主要就是指NO的脱除技
x
术。
Ⅰ.络合脱硝法
六氨合钴溶液中的[Co(NH )]2+能络合烟气中的NO和O ,形成的两种络合物在溶
3 6 2
液中极易发生反应,实现NO的脱除。在吸收液中加入活性炭可有效催化[Co(NH )]2+的
3 6
再生,维持溶液脱除NO的能力,原理下图所示。
(1)写出上述络合脱硝法总反应的离子方程式:________________________。
(2)在不同温度下,将含0.01 mol·L−1 [Co(NH)]3+的溶液以一定流速通过装有活性炭
3 6
的催化器,[Co(NH )]3+的转化率随温度升高而增大,其原因可能是____。
3 6
Ⅱ.氧化脱硝法
ClO 溶液常用于氧化脱除烟气中的NO、SO 等污染物。
2 2
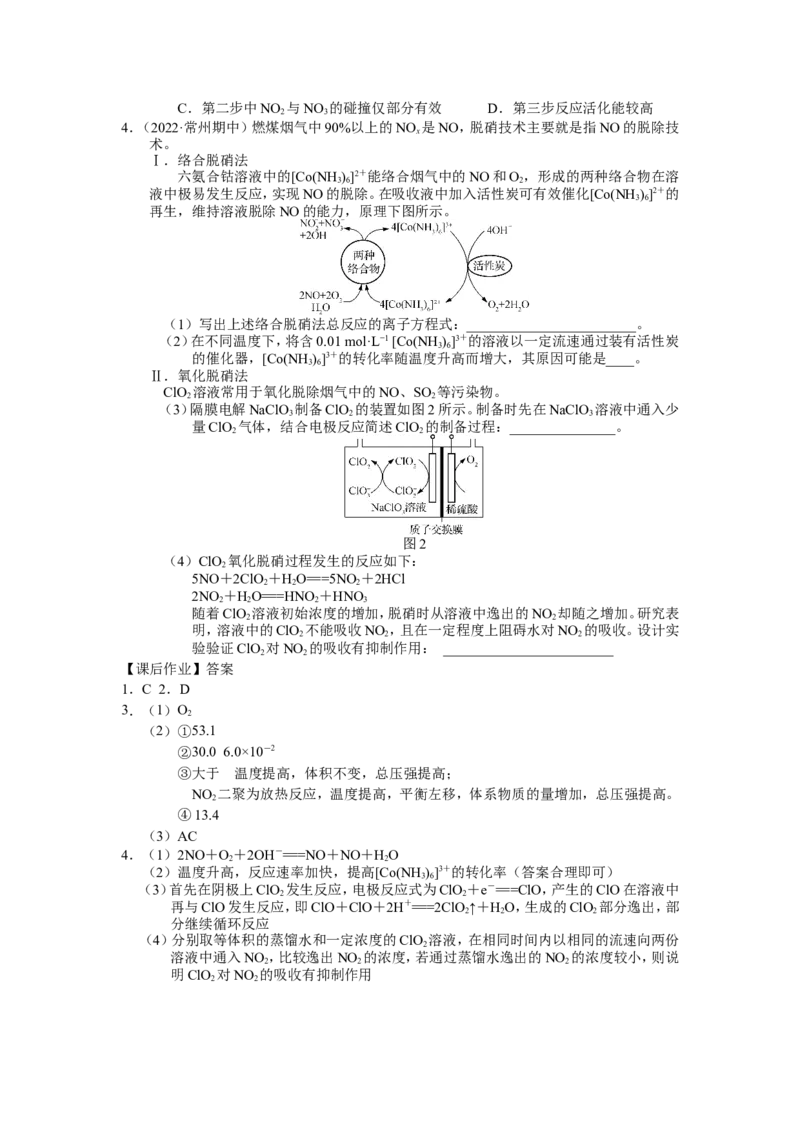
(3)隔膜电解NaClO 制备ClO 的装置如图2所示。制备时先在NaClO 溶液中通入少
3 2 3
量ClO 气体,结合电极反应简述ClO 的制备过程:_______________。
2 2
图2
(4)ClO 氧化脱硝过程发生的反应如下:
2
5NO+2ClO +HO===5NO+2HCl
2 2 2
2NO +HO===HNO +HNO
2 2 2 3
随着ClO 溶液初始浓度的增加,脱硝时从溶液中逸出的NO 却随之增加。研究表
2 2
明,溶液中的ClO 不能吸收NO ,且在一定程度上阻碍水对NO 的吸收。设计实
2 2 2
验验证ClO 对NO 的吸收有抑制作用: ________________________
2 2
【课后作业】答案
1.C 2.D
3.(1)O
2
(2)①53.1
②30.0 6.0×10-2
③大于 温度提高,体积不变,总压强提高;
NO 二聚为放热反应,温度提高,平衡左移,体系物质的量增加,总压强提高。
2
④13.4
(3)AC
4.(1)2NO+O+2OH-===NO+NO+HO
2 2
(2)温度升高,反应速率加快,提高[Co(NH )]3+的转化率(答案合理即可)
3 6
(3)首先在阴极上ClO 发生反应,电极反应式为ClO +e-===ClO,产生的ClO在溶液中
2 2
再与ClO发生反应,即ClO+ClO+2H+===2ClO ↑+HO,生成的ClO 部分逸出,部
2 2 2
分继续循环反应
(4)分别取等体积的蒸馏水和一定浓度的ClO 溶液,在相同时间内以相同的流速向两份
2
溶液中通入NO ,比较逸出NO 的浓度,若通过蒸馏水逸出的NO 的浓度较小,则说
2 2 2
明ClO 对NO 的吸收有抑制作用
2 2