文档内容
2025届高三化学一轮专题复习讲义(19)
专题四 元素及其化合物
4-4 非金属及其化合物(二、硫及其重要化合物)(1课时,共3课时)
【复习目标】
1.掌握硫及其化合物的主要性质和应用。
2.掌握硫及其化合物的转化关系
3.了解SO HSO 等物质对环境的影响。
2 、 2 4
【重点突破】
1.掌握硫及其化合物的转化关系
2.理解硫及其化合物在化工流程中的应用及转化条件
【真题简析】
例题1.(2020江苏)吸收工厂烟气中的SO ,能有效减少SO 对空气的污染。氨水、ZnO悬浊
2 2
液吸收烟气中SO 后经O 催化氧化,可得到硫酸盐。已知:室温下,ZnSO 微溶于水,
2 2 3
Zn(HSO ) 易溶于水;溶液中HSO 、HSO3-、SO 2-的物质的量分数随pH的分布如图-1所
3 2 2 3 3
示。
(1)氨水吸收SO 。向氨水中通入少量SO ,主要反应的离子方程式为_____________;当
2 2
通入SO 至溶液pH=6时,溶液中浓度最大的阴离子是__________(填化学式)。
2
(2)ZnO水悬浊液吸收SO 。向ZnO水悬浊液中匀速缓慢通入SO ,在开始吸收的
2 2
40mim内,SO 吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图-2)。
2
溶液pH几乎不变阶段,主要产物是____________(填化学式);SO 吸收率迅速降
2
低阶段,主要反应的离子方程式为__________________________________。
(3)O 催化氧化。其他条件相同时,调节吸收SO 得到溶液的pH在4.5~6.5范围内,pH
2 2越低SO 2-生成速率越大,其主要原因是____________;随着氧化的进行,溶液的pH
4
将__________(填“增大”、“减小”或“不变”)。
解析:(1)向氨水中通入少量SO 时,SO 与氨水反应生成亚硫酸铵,反应的离子方程式为
2 2
2NH +H O+SO =2NH++SO2(- 或2NH ·H O +SO =2NH++ SO 2-+H O);根据图-1所示,
3 2 2 4 3 3 2 2 4 3 2
pH=6时,溶液中不含有亚硫酸,仅含有HSO3-和SO 2-,根据微粒物质的量分数曲线可以
3
看出溶液中阴离子浓度最大的是HSO3-;(2)反应开始时,悬浊液中的ZnO大量吸收
SO ,生成微溶于水的ZnSO,此时溶液pH几乎不变;一旦ZnO完全反应生成ZnSO 后,
2 3 3
ZnSO 继续吸收SO 生成易溶于水的Zn(HSO ),此时溶液pH逐渐变小,SO 的吸收率
3 2 3 2 2
逐 渐 降 低 , 这 一 过 程 的 离 子 方 程 式 为 ZnSO+SO+H O=Zn2++2 HSO3- ( 或
3 2 2
ZnO+2SO+H O=Zn2++2 HSO -)(3)pH值大于6.5时,SO 以微溶物ZnSO 形式存在,使
2 2 3 2 3
SO 不利于与O 接触,反应速率慢;pH降低,SO 主要以HSO -形式溶于水中,与O 充分
2 2 2 3 2
接触。因而pH降低,SO 2-生成速率增大;随着反应的不断进行,大量的HSO3-反应生成
4
SO 2-,反应的离子方程式为2HSO -+O =2SO2-+2H+,随着反应的不断进行,有大量的氢
4 3 2 4
离子生成,导致氢离子浓度增大,溶液pH减小。
答案:
(1)2NH +H O+SO ===2NH ++ SO 2-或2NH ·H O+SO ===2 NH++ SO 2-+H O
3 2 2 4 3 3 2 2 4 3 2
HSO -
3
(2)ZnSO
3
ZnSO+SO+H O===Zn2++2 HSO -或ZnO+2SO+H O===Zn2++2 HSO3-
3 2 2 3 2 2
(3)随着pH降低,HSO 浓度增大 减小
小结:向氨水中通入少量的SO ,反应生成亚硫酸铵,结合图像分析pH=6时溶液中浓度最大
2
的阴离子;通过分析ZnO吸收SO 后产物的溶解性判断吸收率变化的原因;通过分析
2
HSO -与氧气反应的生成物,分析溶液pH的变化情况。
3
【知识整合】
(1)理清知识主线
HS →S →SO→SO(H SO)
2 2 3 2 4
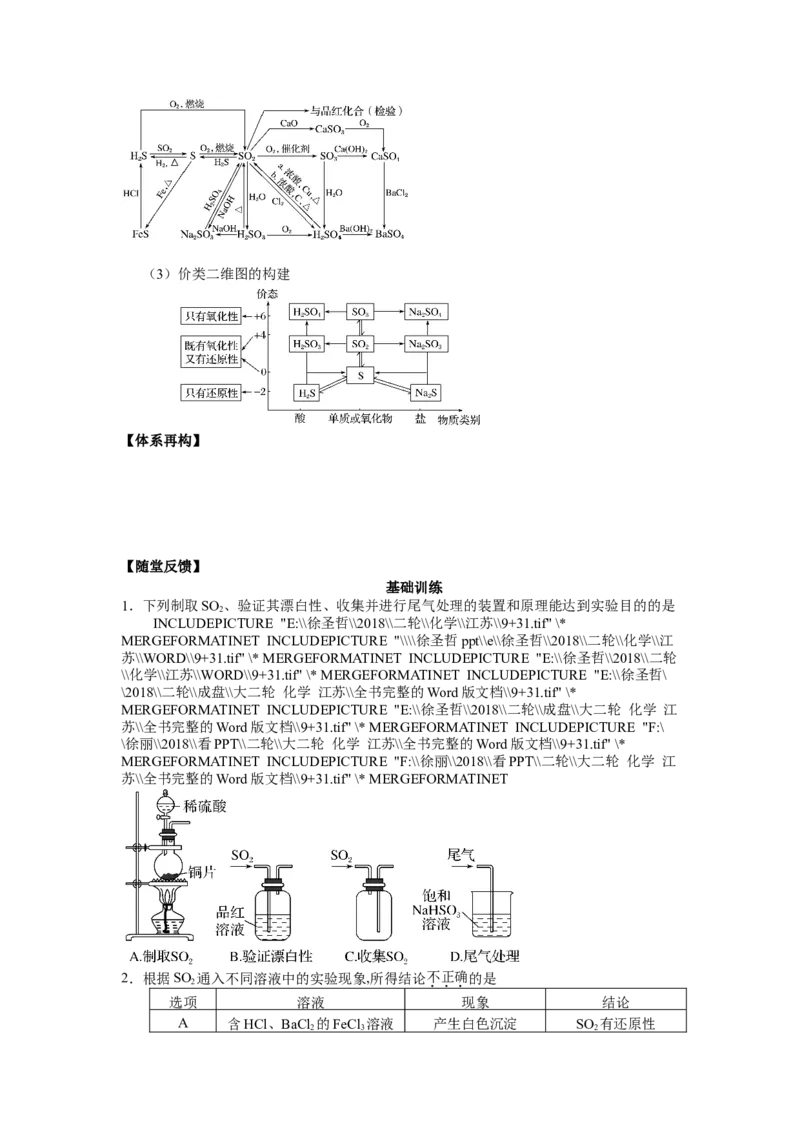
(2)形成网络构建
INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\化学\\江苏\\9+7.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "\\\\徐圣哲ppt\\e\\徐圣哲\\2018\\二轮\\化学\\江
苏\\WORD\\9+7.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮
\\化学\\江苏\\WORD\\9+7.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\
\2018\\二轮\\成盘\\大二轮 化学 江苏\\全书完整的Word版文档\\9+7.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\成盘\\大二轮 化学 江
苏\\全书完整的Word版文档\\9+7.TIF" \* MERGEFORMATINET INCLUDEPICTURE "F:\
\徐丽\\2018\\看PPT\\二轮\\大二轮 化学 江苏\\全书完整的Word版文档\\9+7.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "F:\\徐丽\\2018\\看PPT\\二轮\\大二轮 化学 江
苏\\全书完整的Word版文档\\9+7.TIF" \* MERGEFORMATINET(3)价类二维图的构建
【体系再构】
【随堂反馈】
基础训练
1.下列制取SO 、验证其漂白性、收集并进行尾气处理的装置和原理能达到实验目的的是
2
INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\化学\\江苏\\9+31.tif" \*
MERGEFORMATINET INCLUDEPICTURE "\\\\徐圣哲ppt\\e\\徐圣哲\\2018\\二轮\\化学\\江
苏\\WORD\\9+31.tif" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮
\\化学\\江苏\\WORD\\9+31.tif" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\
\2018\\二轮\\成盘\\大二轮 化学 江苏\\全书完整的Word版文档\\9+31.tif" \*
MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2018\\二轮\\成盘\\大二轮 化学 江
苏\\全书完整的Word版文档\\9+31.tif" \* MERGEFORMATINET INCLUDEPICTURE "F:\
\徐丽\\2018\\看PPT\\二轮\\大二轮 化学 江苏\\全书完整的Word版文档\\9+31.tif" \*
MERGEFORMATINET INCLUDEPICTURE "F:\\徐丽\\2018\\看PPT\\二轮\\大二轮 化学 江
苏\\全书完整的Word版文档\\9+31.tif" \* MERGEFORMATINET
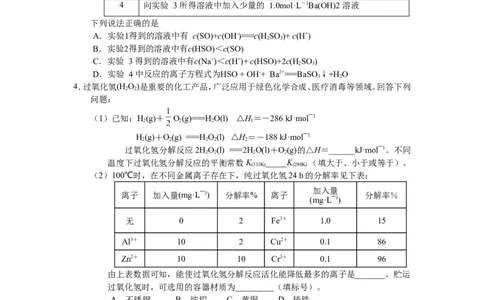
2.根据SO 通入不同溶液中的实验现象,所得结论不正确的是
2
选项 溶液 现象 结论
A 含HCl、BaCl 的FeCl 溶液 产生白色沉淀 SO 有还原性
2 3 2B HS溶液 产生黄色沉淀 SO 有氧化性
2 2
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
D NaSiO 溶液 产生胶状沉淀 酸性:H SO >H SiO
2 3 2 3 2 3
3.室温下,通过实验探究亚硫酸盐的性质。
已知:Ka1(H2SO3)=1.54×10-2、Ka2(H2SO3)=1.02×10-7
实验 实验操作和现象
1 向 10mL1.0mol·L-1NaOH 溶液通入 112mL(标准状况)SO
2
2 向 10mL1.0mol·L-1NaOH 溶液通入 SO 至溶液 pH=7
2
3 向 10mL1.0mol·L-1NaOH 溶液通入 224mL(标准状况)SO
2
4 向实验 3 所得溶液中加入少量的 1.0mol·L-1Ba(OH)2 溶液
下列说法正确的是
A.实验1得到的溶液中有 c(SO)+c(OH-)===c(H SO )+ c(H+)
2 3
B.实验2得到的溶液中有c(HSO)<c(SO)
C.实验 3 得到的溶液中有c(Na+)<c(H+)+ c(HSO)+2c(H SO )
2 3
D.实验 4 中反应的离子方程式为HSO + OH-+ Ba2+===BaSO↓+HO
3 2
4.过氧化氢(H O)是重要的化工产品,广泛应用于绿色化学合成、医疗消毒等领域。回答下列
2 2
问题:
(1)已知:H(g)+ O(g)===HO(l) △H=-286 kJ·mol¯1
2 2 2 1
H(g)+O(g) ===HO(l) △H=-188 kJ·mol¯1
2 2 2 2 2
过氧化氢分解反应2HO(l) ===2HO(l)+O(g)的△H=______kJ·mol¯1。不同
2 2 2 2
温度下过氧化氢分解反应的平衡常数K _____K (填大于、小于或等于)。
(313K) (298K)
(2)100℃时,在不同金属离子存在下,纯过氧化氢24 h的分解率见下表:
加入量
离子 加入量(mg·L¯1) 分解率% 离子 分解率%
(mg·L¯1)
无 0 2 Fe3+ 1.0 15
Al3+ 10 2 Cu2+ 0.1 86
Zn2+ 10 10 Cr3+ 0.1 96
由上表数据可知,能使过氧化氢分解反应活化能降低最多的离子是_______。贮运
过氧化氢时,可选用的容器材质为_________(填标号)。
A.不锈钢 B.纯铝 C.黄铜 D.铸铁
(3)过氧化氢的Ka=2.24×10-12,HO 的酸性________HO(填大于、小于或等于)。研究
1 2 2 2
表明,过氧化氢溶液中HO -的浓度越大,过氧化氢的分解速率越快。常温下,不同浓
2
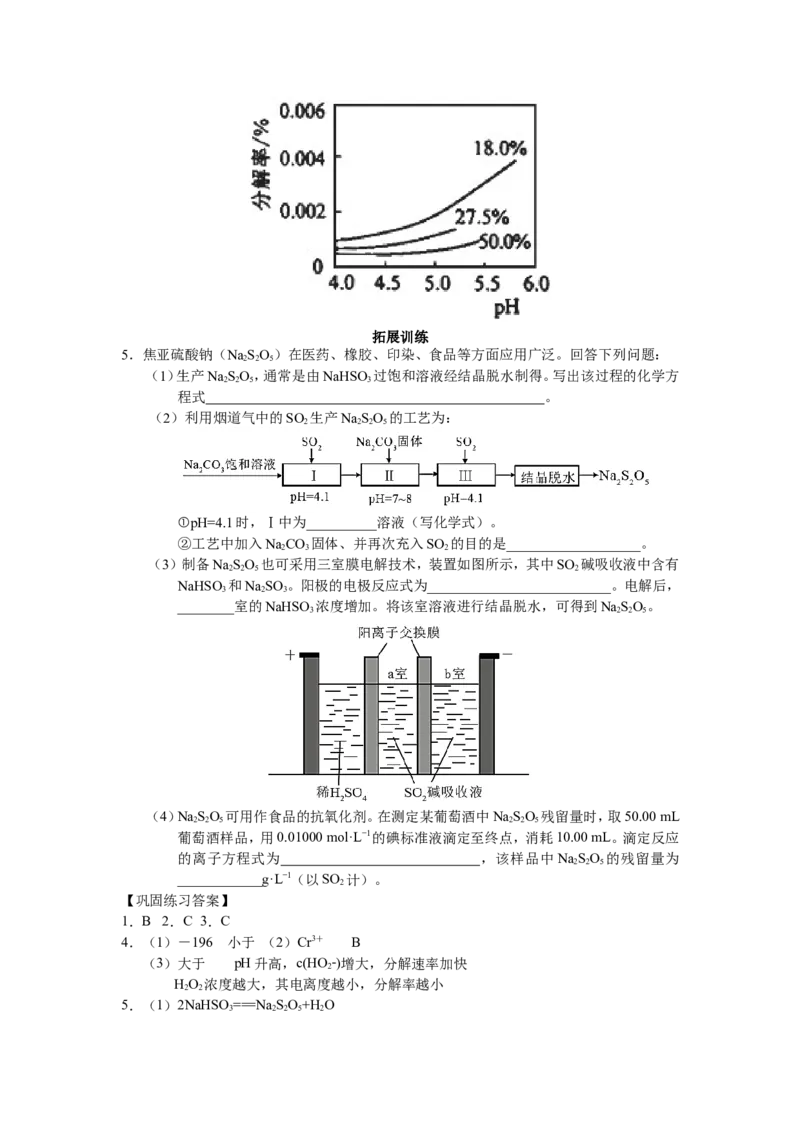
度的过氧化氢分解率与pH的关系如图所示。一定浓度的过氧化氢,pH增大分解率
增大的原因是___________________;相同pH下,过氧化氢浓度越大分解率越低的
原因是__________________________________________。拓展训练
5.焦亚硫酸钠(NaSO)在医药、橡胶、印染、食品等方面应用广泛。回答下列问题:
2 2 5
(1)生产NaSO,通常是由NaHSO 过饱和溶液经结晶脱水制得。写出该过程的化学方
2 2 5 3
程式 。
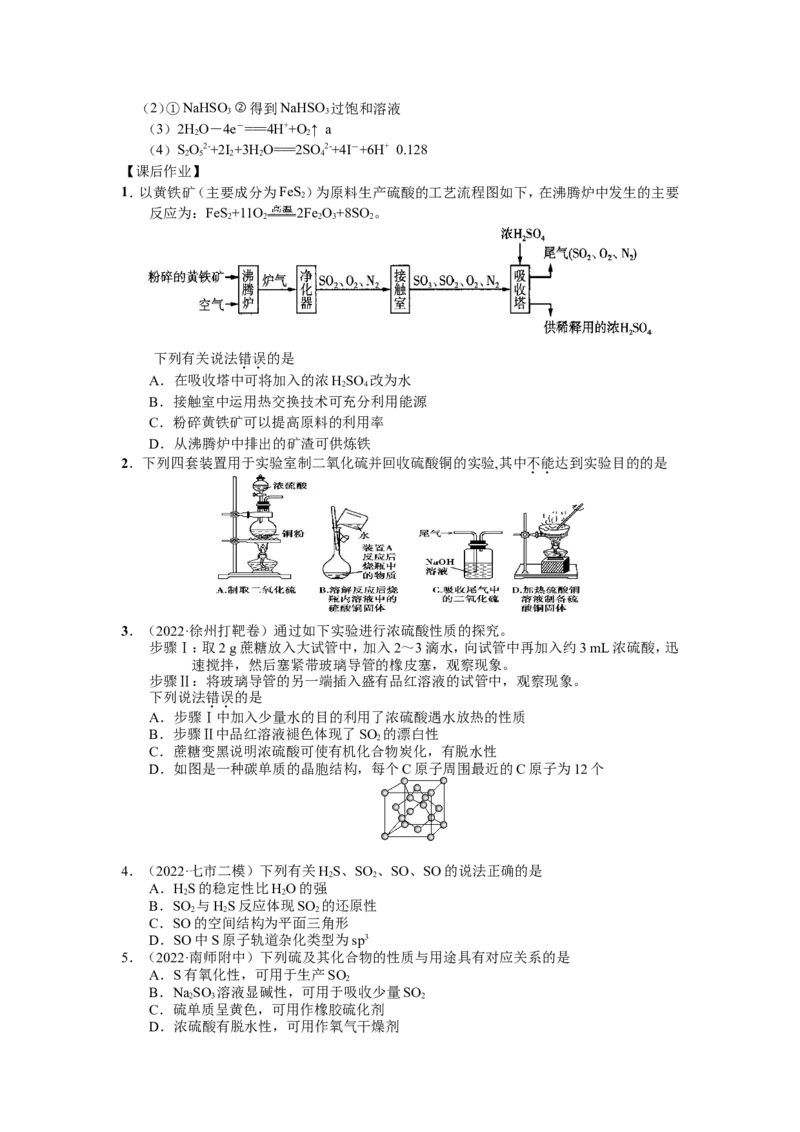
(2)利用烟道气中的SO 生产NaSO 的工艺为:
2 2 2 5
①pH=4.1时,Ⅰ中为__________溶液(写化学式)。
②工艺中加入NaCO 固体、并再次充入SO 的目的是___________________。
2 3 2
(3)制备NaSO 也可采用三室膜电解技术,装置如图所示,其中SO 碱吸收液中含有
2 2 5 2
NaHSO 和NaSO 。阳极的电极反应式为__________________________。电解后,
3 2 3
________室的NaHSO 浓度增加。将该室溶液进行结晶脱水,可得到NaSO。
3 2 2 5
(4)NaSO 可用作食品的抗氧化剂。在测定某葡萄酒中NaSO 残留量时,取50.00 mL
2 2 5 2 2 5
葡萄酒样品,用0.01000 mol·L−1的碘标准液滴定至终点,消耗10.00 mL。滴定反应
的离子方程式为 ,该样品中NaSO 的残留量为
2 2 5
____________g·L−1(以SO 计)。
2
【巩固练习答案】
1.B 2.C 3.C
4.(1)-196 小于 (2)Cr3+ B
(3)大于 pH升高,c(HO -)增大,分解速率加快
2
H O 浓度越大,其电离度越小,分解率越小
2 2
5.(1)2NaHSO===NaSO+H O
3 2 2 5 2(2)①NaHSO ②得到NaHSO 过饱和溶液
3 3
(3)2HO-4e-===4H++O ↑ a
2 2
(4)SO2-+2I +3H O===2SO 2-+4I-+6H+ 0.128
2 5 2 2 4
【课后作业】
1.以黄铁矿(主要成分为FeS)为原料生产硫酸的工艺流程图如下,在沸腾炉中发生的主要
2
反应为:FeS+11O 2Fe O+8SO。
2 2 2 3 2
下列有关说法错误的是
A.在吸收塔中可将加入的浓HSO 改为水
2 4
B.接触室中运用热交换技术可充分利用能源
C.粉碎黄铁矿可以提高原料的利用率
D.从沸腾炉中排出的矿渣可供炼铁
2.下列四套装置用于实验室制二氧化硫并回收硫酸铜的实验,其中不能达到实验目的的是
3.(2022·徐州打靶卷)通过如下实验进行浓硫酸性质的探究。
步骤Ⅰ:取2 g蔗糖放入大试管中,加入2~3滴水,向试管中再加入约3 mL浓硫酸,迅
速搅拌,然后塞紧带玻璃导管的橡皮塞,观察现象。
步骤Ⅱ:将玻璃导管的另一端插入盛有品红溶液的试管中,观察现象。
下列说法错误的是
A.步骤Ⅰ中加入少量水的目的利用了浓硫酸遇水放热的性质
B.步骤Ⅱ中品红溶液褪色体现了SO 的漂白性
2
C.蔗糖变黑说明浓硫酸可使有机化合物炭化,有脱水性
D.如图是一种碳单质的晶胞结构,每个C原子周围最近的C原子为12个
4.(2022·七市二模)下列有关HS、SO 、SO、SO的说法正确的是
2 2
A.HS的稳定性比HO的强
2 2
B.SO 与HS反应体现SO 的还原性
2 2 2
C.SO的空间结构为平面三角形
D.SO中S原子轨道杂化类型为sp3
5.(2022·南师附中)下列硫及其化合物的性质与用途具有对应关系的是
A.S有氧化性,可用于生产SO
2
B.NaSO 溶液显碱性,可用于吸收少量SO
2 3 2
C.硫单质呈黄色,可用作橡胶硫化剂
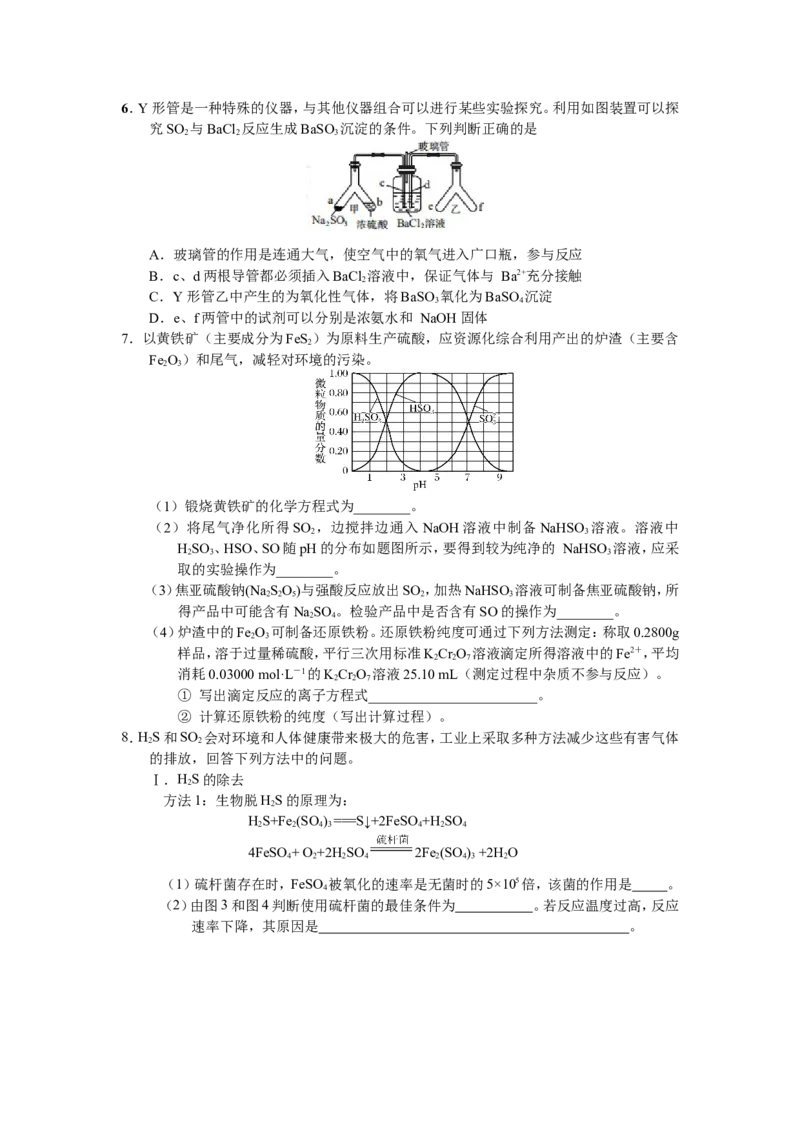
D.浓硫酸有脱水性,可用作氧气干燥剂6.Y 形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究。利用如图装置可以探
究SO 与BaCl 反应生成BaSO 沉淀的条件。下列判断正确的是
2 2 3
A.玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应
B.c、d两根导管都必须插入BaCl 溶液中,保证气体与 Ba2+充分接触
2
C.Y 形管乙中产生的为氧化性气体,将BaSO 氧化为BaSO 沉淀
3 4
D.e、f两管中的试剂可以分别是浓氨水和 NaOH 固体
7.以黄铁矿(主要成分为FeS)为原料生产硫酸,应资源化综合利用产出的炉渣(主要含
2
Fe O)和尾气,减轻对环境的污染。
2 3
(1)锻烧黄铁矿的化学方程式为________。
(2)将尾气净化所得SO ,边搅拌边通入NaOH溶液中制备NaHSO 溶液。溶液中
2 3
HSO 、HSO、SO随pH的分布如题图所示,要得到较为纯净的 NaHSO 溶液,应采
2 3 3
取的实验操作为________。
(3)焦亚硫酸钠(Na SO)与强酸反应放出SO ,加热NaHSO 溶液可制备焦亚硫酸钠,所
2 2 5 2 3
得产品中可能含有NaSO 。检验产品中是否含有SO的操作为________。
2 4
(4)炉渣中的Fe O 可制备还原铁粉。还原铁粉纯度可通过下列方法测定:称取0.2800g
2 3
样品,溶于过量稀硫酸,平行三次用标准KCr O 溶液滴定所得溶液中的Fe2+,平均
2 2 7
消耗0.03000 mol·L-1的KCr O 溶液25.10 mL(测定过程中杂质不参与反应)。
2 2 7
① 写出滴定反应的离子方程式________________________。
② 计算还原铁粉的纯度(写出计算过程)。
8.HS和SO 会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体
2 2
的排放,回答下列方法中的问题。
Ⅰ.HS的除去
2
方法1:生物脱HS的原理为:
2
HS+Fe (SO ) ===S↓+2FeSO +H SO
2 2 4 3 4 2 4
4FeSO + O +2H SO 2Fe (SO ) +2H O
4 2 2 4 2 4 3 2
(1)硫杆菌存在时,FeSO 被氧化的速率是无菌时的5×105倍,该菌的作用是 。
4
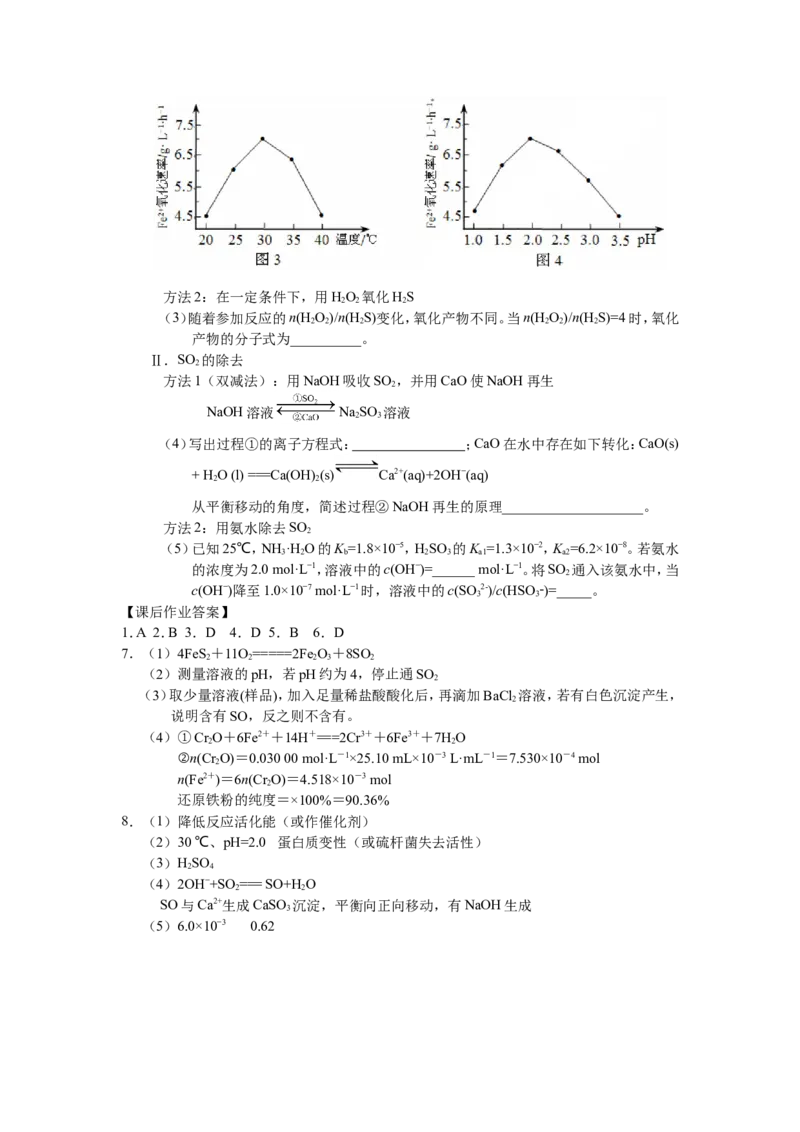
(2)由图3和图4判断使用硫杆菌的最佳条件为 。若反应温度过高,反应
速率下降,其原因是 。方法2:在一定条件下,用HO 氧化HS
2 2 2
(3)随着参加反应的n(H O)/n(H S)变化,氧化产物不同。当n(H O)/n(H S)=4时,氧化
2 2 2 2 2 2
产物的分子式为__________。
Ⅱ.SO 的除去
2
方法1(双减法):用NaOH吸收SO ,并用CaO使NaOH再生
2
NaOH溶液 NaSO 溶液
2 3
(4)写出过程①的离子方程式: ;CaO在水中存在如下转化:CaO(s)
+ H O (l) ===Ca(OH) (s) Ca2+(aq)+2OH−(aq)
2 2
从平衡移动的角度,简述过程②NaOH再生的原理____________________。
方法2:用氨水除去SO
2
(5)已知25℃,NH ·H O的K =1.8×10−5,HSO 的K =1.3×10−2,K =6.2×10−8。若氨水
3 2 b 2 3 a1 a2
的浓度为2.0 mol·L−1,溶液中的c(OH−)=______ mol·L−1。将SO 通入该氨水中,当
2
c(OH−)降至1.0×10−7 mol·L−1时,溶液中的c(SO 2-)/c(HSO -)=_____。
3 3
【课后作业答案】
1.A 2.B 3.D 4.D 5.B 6.D
7.(1)4FeS+11O=====2Fe O+8SO
2 2 2 3 2
(2)测量溶液的pH,若pH约为4,停止通SO
2
(3)取少量溶液(样品),加入足量稀盐酸酸化后,再滴加BaCl 溶液,若有白色沉淀产生,
2
说明含有SO,反之则不含有。
(4)①Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
②n(CrO)=0.030 00 mol·L-1×25.10 mL×10-3 L·mL-1=7.530×10-4 mol
2
n(Fe2+)=6n(CrO)=4.518×10-3 mol
2
还原铁粉的纯度=×100%=90.36%
8.(1)降低反应活化能(或作催化剂)
(2)30 ℃、pH=2.0 蛋白质变性(或硫杆菌失去活性)
(3)HSO
2 4
(4)2OH−+SO=== SO+H O
2 2
SO与Ca2+生成CaSO 沉淀,平衡向正向移动,有NaOH生成
3
(5)6.0×10−3 0.62