文档内容
备战2024年高考化学考前手感保温训练(新高考卷)
专练05 14道选择题+主观流程题
完卷时间:40分钟
可能到的相对原子质量:F-19 K-39 Cu-64
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C B B A B B A B D A C C D B
一、选择题(只有1个正确选项)
1.化学与生产、生活密切相关。下列有关说法正确的是
A.燃煤脱硫有利于实现碳达峰、碳中和
B.向天然水中加入明矶可起到杀菌、消毒的作用
C.在野外被蚊虫叮咬,可在伤口处涂抹肥㒵水来减轻痛痒
D.地沟油变废为宝是实现资源再利用的重要研究课题,地沟油和石蜡油的化学成分相同
【答案】C
【解析】A.燃煤脱硫可以减少二氧化硫的排放,可减少酸雨污染,但不能减少二氧化碳的
排放,没有利于实现“碳达峰、碳中和”的效果,A错误;B.明矾溶解后产生Al3+,铝离
子易水解生成氢氧化铝胶体,胶体聚沉可以去除水中杂质,但是没有杀菌消毒的作用,B
错误;C.在野外被蚊虫叮咬时会注入含甲酸的毒汁,肥皂水呈碱性,可涂抹肥皂水来减轻
痛痒,C正确;D.地沟油是油脂,石蜡油是烃类的化合物,地沟油和石蜡油的化学成分不
相同,D错误;本题选C。
2.下列化学用语或图示表达错误的是
A. 的名称:3-甲基戊烷
B. 的VSEPR模型:
C. 中C原子杂化轨道的电子云轮廓图:
D. 的形成过程:
【答案】B
【解析】A. 主链上有5个碳原子,3号位有1个甲基,名称为3-甲基戊
烷,故A正确;B.SO 的中心原子S原子的价层电子对数为2+ ,含有1对孤电
2子对,其VSEPR模型为 ,故B错误;C. 中C原子为sp3杂化,杂化轨道
的电子云轮廓图: ,故C正确;D. 为离子化合物,用电子式表示形
成过程为: ,故D正确;答案选B。
3.设 为阿伏加德罗常数的值,下列说法不正确的是
A.常温下,1L pH=3的 溶液中,发生电离的水分子数目为
B.标准状况下,11.2L HCl气体中含有的 数目为0.5
C.标准状况下,22.4L 中 键的数目为2
D.标准状况下,22.4L 和22.4L 在光照下充分反应后的分子数为2
【答案】B
【解析】A. 在水溶液中电离出的H+抑制水的电离,常温下,1L pH=3的
溶液中,c(H+)=10-3mol/L,c(OH-)=10-11mol/L,则发生电离的水分子数目为 ,选
项A正确;B.HCl为共价化合物,气体中不含有的 ,选项B不正确;C.每个 中含
有两个碳氧双键,则含有两个 键,标准状况下,22.4L ,即1mol 中 键的数目
为2 ,选项C正确;D.标准状况下,22.4L 和22.4L 在光照下充分反应后,发
生取代反应,分子数目不变,则生成的分子数为2 ,选项D正确;答案选B。
4.实验室合成金属有机骨架化合物ZIF-8的步骤:称取0.5380 g 、0.6480 g 2-甲
基咪唑和0.2680 g 于反应器中,加入50 mL甲醇使其溶解,然后将反应器放
在85℃水浴中加热24 h,冷却至室温后,得到晶体ZIF-8。下列仪器在合成过程中不需选
用的是
A. B. C. D.
【答案】A【分析】根据题中给出的配制步骤需要,从而选择所需要的仪器,以此解题。
【解析】A.称量固体时需精确至0.0001g,需要使用电子天平,不需要选用托盘天平,A
错误;B.该配制过程需要加热,需要酒精灯,B正确;C.该配制过程需要一定体积的甲
醇,需要量筒,C正确;D.该配制过程需要在85℃水浴中加热24 h,需要温度计,D正确;
故选A。
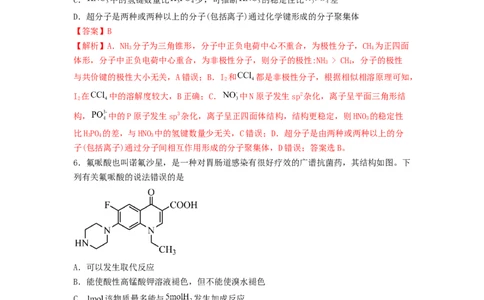
5.下列有关物质结构与性质的表述结构正确的是
A.N-H键的极性大于C-H键的极性, 分子的极性小于
B. 易溶于 ,可从 和 都是非极性分子的角度解释
C. 中的氢键数量比 少,可推断 的稳定性比 差
D.超分子是两种或两种以上的分子(包括离子)通过化学键形成的分子聚集体
【答案】B
【解析】A.NH 分子为三角锥形,分子中正负电荷中心不重合,为极性分子,CH 为正四面
3 4
体形,分子中正负电荷中心重合,为非极性分子,则分子的极性:NH > CH,分子的极性
3 4
与共价键的极性大小无关,A错误;B.I 和 都是非极性分子,根据相似相溶原理可知,
2
I 在 中的溶解度较大,B正确;C. 中N原子发生sp2杂化,离子呈平面三角形结
2
构, 中的P原子发生sp3杂化,离子呈正四面体结构,结构更稳定,则HNO 的稳定性
3
比HPO 的差,与HNO 中的氢键数量少无关,C错误;D.超分子是由两种或两种以上的分
3 4 3
子(包括离子)通过分子间相互作用形成的分子聚集体,D错误;答案选B。
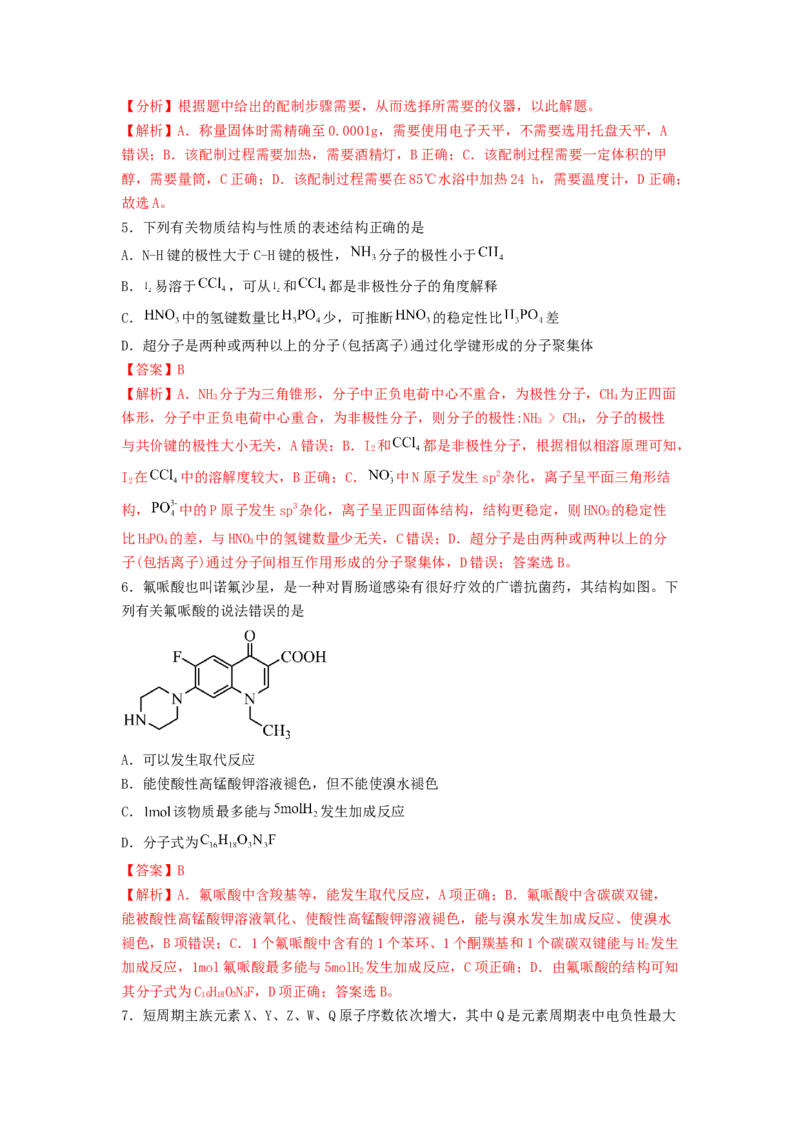
6.氟哌酸也叫诺氟沙星,是一种对胃肠道感染有很好疗效的广谱抗菌药,其结构如图。下
列有关氟哌酸的说法错误的是
A.可以发生取代反应
B.能使酸性高锰酸钾溶液褪色,但不能使溴水褪色
C. 该物质最多能与 发生加成反应
D.分子式为
【答案】B
【解析】A.氟哌酸中含羧基等,能发生取代反应,A项正确;B.氟哌酸中含碳碳双键,
能被酸性高锰酸钾溶液氧化、使酸性高锰酸钾溶液褪色,能与溴水发生加成反应、使溴水
褪色,B项错误;C.1个氟哌酸中含有的1个苯环、1个酮羰基和1个碳碳双键能与H 发生
2
加成反应,1mol氟哌酸最多能与5molH 发生加成反应,C项正确;D.由氟哌酸的结构可知
2
其分子式为C H ONF,D项正确;答案选B。
16 18 3 3
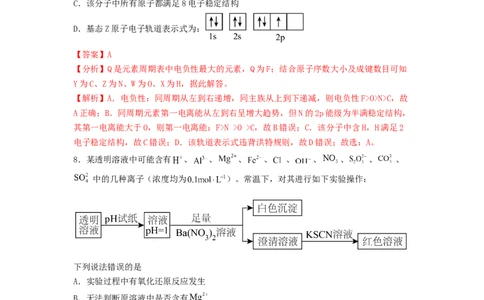
7.短周期主族元素X、Y、Z、W、Q原子序数依次增大,其中Q是元素周期表中电负性最大的元素,由这五种元素组成的某药物结构如图所示。下列有关说法正确的是
A.电负性:
B.第一电离能:
C.该分子中所有原子都满足8电子稳定结构
D.基态Z原子电子轨道表示式为:
【答案】A
【分析】Q是元素周期表中电负性最大的元素,Q为F;结合原子序数大小及成键数目可知
Y为C、Z为N、W为O、X为H,据此解答。
【解析】A.电负性:同周期从左到右递增,同主族从上到下递减,则电负性F>O>N>C,故
A正确;B.同周期元素第一电离能从左到右呈增大趋势,但N的2p能级为半满稳定结构,
其第一电离能大于O,则第一电离能:F>N >O >C,故B错误;C.该分子中含H,H满足2
电子稳定结构,故C错误;D.该轨道表示式违背洪特规则,故D错误;故选:A。
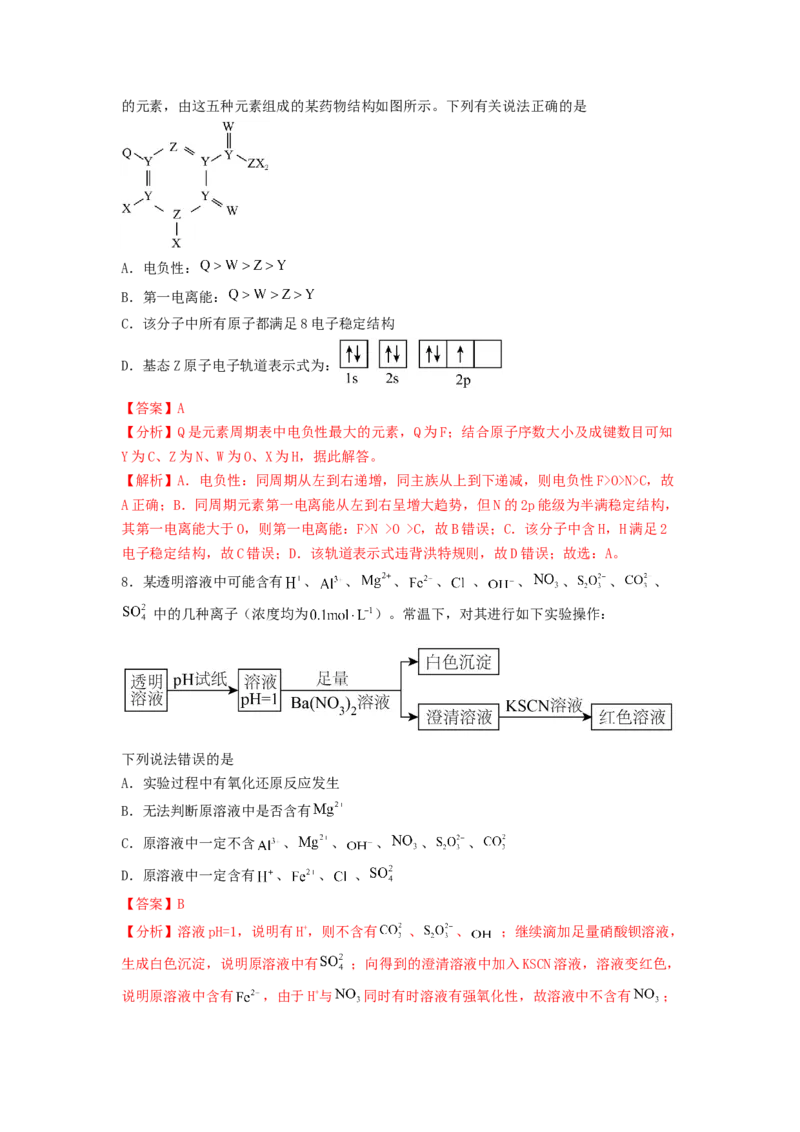
8.某透明溶液中可能含有 、 、 、 、 、 、 、 、 、
中的几种离子(浓度均为 )。常温下,对其进行如下实验操作:
下列说法错误的是
A.实验过程中有氧化还原反应发生
B.无法判断原溶液中是否含有
C.原溶液中一定不含 、 、 、 、 、
D.原溶液中一定含有 、 、 、
【答案】B
【分析】溶液pH=1,说明有H+,则不含有 、 、 ;继续滴加足量硝酸钡溶液,
生成白色沉淀,说明原溶液中有 ;向得到的澄清溶液中加入KSCN溶液,溶液变红色,
说明原溶液中含有 ,由于H+与 同时有时溶液有强氧化性,故溶液中不含有 ;浓度均为 ,根据电荷守恒可以判断出溶液中含有 , 、 都不能含有;
综上,原溶液中一定含有的离子是: 、 、 、 ,一定不含有的离子是 、
、 、 、 、 ;
【解析】A.加入足量硝酸钡溶液时,在酸性溶液中, 将 氧化为Fe3+,发生了氧化
还原反应,故A正确;B.由分析可知,原溶液中不含有 ,故B错误;C.由分析可知,
原溶液中一定不含 、 、 、 、 、 ,故C正确;D.由分析可知,
原溶液中一定含有 、 、 、 ,故D正确。答案选B。
9.利用 、 与 合成 的反应主要历程如图所示。下列说法错误的
是
A. 是合成乙醇的中间体
B.合成过程涉及C―O键的断裂和C―C的形成
C.第③步的反应式为
D.若用 替代 ,可生成
【答案】D
【分析】反应①为CHOH与LiI反应生成LiOH和CHI,此反应中CHOH中的-OH给了
3 3 3
LiOH,-CH 与I生成了CHI,反应②为CO 与H 在Ru的催化作用下生成CO和HO,根据反
3 3 2 2 2
应③可知,反应②产物CO与反应①的产物CHI,再加上H 在催化剂的作用下生成了乙醇,
3 2
由于CHI只能提供1个C原子,那么乙醇中的另一个C原子来自CO,它的3个H原子来自
3
H,据此分析作答。
2
【解析】A.由图可知,CHI是反应①的产物,反应②的反应物,故CHI是合成乙醇的中
3 3
间体,故A正确;B.反应①中甲醇生成CHI,甲醇中的C−O键断裂,反应③中甲醇生成乙
3
醇,涉及C-C键形成,故B正确;C.根据分析可知,第③步的反应式为
CO+2H+CHI→HI+CHCHOH,故C正确;D.根据反应3可知反应产生乙醇中的-OH上H原子
2 3 3 2
种类取决于H 中的H原子的种类,而与CHOH上的H原子种类无关,所以若用CHOD替代
2 3 3
CHOH,生成的乙醇仍然是CHCHOH ,而不会是CHCHOD,故D错误;故选:D。
3 3 2 3 2
10.下列有关实验操作、现象都正确且能推出结论的是选
实验操作及现象 结论
项
向浓度均为 的 和 混合溶液中滴加少量银
A
氨溶液,出现黄色沉淀
向淀粉溶液中加入适量稀硫酸微热一段时间,再加入新制 淀粉水解产物中无还原
B
悬浊液并加热,无砖红色沉淀 糖
C 将 气体通入 溶液中,生成白色沉淀 此沉淀是
向 溶液中加入冰醋酸,将产生的气体通入苯酚钠
D 酸性:醋酸>碳酸>苯酚
溶液中,出现白色浑浊
A.A B.B C.C D.D
【答案】A
【解析】A.银氨溶液中存在 ,向混合溶液中滴加少量银氨溶
液出现黄色沉淀,说明 与 结合生成 沉淀, ,A正确;
B.淀粉水解液冷却后应先加 溶液中和稀硫酸,再加新制 悬浊液加热检验还
原糖,B错误;C. 酸性弱于盐酸,不能与 溶液反应生成 沉淀,C错误;
D.醋酸有挥发性,向 溶液中加入冰醋酸产生的气体中不仅有 ,还有
,在通入苯酚钠溶液之前应先通过盛有饱和 溶液的洗气瓶除去
中的 ,D错误;故选A。
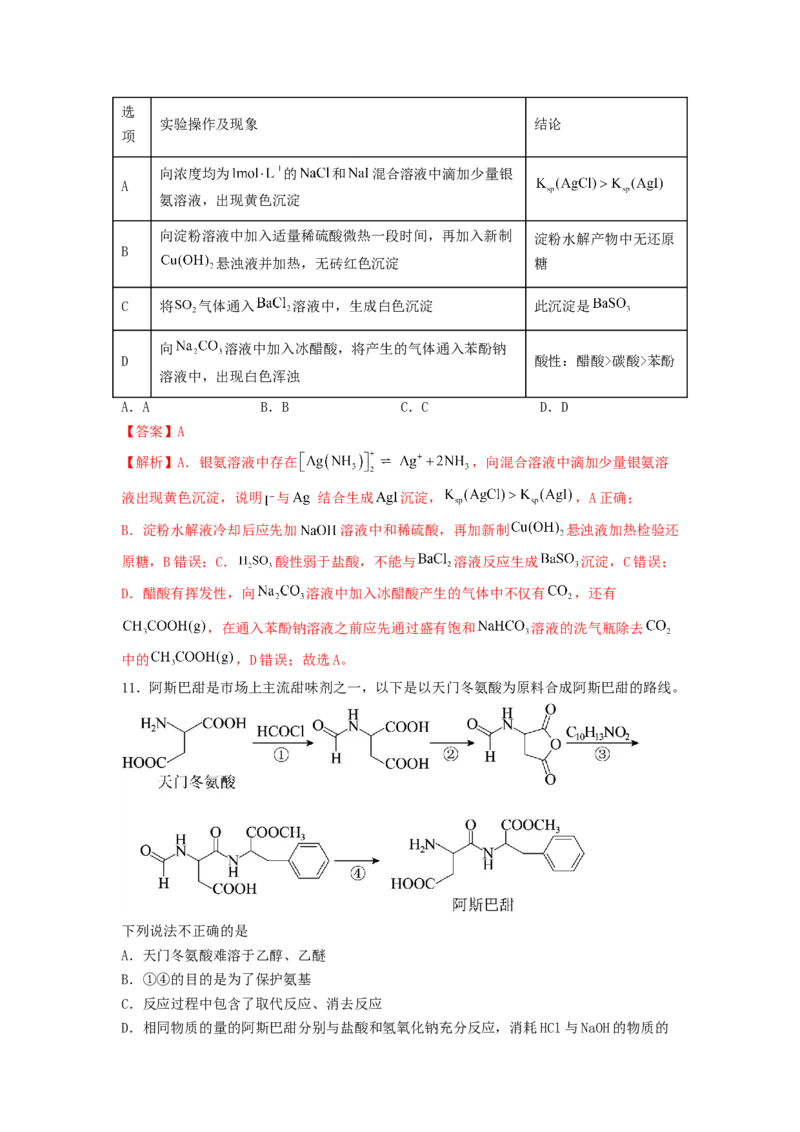
11.阿斯巴甜是市场上主流甜味剂之一,以下是以天门冬氨酸为原料合成阿斯巴甜的路线。
下列说法不正确的是
A.天门冬氨酸难溶于乙醇、乙醚
B.①④的目的是为了保护氨基
C.反应过程中包含了取代反应、消去反应
D.相同物质的量的阿斯巴甜分别与盐酸和氢氧化钠充分反应,消耗HCl与NaOH的物质的量之比为2∶3
【答案】C
【解析】A.常温下,天冬氨酸微溶于水,难溶于乙醇和乙醚,溶于沸水,A正确;B.根
据反应可知,反应①氨基转化为酰胺基,反应④酰胺基转化为氨基,故①④的目的是为了
保护氨基,B正确;C.反应过程中包含了取代反应、消去反应、加成反应,C不正确;D.
阿斯巴甜分子中含有一个羧基、一个酯基和一个酰胺基,相同物质的量的阿斯巴甜分别与
盐酸和氢氧化钠充分反应,消耗HCl与NaOH的物质的量之比为2∶3,D正确;答案选C。
12.以甲苯为原料通过间接氧化法可以制取苯甲醛、苯甲酸等物质,反应原理如下图所示.
下列说法正确的是
A.电解时的阳极反应为:
B.电解结束后,阴极区溶液 升高
C. 甲苯氧化为 苯甲醛和 苯甲酸时,共消耗
D.甲苯、苯甲醛、苯甲酸的混合物可以通过分液的方法分离
【答案】C
【分析】由图可知,左侧电极为阳极,水分子作用下铬离子在阳极失去电子发生氧化反应
生成重铬酸根离子和氢离子,电极反应式为 ,阳极槽外
中重铬酸根离子与甲苯在酸性条件下反应生成苯甲醛或苯甲酸,反应的离子方程式为
3CH-CH+2 +16H+ 3CH-CHO +4Cr3++11HO, CH-CH+ +8H+ CH-COOH +2Cr3+
6 5 3 6 5 2 6 5 3 6 5
+5HO,电解时,氢离子通过阳离子交换膜由阳极区进入阴极区,右侧电极为电解池的阴极,
2
阴极氢离子放电,电极反应为: ,据此作答。
【解析】A. 电解时的阳极发生氧化反应,电极反应为: ,
A错误;B. 阳极区产生的氢离子透过质子交换膜进入阴极区,阴极上氢离子放电,电极反
应为: ,电极上每消耗2molH+,就有2molH+进入阴极区,故电极电解结束后,
阴极区溶液 不变,B错误;C. 结合3CH-CH+2 +16H+ 3CH-CHO +4Cr3++11HO,
6 5 3 6 5 2
甲苯氧化为 苯甲醛时消耗 ,根据CH-CH+ +8H+ CH-COOH
6 5 3 6 5
+2Cr3++5HO, 甲苯氧化为 苯甲酸时消耗 ,则 甲苯氧化为
2苯甲醛和 苯甲酸时,共消耗 ,C正确;D. 甲苯、苯甲醛、苯甲
酸的混合物是互溶的液体,不可以通过分液的方法分离,D错误;答案选C。
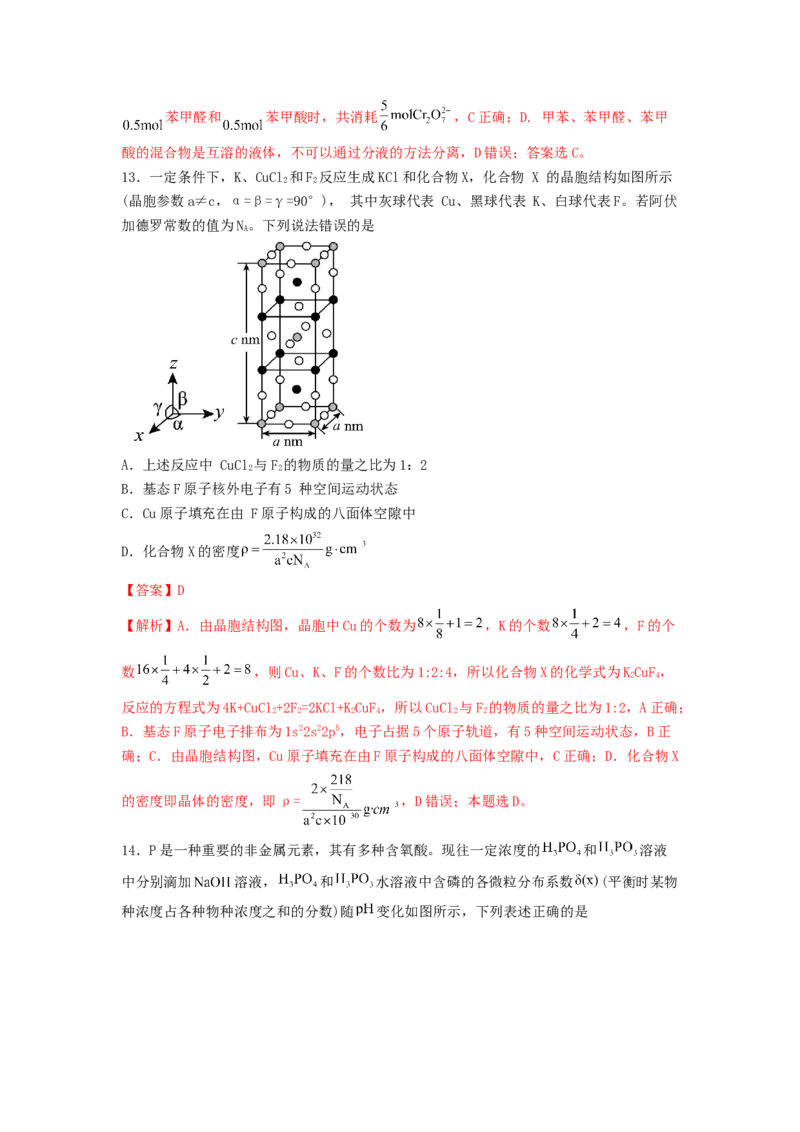
13.一定条件下,K、CuCl 和F 反应生成KCl和化合物X,化合物 X 的晶胞结构如图所示
2 2
(晶胞参数a≠c,α=β=γ=90°), 其中灰球代表 Cu、黑球代表 K、白球代表F。若阿伏
加德罗常数的值为N。下列说法错误的是
A
A.上述反应中 CuCl 与F 的物质的量之比为1:2
2 2
B.基态F原子核外电子有5 种空间运动状态
C.Cu原子填充在由 F原子构成的八面体空隙中
D.化合物X的密度
【答案】D
【解析】A.由晶胞结构图,晶胞中Cu的个数为 ,K的个数 ,F的个
数 ,则Cu、K、F的个数比为1:2:4,所以化合物X的化学式为KCuF,
2 4
反应的方程式为4K+CuCl+2F=2KCl+KCuF,所以CuCl 与F 的物质的量之比为1:2,A正确;
2 2 2 4 2 2
B.基态F原子电子排布为1s22s22p5,电子占据5个原子轨道,有5种空间运动状态,B正
确;C.由晶胞结构图,Cu原子填充在由F原子构成的八面体空隙中,C正确;D.化合物X
的密度即晶体的密度,即ρ= ,D错误;本题选D。
14.P是一种重要的非金属元素,其有多种含氧酸。现往一定浓度的 和 溶液
中分别滴加 溶液, 和 水溶液中含磷的各微粒分布系数 (平衡时某物
种浓度占各种物种浓度之和的分数)随 变化如图所示,下列表述正确的是A. 和 均为三元弱酸
B. 的结构式为:
C. 溶液中:
D.往 溶液中加入过量的 的离子方程式为:
【答案】B
【解析】A.加入过量的NaOH, 和 分别转化为 、 , 为三元
弱酸, 为二元弱酸,A错误;B.根据价层电子对数计算 ,这表明
中心磷原子以sp3杂化,空间构型为四面体形,与相邻原子形成两个P-OHσ键,一个H-
Pσ键,磷和非羟基氧形成一个P=O双键(σ键和π键) ,且 为二元弱酸,结构式
为: ,B正确;C.根据pH=6.6时, ,可得K (
a2
)= , 水解常数为 ,电离大于水解,故
溶液中: ,C错误;D.结合图像,可
得K (HPO)=10-2.1,K (HPO)=10-7.2,K (HPO)=10-12.4,K (HPO)=10-1.3,K
a1 3 4 a2 3 4 a3 3 4 a1 3 3 a2
(HPO)=10-6.6,根据强酸制取弱酸的原则,往 溶液中加入过量的 的离子
3 3
方程式为: ,D错误;故选B。
二、主观题
15.(14分)氢镍电池是目前使用最广的含镍电池,废旧电池的处理对环境保护和资源的再
利用意义重大。一种对废旧氢镍电池负极材料(含有NiO、Ni和少量La、Fe、Mg、MnO、
2
石墨粉等)进行湿法处理的流程如图所示:已知:①Ni2+可形成 [Ni(NH)]2+;②K (MgF)=6.4 ;③HSO 第一步完全电离,
3 6 sp 2 2 4
。
回答下列问题:
(1)Ni2+的价层电子排布式为 。
(2)能提高“酸浸”效率的措施有 (任写一种)。
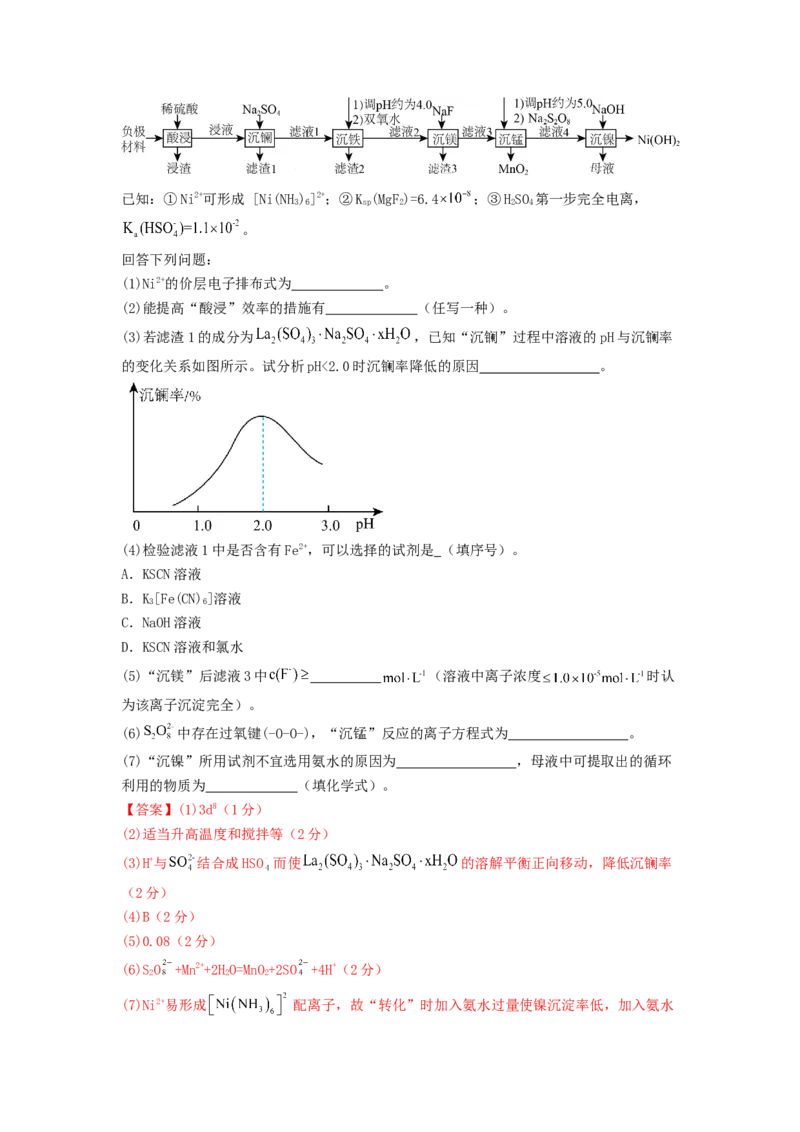
(3)若滤渣1的成分为 ,已知“沉镧”过程中溶液的pH与沉镧率
的变化关系如图所示。试分析pH<2.0时沉镧率降低的原因 。
(4)检验滤液1中是否含有Fe2+,可以选择的试剂是 (填序号)。
A.KSCN溶液
B.K[Fe(CN)]溶液
3 6
C.NaOH溶液
D.KSCN溶液和氯水
(5)“沉镁”后滤液3中 (溶液中离子浓度 时认
为该离子沉淀完全)。
(6) 中存在过氧键(-O-O-),“沉锰”反应的离子方程式为 。
(7)“沉镍”所用试剂不宜选用氨水的原因为 ,母液中可提取出的循环
利用的物质为 (填化学式)。
【答案】(1)3d8(1分)
(2)适当升高温度和搅拌等(2分)
(3)H+与 结合成HSO 而使 的溶解平衡正向移动,降低沉镧率
(2分)
(4)B(2分)
(5)0.08(2分)
(6)SO +Mn2++2HO=MnO+2SO +4H+(2分)
2 2 2
(7)Ni2+易形成 配离子,故“转化”时加入氨水过量使镍沉淀率低,加入氨水不足镍离子沉淀不完全也使镍沉淀率低,即氨水用量不易控制(2分) NaSO(1分)
2 4
【分析】由题给流程可知,向负极材料中加入稀硫酸酸浸时,少量二氧化锰与负极中的金
属材料在酸性条件下反应生成硫酸锰,一氧化镍与稀硫酸反应生成二价镍离子,镍、镧、
铁、镁与稀硫酸反应生成可溶性硫酸盐,石墨粉与稀硫酸不反应,过滤得到含有石墨粉的
滤渣和含有可溶性硫酸盐的滤液;向滤液中加入硫酸钠溶液,将溶液中的镧离子转化为
沉淀,过滤得到 和滤液1;向滤液1调
节pH至4.0的溶液中加入过氧化氢溶液将溶液中的铁元素转化为FeOOH沉淀,过滤得到含
有FeOOH的滤渣1和滤液2;向滤液2中加入氟化钠溶液,将镁离子转化为氟化镁沉淀,过
滤得到含有氟化镁的滤渣2和滤液3;向滤液3调节pH约为5.0的溶液中加入过二硫酸铵
溶液,将锰离子转化为二氧化锰沉淀,过滤得到二氧化锰和滤液4;向滤液4中加入氢氧
化钠溶液,将镍离子转化为氢氧化镍沉淀,过滤得到母液和氢氧化镍。
【解析】(1)Ni元素为28号元素,原子核外有28个电子,所以核外电子排布式为:
1s22s22p63s23p63d84s2,Ni原子失去最外层4s能级2个电子,形成Ni2+,则Ni2+价电子排布
式是3d8。
(2)能提高“酸浸”效率的措施有:适当升高温度和搅拌等操作。
(3)由信息知,“沉镧”工序中,镧离子形成 后过滤分离出来,
若溶液的pH<2.0,H+与 结合成HSO 而使 的溶解平衡正向移
动,降低沉镧率。
(4)检验Fe2+可以选择K[Fe(CN)]溶液,现象是生成蓝色沉淀,故选B。
3 6
(5)“沉镁”后滤液3中c(Mg2+)= 时认为Mg2+沉淀完全,
。
(6)由题意可知,沉锰发生的反应为溶液中锰离子与过二硫酸根离子反应生成二氧化锰、
硫酸根离子和氢离子,反应的离子方程式为SO +Mn2++2HO=MnO+2SO +4H+。
2 2 2
(7)Ni2+易形成 配离子,故“转化”时加入氨水过量使镍沉淀率低,加入氨
水不足镍离子沉淀不完全也使镍沉淀率低,即氨水用量不易控制;母液的成分为
(NH)SO、NaSO,处理后可得NaSO,NaSO 在沉镧时可循环使用。
4 2 4 2 4 2 4 2 4