文档内容
专练 34 金属的腐蚀与防护
一、单项选择题
1.[2022·广东卷]为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀
锌铁片放入酸化的3% NaCl溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐
蚀的是( )
A.加入AgNO 溶液产生沉淀
3
B.加入淀粉碘化钾溶液无蓝色出现
C.加入KSCN溶液无红色出现
D.加入K[Fe(CN) ]溶液无蓝色沉淀生成
3 6
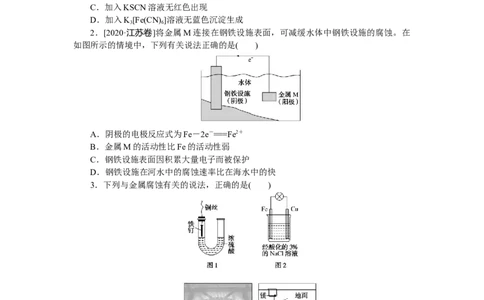
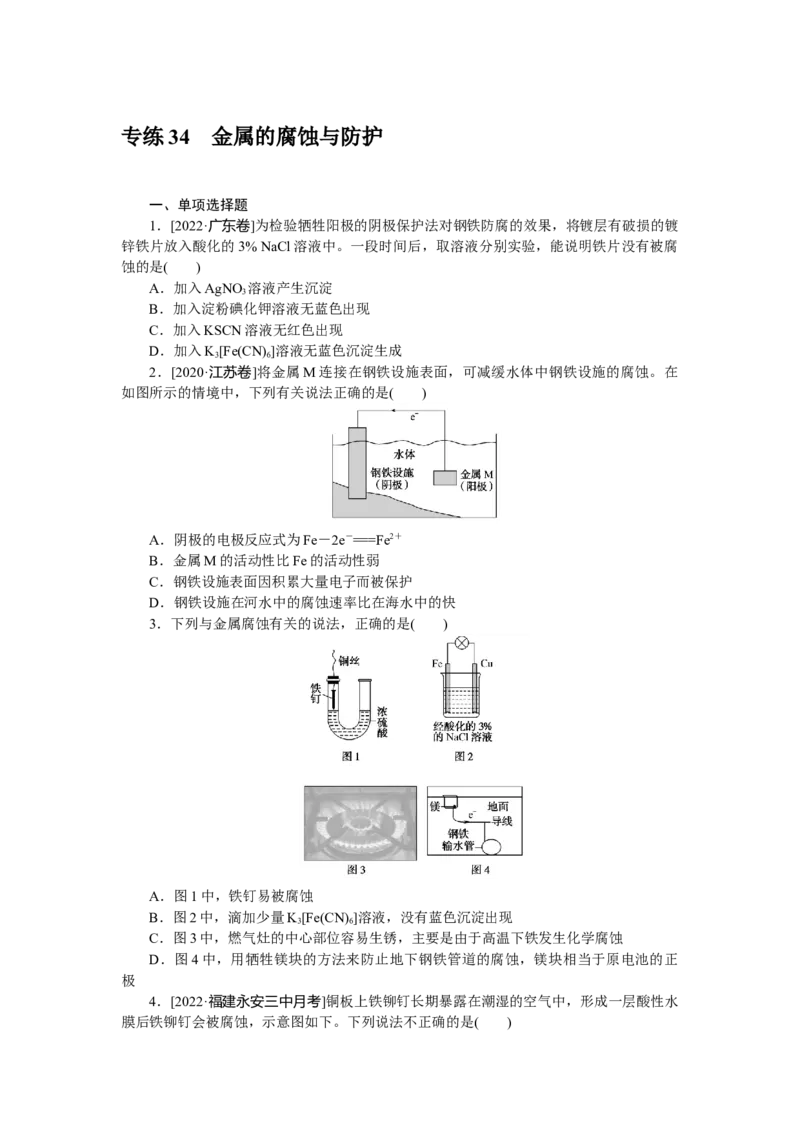
2.[2020·江苏卷]将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在
如图所示的情境中,下列有关说法正确的是( )
A.阴极的电极反应式为Fe-2e-===Fe2+
B.金属M的活动性比Fe的活动性弱
C.钢铁设施表面因积累大量电子而被保护
D.钢铁设施在河水中的腐蚀速率比在海水中的快
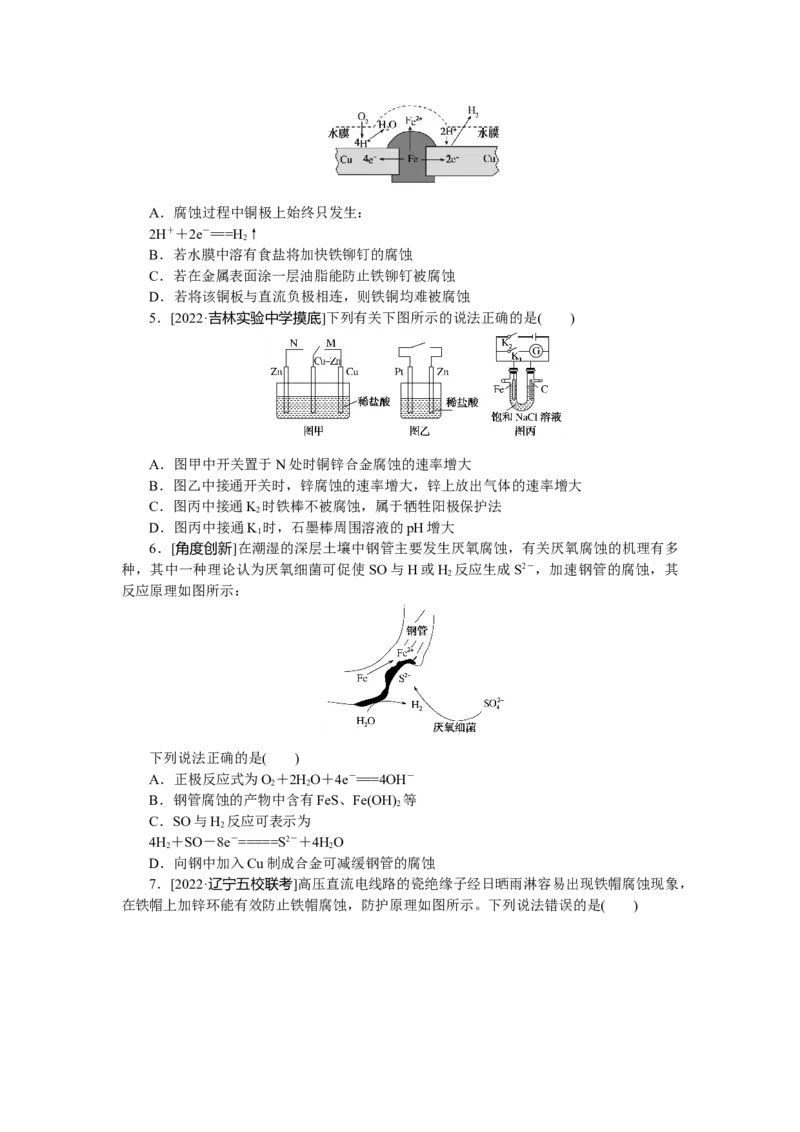
3.下列与金属腐蚀有关的说法,正确的是( )
A.图1中,铁钉易被腐蚀
B.图2中,滴加少量K[Fe(CN) ]溶液,没有蓝色沉淀出现
3 6
C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀
D.图4中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正
极
4.[2022·福建永安三中月考]铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水
膜后铁铆钉会被腐蚀,示意图如下。下列说法不正确的是( )A.腐蚀过程中铜极上始终只发生:
2H++2e-===H ↑
2
B.若水膜中溶有食盐将加快铁铆钉的腐蚀
C.若在金属表面涂一层油脂能防止铁铆钉被腐蚀
D.若将该铜板与直流负极相连,则铁铜均难被腐蚀
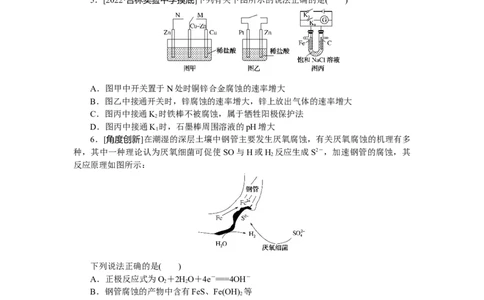
5.[2022·吉林实验中学摸底]下列有关下图所示的说法正确的是( )
A.图甲中开关置于N处时铜锌合金腐蚀的速率增大
B.图乙中接通开关时,锌腐蚀的速率增大,锌上放出气体的速率增大
C.图丙中接通K 时铁棒不被腐蚀,属于牺牲阳极保护法
2
D.图丙中接通K 时,石墨棒周围溶液的pH增大
1
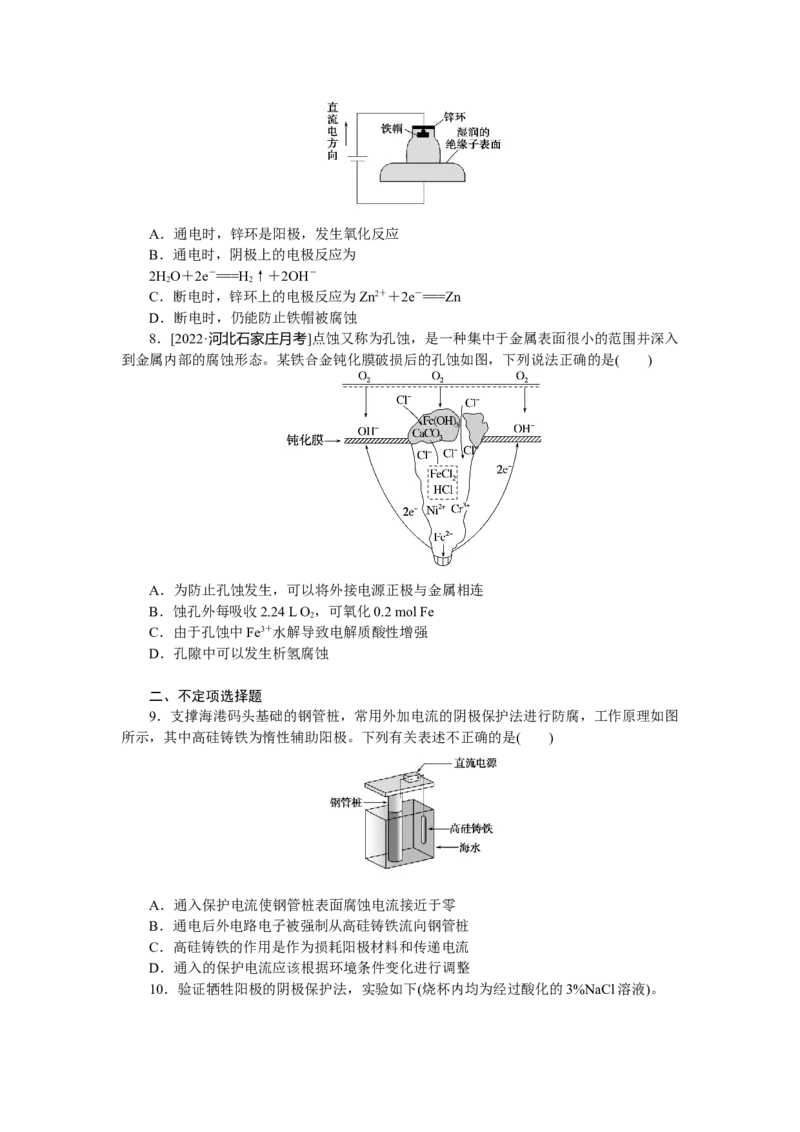
6.[角度创新]在潮湿的深层土壤中钢管主要发生厌氧腐蚀,有关厌氧腐蚀的机理有多
种,其中一种理论认为厌氧细菌可促使 SO与H或H 反应生成S2-,加速钢管的腐蚀,其
2
反应原理如图所示:
下列说法正确的是( )
A.正极反应式为O+2HO+4e-===4OH-
2 2
B.钢管腐蚀的产物中含有FeS、Fe(OH) 等
2
C.SO与H 反应可表示为
2
4H+SO-8e-=====S2-+4HO
2 2
D.向钢中加入Cu制成合金可减缓钢管的腐蚀
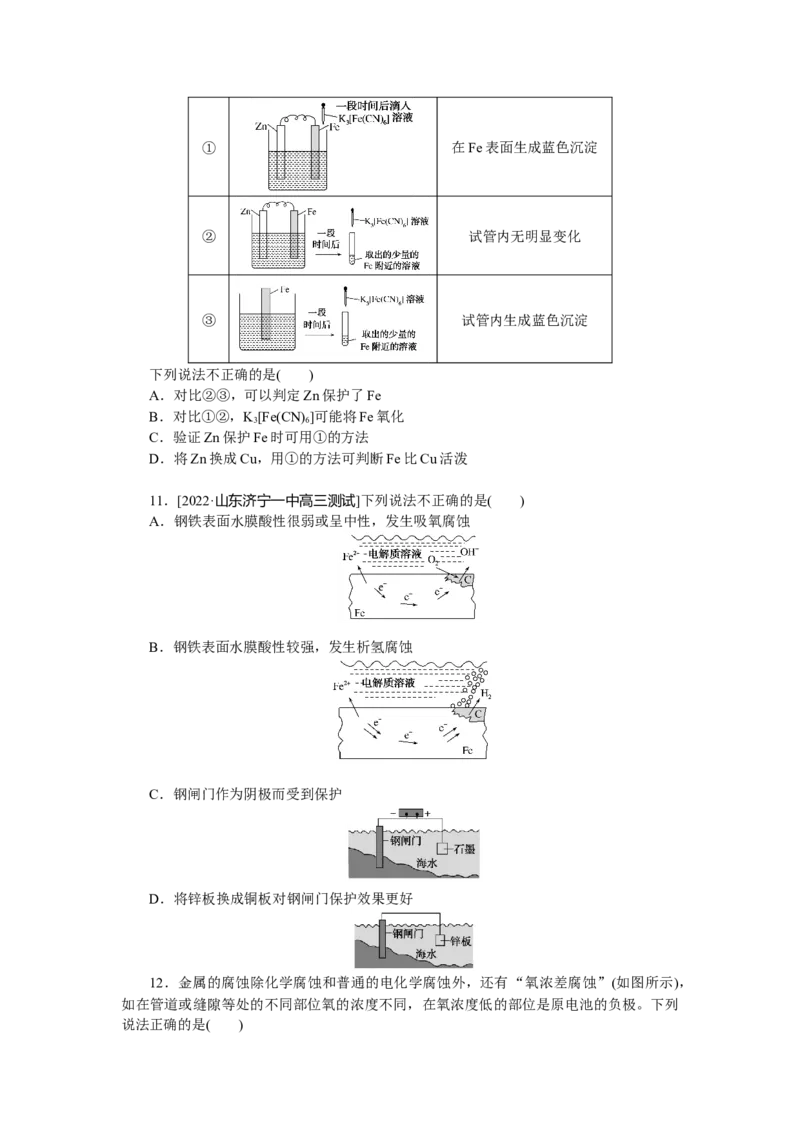
7.[2022·辽宁五校联考]高压直流电线路的瓷绝缘子经日晒雨淋容易出现铁帽腐蚀现象,
在铁帽上加锌环能有效防止铁帽腐蚀,防护原理如图所示。下列说法错误的是( )A.通电时,锌环是阳极,发生氧化反应
B.通电时,阴极上的电极反应为
2HO+2e-===H ↑+2OH-
2 2
C.断电时,锌环上的电极反应为Zn2++2e-===Zn
D.断电时,仍能防止铁帽被腐蚀
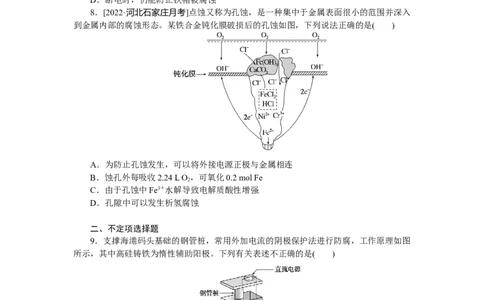
8.[2022·河北石家庄月考]点蚀又称为孔蚀,是一种集中于金属表面很小的范围并深入
到金属内部的腐蚀形态。某铁合金钝化膜破损后的孔蚀如图,下列说法正确的是( )
A.为防止孔蚀发生,可以将外接电源正极与金属相连
B.蚀孔外每吸收2.24 L O ,可氧化0.2 mol Fe
2
C.由于孔蚀中Fe3+水解导致电解质酸性增强
D.孔隙中可以发生析氢腐蚀
二、不定项选择题
9.支撑海港码头基础的钢管桩,常用外加电流的阴极保护法进行防腐,工作原理如图
所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是( )
A.通入保护电流使钢管桩表面腐蚀电流接近于零
B.通电后外电路电子被强制从高硅铸铁流向钢管桩
C.高硅铸铁的作用是作为损耗阳极材料和传递电流
D.通入的保护电流应该根据环境条件变化进行调整
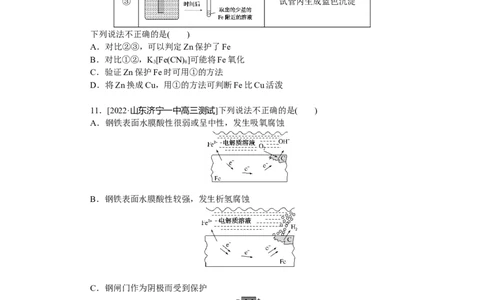
10.验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。① 在Fe表面生成蓝色沉淀
② 试管内无明显变化
③ 试管内生成蓝色沉淀
下列说法不正确的是( )
A.对比②③,可以判定Zn保护了Fe
B.对比①②,K[Fe(CN) ]可能将Fe氧化
3 6
C.验证Zn保护Fe时可用①的方法
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼
11.[2022·山东济宁一中高三测试]下列说法不正确的是( )
A.钢铁表面水膜酸性很弱或呈中性,发生吸氧腐蚀
B.钢铁表面水膜酸性较强,发生析氢腐蚀
C.钢闸门作为阴极而受到保护
D.将锌板换成铜板对钢闸门保护效果更好
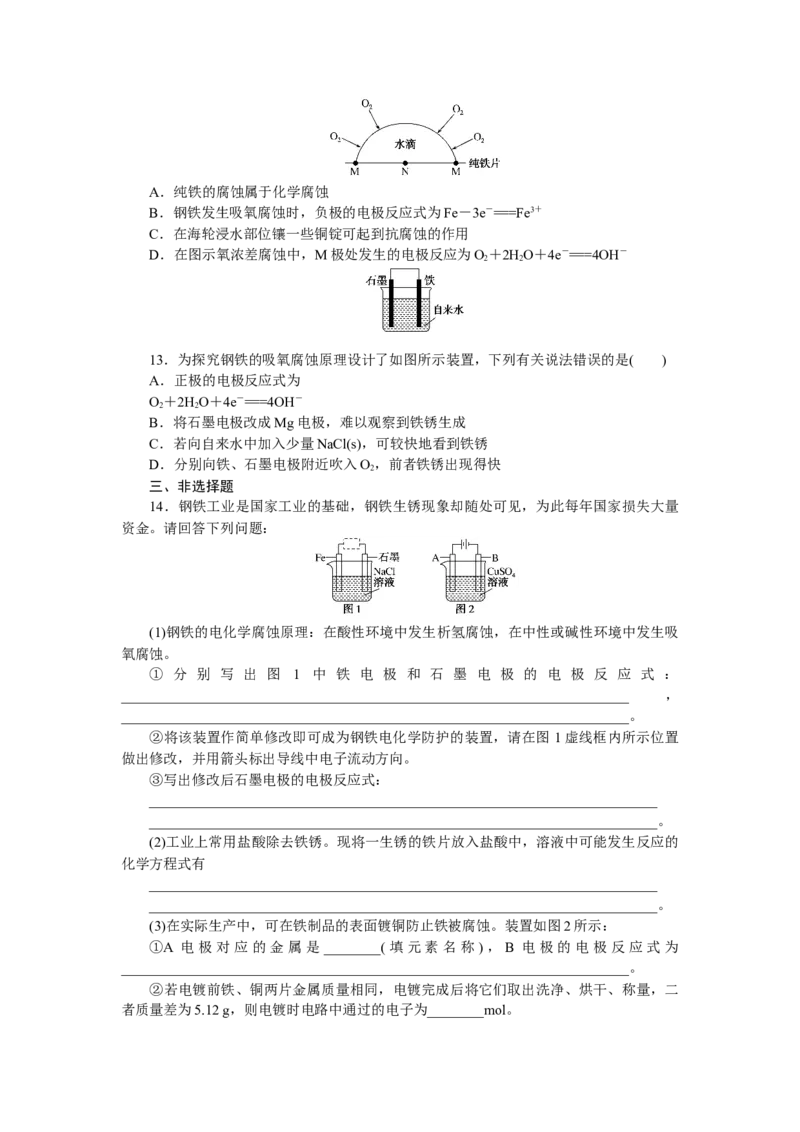
12.金属的腐蚀除化学腐蚀和普通的电化学腐蚀外,还有“氧浓差腐蚀”(如图所示),
如在管道或缝隙等处的不同部位氧的浓度不同,在氧浓度低的部位是原电池的负极。下列
说法正确的是( )A.纯铁的腐蚀属于化学腐蚀
B.钢铁发生吸氧腐蚀时,负极的电极反应式为Fe-3e-===Fe3+
C.在海轮浸水部位镶一些铜锭可起到抗腐蚀的作用
D.在图示氧浓差腐蚀中,M极处发生的电极反应为O+2HO+4e-===4OH-
2 2
13.为探究钢铁的吸氧腐蚀原理设计了如图所示装置,下列有关说法错误的是( )
A.正极的电极反应式为
O+2HO+4e-===4OH-
2 2
B.将石墨电极改成Mg电极,难以观察到铁锈生成
C.若向自来水中加入少量NaCl(s),可较快地看到铁锈
D.分别向铁、石墨电极附近吹入O,前者铁锈出现得快
2
三、非选择题
14.钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大量
资金。请回答下列问题:
(1)钢铁的电化学腐蚀原理:在酸性环境中发生析氢腐蚀,在中性或碱性环境中发生吸
氧腐蚀。
① 分 别 写 出 图 1 中 铁 电 极 和 石 墨 电 极 的 电 极 反 应 式 :
________________________________________________________________________ ,
________________________________________________________________________。
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在图 1虚线框内所示位置
做出修改,并用箭头标出导线中电子流动方向。
③写出修改后石墨电极的电极反应式:
________________________________________________________________________
________________________________________________________________________。
(2)工业上常用盐酸除去铁锈。现将一生锈的铁片放入盐酸中,溶液中可能发生反应的
化学方程式有
________________________________________________________________________
________________________________________________________________________。
(3)在实际生产中,可在铁制品的表面镀铜防止铁被腐蚀。装置如图2所示:
①A 电极对应的金属是 ________(填元素名称),B 电极的电极反应式为
________________________________________________________________________。
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二
者质量差为5.12 g,则电镀时电路中通过的电子为________mol。③ 镀 层 破 损 后 , 镀 铜 铁 比 镀 锌 铁 更 容 易 被 腐 蚀 , 请 简 要 说 明 原 因 :
_______________________________________________________________________________
_______________________________________________________________________________
__________________________________________________________。