文档内容
专练 34 金属的腐蚀与防护
1.[2022·广东卷]为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀
锌铁片放入酸化的3% NaCl溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐
蚀的是( )
A.加入AgNO 溶液产生沉淀
3
B.加入淀粉碘化钾溶液无蓝色出现
C.加入KSCN溶液无红色出现
D.加入K[Fe(CN) ]溶液无蓝色沉淀生成
3 6
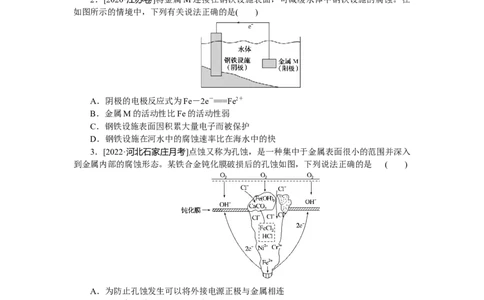
2.[2020·江苏卷]将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在
如图所示的情境中,下列有关说法正确的是( )
A.阴极的电极反应式为Fe-2e-===Fe2+
B.金属M的活动性比Fe的活动性弱
C.钢铁设施表面因积累大量电子而被保护
D.钢铁设施在河水中的腐蚀速率比在海水中的快
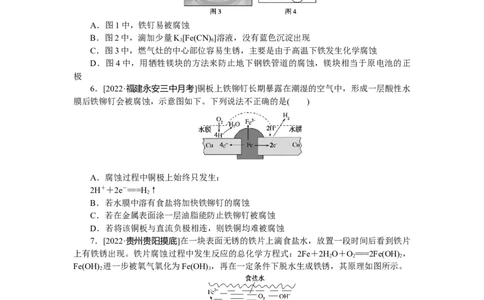
3.[2022·河北石家庄月考]点蚀又称为孔蚀,是一种集中于金属表面很小的范围并深入
到金属内部的腐蚀形态。某铁合金钝化膜破损后的孔蚀如图,下列说法正确的是 ( )
A.为防止孔蚀发生可以将外接电源正极与金属相连
B.孔蚀外每吸收2.24 L O ,可氧化0.2 mol Fe
2
C.由于孔蚀中Fe3+水解导致电解质酸性增强
D.孔隙中可以发生析氢腐蚀
4.[2022·宁夏育才中学考试]港珠澳大桥的设计使用寿命高达120年,主要的防腐方法
有:①钢梁上安装铝片;②使用高性能富锌(富含锌粉)底漆;③使用高附着性防腐涂料;
④预留钢铁腐蚀量。下列分析不合理的是( )
A.防腐涂料可以防水、隔离O,降低吸氧腐蚀速率
2
B.防腐过程中铝和锌均作为负极,失去电子
C.钢铁在海水中发生吸氧腐蚀时正极反应为O+4e-===2O2-
2
D.方法①②③只能减缓钢铁腐蚀,未能完全消除5.下列与金属腐蚀有关的说法,正确的是( )
A.图1中,铁钉易被腐蚀
B.图2中,滴加少量K[Fe(CN) ]溶液,没有蓝色沉淀出现
3 6
C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀
D.图4中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正
极
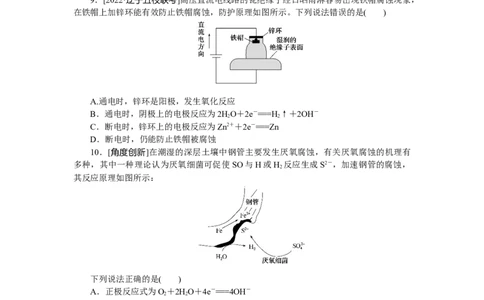
6.[2022·福建永安三中月考]铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水
膜后铁铆钉会被腐蚀,示意图如下。下列说法不正确的是( )
A.腐蚀过程中铜极上始终只发生:
2H++2e-===H ↑
2
B.若水膜中溶有食盐将加快铁铆钉的腐蚀
C.若在金属表面涂一层油脂能防止铁铆钉被腐蚀
D.若将该铜板与直流负极相连,则铁铜均难被腐蚀
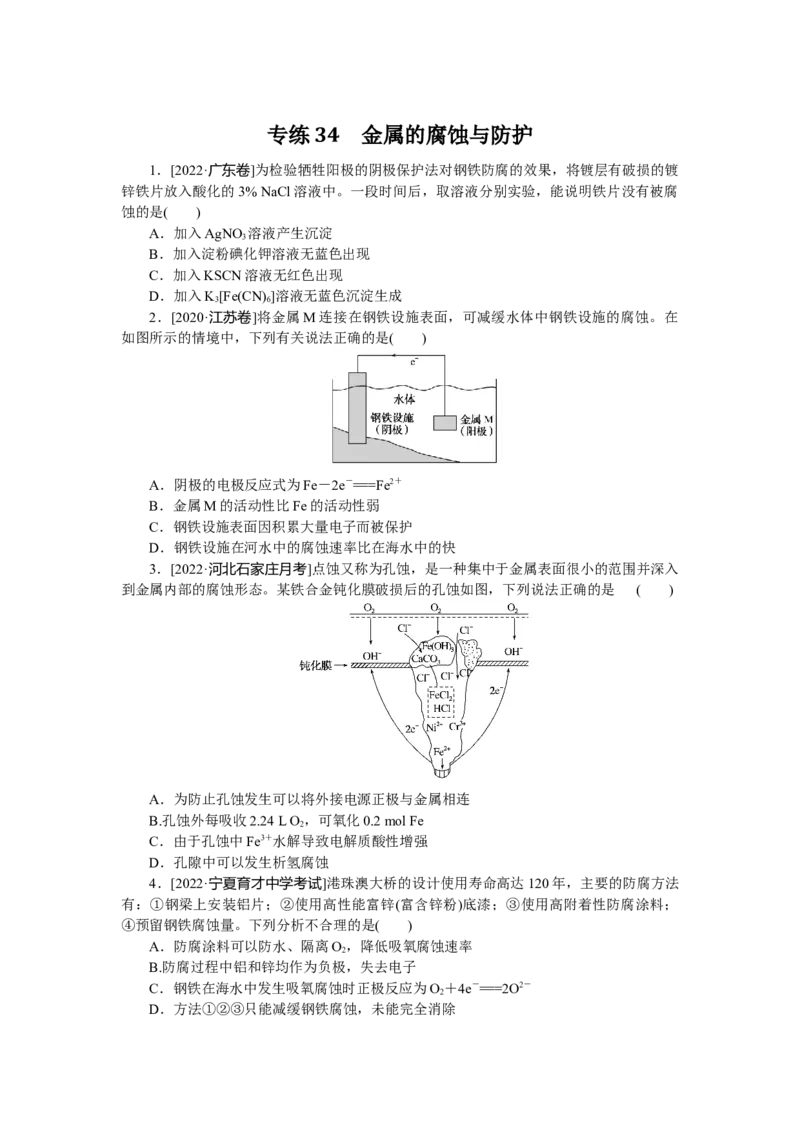
7.[2022·贵州贵阳摸底]在一块表面无锈的铁片上滴食盐水,放置一段时间后看到铁片
上有铁锈出现。铁片腐蚀过程中发生反应的总化学方程式:2Fe+2HO+O===2Fe(OH) ,
2 2 2
Fe(OH) 进一步被氧气氧化为Fe(OH) ,再在一定条件下脱水生成铁锈,其原理如图所示。
2 3
下列说法正确的是( )
A.铁片发生还原反应而被腐蚀
B.铁片腐蚀生成的铁锈可以保护内层的铁不被腐蚀
C.铁片腐蚀过程中负极发生的电极反应:2HO+O+4e-===4OH-
2 2
D.铁片里的铁和碳与食盐水形成了无数微小原电池,发生了电化学腐蚀
8.[2022·吉林实验中学摸底]下列有关下图所示的说法正确的是( )A.图甲中开关置于N处时铜锌合金腐蚀的速率增大
B.图乙中接通开关时,锌腐蚀的速率增大,锌上放出气体的速率增大
C.图丙中接通K 时铁棒不被腐蚀,属于牺牲阳极保护法
2
D.图丙中接通K 时,石墨棒周围溶液的pH增大
1
9.[2022·辽宁五校联考]高压直流电线路的瓷绝缘子经日晒雨淋容易出现铁帽腐蚀现象,
在铁帽上加锌环能有效防止铁帽腐蚀,防护原理如图所示。下列说法错误的是( )
A.通电时,锌环是阳极,发生氧化反应
B.通电时,阴极上的电极反应为2HO+2e-===H ↑+2OH-
2 2
C.断电时,锌环上的电极反应为Zn2++2e-===Zn
D.断电时,仍能防止铁帽被腐蚀
10.[角度创新]在潮湿的深层土壤中钢管主要发生厌氧腐蚀,有关厌氧腐蚀的机理有
多种,其中一种理论认为厌氧细菌可促使SO与H或H 反应生成S2-,加速钢管的腐蚀,
2
其反应原理如图所示:
下列说法正确的是( )
A.正极反应式为O+2HO+4e-===4OH-
2 2
B.钢管腐蚀的产物中含有FeS、Fe(OH) 等
2
C.SO与H 反应可表示为4H+SO-8e-=====S2-+4HO
2 2 2
D.向钢中加入Cu制成合金可减缓钢管的腐蚀
11.支撑海港码头基础的钢管桩,常用外加电流的阴极保护法进行防腐,工作原理如
图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是( )A.通入保护电流使钢管桩表面腐蚀电流接近于零
B.通电后外电路电子被强制从高硅铸铁流向钢管桩
C.高硅铸铁的作用是作为损耗阳极材料和传递电流
D.通入的保护电流应该根据环境条件变化进行调整