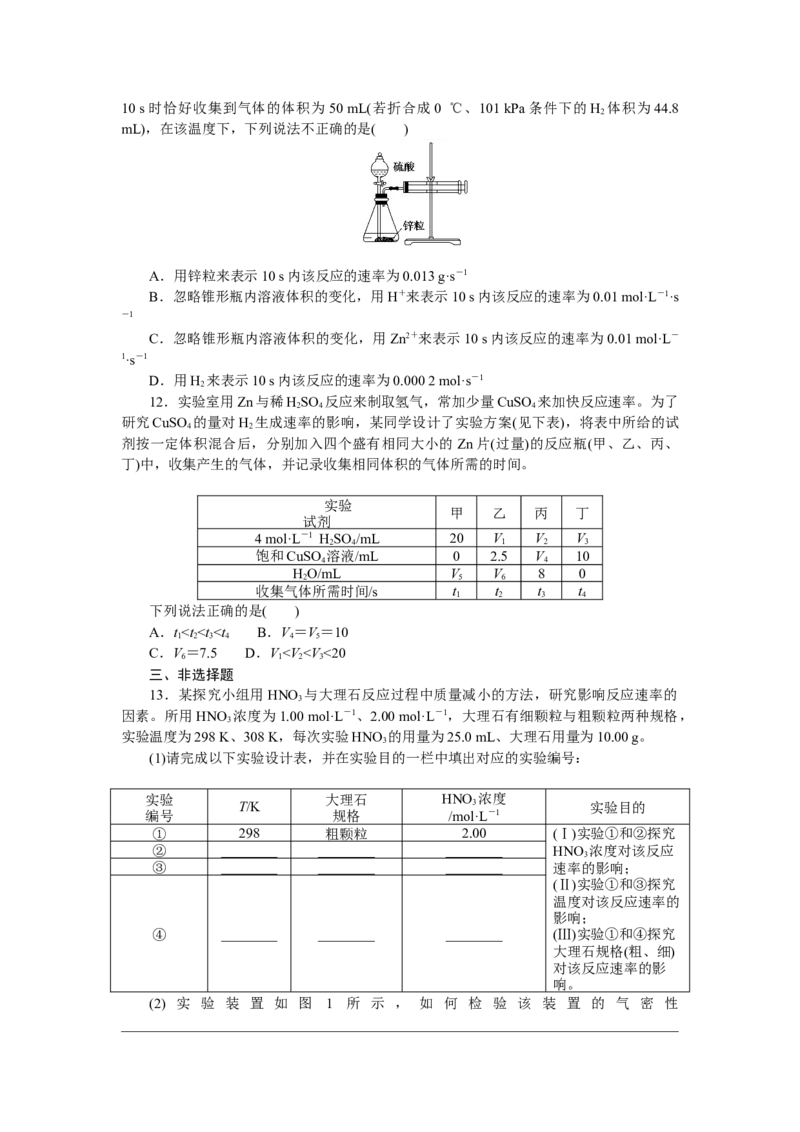
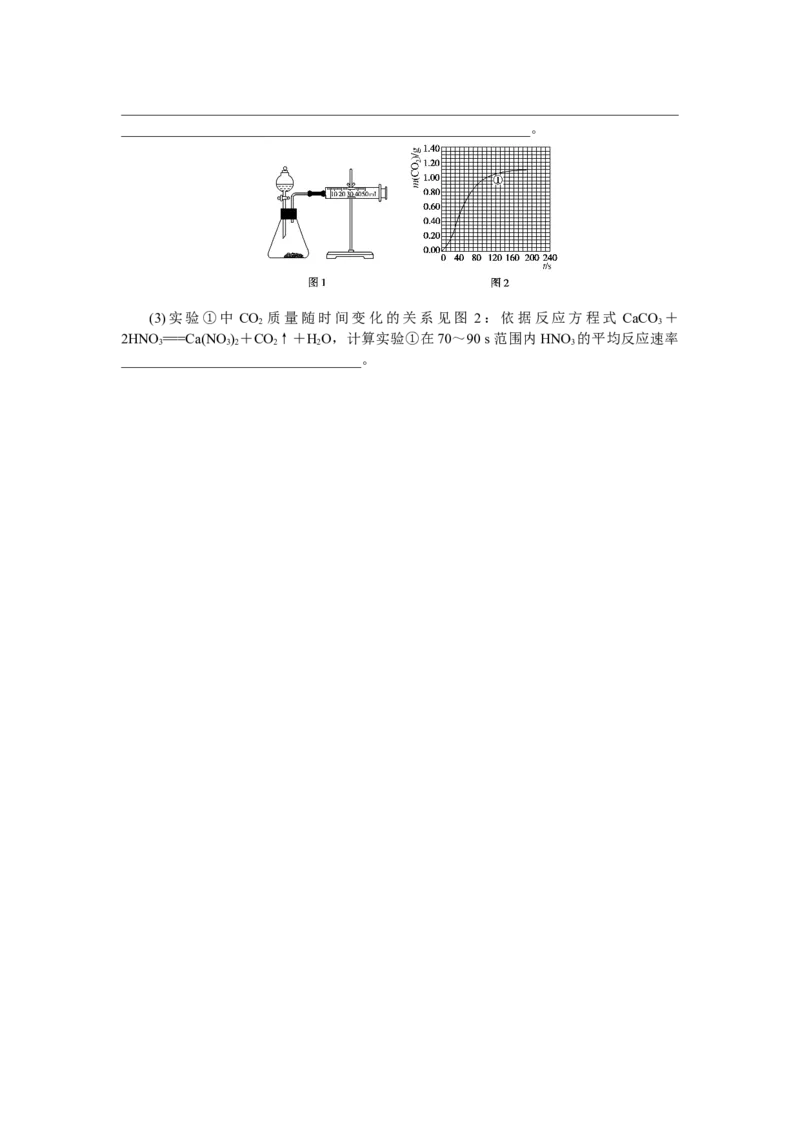
文档内容
专练 35 化学反应速率及影响因素
一、单项选择题
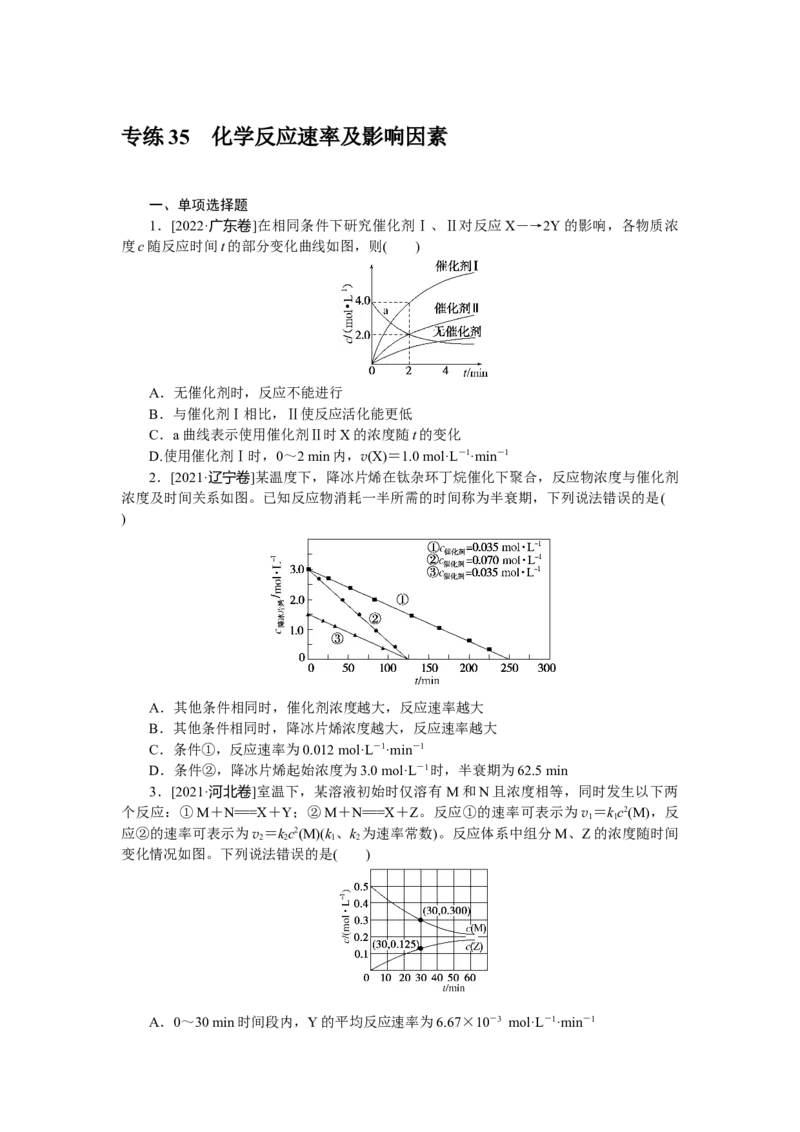
1.[2022·广东卷]在相同条件下研究催化剂Ⅰ、Ⅱ对反应X―→2Y的影响,各物质浓
度c随反应时间t的部分变化曲线如图,则( )
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时,0~2 min内,v(X)=1.0 mol·L-1·min-1
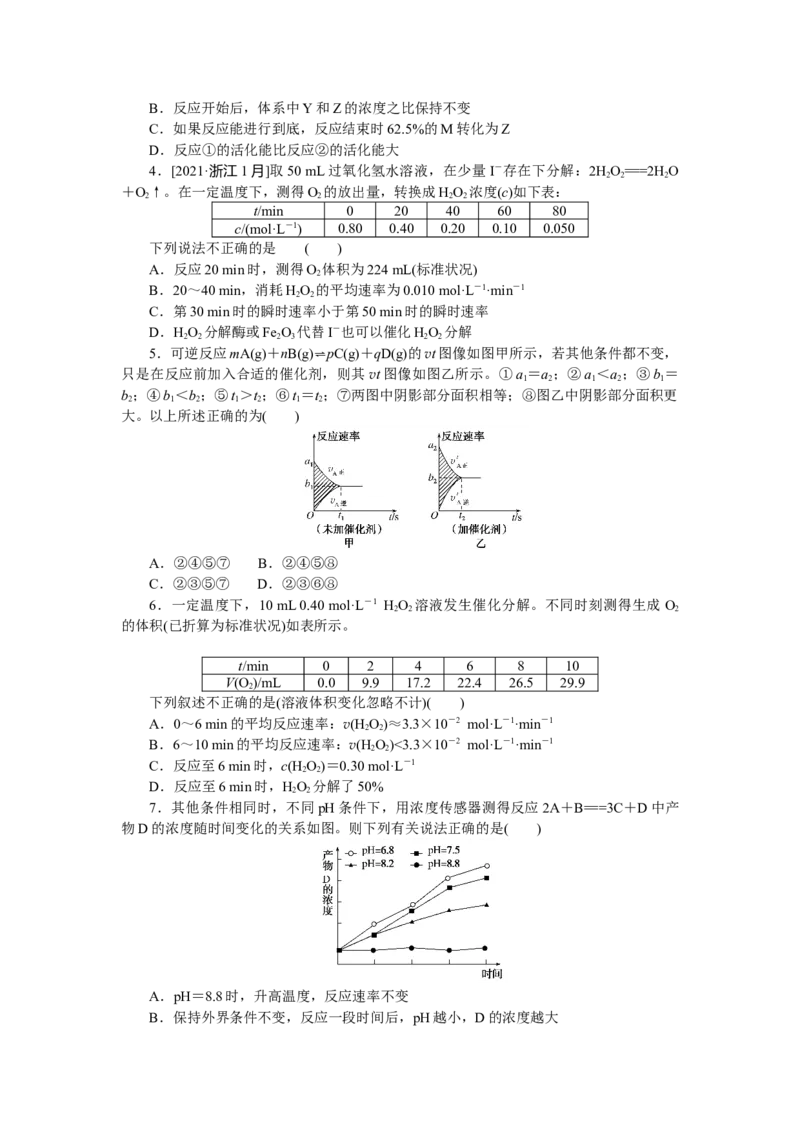
2.[2021·辽宁卷]某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂
浓度及时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是(
)
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为0.012 mol·L-1·min-1
D.条件②,降冰片烯起始浓度为3.0 mol·L-1时,半衰期为62.5 min
3.[2021·河北卷]室温下,某溶液初始时仅溶有 M和N且浓度相等,同时发生以下两
个反应:①M+N===X+Y;②M+N===X+Z。反应①的速率可表示为v =kc2(M),反
1 1
应②的速率可表示为v =kc2(M)(k 、k 为速率常数)。反应体系中组分M、Z的浓度随时间
2 2 1 2
变化情况如图。下列说法错误的是( )
A.0~30 min时间段内,Y的平均反应速率为6.67×10-3 mol·L-1·min-1B.反应开始后,体系中Y和Z的浓度之比保持不变
C.如果反应能进行到底,反应结束时62.5%的M转化为Z
D.反应①的活化能比反应②的活化能大
4.[2021·浙江1月]取50 mL过氧化氢水溶液,在少量I-存在下分解:2HO===2H O
2 2 2
+O↑。在一定温度下,测得O 的放出量,转换成HO 浓度(c)如下表:
2 2 2 2
t/min 0 20 40 60 80
c/(mol·L-1) 0.80 0.40 0.20 0.10 0.050
下列说法不正确的是 ( )
A.反应20 min时,测得O 体积为224 mL(标准状况)
2
B.20~40 min,消耗HO 的平均速率为0.010 mol·L-1·min-1
2 2
C.第30 min时的瞬时速率小于第50 min时的瞬时速率
D.HO 分解酶或Fe O 代替I-也可以催化HO 分解
2 2 2 3 2 2
5.可逆反应mA(g)+nB(g)⇌pC(g)+qD(g)的vt图像如图甲所示,若其他条件都不变,
只是在反应前加入合适的催化剂,则其 vt图像如图乙所示。①a =a ;②a <a ;③b =
1 2 1 2 1
b ;④b <b ;⑤t >t ;⑥t =t ;⑦两图中阴影部分面积相等;⑧图乙中阴影部分面积更
2 1 2 1 2 1 2
大。以上所述正确的为( )
A.②④⑤⑦ B.②④⑤⑧
C.②③⑤⑦ D.②③⑥⑧
6.一定温度下,10 mL 0.40 mol·L-1 HO 溶液发生催化分解。不同时刻测得生成 O
2 2 2
的体积(已折算为标准状况)如表所示。
t/min 0 2 4 6 8 10
V(O )/mL 0.0 9.9 17.2 22.4 26.5 29.9
2
下列叙述不正确的是(溶液体积变化忽略不计)( )
A.0~6 min的平均反应速率:v(H O)≈3.3×10-2 mol·L-1·min-1
2 2
B.6~10 min的平均反应速率:v(H O)<3.3×10-2 mol·L-1·min-1
2 2
C.反应至6 min时,c(H O)=0.30 mol·L-1
2 2
D.反应至6 min时,HO 分解了50%
2 2
7.其他条件相同时,不同pH条件下,用浓度传感器测得反应2A+B===3C+D中产
物D的浓度随时间变化的关系如图。则下列有关说法正确的是( )
A.pH=8.8时,升高温度,反应速率不变
B.保持外界条件不变,反应一段时间后,pH越小,D的浓度越大C.为了实验取样,可以采用调节pH的方法迅速停止反应
D.减小外界压强,反应速率一定减小
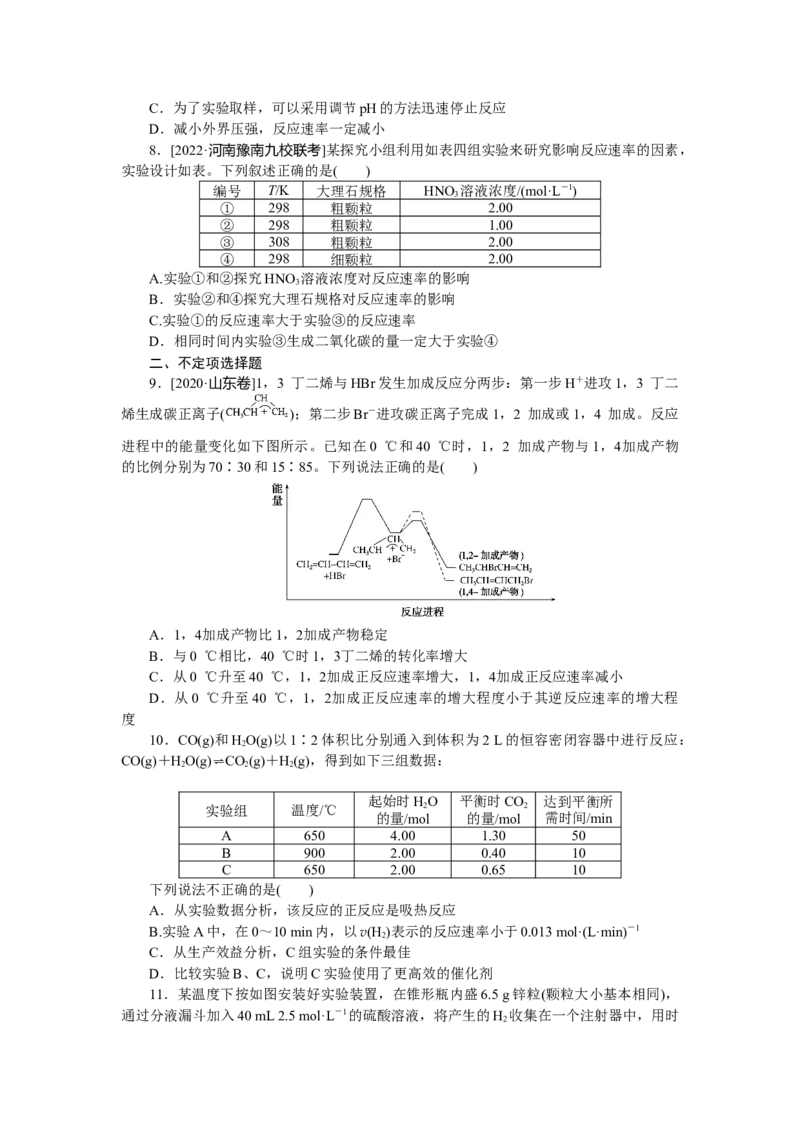
8.[2022·河南豫南九校联考]某探究小组利用如表四组实验来研究影响反应速率的因素,
实验设计如表。下列叙述正确的是( )
编号 T/K 大理石规格 HNO 溶液浓度/(mol·L-1)
3
① 298 粗颗粒 2.00
② 298 粗颗粒 1.00
③ 308 粗颗粒 2.00
④ 298 细颗粒 2.00
A.实验①和②探究HNO 溶液浓度对反应速率的影响
3
B.实验②和④探究大理石规格对反应速率的影响
C.实验①的反应速率大于实验③的反应速率
D.相同时间内实验③生成二氧化碳的量一定大于实验④
二、不定项选择题
9.[2020·山东卷]1,3 丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3 丁二
烯生成碳正离子( );第二步Br-进攻碳正离子完成1,2 加成或1,4 加成。反应
进程中的能量变化如下图所示。已知在0 ℃和40 ℃时,1,2 加成产物与1,4加成产物
的比例分别为70∶30和15∶85。下列说法正确的是( )
A.1,4加成产物比1,2加成产物稳定
B.与0 ℃相比,40 ℃时1,3丁二烯的转化率增大
C.从0 ℃升至40 ℃,1,2加成正反应速率增大,1,4加成正反应速率减小
D.从0 ℃升至40 ℃,1,2加成正反应速率的增大程度小于其逆反应速率的增大程
度
10.CO(g)和HO(g)以1∶2体积比分别通入到体积为2 L的恒容密闭容器中进行反应:
2
CO(g)+H
2
O(g)⇌CO
2
(g)+H
2
(g),得到如下三组数据:
起始时HO 平衡时CO 达到平衡所
实验组 温度/℃ 2 2
的量/mol 的量/mol 需时间/min
A 650 4.00 1.30 50
B 900 2.00 0.40 10
C 650 2.00 0.65 10
下列说法不正确的是( )
A.从实验数据分析,该反应的正反应是吸热反应
B.实验A中,在0~10 min内,以v(H )表示的反应速率小于0.013 mol·(L·min)-1
2
C.从生产效益分析,C组实验的条件最佳
D.比较实验B、C,说明C实验使用了更高效的催化剂
11.某温度下按如图安装好实验装置,在锥形瓶内盛6.5 g锌粒(颗粒大小基本相同),
通过分液漏斗加入40 mL 2.5 mol·L-1的硫酸溶液,将产生的H 收集在一个注射器中,用时
210 s时恰好收集到气体的体积为50 mL(若折合成0 ℃、101 kPa条件下的H 体积为44.8
2
mL),在该温度下,下列说法不正确的是( )
A.用锌粒来表示10 s内该反应的速率为0.013 g·s-1
B.忽略锥形瓶内溶液体积的变化,用H+来表示10 s内该反应的速率为0.01 mol·L-1·s
-1
C.忽略锥形瓶内溶液体积的变化,用Zn2+来表示10 s内该反应的速率为0.01 mol·L-
1·s-1
D.用H 来表示10 s内该反应的速率为0.000 2 mol·s-1
2
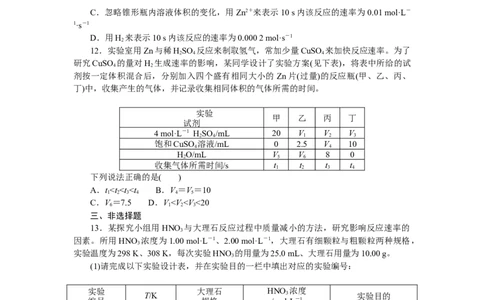
12.实验室用Zn与稀HSO 反应来制取氢气,常加少量CuSO 来加快反应速率。为了
2 4 4
研究CuSO 的量对H 生成速率的影响,某同学设计了实验方案(见下表),将表中所给的试
4 2
剂按一定体积混合后,分别加入四个盛有相同大小的 Zn片(过量)的反应瓶(甲、乙、丙、
丁)中,收集产生的气体,并记录收集相同体积的气体所需的时间。
实验
甲 乙 丙 丁
试剂
4 mol·L-1 HSO /mL 20 V V V
2 4 1 2 3
饱和CuSO 溶液/mL 0 2.5 V 10
4 4
HO/mL V V 8 0
2 5 6
收集气体所需时间/s t t t t
1 2 3 4
下列说法正确的是( )
A.t