文档内容
专练 55 分子结构与性质
一、单项选择题
1.[2021·山东卷]关于CHOH、NH 和(CH)NNH 的结构与性质,下列说法错误的是(
3 2 4 3 2 2
)
A.CHOH为极性分子
3
B.NH 空间结构为平面形
2 4
C.NH 的沸点高于(CH)NNH
2 4 3 2 2
D.CHOH和(CH)NNH 中C、O、N杂化方式均相同
3 3 2 2
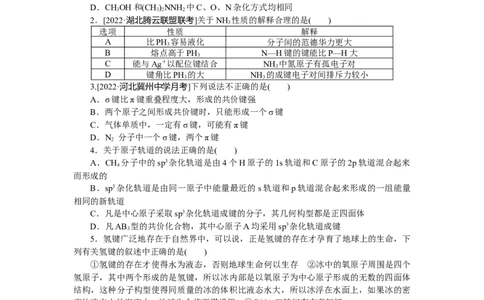
2.[2022·湖北腾云联盟联考]关于NH 性质的解释合理的是( )
3
选项 性质 解释
A 比PH 容易液化 分子间的范德华力更大
3
B 熔点高于PH N—H键的键能比P—H大
3
C 能与Ag+以配位键结合 NH 中氮原子有孤电子对
3
D 键角比PH 的大 NH 的成键电子对间排斥力较小
3 3
3.[2022·河北冀州中学月考]下列说法不正确的是( )
A.σ键比π键重叠程度大,形成的共价键强
B.两个原子之间形成共价键时,只能形成一个σ键
C.气体单质中,一定有σ键,可能有π键
D.N 分子中一个σ键,两个π键
2
4.关于原子轨道的说法正确的是( )
A.CH 分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来
4
而形成的
B.sp3杂化轨道是由同一原子中能量最近的s轨道和p轨道混合起来形成的一组能量
相同的新轨道
C.凡是中心原子采取sp3杂化轨道成键的分子,其几何构型都是正四面体
D.凡AB 型的共价化合物,其中心原子A均采用sp3杂化轨道成键
3
5.氢键广泛地存在于自然界中,可以说,正是氢键的存在才孕育了地球上的生命,下
列有关氢键的叙述中正确的是( )
①氢键的存在才使得水为液态,否则地球生命何以生存 ②冰中的氧原子周围是四个
氢原子,其中两个形成的是氢键,所以冰内部是以氧原子为中心原子形成的无数的四面体
结构,这种分子构型使得同质量的冰的体积比液态水大,所以冰浮在水面上,如果冰的密
度比液态水的密度大,地球生命将不堪设想 ③DNA双链间存在着氢键
④蛋白质分子中存在氢键
A.①②③④ B.①③④
C.②③④ D.③④
6.[2022·郑州一中月考]下列叙述正确的是( )
A.NO 、SO 、BF 、NCl 分子中没有一个分子中原子的最外层电子都满足了8e-稳定
2 2 3 3
结构
B.CCl 和NH 都是以极性键结合的极性分子,P 和NO 都是共价化合物
4 3 4 2
C.在CaO和SiO 晶体中,都不存在单个小分子
2
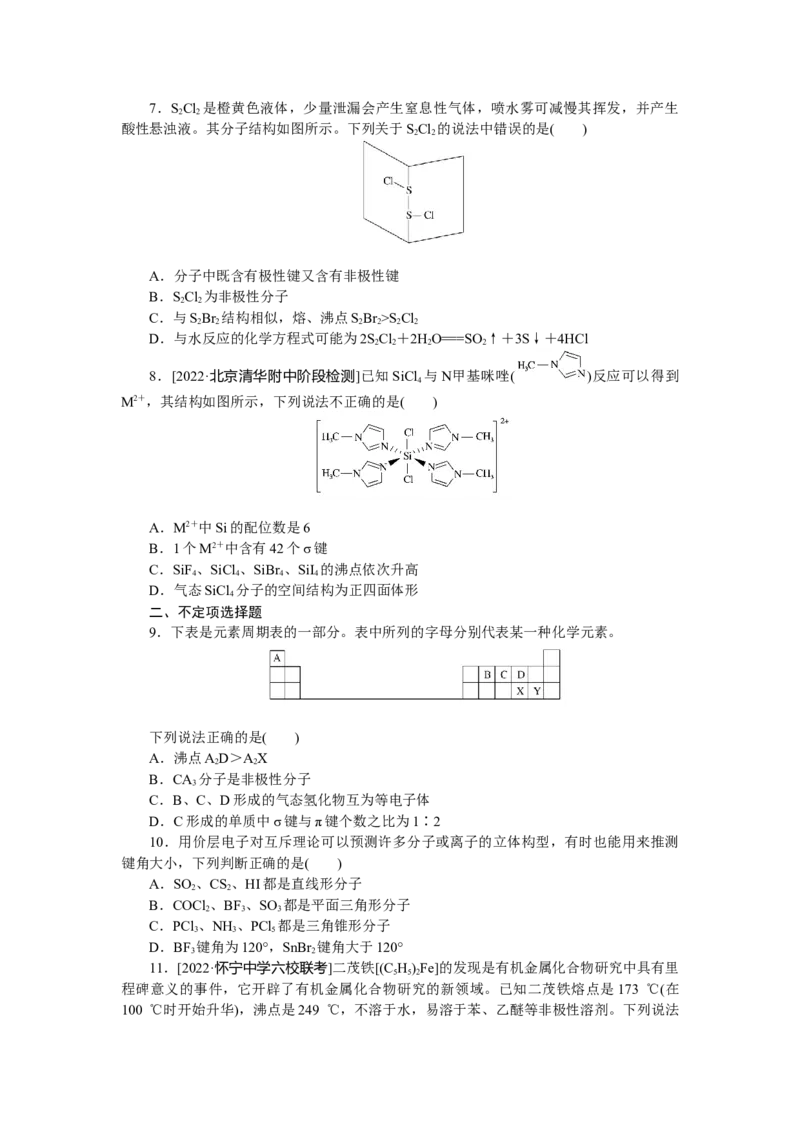
D.π键是由两个p电子“头碰头”重叠形成,σ键是镜面对称、而π键是轴对称7.SCl 是橙黄色液体,少量泄漏会产生窒息性气体,喷水雾可减慢其挥发,并产生
2 2
酸性悬浊液。其分子结构如图所示。下列关于SCl 的说法中错误的是( )
2 2
A.分子中既含有极性键又含有非极性键
B.SCl 为非极性分子
2 2
C.与SBr 结构相似,熔、沸点SBr >S Cl
2 2 2 2 2 2
D.与水反应的化学方程式可能为2SCl+2HO===SO↑+3S↓+4HCl
2 2 2 2
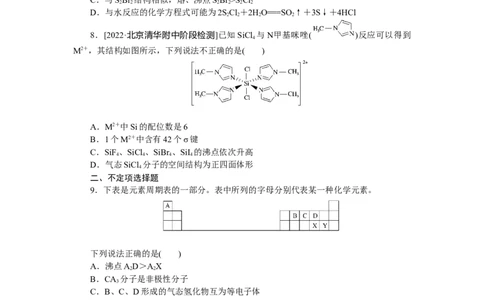
8.[2022·北京清华附中阶段检测]已知SiCl 与N甲基咪唑( )反应可以得到
4
M2+,其结构如图所示,下列说法不正确的是( )
A.M2+中Si的配位数是6
B.1个M2+中含有42个σ键
C.SiF、SiCl 、SiBr 、SiI 的沸点依次升高
4 4 4 4
D.气态SiCl 分子的空间结构为正四面体形
4
二、不定项选择题
9.下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。
下列说法正确的是( )
A.沸点AD>AX
2 2
B.CA 分子是非极性分子
3
C.B、C、D形成的气态氢化物互为等电子体
D.C形成的单质中σ键与π键个数之比为1∶2
10.用价层电子对互斥理论可以预测许多分子或离子的立体构型,有时也能用来推测
键角大小,下列判断正确的是( )
A.SO 、CS、HI都是直线形分子
2 2
B.COCl 、BF、SO 都是平面三角形分子
2 3 3
C.PCl 、NH 、PCl 都是三角锥形分子
3 3 5
D.BF 键角为120°,SnBr 键角大于120°
3 2
11.[2022·怀宁中学六校联考]二茂铁[(C H)Fe]的发现是有机金属化合物研究中具有里
5 5 2
程碑意义的事件,它开辟了有机金属化合物研究的新领域。已知二茂铁熔点是173 ℃(在
100 ℃时开始升华),沸点是249 ℃,不溶于水,易溶于苯、乙醚等非极性溶剂。下列说法不正确的是( )
A.二茂铁属于分子晶体
B.在二茂铁结构中 与Fe2+之间形成的化学键类型是离子键
,C H−
5 5
C.已知:环戊二烯的结构式为: ,则其中仅有1个碳原子采取sp3杂
化
中一定含π键
D.C H−
5 5
三、非选择题
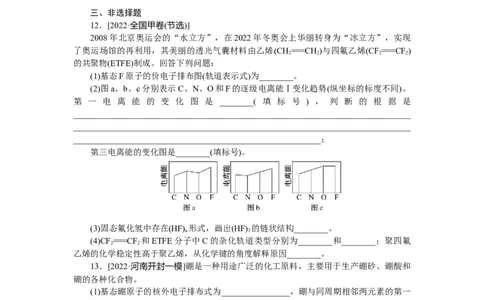
12.[2022·全国甲卷(节选)]
2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现
了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH===CH )与四氟乙烯(CF===CF )
2 2 2 2
的共聚物(ETFE)制成。回答下列问题:
(1)基态F原子的价电子排布图(轨道表示式)为________。
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。
第 一 电 离 能 的 变 化 图 是 ________( 填 标 号 ) , 判 断 的 根 据 是
_______________________________________________________________________________
_______________________________________________________________________________
__________________________________________________________;
第三电离能的变化图是________(填标号)。
(3)固态氟化氢中存在(HF) 形式,画出(HF) 的链状结构________。
n 3
(4)CF ===CF 和ETFE分子中C的杂化轨道类型分别为________和________;聚四氟
2 2
乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因________。
13.[2022·河南开封一模]硼是一种用途广泛的化工原料,主要用于生产硼砂、硼酸和
硼的各种化合物。
(1)基态硼原子的核外电子排布式为________________,硼与同周期相邻两元素的第一
电离能由大到小的顺序是________________。
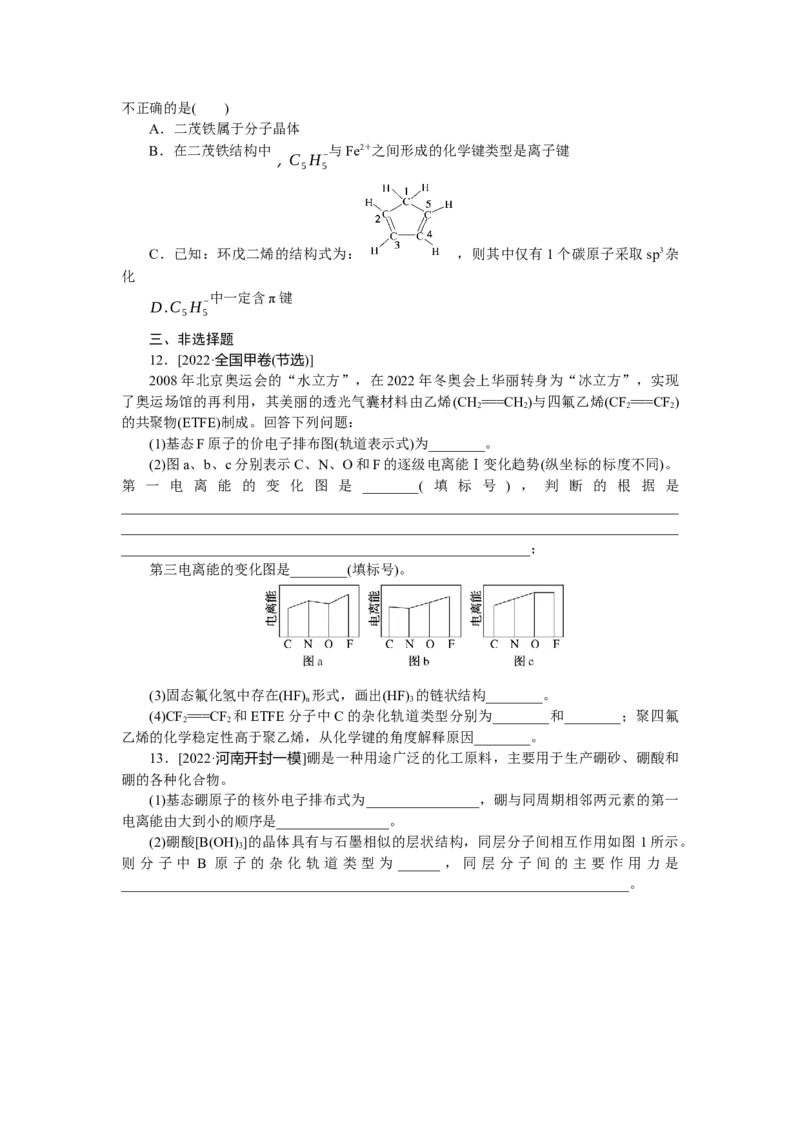
(2)硼酸[B(OH) ]的晶体具有与石墨相似的层状结构,同层分子间相互作用如图 1所示。
3
则 分 子 中 B 原 子 的 杂 化 轨 道 类 型 为 ______ , 同 层 分 子 间 的 主 要 作 用 力 是
________________________________________________________________________。(3)在BF 分子中,F—B—F的键角是______,该分子为________(填“极性分子”或
3
“非极性分子”),BF 和过量NaF作用可生成 的空间构型为________。
3 NaBF ,BF−
4 4
(4)一种硼酸盐的阴离子为 ,其结构中只有一个六元环,B的空间化学环境相同,
B On−
3 6
O有两种空间化学环境,画出 的结构图(注明所带电荷数)________。
B On−
3 6
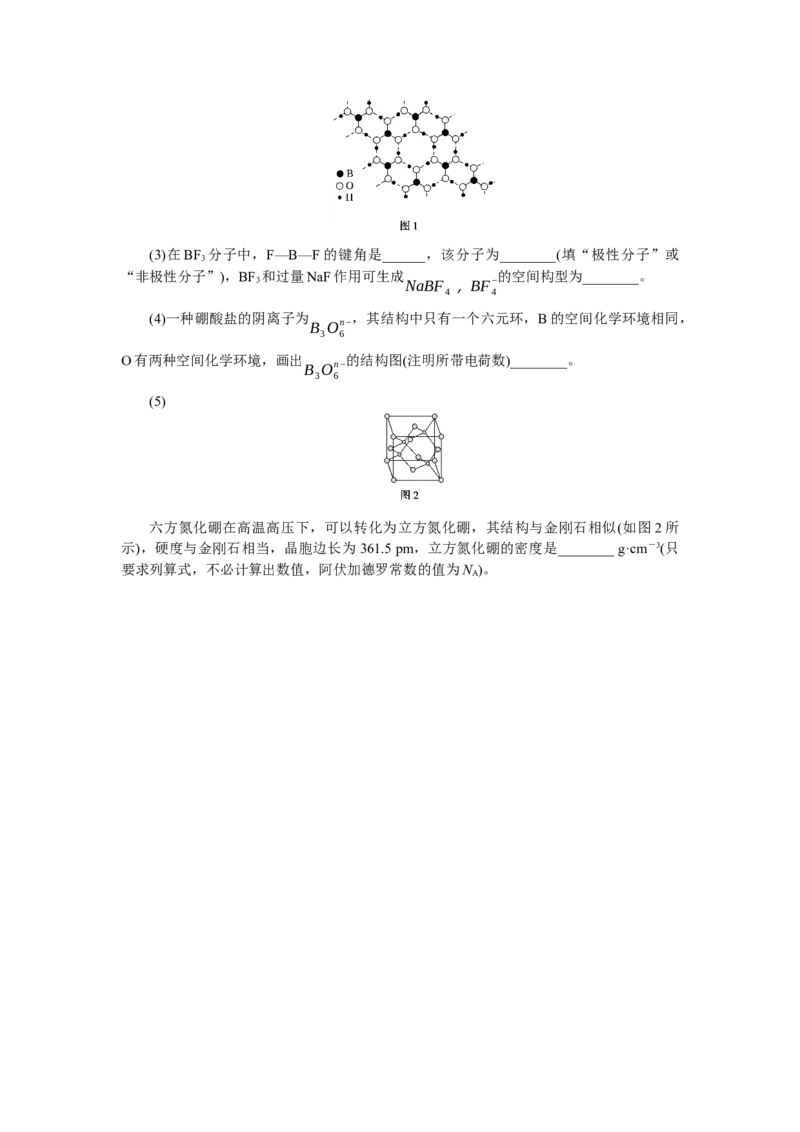
(5)
六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似(如图2所
示),硬度与金刚石相当,晶胞边长为361.5 pm,立方氮化硼的密度是________ g·cm-3(只
要求列算式,不必计算出数值,阿伏加德罗常数的值为N )。
A