文档内容
第五篇 水溶液中的离子反应与平衡
专项 33 对数关系图象
图象是高考试题的数字化语言,用图象表述化学反应过程或者呈现信息情景是近几年高考化学综合试
题常见的表达方式。它往往拥有较大的信息存储量,能够很全面地考查学生分析、比较、概括和归纳问题
的能力。近年来借助数学的对数知识,把浓度的对数融于离子反应平衡图象中,把所要考查的知识简明、
直观、形象的寓于坐标曲线上。
将溶液中某一微粒的浓度[如c(A)]或某些微粒浓度的比值[如c(A)/c(B)]取常用对数,即lg c(A)或
lg[c(A)/c(B)],与溶液中的pH或溶液的体积等关系作出的图像称为对数图像。常考对数图像的类型如下:
图像种类 具体类型 含义 变化规律
c(H X-)
c(H X-) 生成物与反应物离子浓 lg 越大,反应向正反应方向
lg
c(H X)
c(H X)
度比的常用对数
2
2
进行的程度越大
稀释后与稀释前体积比
对数图像 lg lg越大,稀释程度越大
的常用对数
AG=lg AG越大,酸性越强,中性时,
氢离子与氢氧根离子浓
c(H+) c(H+)
度比的常用对数 =1,AG=0
c(OH-) c(OH-)
pH=-lg c(H 氢离子浓度的常用对数
pH越大,c(H+)越小,溶液的碱性越强
负对数图 +) 负值
像 C离子浓度的常用对数
pC=-lgc(C) pC越大,c(C)越小
负值
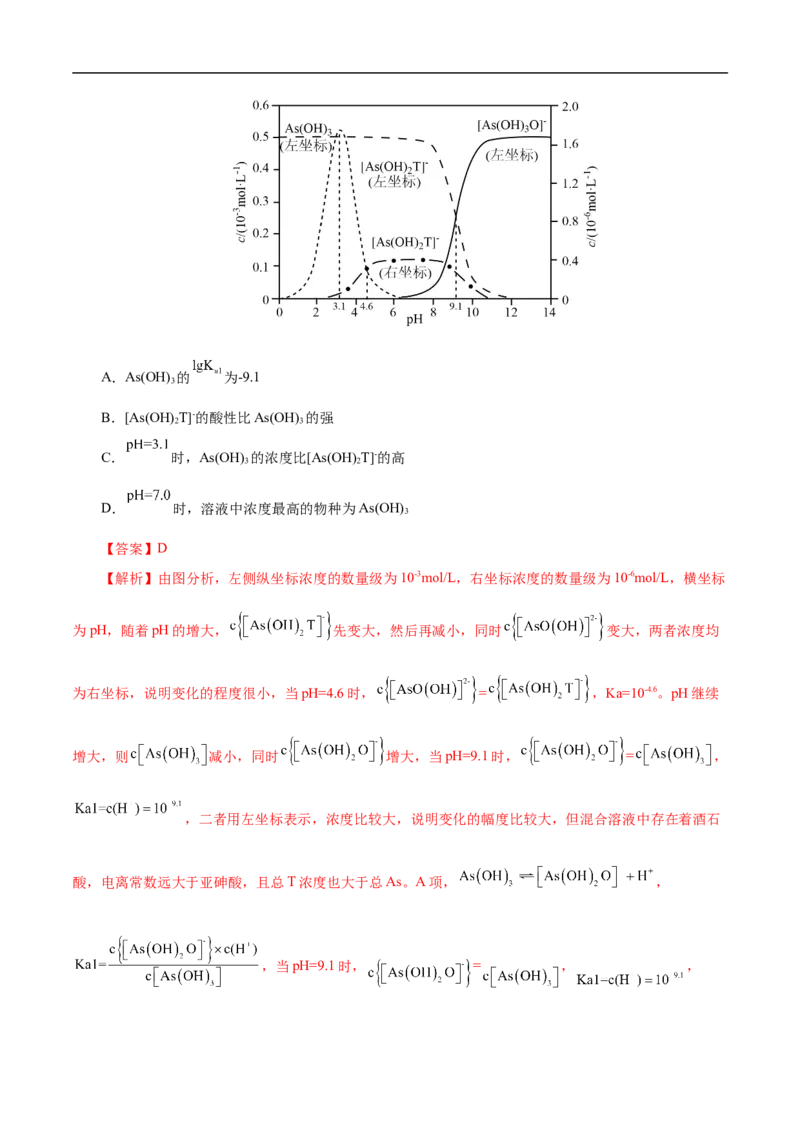
1.(2022•湖北省选择性考试)下图是亚砷酸As(OH) 和酒石酸 混合体系
3
中部分物种的 图(浓度:总 为 ,总T为 )。下列说法错误的是( )A.As(OH) 的 为-9.1
3
B.[As(OH) T]-的酸性比As(OH) 的强
2 3
C. 时,As(OH) 的浓度比[As(OH) T]-的高
3 2
D. 时,溶液中浓度最高的物种为As(OH)
3
【答案】D
【解析】由图分析,左侧纵坐标浓度的数量级为10-3mol/L,右坐标浓度的数量级为10-6mol/L,横坐标
为pH,随着pH的增大, 先变大,然后再减小,同时 变大,两者浓度均
为右坐标,说明变化的程度很小,当pH=4.6时, = ,Ka=10-4.6。pH继续
增大,则 减小,同时 增大,当pH=9.1时, = ,
,二者用左坐标表示,浓度比较大,说明变化的幅度比较大,但混合溶液中存在着酒石
酸,电离常数远大于亚砷酸,且总T浓度也大于总As。A项, ,
,当pH=9.1时, = , ,为-9.1,A正确;B项,[As(OH) T]- [As(OH)T]2-+H+ ,当pH=4.6
2
时, = ,Ka=10-4.6,而由A选项计算得HAsO 的 ,即
3 3
Ka > Ka1,所以[As(OH) T]-的酸性比As(OH) 的强,B正确;C项,由图可知As(OH) 的浓度为左坐标,浓
2 3 3
度的数量级为10-3mol/L,[As(OH) T]-的浓度为右坐标,浓度的数量级为10-6mol/L,所以pH=3.0时,
2
As(OH) 的浓度比[As(OH) T]-的高,C正确;D项,由可知条件,酒石酸 ,
3 2
As(OH) 的 为-9.1,即酒石酸的第一部电离常数远大于亚砷酸的第一步电离常数,所以酒石酸的酸性
3
远强于As(OH) ,另外总As的浓度也小于总T的浓度,所以当pH=7.0时,溶液中浓度最高的物种不是
3
As(OH) ,D错误;故选D。
3
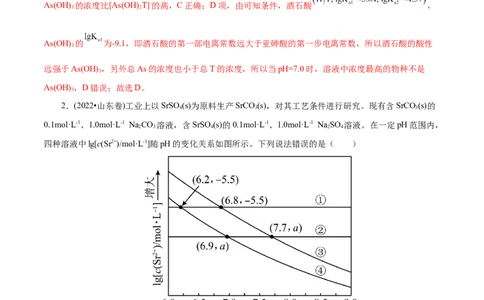
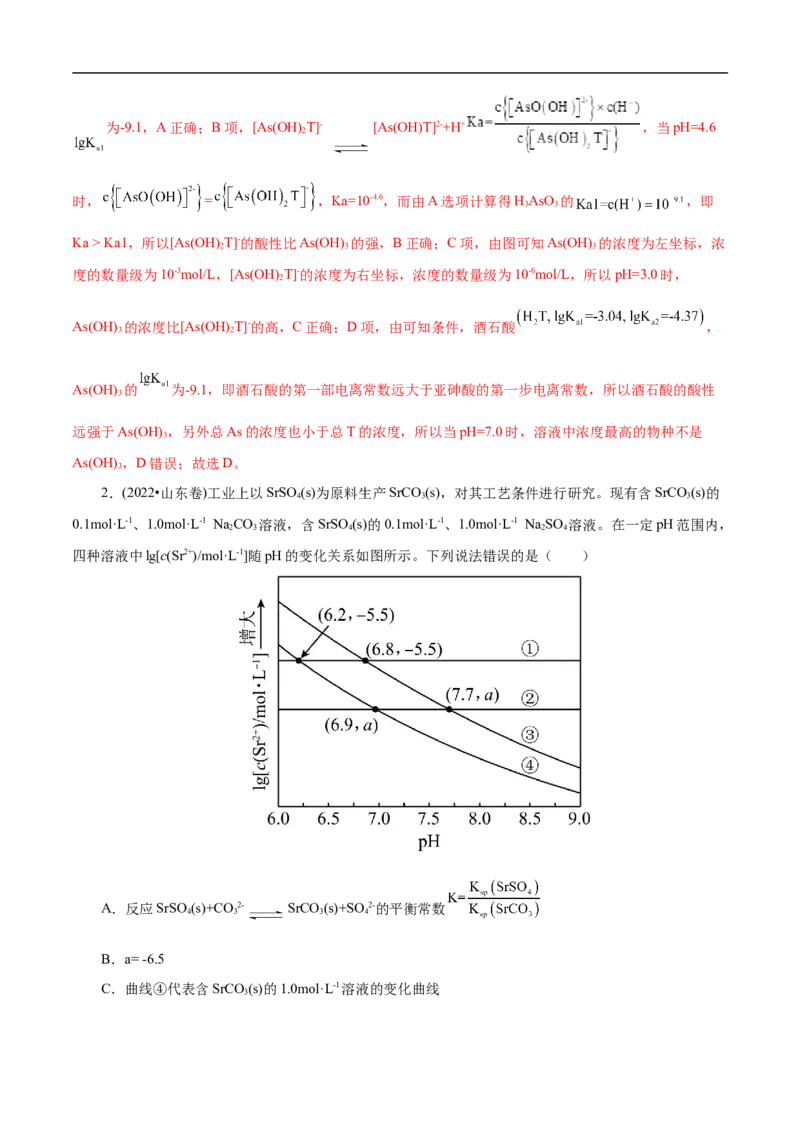
2.(2022•山东卷)工业上以SrSO (s)为原料生产SrCO (s),对其工艺条件进行研究。现有含SrCO (s)的
4 3 3
0.1mol·L-1、1.0mol·L-1 Na CO 溶液,含SrSO (s)的0.1mol·L-1、1.0mol·L-1 Na SO 溶液。在一定pH范围内,
2 3 4 2 4
四种溶液中lg[c(Sr2+)/mol·L-1]随pH的变化关系如图所示。下列说法错误的是( )
A.反应SrSO (s)+CO2- SrCO (s)+SO 2-的平衡常数
4 3 3 4
B.a= -6.5
C.曲线④代表含SrCO (s)的1.0mol·L-1溶液的变化曲线
3D.对含SrCO (s)且NaSO 和NaCO 初始浓度均为1.0mol·L-1的混合溶液, 时才发生沉淀转
4 2 4 2 3
化
【答案】D
【解析】分析题给图象,硫酸是强酸,溶液pH变化,溶液中硫酸根离子浓度几乎不变,则含硫酸锶
固体的硫酸钠溶液中锶离子的浓度几乎不变,pH相同时,溶液中硫酸根离子越大,锶离子浓度越小,所以
曲线①代表含硫酸锶固体的0.1 mol·L-1硫酸钠溶液的变化曲线,曲线②代表含硫酸锶固体的1 mol·L-1硫酸
钠溶液的变化曲线;碳酸是弱酸,溶液pH减小,溶液中碳酸根离子离子浓度越小,锶离子浓度越大,pH
相同时,1 mol·L-1碳酸钠溶液中碳酸根离子浓度大于0.1 mol·L-1碳酸钠溶液,则曲线③表示含碳酸锶固体
的0.1 mol·L-1碳酸钠溶液的变化曲线,曲线④表示含碳酸锶固体的1 mol·L-1碳酸钠溶液的变化曲线。A项,
反应SrSO (s)+CO2- SrCO (s)+SO 2-的平衡常数K= = = ,故A正确;
4 3 3 4
B项,曲线①代表含硫酸锶固体的0.1mol/L硫酸钠溶液的变化曲线,则硫酸锶的溶度积K (SrSO )=10—
sp 4
5.5×0.1=10—6.5,温度不变,溶度积不变,则溶液pH为7.7时,锶离子的浓度为 =10—6.5,则a为-6.5;
C项,曲线④表示含碳酸锶固体的1 mol·L-1碳酸钠溶液的变化曲线,故C正确;D项,硫酸是强酸,溶液
pH变化,溶液中硫酸根离子浓度几乎不变,则含硫酸锶固体的硫酸钠溶液中锶离子的浓度几乎不变,所以
硫酸锶的生成与溶液pH无关,故D错误;故选D。
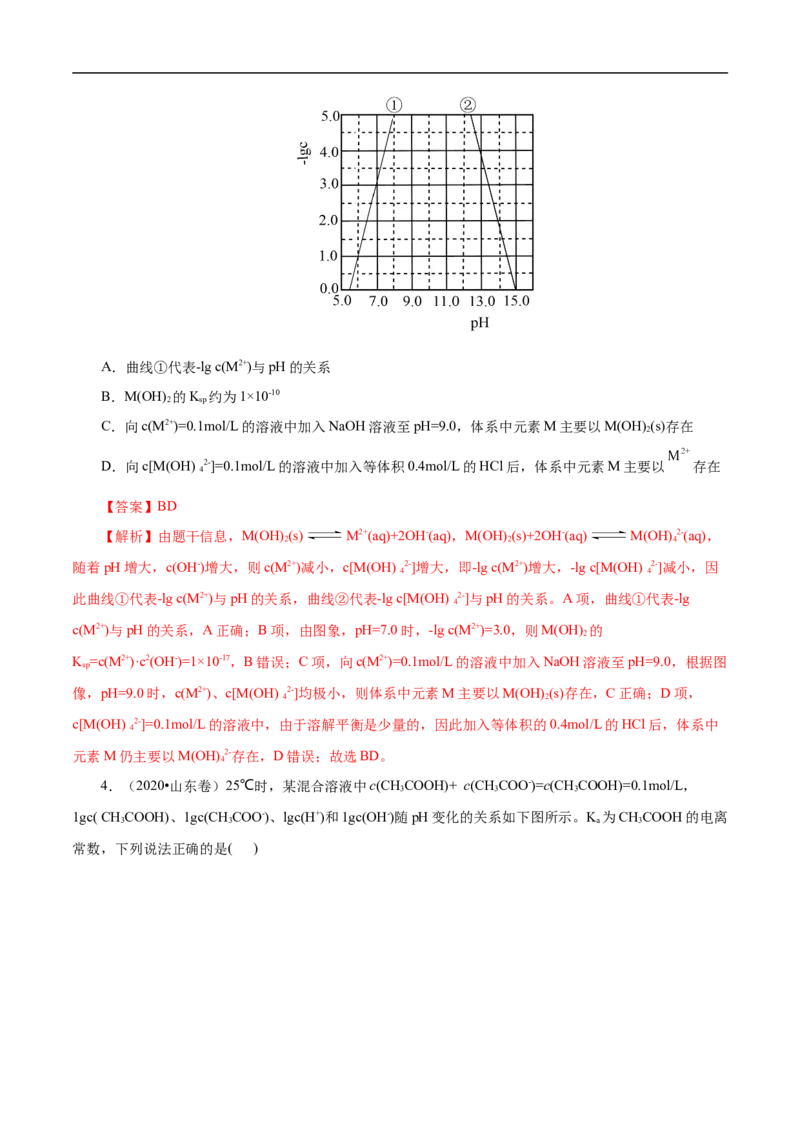
3.(2022•海南省选择性考试)某元素M的氢氧化物M(OH) (s)在水中的溶解反应为:M(OH) (s)
2 2
M2+(aq)+2OH-(aq),M(OH) (s)+2OH-(aq) M(OH) 2-(aq),25℃,-lgc与pH的关系如图所示,c为M2+或
2 4
M(OH) 2-浓度的值。下列说法错误的是( )
4A.曲线①代表-lg c(M2+)与pH的关系
B.M(OH) 的K 约为1×10-10
2 sp
C.向c(M2+)=0.1mol/L的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以M(OH) (s)存在
2
D.向c[M(OH) 2-]=0.1mol/L的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主要以 存在
4
【答案】BD
【解析】由题干信息,M(OH) (s) M2+(aq)+2OH-(aq),M(OH) (s)+2OH-(aq) M(OH) 2-(aq),
2 2 4
随着pH增大,c(OH-)增大,则c(M2+)减小,c[M(OH) 2-]增大,即-lg c(M2+)增大,-lg c[M(OH) 2-]减小,因
4 4
此曲线①代表-lg c(M2+)与pH的关系,曲线②代表-lg c[M(OH) 2-]与pH的关系。A项,曲线①代表-lg
4
c(M2+)与pH的关系,A正确;B项,由图象,pH=7.0时,-lg c(M2+)=3.0,则M(OH) 的
2
K =c(M2+)·c2(OH-)=1×10-17,B错误;C项,向c(M2+)=0.1mol/L的溶液中加入NaOH溶液至pH=9.0,根据图
sp
像,pH=9.0时,c(M2+)、c[M(OH) 2-]均极小,则体系中元素M主要以M(OH) (s)存在,C正确;D项,
4 2
c[M(OH) 2-]=0.1mol/L的溶液中,由于溶解平衡是少量的,因此加入等体积的0.4mol/L的HCl后,体系中
4
元素M仍主要以M(OH) 2-存在,D错误;故选BD。
4
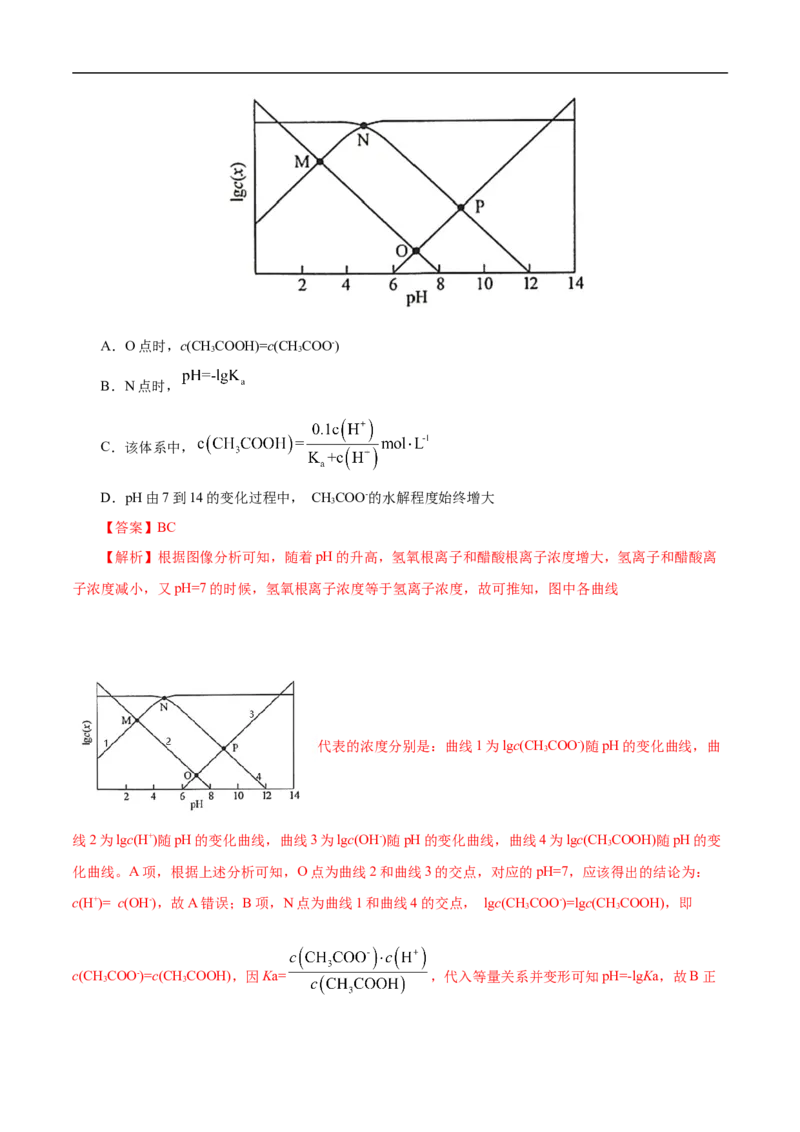
4.(2020•山东卷)25℃时,某混合溶液中c(CHCOOH)+ c(CHCOO-)=c(CHCOOH)=0.1mol/L,
3 3 3
1gc( CH COOH)、1gc(CHCOO-)、lgc(H+)和1gc(OH-)随pH变化的关系如下图所示。K 为CHCOOH的电离
3 3 a 3
常数,下列说法正确的是( )A.O点时,c(CHCOOH)=c(CHCOO-)
3 3
B.N点时,
C.该体系中,
D.pH由7到14的变化过程中, CHCOO-的水解程度始终增大
3
【答案】BC
【解析】根据图像分析可知,随着pH的升高,氢氧根离子和醋酸根离子浓度增大,氢离子和醋酸离
子浓度减小,又pH=7的时候,氢氧根离子浓度等于氢离子浓度,故可推知,图中各曲线
代表的浓度分别是:曲线1为lgc(CHCOO-)随pH的变化曲线,曲
3
线2为lgc(H+)随pH的变化曲线,曲线3为lgc(OH-)随pH的变化曲线,曲线4为lgc(CHCOOH)随pH的变
3
化曲线。A项,根据上述分析可知,O点为曲线2和曲线3的交点,对应的pH=7,应该得出的结论为:
c(H+)= c(OH-),故A错误;B项,N点为曲线1和曲线4的交点, lgc(CHCOO-)=lgc(CHCOOH),即
3 3
c(CHCOO-)=c(CHCOOH),因Ka= ,代入等量关系并变形可知pH=-lgKa,故B正
3 3确;C项,c(CHCOO-)+c(CHCOOH)=0.1mol/L,则c(CHCOO-)=0.1mol/L- c(CHCOOH),又Ka=
3 3 3 3
,联立两式消去c(CHCOO-)并化简整理可得出,c(CHCOOH)= mol/L
3 3
,故C正确;D项,醋酸根离子的水解平衡为:CHCOO-+H O CHCOOH +OH-,pH由7到14的
3 2 3
变化过程中,碱性不断增强,c(OH-)不断增大,则使不利于醋酸根离子的水解平衡,会使其水解程度减小,
故D错误;故选BC。
对数图像的解题策略
(1)先确定图像的类型是对数图像还是负对数图像。
(2)再弄清楚图像中横坐标和纵坐标的含义,是浓度对数还是比值对数。
(3)抓住图像中特殊点:如pH=7、lg x=0,交叉点。
(4)理清图像中曲线的变化趋势及含义,根据含义判断线上、线下的点所表示的意义。
(5)将图像中数据或曲线的变化与所学知识对接,作出选项的正误判断。
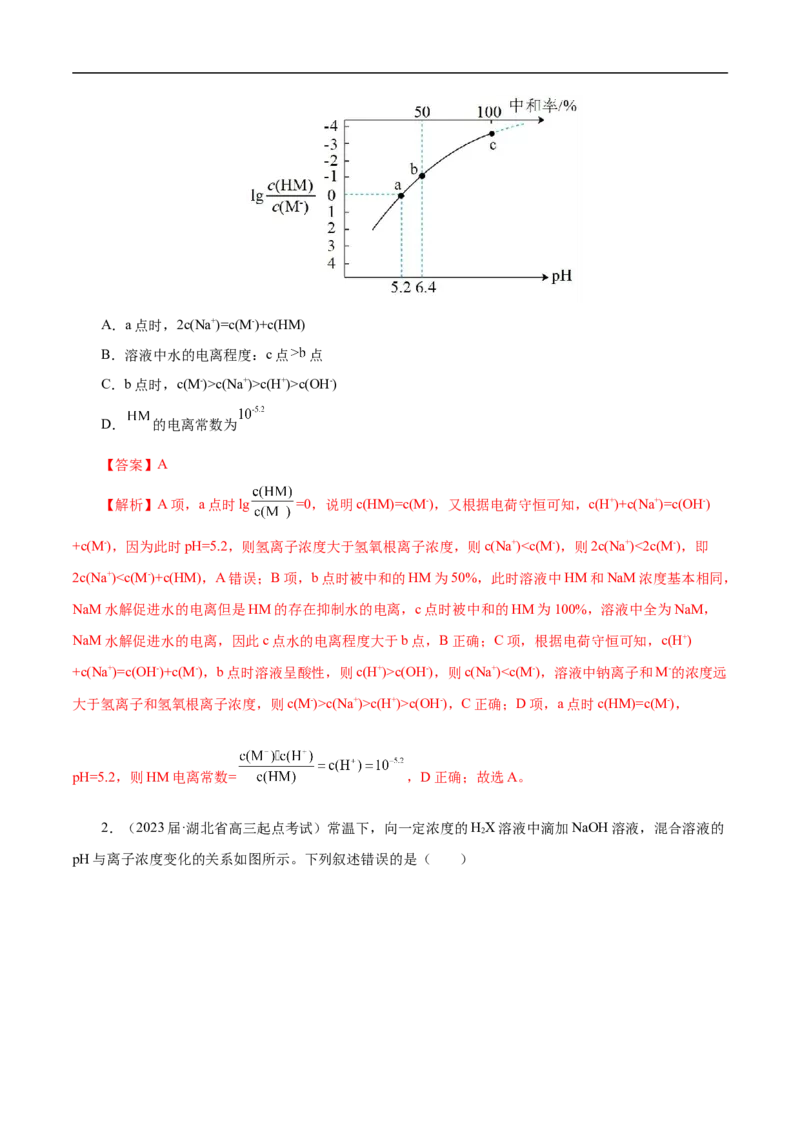
1.(2023届·辽宁省鞍山市普通高中高三一模) 是一种一元弱酸,常温下,向
溶液中逐滴加入浓度为 的 溶液,溶液中 、 、中和率(中和
率 )的变化如图所示。下列说法错误的是( )A.a点时,2c(Na+)=c(M-)+c(HM)
B.溶液中水的电离程度:c点 点
C.b点时,c(M-)>c(Na+)>c(H+)>c(OH-)
D. 的电离常数为
【答案】A
【解析】A项,a点时lg =0,说明c(HM)=c(M-),又根据电荷守恒可知,c(H+)+c(Na+)=c(OH-)
+c(M-),因为此时pH=5.2,则氢离子浓度大于氢氧根离子浓度,则c(Na+)c(OH-),则c(Na+)c(Na+)>c(H+)>c(OH-),C正确;D项,a点时c(HM)=c(M-),
pH=5.2,则HM电离常数= ,D正确;故选A。
2.(2023届·湖北省高三起点考试)常温下,向一定浓度的HX溶液中滴加NaOH溶液,混合溶液的
2
pH与离子浓度变化的关系如图所示。下列叙述错误的是( )A.HX的电离常数K 的数量级为10-2
2 a1
B.水电离的(H+):N点c(X²-)>c(HX-)>c(H+)=c(OH-)
【答案】B
【解析】根据直线m,当pH=0时 或 =-1.3,对应电离常数为10-1.3;根据直线n,
当pH=0时 或 =-4.3,对应电离常数为10-4.3, K >K ,所以K =1.0×10-1.3,
a1 a2 a1
K =1.0×104.3。A项,K =1.0×10-1.3,A正确;B项,直线n表示pH与 的关系, ,N
a2 a1
点 =0,则c(H+)=1×10-4.3, HX-电离出氢离子使溶液呈酸性,则M点氢离子浓度更大,氢离子抑
制水的电离,故水的电离程度N点>M点,B错误;C项,N点存在电荷守恒,c(Na+)+ c(H+)=2c(X2-)
+c(HX-)+c(OH-),由图可知N点时c(X2-)=c(HX-),由选项B分析可知,此时溶液显酸性,c(H+)>c(OH-),则
c(Na+)<3c(X2-),C正确;D项,当混合溶液呈中性时 , ,所以
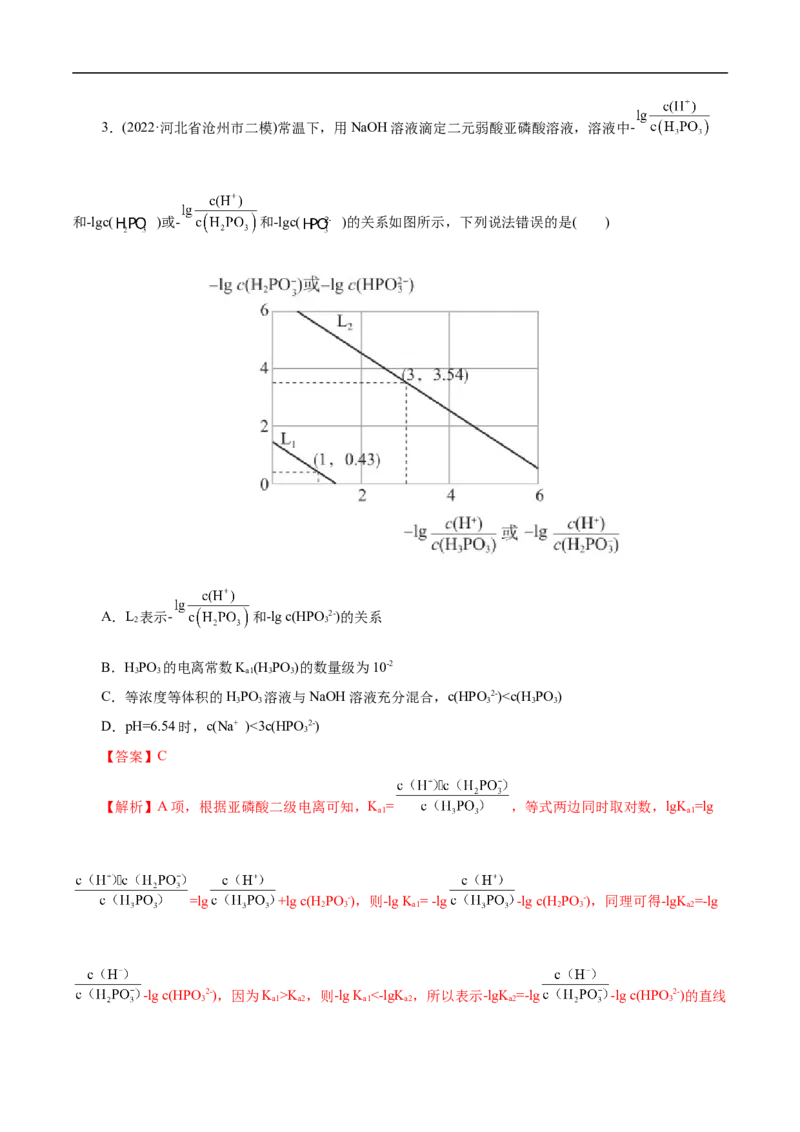
c(Na+)>c(X2-)>c(HX-)>c(H+)=c(OH-),D正确;故选B。3.(2022·河北省沧州市二模)常温下,用NaOH溶液滴定二元弱酸亚磷酸溶液,溶液中-
和-lgc( )或- 和-lgc( )的关系如图所示,下列说法错误的是( )
A.L 表示- 和-lg c(HPO 2-)的关系
2 3
B.HPO 的电离常数K (H PO )的数量级为10-2
3 3 a1 3 3
C.等浓度等体积的HPO 溶液与NaOH溶液充分混合,c(HPO 2-)K ,则-lg K <-lgK ,所以表示-lgK =-lg -lg c(HPO 2-)的直线
3 a1 a2 a1 a2 a2 3应该在上方即L,故A正确;B项,-lg K = -lg -lg c(H PO -),对应直线为L,将点(1,0.43)代
2 a1 2 3 1
入得,-lg K =1.43,K =10-1.43,K 数量级为10-2,B正确;C项,等浓度等体积的HPO 溶液与NaOH溶
a1 a1 a1 3 3
液充分混合,生成NaH PO 溶液,HPO -既电离又水解,电离平衡常数K =10-6.54,水解平衡常数K=
2 3 2 3 a2 h
=10-12.57,水解程度小于电离程度,故c(HPO 2-)>c(H PO ),C项错误;D项,将-lgK =-lg -lg
3 3 3 a2
c(HPO 2-)变形可得到 ,pH等于6.54时, c(HPO -)=c(HPO 2-),
3 2 3 3
根据电荷守恒,c(HA)+c(H+)= c(OH―)+ c(HPO -)+2c(HPO 2-)= c(OH―)+ 3c(HPO 2-),此时溶液呈酸性,
2 3 3 3
c(H+)>c(OH-),则c(Na+)<3c(HPO 2-),D项正确;故选C。
3
4.(2022·河南省安阳市考前适应性测试)室温下,某混合溶液中c(M+) +c(MOH) =c(R-) +c(HR) ,
和 随pH变化关系如图所示,已知pX = -lg X。下列说法错误的是( )
A.曲线I表示 与pH关系曲线,pK=pK -2
a b
B.b点溶液中c(M+)>c(R-),x= - 2
C.MR溶液显碱性,且MR溶液溶液中c(MOH)<c( HR)D.等物质的量的NaR与HR混合溶液中,c(HR)>c(Na+)>c(R-)>c(OH-)>c(H+)
【答案】D
【解析】由 ,当 =0即c(M+)= c(MOH)时,K= c(OH-),同理,K=
b a
c(H+),由lgX=0时,pH分别为6、10,则曲线I表示 与pH关系,曲线II表示 与pH关
系。A项,由lgX=0时,pH分别为6、10,则曲线I表示 与pH关系,K= c(H+)=10-6,常温下c点
a
c(OH-)= ,K= c(OH-)=10-4,则pK=pK -2,A正确;B项,b点溶液pH=8,溶液呈碱性,
b a b
说明MOH电离程度比HR电离程度大,则c(M+) >c(R-),c(OH-)= ,由
,则 ,则lgx=- =-2,B正确;C项,由K= 10-6,
a
K=10-4,相对而言MOH碱性较强、HR酸性较弱,则MR溶液显碱性,由越弱越水解规律可知,R-水解程
b
度大于M+,则MR溶液溶液中c(MOH) <c( HR),C正确;D项,由K= 10-6,R-水解常数为
a
< K,则HR电离程度大于R-水解程度,等物质的量的NaR与HR混合溶液中,c(R-)>
a
c(Na+)>c(HR)>c(H+)>c(OH-),D错误;故选D。
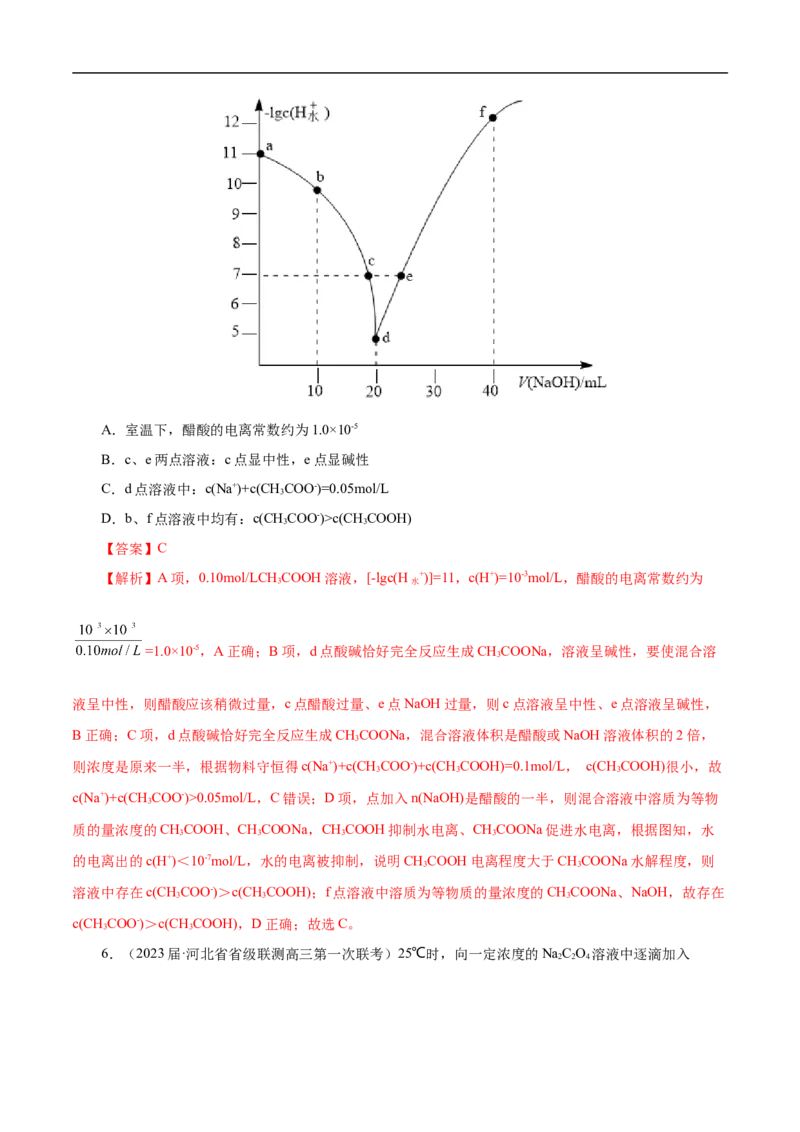
5.(2022·广东省东莞市高三模拟)窒温下,向20mL0.10mol/LCH COOH溶液中逐滴加入0.10mol/
3
LNaOH溶液,溶液中由水电离出H+浓度的负对数[-lgc(H +)]与所加NaOH溶液体积关系如图所示。(忽略
水
溶液混合引起的体积变化)。下列说法错误的是( )A.室温下,醋酸的电离常数约为1.0×10-5
B.c、e两点溶液:c点显中性,e点显碱性
C.d点溶液中:c(Na+)+c(CH COO-)=0.05mol/L
3
D.b、f点溶液中均有:c(CHCOO-)>c(CH COOH)
3 3
【答案】C
【解析】A项,0.10mol/LCH COOH溶液,[-lgc(H +)]=11,c(H+)=10-3mol/L,醋酸的电离常数约为
3 水
=1.0×10-5,A正确;B项,d点酸碱恰好完全反应生成CHCOONa,溶液呈碱性,要使混合溶
3
液呈中性,则醋酸应该稍微过量,c点醋酸过量、e点NaOH过量,则c点溶液呈中性、e点溶液呈碱性,
B正确;C项,d点酸碱恰好完全反应生成CHCOONa,混合溶液体积是醋酸或NaOH溶液体积的2倍,
3
则浓度是原来一半,根据物料守恒得c(Na+)+c(CH COO-)+c(CH COOH)=0.1mol/L, c(CHCOOH)很小,故
3 3 3
c(Na+)+c(CH COO-)>0.05mol/L,C错误;D项,点加入n(NaOH)是醋酸的一半,则混合溶液中溶质为等物
3
质的量浓度的CHCOOH、CHCOONa,CHCOOH抑制水电离、CHCOONa促进水电离,根据图知,水
3 3 3 3
的电离出的c(H+)<10-7mol/L,水的电离被抑制,说明CHCOOH电离程度大于CHCOONa水解程度,则
3 3
溶液中存在c(CHCOO-)>c(CHCOOH);f点溶液中溶质为等物质的量浓度的CHCOONa、NaOH,故存在
3 3 3
c(CHCOO-)>c(CHCOOH),D正确;故选C。
3 3
6.(2023届·河北省省级联测高三第一次联考)25℃时,向一定浓度的NaC O 溶液中逐滴加入
2 2 4HCl,以X表示 或 。已知 ,混合溶液 与 的关系如图所示。下列说法正
确的是( )
A.曲线Ⅱ表示 与 的关系
B.HC O 第一步电离常数的数量级为10-2
2 2 4
C.pH=2.71时,c(HC O-)>c(C O2-)=c(H C O)
2 4 2 4 2 2 4
D.pH=1.23时,3c(H C O)+c(H+)=c(Cl-)
2 2 4
【答案】C
【 解 析 】 当 , , ; 当 ,
c(HC O-)=c(H C O), ;由于 K >K ,结合图像可知,曲线Ⅱ表示
2 4 2 2 4 a1 a2
与pH的关系、曲线Ⅰ表示 与pH的关系。A项,曲线Ⅱ表示 与
的 关 系 , A 错 误 ; B 项 , 由 点 ( 2.23 , -1 ) 可 知 , HC O 第 一 步 电 离 常 数 的 数 量 级 为
2 2 4
,B 错误;C 项,由图可知,pH=2.71 时, >0,则
; , 由 点 ( 3.19 , 1 ) 可 知 ,; , 此 时 pH=2.71 , 则
,得 c(C O2-)=c(H C O),C 正确。D 项,由电荷守恒可知,c(Na+)
2 4 2 2 4
+c(H+)=c(Cl-)+c(OH-)+ c(HC O-)+2c(C O2-);由物料守恒可知,c(Na+)=2c(HC O-)+2c(H C O)+
2 4 2 4 2 4 2 2 4
2c(C O);两式联立可得:c(HC O-)+2c(H C O)+c(H+)=c(Cl-)+c(OH-); ,
2 2 4 2 2 4
pH=1.23时,c(HC O-)=c(H C O),则有3c(H C O)+c(H+)=c(Cl-)+c(OH-),D错误。 故选C。
2 4 2 2 4 2 2 4
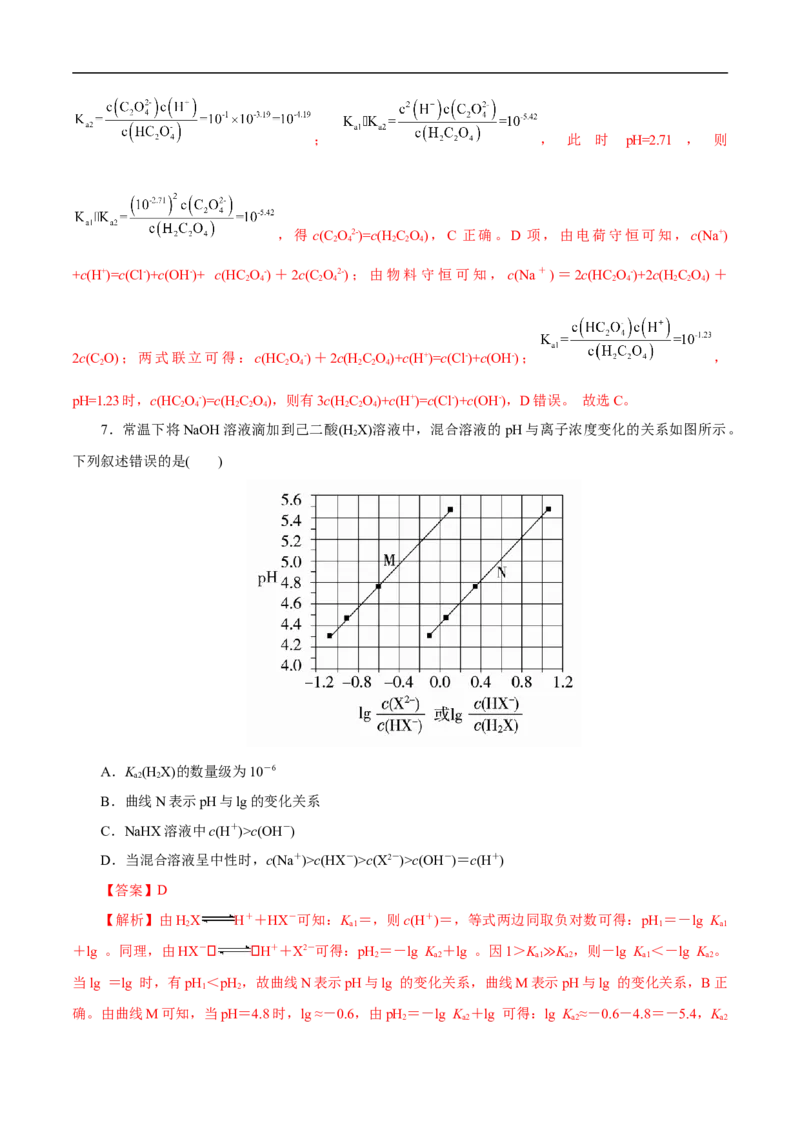
7.常温下将NaOH溶液滴加到己二酸(H X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。
2
下列叙述错误的是( )
A.K (H X)的数量级为10-6
a2 2
B.曲线N表示pH与lg的变化关系
C.NaHX溶液中c(H+)>c(OH-)
D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(OH-)=c(H+)
【答案】D
【解析】由HX H++HX-可知:K =,则c(H+)=,等式两边同取负对数可得:pH =-lg K
2 a1 1 a1
+lg 。同理,由HX- H++X2-可得:pH=-lg K +lg 。因1>K K ,则-lg K <-lg K 。
2 a2 a1 a2 a1 a2
当lg =lg 时,有pH<pH,故曲线N表示pH与lg 的变化关系,曲线M表≫示pH与lg 的变化关系,B正
1 2
确。由曲线M可知,当pH=4.8时,lg ≈-0.6,由pH=-lg K +lg 可得:lg K ≈-0.6-4.8=-5.4,K
2 a2 a2 a2=10-5.4=100.6×10-6,故K 的数量级为10-6,A正确。NaHX溶液中,<1,则lg <0,此时溶液pH<
a2
5.4,溶液呈酸性,所以c(H+)>c(OH-),C正确。由图可知,当溶液呈中性时lg >0,则c(X2-)>c(HX-),
D错误。
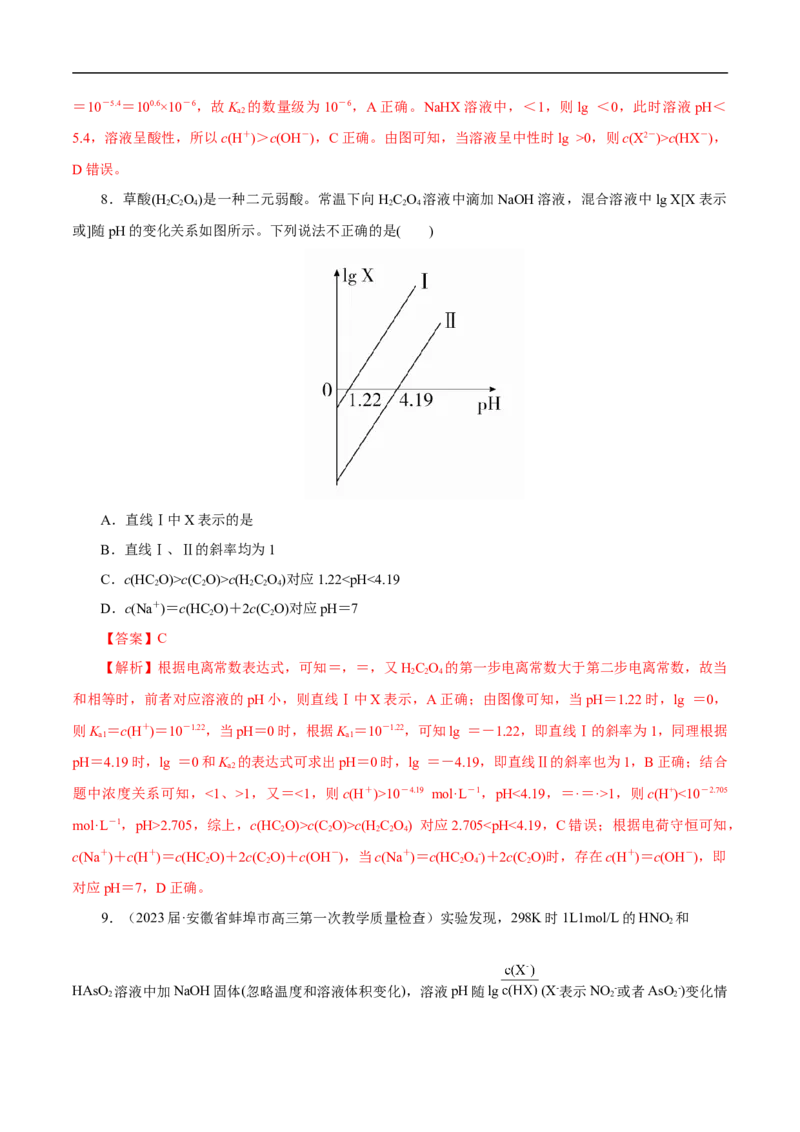
8.草酸(H C O)是一种二元弱酸。常温下向HC O 溶液中滴加NaOH溶液,混合溶液中lg X[X表示
2 2 4 2 2 4
或]随pH的变化关系如图所示。下列说法不正确的是( )
A.直线Ⅰ中X表示的是
B.直线Ⅰ、Ⅱ的斜率均为1
C.c(HC O)>c(C O)>c(H C O)对应1.221,又=<1,则c(H+)>10-4.19 mol·L-1,pH<4.19,=·=·>1,则c(H+)<10-2.705
mol·L-1,pH>2.705,综上,c(HC O)>c(C O)>c(H C O) 对应2.705c(HX)>c(OH-)>c(H+)
【答案】B
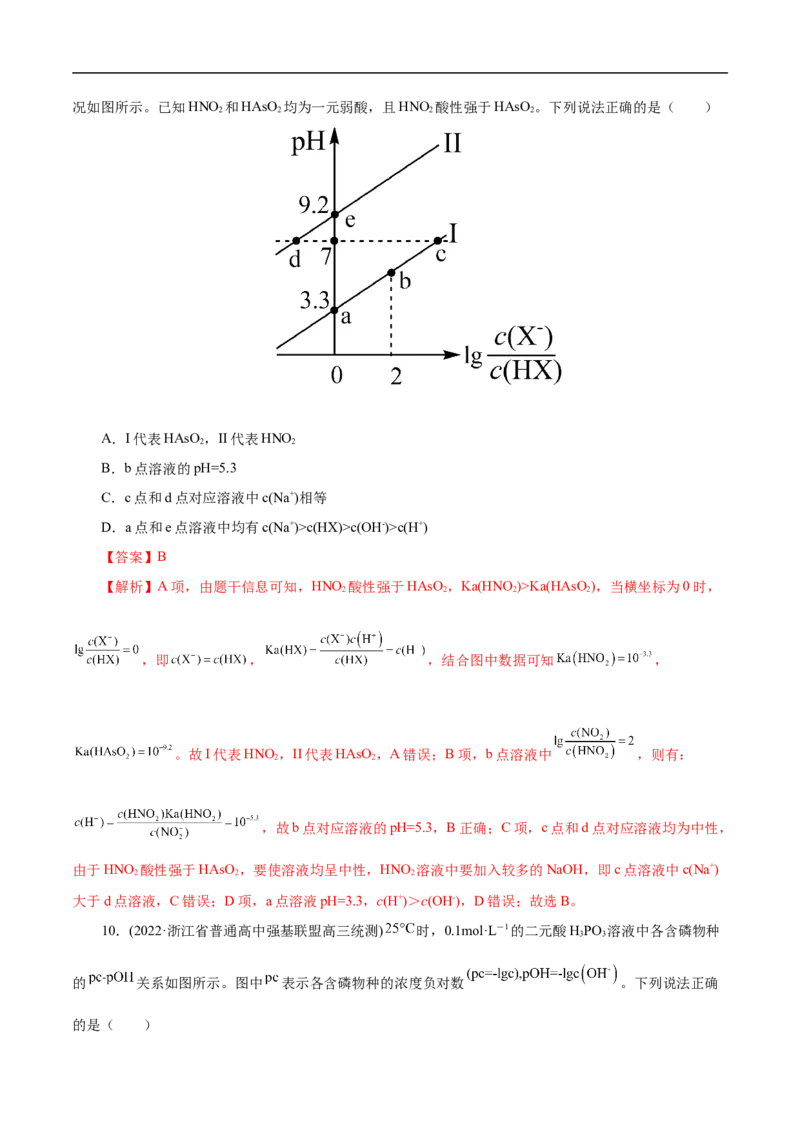
【解析】A项,由题干信息可知,HNO 酸性强于HAsO,Ka(HNO)>Ka(HAsO ),当横坐标为0时,
2 2 2 2
,即 , ,结合图中数据可知 ,
。故I代表HNO,II代表HAsO,A错误;B项,b点溶液中 ,则有:
2 2
,故b点对应溶液的pH=5.3,B正确;C项,c点和d点对应溶液均为中性,
由于HNO 酸性强于HAsO,要使溶液均呈中性,HNO 溶液中要加入较多的NaOH,即c点溶液中c(Na+)
2 2 2
大于d点溶液,C错误;D项,a点溶液pH=3.3,c(H+)>c(OH-),D错误;故选B。
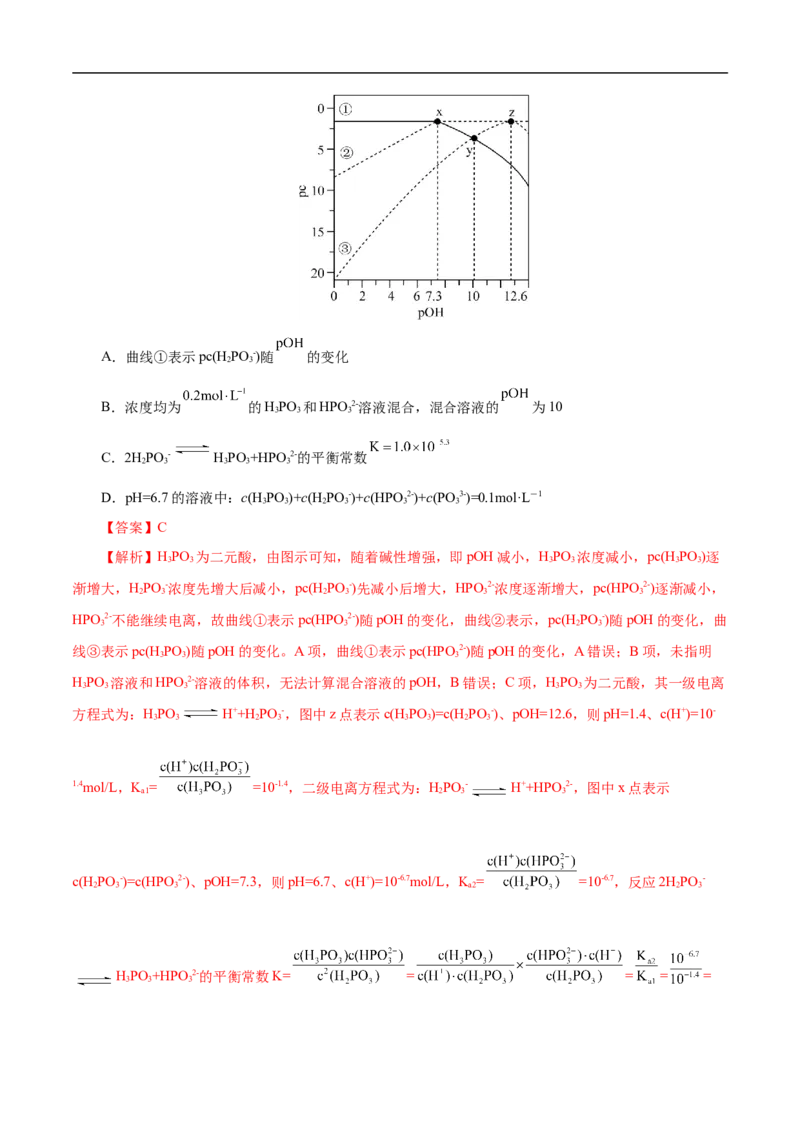
10.(2022·浙江省普通高中强基联盟高三统测) 时,0.1mol·L-1的二元酸HPO 溶液中各含磷物种
3 3
的 关系如图所示。图中 表示各含磷物种的浓度负对数 。下列说法正确
的是( )A.曲线①表示pc(HPO -)随 的变化
2 3
B.浓度均为 的HPO 和HPO 2-溶液混合,混合溶液的 为10
3 3 3
C.2HPO - HPO +HPO 2-的平衡常数
2 3 3 3 3
D.pH=6.7的溶液中:c(H PO )+c(H PO -)+c(HPO 2-)+c(PO 3-)=0.1mol·L-1
3 3 2 3 3 3
【答案】C
【解析】HPO 为二元酸,由图示可知,随着碱性增强,即pOH减小,HPO 浓度减小,pc(HPO )逐
3 3 3 3 3 3
渐增大,HPO -浓度先增大后减小,pc(HPO -)先减小后增大,HPO 2-浓度逐渐增大,pc(HPO 2-)逐渐减小,
2 3 2 3 3 3
HPO 2-不能继续电离,故曲线①表示pc(HPO 2-)随pOH的变化,曲线②表示,pc(HPO -)随pOH的变化,曲
3 3 2 3
线③表示pc(HPO )随pOH的变化。A项,曲线①表示pc(HPO 2-)随pOH的变化,A错误;B项,未指明
3 3 3
HPO 溶液和HPO 2-溶液的体积,无法计算混合溶液的pOH,B错误;C项,HPO 为二元酸,其一级电离
3 3 3 3 3
方程式为:HPO H++H PO -,图中z点表示c(HPO )=c(H PO -)、pOH=12.6,则pH=1.4、c(H+)=10-
3 3 2 3 3 3 2 3
1.4mol/L,K = =10-1.4,二级电离方程式为:HPO - H++HPO 2-,图中x点表示
a1 2 3 3
c(HPO -)=c(HPO 2-)、pOH=7.3,则pH=6.7、c(H+)=10-6.7mol/L,K = =10-6.7,反应2HPO -
2 3 3 a2 2 3
HPO +HPO 2-的平衡常数K= = = = =
3 3 3,C正确;D项,HPO 为二元酸,不能电离出PO 3-,溶液中无PO 3-,D错误;故选C。
3 3 3 3