文档内容
专项训练 配合物中心离子的化合价
一、单选题
1.配合物 中,中心离子的化合价是
A.+1 B.+2 C.+3 D.无法确定
2.配位化合物的数量巨大,组成和结构形形色色。配合物[Cu(NH )](OH) 的中心离子、
3 4 2
配体、中心离子的化合价和配位数分别为
A.Cu2+、NH 、+2、4 B.Cu+、NH 、+1、4
3 3
C.Cu2+、OH-、+2、2 D.Cu2+、NH 、+2、2
3
3.配合物K[Fe(CN) ]中,中心离子的化合价是
3 6
A.+3 B.-3 C.+1 D.—1
4.下列有关配合物的论述不合理的是
A.Na[Al(OH)]和[Ag(NH)]OH都是配合物
4 3 2
B.Na[AlF ]、Na[SiF]和[Cu(NH )]Cl 的配位数都是6
3 6 2 6 3 4 2
C.[ZnCl ]2-的空间构型为正四面体形
4
D.配合物[Cr(H O) Br ]Br·2H O中,中心离子的化合价为+3价,配离子带1个单
2 4 2 2
位的正电荷
5.如图所示,向CuSO 溶液中逐滴加入浓氨水至过量,得到透明的深蓝色溶液,其溶
4
质为配合物[Cu(NH )]SO ;再向其中加入乙醇,将析出深蓝色的晶体,其组成为
3 4 4
[Cu(NH )]SO •H O。下列说法错误的是
3 4 4 2
A.该过程中涉及的反应有CuSO +2NH•H O=Cu(OH) ↓+(NH)SO
4 3 2 2 4 2 4
B.配合物[Cu(NH )]SO 中,中心离子的化合价为+2价
3 4 4
C.配合物[Cu(NH )]SO •H O中,Cu2+给出孤电子对,NH 提供空轨道
3 4 4 2 3
D.由上述实验可知,加入乙醇后,配合物[Cu(NH )]SO 在水中的溶解度减小
3 4 4
6.已知NO能被FeSO 溶液吸收生成配合物[Fe(NO)(H O) ]SO 。下列说法正确的是
4 2 5 4
A.中心离子的配位数为5
B.配体为NO中,配位原子为O
C.该配合物中Fe的化合价为+2价,价层电子排布式为3d54s1,易被氧化为Fe3+
D.HO的VSEPR模型为四面体形,空间结构为V形
2
资料收集整理【淘宝店铺:向阳百分百】7.对配合物[Cr(H O) Br ]Br·2H O的说法正确的是
2 4 2 2
A.配体为水分子,配原子为O,外界为Br-
B.中心离子的配位数为6
C.1mol该配合物可以与足量AgNO 溶液反应生成3molAgBr沉淀
3
D.中心离子的化合价为+2
8.许多过渡金属离子对多种配位体有很强的结合力,能形成种类繁多的配合物.下列
说法正确的
A.向配合物 的溶液中加入足量的 溶液,所有的
均被完全沉淀
B. 和 中其中心离子的化合价都是+2价
C.配合物 的配体为 和
D.配合物 的配位数为6
9.下列关于化学式 [TiCl(H O) ]Cl ·H O的配合物的说法中正确的是
2 5 2 2
A.配体是Cl-和HO,配位数是9
2
B.中心离子是Ti4+,配离子是[TiCl(H O) ]2+
2 5
C.该配合物中存在离子键、配位键、极性键和非极性键
D.在含1mol该配合物的溶液中加入足量AgNO 溶液,可生成2mol AgCl沉淀
3
10.下列关于化学式为 的配合物的说法中正确的是
A.配位体是 和
B.中心离子是 ,配离子是
C.内界和外界中的 的数目比是1∶2
D.加入足量 溶液, 该配合物可生成
11.配合物Na[Fe(CN) (NO)]可用于离子检验,下列说法正确的是
2 5
A.配离子为[Fe(CN) (NO)]2-,中心离子为Fe2+,配位数为6
5
B.向该配合物的溶液中滴加NaOH溶液,有红褐色沉淀产生
C.该物质存在金属键
D.该配合物为离子化合物,易电离,1mol配合物电离得到的离子数为3N
A
资料收集整理【淘宝店铺:向阳百分百】12.配合物 可用于离子检验,下列说法不正确的是
A.此配合物中存在离子键、配位键、极性键
B.1mol配合物中 键数目为6N
A
C.配离子为[Fe(CN) ]3−,中心离子为 ,配位数为6
6
D.该配合物易电离,1mol该配合物电离得到阴、阳离子的数目共
13.某配合物的化学式为[CrCl (H O) ]Cl·2HO,下列说法正确的是
2 2 4 2
A.配位体是Cl-,配位原子数是2
B.配离子是[CrCl (H O) ]+,中心离子是Cr3+
2 2 4
C.1mol该化合物溶于水可电离出3molCl-
D.加入足量AgNO 溶液,Cl元素可被完全沉淀
3
14.下列关于化学式为 的配合物的说法中正确的是
A.配体是 和 ,配位数是9
B.中心离子是 ,配离子是
C.内界和外界中的 的数目比是 2:1
D.加入足量 溶液,所有 均被完全沉淀
二、填空题
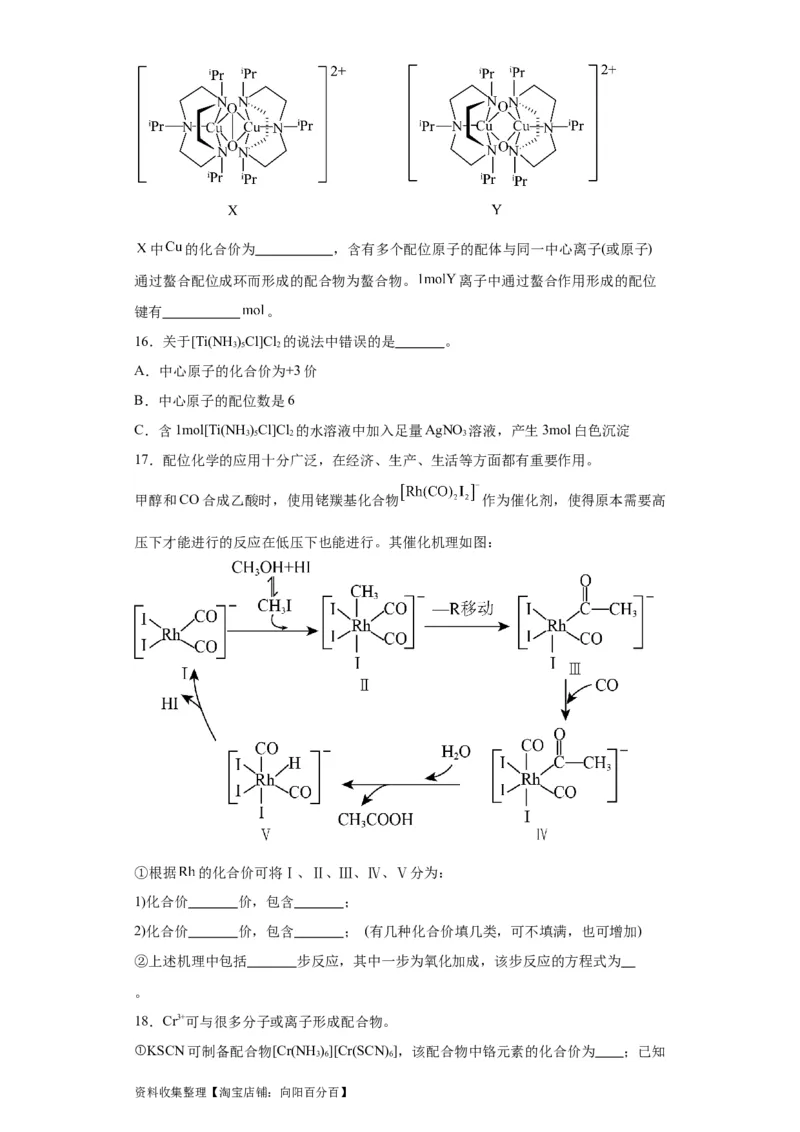
15. 人体内氧气的输送主要由红细胞内的血红蛋白负责,而红细胞以及血浆中还有少
量的血蓝蛋白也能和氧气反应。用配体 离子和氧气能合成类似血监蛋白的模型配
合物 ,该结构呈现出强烈的 键断裂趋势,成键形态 与断键形态
达成快速平衡。( 为异丙基)
资料收集整理【淘宝店铺:向阳百分百】中 的化合价为 ,含有多个配位原子的配体与同一中心离子(或原子)
通过螯合配位成环而形成的配合物为螯合物。 离子中通过螯合作用形成的配位
键有 。
16.关于[Ti(NH )Cl]Cl 的说法中错误的是 。
3 5 2
A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol[Ti(NH )Cl]Cl 的水溶液中加入足量AgNO 溶液,产生3mol白色沉淀
3 5 2 3
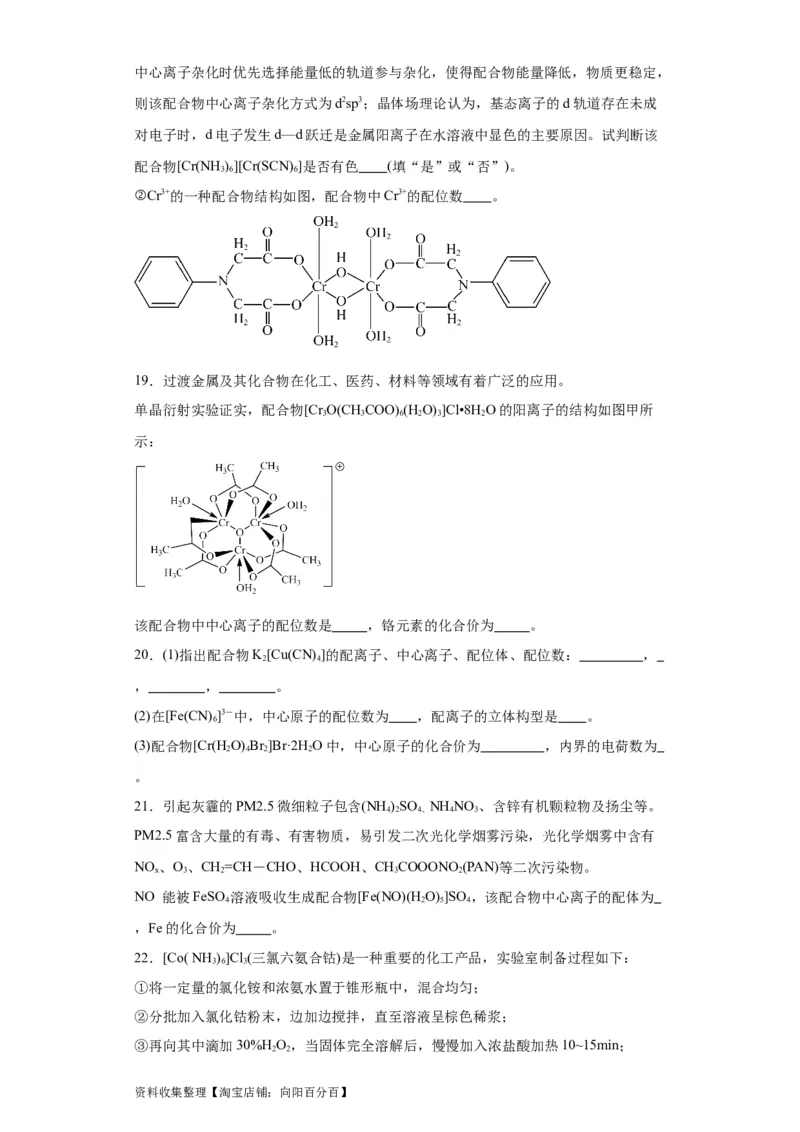
17.配位化学的应用十分广泛,在经济、生产、生活等方面都有重要作用。
甲醇和CO合成乙酸时,使用铑羰基化合物 作为催化剂,使得原本需要高
压下才能进行的反应在低压下也能进行。其催化机理如图:
①根据 的化合价可将Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ分为:
1)化合价 价,包含 ;
2)化合价 价,包含 ; (有几种化合价填几类,可不填满,也可增加)
②上述机理中包括 步反应,其中一步为氧化加成,该步反应的方程式为
。
18.Cr3+可与很多分子或离子形成配合物。
①KSCN可制备配合物[Cr(NH )][Cr(SCN) ],该配合物中铬元素的化合价为 ;已知
3 6 6
资料收集整理【淘宝店铺:向阳百分百】中心离子杂化时优先选择能量低的轨道参与杂化,使得配合物能量降低,物质更稳定,
则该配合物中心离子杂化方式为d2sp3;晶体场理论认为,基态离子的d轨道存在未成
对电子时,d电子发生d—d跃迁是金属阳离子在水溶液中显色的主要原因。试判断该
配合物[Cr(NH )][Cr(SCN) ]是否有色 (填“是”或“否”)。
3 6 6
②Cr3+的一种配合物结构如图,配合物中Cr3+的配位数 。
19.过渡金属及其化合物在化工、医药、材料等领域有着广泛的应用。
单晶衍射实验证实,配合物[CrO(CH COO) (H O) ]Cl•8H O的阳离子的结构如图甲所
3 3 6 2 3 2
示:
该配合物中中心离子的配位数是 ,铬元素的化合价为 。
20.(1)指出配合物K[Cu(CN) ]的配离子、中心离子、配位体、配位数: ,
2 4
, , 。
(2)在[Fe(CN) ]3-中,中心原子的配位数为 ,配离子的立体构型是 。
6
(3)配合物[Cr(H O) Br ]Br·2H O中,中心原子的化合价为 ,内界的电荷数为
2 4 2 2
。
21.引起灰霾的PM2.5微细粒子包含(NH )SO NH NO 、含锌有机颗粒物及扬尘等。
4 2 4、 4 3
PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有
NO 、O、CH=CH-CHO、HCOOH、CHCOOONO (PAN)等二次污染物。
x 3 2 3 2
NO 能被FeSO 溶液吸收生成配合物[Fe(NO)(H O) ]SO ,该配合物中心离子的配体为
4 2 5 4
,Fe的化合价为 。
22.[Co( NH)]Cl (三氯六氨合钴)是一种重要的化工产品,实验室制备过程如下:
3 6 3
①将一定量的氯化铵和浓氨水置于锥形瓶中,混合均匀;
②分批加入氯化钴粉末,边加边搅拌,直至溶液呈棕色稀浆;
③再向其中滴加30%H O,当固体完全溶解后,慢慢加入浓盐酸加热10~15min;
2 2
资料收集整理【淘宝店铺:向阳百分百】④在室温下冷却,过滤,可得到橙黄色[Co(NH )]Cl 晶体。
3 6 3
[ Co( NH )]Cl 中Co的化合价是 ,该配合物中心离子的核外电子排布式为
3 6 3
。
资料收集整理【淘宝店铺:向阳百分百】