文档内容
1.现有下列9种微粒: 、 、 、 、 、 、 、 、 。按要求完成以下各题:
(1) 、 、 分别是氢元素的一种____________,它们互称为____________。
(2)互为同素异形体的微粒是____________。
(3)对于 ,按下列要求各举一例(要求:每小题分别写出符合题意的两种粒子,且从以上所给微粒中
选择):
①Z、n、b相同而A不同:___________________________________________;
②A、n、b相同而Z不同:______________________________________;
③A、Z、b相同而n不同:________________________________________;
④Z、n、A相同而b不同:____________________________________________。
【错因分析】若对同位素、核素、同素异形体的概念理解错误,则容易出错。紧扣概念即可正确解答此类题目。
【参考答案】(1)核素 同位素
(2) 和
(3)① 、 (或 、 ) ② 、
③ 、 ④ 、(1)一种元素可能有多种核素,也可能只有一种核素。
(2)有多少种核素就有多少种原子。
(3)不同的核素可能具有相同的质子数,如 与 ;也可能具有相同的中子数,如 与 ;也可能具有
相同的质量数,如 与 ;也可能质子数、中子数、质量数均不相同,如 与 。
(4)在区别同位素、同素异形体的概念时,可从概念的字面加深理解。
同位素的研究对象是原子,“同位”是指同一种元素的几种核素在元素周期表中的位置相同,即质子数相同,
中子数不同;同素异形体的研究对象为单质,“同素”是指元素种类相同。
1.下列说法中正确的是
A.34S原子核内的中子数为16
B.1H和2H的化学性质相同
C.H16O与H18O互为同素异形体
2 2
D.Na和Na+属于同种元素,且性质相同
【答案】B
易错点2 混淆原子结构中的数量关系2.下列有关 的说法中正确的是
A. 与 互为同素异形体
B. 含有43个中子
C. 与 的物理性质、化学性质均相同
D. 的中子数比电子数多13
【错因分析】一些考生易混淆同位素和同素异形体的概念,错选A;一些考生不能根据质量数=质子数+中子数
来进行相应的换算,错选B;一些考生误认为同位素的物理性质和化学性质都是相同的,错选C。牢记符号
的含义(即A为质量数、Z为质子数)是求解的关键。学*科网
【 参 考 答 案 】 D
微粒之间的关系:
(1)质子数(Z)=核电荷数=核外电子数;
(2)质量数(A)=质子数(Z)+中子数(N);
(3)阳离子的核外电子数=质子数-阳离子所带的电荷数;
(4)阴离子的核外电子数=质子数+阴离子所带的电荷数。
规避4个易失分点
(1)任何微粒中,质量数=质子数+中子数,但质子数与电子数不一定相等,如阴、阳离子 中;(2)有质子的微粒不一定有中子,如1H,有质子的微粒不一定有电子,如H+;
(3)质子数相同的微粒不一定属于同一种元素,如F与OH-;
(4)核外电子数相同的微粒,其质子数不一定相同,如Al3+和Na+、F-等, 与OH-等。
2.已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则ω g R原子完全转化为R2-时,含有电子的物
质的量是
A. mol B. mol
C.ω( ) mol D.ω( ) mol
【答案】D
易错点3 混淆元素周期表中的一般规律与特殊性
3.元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是
A.短周期元素形成离子后,最外层电子都达到8电子稳定结构
B.所有主族元素的正化合价数等于它的族序数
C.第3、4、5、6周期元素的数目分别是8、18、32、32
D.第4周期由左至右第8、9、10三列中没有非金属元素
【错因分析】元素周期表的编排有一定的规律但也有一定的特殊性,若对元素周期表的结构不熟悉,对常见的
特殊性不能熟练掌握,容易因考虑不周全而失分。
【试题解析】短周期元素形成离子后,最外层不一定均达8电子稳定结构,例如氢离子和Li+等,故A错。氧、
氟没有正价,故B错。第3、4、5、6周期元素的数目分别是8、18、18、32,故C错。第4周期由左至右第8、9、10
三列中的元素分别为铁、钴、镍,全部为金属元素,故D正确。学*科网
【 参 考 答 案 】 D常见错误
(1)误认为主族元素的最高正价一定等于族序数。忽视了氧无最高正价,氟无正价。
(2)误认为元素的非金属性越强,其氧化物对应水化物的酸性就越强。但HClO、HSO 是弱酸,忽视了关键词
2 3
“最高价”。
(3)误认为失电子难的元素原子得电子的能力一定强。忽视了稀有气体元素原子失电子难、得电子也难。
(4)误认为得(失)电子的数目越多,元素的非金属性(金属性)越强。元素原子得失电子的数目与元素的非金
属性、金属性强弱没有必然联系。
(5)误认为同周期相邻两主族元素原子序数之差都等于1,忽视了长周期有相差11或25的情况。
(6)误认为最高正价和最低负价绝对值相等的元素只有第ⅣA族的某些元素。忽视了第ⅠA族中H的最高
正价为+1,最低负价为-1。
3.下列说法中正确的是
A.每一周期的元素都从碱金属开始,最后以稀有气体结束
B.同一周期中,从左到右,各元素最外层电子数都是从1个逐渐增加到8个
C.第二、三周期上下相邻元素的原子核外电子数相差8个
D.第七周期只有26种元素
【答案】C
易错点4 混淆“四量”的概念
4.230Th和232Th是钍的两种同位素,232Th可以转化成233U。下列有关Th的说法正确的是
A.Th元素的质量数是232 B.Th元素的相对原子质量是231
C.232Th转化成233U是化学变化 D.230Th和232Th的化学性质相同【错因分析】质量数是针对某一核素而言,若不清楚质量数的定义,易误选A;若不清楚相对原子质量的概念
和计算方法,易误选B。学*科网
【试题解析】质量数指的是核素中质子数与中子数之和,相同元素的不同核素的质量数不同,故不能说Th元
素的质量数为232,A错误;题中没有给出Th的各种核素的原子数百分比,所以无法计算出Th元素的相对原
子质量,B错误;化学变化的最小微粒是原子,在化学变化中原子不发生改变,但232Th转化成233U,原子发生
了变化,C错误;同位素的物理性质不同,但化学性质相同,D正确。
【 参 考 答 案 】 D
“四量”的比较
类别 定义 实例
原子质量 某元素某种核素的一个原子的真实质 一个 原子的质量是
量
2.657×10−26 kg
原子的相对原子质量 一个原子的质量与一个 原子质量 的相对原子质量约为16
的 的比值
元素的相对原子质量 元素的各种天然同位素的相对原子质 A=A(A)·a%+A(B)·b%+…
r r r
量与其在自然界中所占的原子个数百 (其中a%+b%+…=1)
分比(或称丰度)算出的平均值
质量数 某原子核内质子数与中子数之和 的质量数为18
4.在元素周期表中,一个"格子"就表示了一种元素,这个格子承载着大量的信息,如图所示是元素周期表中
表示铁元素的"格子"。由此判断,下列说法不正确的是
A.由图示可知该元素的核外电子数
B.由图示可知该元素属于金属元素还是非金属元素
C.由图示可知该元素原子的电子层数
D.由图示可知该元素的相对原子质量【答案】C
偏旁部首可确定该元素属于金属元素还是非金属元素,选项B正确;由图示中的信息无法确定该元素原子的
电子层数,选项C错误。
易错点5 不能熟记原子序数与元素在周期表中的位置关系
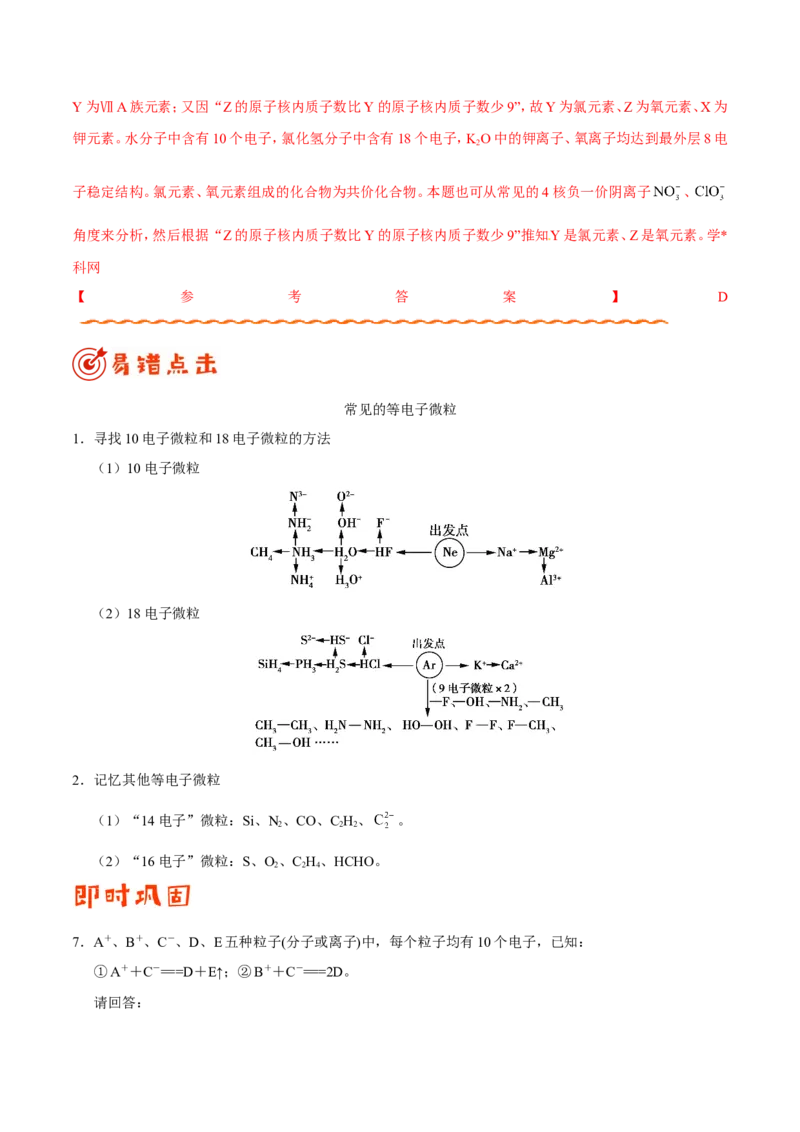
5.已知X、Y、Z三种主族元素在元素周期表中的位置如图所示,设X的原子序数为a。则下列说法不正确的是
A.Y与Z的原子序数之和可能为2a
B.Y的原子序数可能为a-17
C.Z的原子序数可能为a+31
D.X、Y、Z一定为短周期元素
【错因分析】根据原子序数可以推断元素在周期表中的位置,根据元素在周期表中的位置可以推断元素之间
可能的原子序数关系,若不熟记二者之间的关系,则相关问题的解决会变得更复杂。
【 参 考 答 案 】 D
原子序数与元素在周期表中的位置关系
1.同周期主族元素原子序数差的关系
(1)短周期元素原子序数差=族序数差;(2)两元素分布在过渡元素同侧时,原子序数差=族序数差。两元素分布在过渡元素两侧时,第四或第五
周期元素原子序数差=族序数差+10,第六周期元素原子序数差=族序数差+24;
(3)第四、第五周期的第ⅡA与第ⅢA族原子序数之差都为11,第六、第七周期的第ⅡA与第ⅢA族原子
序数之差都为25。
2.同主族、邻周期元素的原子序数差的关系
(1)第ⅠA族元素随电子层数的增加,原子序数依次相差2、8、8、18、18、32;
(2)第ⅡA族和0族元素随电子层数的增加,原子序数依次相差8、8、18、18、32;
(3)第ⅢA族~第ⅦA族元素随电子层数的增加,原子序数依次相差8、18、18、32。
3.根据原子序数确定元素在元素周期表中的位置
(1)熟记每周期中稀有气体元素的原子序数
周期数 1 2 3 4 5 6 7
0族元素原子序数 2 10 18 36 54 85 118(若填满)
(2)比大小定周期
比较该元素的原子序数与0族元素原子序数的大小,找出与其相近的0族元素,那么该元素就和原子序数
大的0族元素处于同一周期。
(3)求差值定族数
①若某元素的原子序数比相应0族元素多1或2,则该元素应位于0族元素所在周期的下一个周期的第Ⅰ
A族或第ⅡA族。
②若比相应0族元素的原子序数少1~5时,则该元素应位于同周期的第ⅦA~ⅢA族。
③若差值为其他数,则由相应差数找出相应的族。
(4)实例
①53号元素
由于36<53<54,则53号元素位于第五周期,54−53=1,则53号元素位于54号元素左侧第一格,即第ⅦA
族,所以53号元素位于第五周期第ⅦA族。
②88号元素
由于86<88<118,则88号元素位于第七周期,88−86=2,则88号元素位于第七周期的第二格,即第ⅡA族,
所以88号元素位于第七周期第ⅡA族。
5.原子序数为x的元素R。在周期表中位于A、B、C、D 4种元素的中间。A、B、C、D 4种元素的原子序数之和
不可能为A.4x B.4x+10 C.4x+5 D.4x+14
【答案】C
6.下列各图若为元素周期表的一部分(表中数字代表原子序数),其中合理的是
【答案】D
【解析】解题时可根据稀有气体2号、10号元素应在周期表的最右端和3号元素在周期表的最左端排除A、
B、C三项。学*科网
易错点6 不能熟练运用等电子微粒推断
6.设X、Y、Z代表元素周期表中前4周期中的三种元素,已知X+和Y-具有相同的电子层结构;Z的原子核内
质子数比Y的原子核内质子数少9;Y和Z可形成含4个原子核、42个电子的负一价阴离子。
下列说法不正确的是
A.Z的气态氢化物分子中含有10个电子
B.Y的气态氢化物分子中含有18个电子
C.Z与元素X形成的化合物XZ中离子都达到稳定结构
2
D.Y、Z组成的化合物属于离子化合物
【错因分析】如果不能厘清离子中的电荷关系:阴离子所带电荷数=核外电子数-核内质子数,阳离子所带电荷
数=核内质子数-核外电子数并牢记常见的10电子和18电子微粒,则易导致错选A、B。
【试题解析】由“X+和Y-具有相同的电子层结构”知X+和Y-的最外层都是8电子,不难推知X为ⅠA族元素、Y为ⅦA族元素;又因“Z的原子核内质子数比Y的原子核内质子数少9”,故Y为氯元素、Z为氧元素、X为
钾元素。水分子中含有10个电子,氯化氢分子中含有18个电子,KO中的钾离子、氧离子均达到最外层8电
2
子稳定结构。氯元素、氧元素组成的化合物为共价化合物。本题也可从常见的4核负一价阴离子 、
角度来分析,然后根据“Z的原子核内质子数比Y的原子核内质子数少9”推知Y是氯元素、Z是氧元素。学*
科网
【 参 考 答 案 】 D
常见的等电子微粒
1.寻找10电子微粒和18电子微粒的方法
(1)10电子微粒
(2)18电子微粒
2.记忆其他等电子微粒
(1)“14电子”微粒:Si、N、CO、C H、 。
2 2 2
(2)“16电子”微粒:S、O、C H、HCHO。
2 2 4
7.A+、B+、C-、D、E五种粒子(分子或离子)中,每个粒子均有10个电子,已知:
①A++C-===D+E↑;②B++C-===2D。
请回答:(1)C-离子的电子式是________________。
(2)A+离子中的键角为______________。
(3)分别写出A+和D反应、B+和E反应的离子方程式____________、____________。
(4)除D、E外,请再写出两种含10个电子的分子的分子式____________。
(5)除A+、B+外,请再写出两种含10个电子的阳离子________。
【答案】(1) (2)109.5°
(3) +HO NH ·H O+H+ HO++NH === +HO (4)CH、Ne(答案合理即可)
2 3 2 3 3 2 4
(5)Na+、Mg2+(答案合理即可)
易错点7 忽视元素周期表结构和元素性质的特殊性
7.短周期元素W、X、Y、Z的原子序数依次增大。其中W的阴离子的核外电子数与X、Y、Z原子的核外内层
电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产
Y的单质,而Z不能形成双原子分子。根据以上叙述,下列说法中正确的是
A.上述四种元素的原子半径大小为WHI>HBr>HCl,HO>HSe>H S,
2 2 2
NH >AsH >PH。
3 3 3
4.电子层结构相同的微粒的位置特征。阴离子在具有相同电子层结构的稀有气体元素的前面,阳离子在具有
相同电子层结构的稀有气体元素的下一周期的左边。
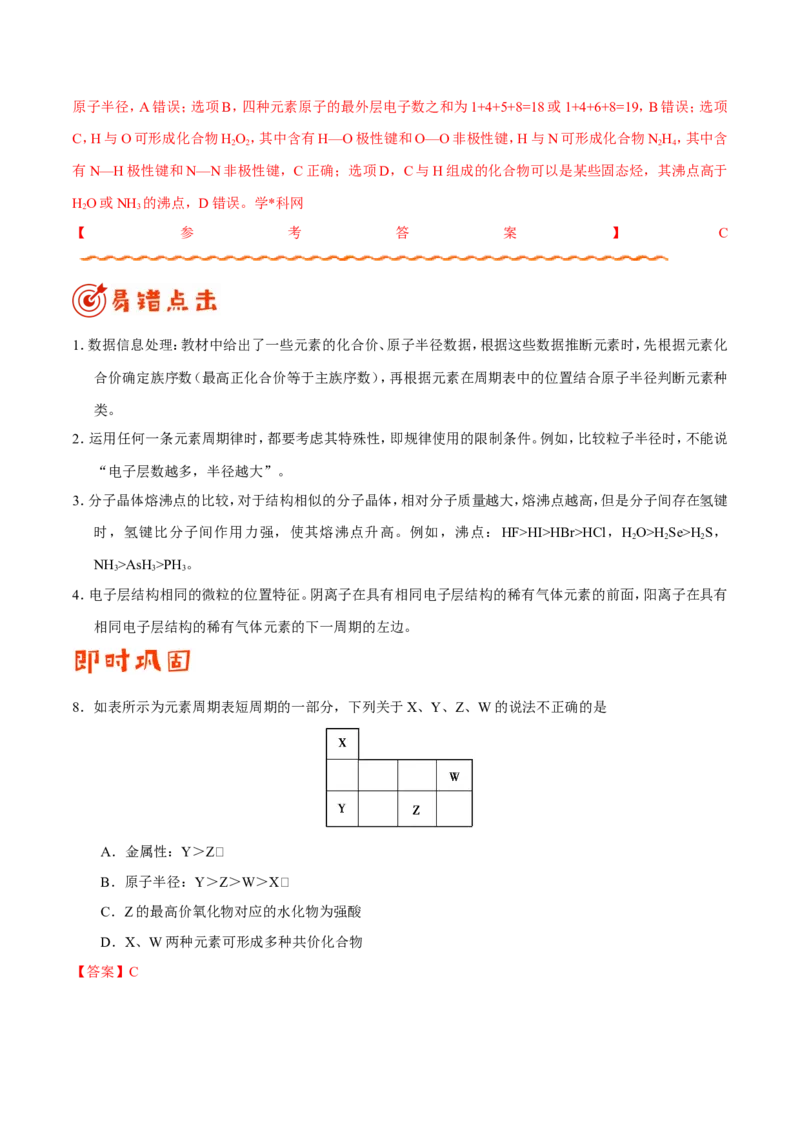
8.如表所示为元素周期表短周期的一部分,下列关于X、Y、Z、W的说法不正确的是
A.金属性:Y>Z
B.原子半径:Y>Z>W>X
C.Z的最高价氧化物对应的水化物为强酸
D.X、W两种元素可形成多种共价化合物
【答案】C为Al(OH) ,C错误。
3
易错点8 不能熟练运用元素周期律进行元素推断
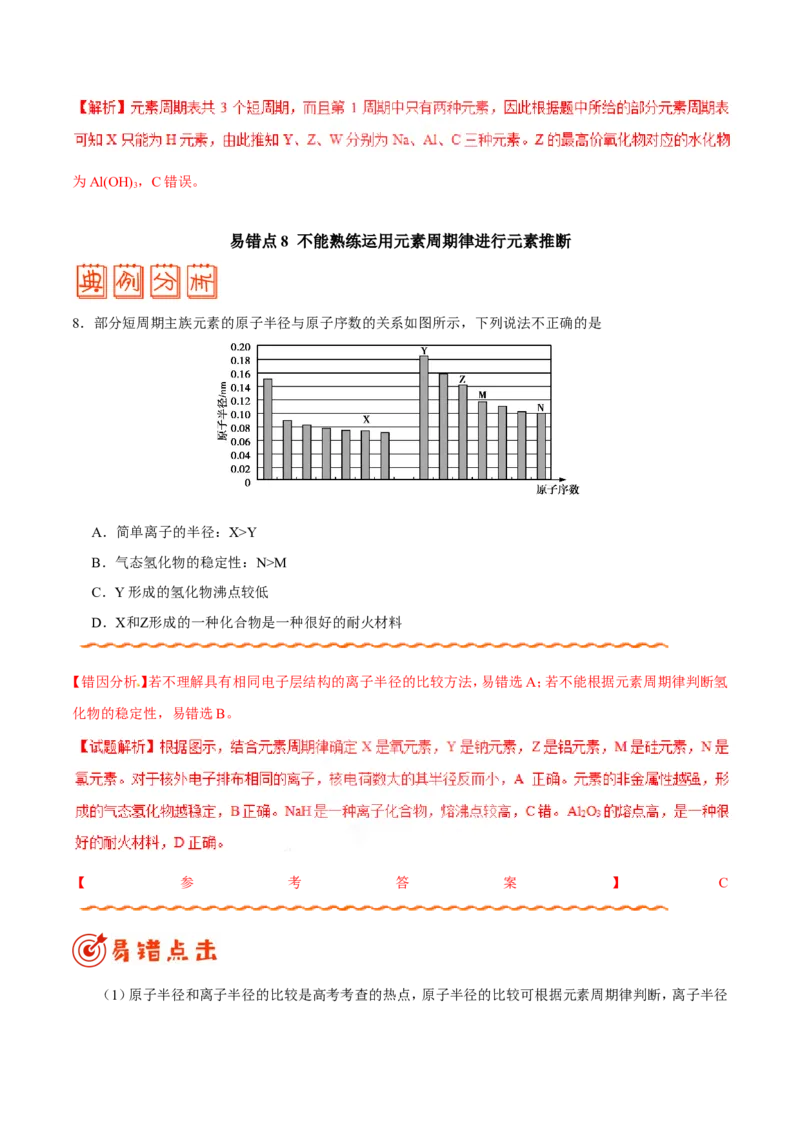
8.部分短周期主族元素的原子半径与原子序数的关系如图所示,下列说法不正确的是
A.简单离子的半径:X>Y
B.气态氢化物的稳定性:N>M
C.Y形成的氢化物沸点较低
D.X和Z形成的一种化合物是一种很好的耐火材料
【错因分析】若不理解具有相同电子层结构的离子半径的比较方法,易错选A;若不能根据元素周期律判断氢
化物的稳定性,易错选B。
【 参 考 答 案 】 C
(1)原子半径和离子半径的比较是高考考查的热点,原子半径的比较可根据元素周期律判断,离子半径比较中要注意:①核外电子排布相同的离子,核电荷数大的半径反而小;②第3周期元素形成的简单金属离
子中Al3+的半径最小。
(2)注意元素周期律的“共性”与“个性”
在运用元素周期律推断元素性质时,既要关注元素共性,又要注意元素个性。同主族元素中,某元素的性
质与同族其他元素性质差别较大,例如,氟的性质与氯、溴、碘的性质差别较大;锂的一些性质不同于钠、钾
的性质。同主族元素,相邻元素的性质相似程度大些,例如氮、磷、砷,砷的性质与磷的相似程度大些,砷酸的
化学式是HAsO ,而不是HNO 的形式。
3 4 3
9.短周期元素X、Y、Z、W,它们的原子序数依次增大。X与Z同主族,并且原子序数之和为20。Y原子的质子
数为Z原子的质子数的一半,W原子的最外层电子数比Y原子的最外层电子数多2个。下列叙述正确的
是
A.Y的最高价氧化物对应的水化物可与其气态氢化物发生化合反应
B.原子半径Z>W>Y>X
C.气态氢化物的稳定性Z>W
D.X的气态氢化物与足量W单质在光照条件下反应生成物均为气体
【答案】A
易错点9 不能熟练进行元素“位-构-性”的综合推断
9.现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A、D同主族,C与E同主族,D、E、F同
周期,A、B原子的最外层电子数之和与C原子的最外层电子数相等,A能分别与B、C形成电子总数相等
的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气态分子。
试回答下列问题:
(1)E、F的气态氢化物的稳定性为___________>___________(填化学式)。(2)E与F可形成EF 的化合物,其化学式为___________。
2 2
(3)C、D形成的一种化合物能与D、E形成的化合物在溶液中发生氧化还原反应,其离子方程式为
_________________________________。
(4)A、C、E三种元素形成的一种常见化合物H,其浓溶液在加热条件下可与a g铜反应,则被还原的H的
物质的量为___________。
【错因分析】题目给出了六种元素,首先要根据这些元素在周期表中的相对位置和结构特点,正确推断出它们
为何种元素。推断时要抓住关键信息,大胆猜测,采用逐一验证的方法进行推断。若不能推断出各元素,则无
法解答所给问题。学*科网
【参考答案】(1)HCl HS (2)SCl (3)NaO+S2-+2H O S↓+2Na++4OH−
2 2 2 2 2 2
( 4 ) a/64 mol
根据原子结构、元素周期表的知识及相关已知条件,可推算原子序数,判断元素在元素周期表中的位置等,基
本思路如图所示:1.由主族元素在元素周期表中的位置推断
(1)牢记元素周期表的结构(能区分长短周期、主副族、每周期的元素种数等)是求解的基础,一定要“心中
有表”。
(2)几个重要关系式
①原子核外电子层数=周期数;
②主族序数=最外层电子数=最高正价=8-|最低负价|;
③|最高正价|-|最低负价|=0、2、4、6的主族序数依次为第Ⅳ族、第Ⅴ族、第Ⅵ族、第Ⅶ族。
(3)熟悉主族元素在元素周期表中的特殊位置
①族序数等于周期数的元素:H、Be、Al。
②族序数等于周期数2倍的元素:C、S。
③族序数等于周期数3倍的元素:O。
④周期数是族序数2倍的元素:Li、Ca。
⑤周期数是族序数3倍的元素:Na、Ba。
⑥最高正价与最低负价代数和为零的短周期元素:H、C、Si。
⑦最高正价是最低负价绝对值3倍的短周期元素:S。
⑧除H外,原子半径最小的元素:F。
⑨最高正价不等于族序数的短周期元素:O(F无正价)。
2.由元素原子的核外电子排布推断
(1)最外层有1个电子的元素:H、Li、Na、K。
(2)最外层电子数等于次外层电子数的元素:Be、Ar。
(3)最外层电子数是次外层电子数2倍的元素:C;最外层电子数是次外层电子数3倍的元素:O;最外层
电子数是次外层电子数4倍的元素:Ne。
(4)最外层电子数是内层电子数总数一半的元素:Li、P。
(5)次外层电子数是最外层电子数2倍的元素:Li、Si。
(6)次外层电子数是其他各层电子总数2倍的元素:Li、Mg。
(7)次外层电子数与其他各层电子总数相等的元素:Be、S。
(8)电子层数与最外层电子数相等的元素:H、Be、Al。
3.由元素及其化合物的特性推断
(1)形成化合物种类最多的元素或单质是自然界中硬度最大的物质的元素或气态氢化物中氢的质量分数
最大的元素:C。
(2)空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素:N。(3)地壳中含量最多的元素或同周期中气态氢化物的沸点最高的元素或氢化物在通常情况下呈液态的元
素:O。
(4)地壳中含量最多的金属元素:Al。
(5)最高价氧化物及其对应的水化物既能与强酸反应,又能与强碱反应的元素:Be、Al。
(6)最活泼的非金属元素或无正价的元素或无含氧酸的非金属元素或无氧酸(气态氢化物)可腐蚀玻璃的
元素或气态氢化物最稳定的元素或阴离子的还原性最弱的元素:F。
(7)最活泼的金属元素或最高价氧化物对应的水化物碱性最强的元素或阳离子的氧化性最弱的元素:Cs。
(8)常温下单质最易着火的元素:P。
(9)焰色反应呈黄色的元素:Na。
(10)焰色反应呈紫色(透过蓝色钴玻璃观察)的元素:K。
(11)单质密度最小的元素:H;密度最小的金属元素:Li。
(12)常温下单质呈液态的非金属元素:Br;金属元素:Hg。
(13)元素的气态氢化物和它的最高价氧化物对应的水化物起化合反应的元素:N;能起氧化还原反应的元
素:S。
(14)元素的气态氢化物能与它的氧化物在常温下反应生成该元素单质的元素:S。
(15)元素的单质在常温下能与水反应放出气体的短周期元素:Li、Na、F。
(16)常见的能形成同素异形体的元素:C、P、O、S,其中一种同素异形体易着火的元素:P。
4.“位”、“构”、“性”规律中的特例:
(1) 中无中子。
(2)元素周期表中每一个周期一般都是从金属元素开始,但第一周期从氢元素开始。
(3)大多数元素在自然界中都有稳定的同位素,但Na、F、P、Al等20种元素未发现稳定的同位素。
(4)元素的原子序数大,相对原子质量不一定大,如 Ar的相对原子质量为39.95大于 K的39.10。
18 19
(5)一般元素性质越活泼,其单质性质也越活泼,但N与P相反,N的非金属性强于P的,但N 比白磷、红
2
磷稳定得多。
10.A、B、C、D、E是元素周期表中前20号元素,原子序数依次增大,A是地壳中含量最高的元素,B、C、D同
周期,E和其他元素既不在同周期也不在同主族,D的氢化物和最高价氧化物对应的水化物均为强酸,且
B、C、D的最高价氧化物对应的水化物两两混合均能发生反应生成盐和水,A、D、E可以形成多种盐,其
中一种盐中A、D、E三种元素的原子个数比为2∶2∶1。据此回答下列问题:
(1)A和D的氢化物中,沸点较低的是__________________ (填“A”或“D”)。
(2)元素C在元素周期表中的位置是__________________,B的最高价氧化物对应的水化物的电子式为
__________________。
(3)由A、D、E形成的原子个数比为2∶2∶1的盐的名称为__________________。它的水溶液与D的氢化
物的水溶液反应可生成D的单质,该反应的离子方程式为____________________________。
【答案】(1)D (2)第三周期第ⅢA族
(3)次氯酸钙 ClO-+2H++Cl- Cl↑+HO
2 2
易错点10 化学键与物质类别关系判断错误
10.下列说法正确的是
A.共价化合物中可能含有离子键
B.区别离子化合物和共价化合物的方法是看其水溶液是否能够导电
C.离子化合物中只含有离子键
D.离子化合物在熔融状态下能电离出自由移动的离子,而共价化合物不能
【错因分析】解答本题需明确以下两点:(1)共价化合物只有共价键,若含有离子键,此化合物肯定是离子化
合物;(2)某些共价化合物溶于水也能电离,如HCl、HSO 等,不能根据其溶于水是否导电来判断其是不是
2 4
离子化合物。不能掌握化学键与物质类别的关系和常见典型化合物,容易分析不全面而出错。
【试题解析】A项,共价化合物中只含有共价键,错误;B项,区别离子化合物和共价化合物要看其在熔融状态
下能否导电,而不能根据其溶于水是否导电来判断;C项,离子化合物中一定含有离子键,可能含有共价键,
如NaOH、NH NO 等。学*科网
4 3
【 参 考 答 案 】 D1.化学键与化学反应
旧化学键的断裂和新化学键的形成是化学反应的本质,是反应中能量变化的根本。
2.物质的溶解或熔化与化学键变化
(1)离子化合物的溶解或熔化过程
离子化合物溶于水或熔化后均电离成自由移动的阴、阳离子,离子键被破坏。
(2)共价化合物的溶解过程
①有些共价化合物溶于水后,能与水反应,其分子内共价键被破坏,如CO 和SO 等。
2 2
②有些共价化合物溶于水后,与水分子作用形成水合离子,从而发生电离,形成阴、阳离子,其分子内的共
价键被破坏,如HCl、HSO 等。
2 4
③某些共价化合物溶于水后,其分子内的共价键不被破坏,如蔗糖(C H O )、酒精(C HOH)等。
12 22 11 2 5
(3)单质的溶解过程
某些活泼的非金属单质溶于水后,能与水反应,其分子内的共价键被破坏,如Cl、F 等。
2 2
3.化学键与物质类型的关系
(1)离子化合物中一定含有离子键,可能含有共价键。简单离子组成的离子化合物中只有离子键,如MgO、
NaCl等;复杂离子(原子团)组成的离子化合物中既有离子键,又有共价键,如(NH )SO 、NH NO 、NaOH、
4 2 4 4 3
NaO 等。
2 2
(2)共价化合物中只有共价键,一定没有离子键。
(3)在非金属单质中只有共价键,如Cl、O 等。
2 2
(4)稀有气体是单原子分子,不存在化学键。
化学键与物质的类别
除稀有气体内部无化学键外,其他物质内部都存在化学键。化学键与物质的类别之间的关系可概括如下:
(1)只含有极性共价键的物质一般是不同种非金属元素形成的共价化合物,如SiO、HCl、CH 等。
2 4
(2)只含有非极性共价键的物质是同种非金属元素形成的单质,如Cl、P、金刚石等。
2 4
(3)既有极性键又有非极性键的共价化合物一般由多个原子组成,如HO、C H 等。
2 2 2 4
(4)只含离子键的物质主要是由活泼非金属元素与活泼金属元素形成的化合物,如NaS、CaCl 、NaCl等。
2 2
(5)既有离子键又有极性共价键的物质,如NaOH、KSO 等;既有离子键又有非极性共价键的物质,如
2 4NaO 等。
2 2 [来源:学科网]
(6)仅由非金属元素形成的离子化合物,如NH Cl、NH NO 等。
4 4 3
(7)金属元素和非金属元素间可能存在共价键,如AlCl 等。
3
11.下列有关化学键的叙述,正确的是
A.离子化合物中一定含有离子键
B.单质分子中均不存在化学键
C.氯化氢和氯化钾溶解时破坏的化学键相同
D.含有共价键的化合物一定是共价化合物
【答案】A
1.原子的结构
(1)原子的组成
(2)原子的表示方法
(3)构成原子或离子的微粒间的数量关系
质子数(Z)+中子数(N)=质量数(A)=原子的近似相对原子质量(质量关系)原子的核外电子数=核内质子数=核电荷数=原子序数
阳离子的核外电子数=核内质子数-阳离子所带电荷数
阴离子的核外电子数=核内质子数+阴离子所带电荷数
2.元素周期表
(1)结构
①周期(7个横行,7个周期):
短周期 长周期
序号 1 2 3 4 5 6 7
元素种数 2 8 8 18 18 32 32(若排满)
0族元素
2 10 18 36 54 86 118(若排满)
原子序数
②族(18个纵行,16个族)
列 1 2 13 14 15 16 17
主族
[来源:Z#xx#k.Com] [来源:Z+xx+k.Com] [来源:学科网]
族 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
列 3 4 5 6 7 11 12
副族
族 ⅢB ⅣB ⅤB ⅥB ⅦB ⅠB ⅡB
Ⅷ族 第 8、9、10,共3个纵行
0族 第 18纵行
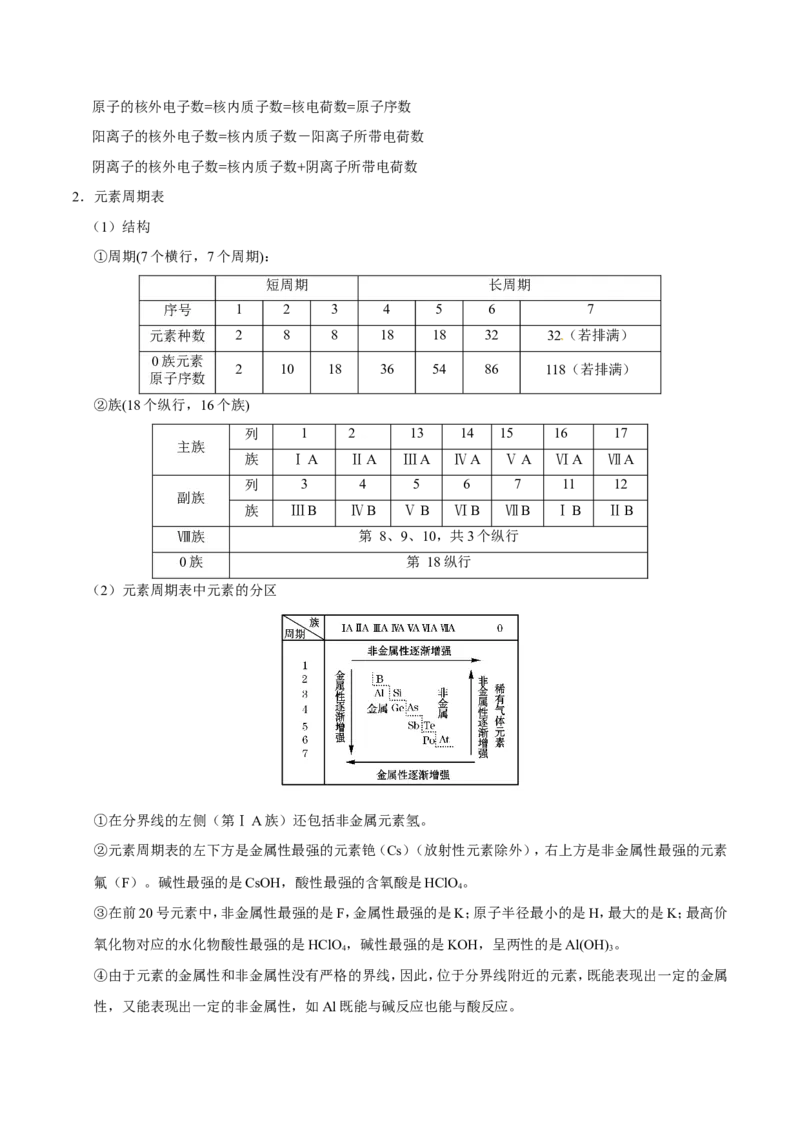
(2)元素周期表中元素的分区
①在分界线的左侧(第ⅠA族)还包括非金属元素氢。
②元素周期表的左下方是金属性最强的元素铯(Cs)(放射性元素除外),右上方是非金属性最强的元素
氟(F)。碱性最强的是CsOH,酸性最强的含氧酸是HClO。
4
③在前20号元素中,非金属性最强的是F,金属性最强的是K;原子半径最小的是H,最大的是K;最高价
氧化物对应的水化物酸性最强的是HClO,碱性最强的是KOH,呈两性的是Al(OH) 。
4 3
④由于元素的金属性和非金属性没有严格的界线,因此,位于分界线附近的元素,既能表现出一定的金属
性,又能表现出一定的非金属性,如Al既能与碱反应也能与酸反应。(3)元素周期表所包含的规律
①电子排布规律
a.最外层电子数等于或大于3且小于8的一定是主族元素。
b.最外层有1个或2个电子,则可能是第ⅠA族、ⅡA族元素,也可能是副族元素、第Ⅷ族元素或0族
元素氦。
c.最外层电子数比次外层电子数多的短周期元素一定位于第二周期。
d.某元素阴离子的最外层电子数与次外层电子数相同,该元素位于第三周期。
e.电子层结构相同的离子,若电性相同,则对应的元素位于同周期;若电性不同,则阳离子对应的元素位
于阴离子对应的元素的下一周期。
②元素化合价的规律
a.主族元素的最高正价等于主族序数,等于主族元素原子的最外层电子数(氧、氟除外)。非金属元素除
氢外,均不能形成简单阳离子,金属元素不能形成简单阴离子。
b.最高正价与最低负价的绝对值之和为8,绝对值之差为0、2、4、6的主族元素依次位于第ⅣA、ⅤA、
ⅥA、ⅦA族。
c.非金属元素的正价一般相差2,如氯元素正化合价有+7、+5、+3、+1等;某些金属元素也符合此规律,
如锡元素正化合价有+4、+2。
③相似规律
a.周期表中位于对角线位置的元素性质相似,如Li 和Mg、Be和Al等。
b.同主族元素性质相似,如C和Si、O和S等。
c.同周期相邻元素性质差别不大。
3.元素周期律
(1)具体表现形式
项目 同周期(左→右) 同主族(上→下)
原子 核电荷数 逐渐增大 逐渐增大
结构
电子层数 相同 逐渐增多
原子半径 逐渐减小 逐渐增大
阳离子逐渐减小
离子半径 逐渐增大
阴离子逐渐减小
最高正化合价由+1→+
性质 化合价
7(O、F除外) 相同最高正化合价=主
族序数(O、F除外)
负化合价=-(8-主族序数)元素的金属 金属性逐渐减弱 金属性逐渐增强
性和非金属
性 非金属性逐渐增强 非金属性逐渐减弱
离子的氧化 阳离子氧化性逐渐增强阴离 阳离子氧化性逐渐减弱
性、还原性 子还原性逐渐减弱 阴离子还原性逐渐增强
气态氢化物
逐渐增强 逐渐减弱
稳定性
最高价氧化
物对应的水 碱性逐渐减弱 碱性逐渐增强
化物的酸碱 酸性逐渐增强 酸性逐渐减弱
性
(2)元素金属性强弱的比较
①结构比较法:最外层电子数越少,电子层数越多,元素金属性越强。
②
③实验比较法
最高价氧化物对应水化物碱性强弱比较:碱性强,对应元素金属性强。
与水、酸反应的难易或剧烈程度:越易反应或反应越剧烈,对应元素金属性越强。
单质的还原性强弱:还原性越强,对应元素的金属性越强。
阳离子氧化性的强弱:氧化性越弱,对应元素的金属性越强。
单质与同一物质反应的难易程度:越易进行反应,对应元素的金属性越强。
原电池正负极:一般来说,作负极的金属对应元素的金属性强。
(3)元素非金属性强弱的比较
①结构比较法:最外层电子数越多,电子层数越少,非金属性越强。
②
③实验比较法
最高价氧化物对应水化物酸性强弱比较:酸性强的对应元素非金属性强。
与H 反应的难易或剧烈程度:越易反应或反应越剧烈,对应元素非金属性越强。
2
单质的氧化性强弱:氧化性越强,对应元素的非金属性越强。
简单阴离子的还原性强弱:还原性越弱,对应元素的非金属性越强。
单质与同一物质反应的难易程度:越易进行反应,对应元素的非金属性越强。
置换反应:非金属性较强的元素单质能置换出非金属性较弱的元素单质。4.元素“位-构-性”之间的关系
(1)元素“位-构-性”三者之间的关系
(2)元素“位-构-性”三者关系的应用
利用元素的原子结构、元素在元素周期表中的位置及元素性质三者的关系,可以比较或推断某些元素的
性质,如:
①比较同主族元素的金属性、非金属性、最高价氧化物对应水化物的酸性或碱性、气态氢化物的稳定性等。
②比较同周期元素及其化合物的性质。
③比较不同周期、不同主族元素的性质时,要找出参照物。
④推断一些相对较陌生的元素的某些性质。
1.[2017北京]2016年IUPAC命名117号元素为Ts(中文名“ ”,tián),Ts的原子核外最外层电子数是7。
下列说法不正确的是
A.Ts是第七周期第ⅦA族元素 B.Ts的同位素原子具有相同的电子数
C.Ts在同族元素中非金属性最弱 D.中子数为176的Ts核素符号是
【答案】D
【名师点睛】明确元素周期表的结构以及编制原则是解答的关键,元素周期表每一周期元素种类依次为2、8、
8、18、18、32、32(周期表未排满),则每一周期最后一种惰性气体原子序数依次为2、10、18、36、54、86、118,因此只要记住了稀有气体元素的原子序数,就可由主族元素的原子序数推出主族元素的位置。即(1)若比相
应的稀有气体元素多1或2,则应处在下周期的第ⅠA族或第ⅡA族,如88号元素:88-86=2,则应在第七
周期第ⅡA族;(2)若比相应的稀有气体元素少1~5时,则应处在同周期的第ⅦA族~第ⅢA族,如84号
元素应在第六周期第ⅥA族;(3)若预测新元素,可与未发现的稀有气体元素(118号)比较,按上述方法推测
知:117号元素应为第七周期第ⅦA族。学*科网
2.[2017江苏]短周期主族元素X、Y、Z、W原子序数依次增大,其中只有Y、Z处于同一周期且相邻,Z是地壳
中含量最多的元素,W是短周期中金属性最强的元素。下列说法正确的是
A.原子半径:r(X) < r(Y) < r(Z) < r(W)
B.W的最高价氧化物的水化物是一种弱碱
C.Y的单质的氧化性比Z的强
D.X、Y、Z 三种元素可以组成共价化合物和离子化合物
【答案】D
3.[2017天津]根据元素周期表和元素周期律,判断下列叙述不正确的是
A.气态氢化物的稳定性:HO>NH >SiH
2 3 4
B.氢元素与其他元素可形成共价化合物或离子化合物
C.图1所示实验可证明元素的非金属性:Cl>C>SiD.用中文“ ”(ào)命名的第118号元素在周期表中位于第七周期0族
【答案】C
【解析】A、气态氢化物稳定性与非金属性一致,非金属性O>N>Si,所以气态氢化物稳定性HO>NH >
2 3
SiH,A正确;B、氢元素可与非金属元素形成共价化合物如HO等,也可以与某些金属生成离子化合物如
4 2
NaH等,B正确;C、不能用氢化物的酸性来验证非金属性强弱,可以采用最高价含氧酸酸性强弱来验证,C错
误;D、根据元素周期表知识判断,各周期0族元素的原子序数依次为2、10、18、36、54、86、118,所以第118
号元素在周期表中位于第七周期0族,D正确。故选C。
考点:元素周期表、元素周期律
【名师点睛】熟练应用元素周期律是准确解题的核心。A、C两项元素的非金属性可以用氢化物的稳定性,最
高价氧化物对应水化物的酸性,相互置换能力等来判断。B项则涉及到离子化合物、共价化合物的判断,可以
根据组成元素来判断。
4.[2017新课标Ⅰ]短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原
子半径是所有短周期主族元素中最大的。由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有
黄色沉淀析出,同时有刺激性气体产生。下列说法不正确的是
A.X的简单氢化物的热稳定性比W强
B.Y的简单离子与X的具有相同的电子层结构
C.Y与Z形成化合物的水溶液可使蓝色石蕊试纸变红
D.Z与X属于同一主族,与Y属于同一周期
【答案】C5.[2017新课标Ⅱ]a、b、c、d为原子序数依次增大的短周期主族元素,a原子核外电子总数与b原子次外层
的电子数相同;c所在周期数与族数相同;d与a同族。下列叙述正确的是
A.原子半径:d>c>b>a B.4种元素中b的金属性最强
C.c的氧化物的水化物是强碱 D.d单质的氧化性比a单质的氧化性强
【答案】B
【名师点睛】本题考查元素周期表和元素周期律的知识,首先根据题目信息判断出元素名称,再根据元素周期
律进行知识的判断,这就需要掌握(非)金属性的强弱、微粒半径的大小比较等知识,因此平时夯实基础知识
是关键,同时应注意知识的灵活运用,审清题意。元素周期表、元素周期律是学习化学的工具和基本规律。元
素周期表反映了元素的原子结构、元素的性质及相互转化关系的规律,是根据元素周期律的具体表现形式,
元素周期律是元素周期表排布的依据。元素的原子半径、元素的化合价、元素的金属性、非金属性、原子核外电子排布都随着原子序数的递增而呈周期性的变化。同一周期的元素原子核外电子层数相同,从左到右原子
序数逐渐增大;同一主族的元素,原子最外层电子数相同,从上到下原子核外电子层数逐渐增大。原子核外电
子排布的周期性变化是元素周期律变化的原因,掌握元素的单质及化合物的结构、物质的物理性质、化学性
质等是进行元素及化合物推断的关键。
6.[2016江苏]短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的
非金属性最强的元素,在周期表中Z位于ⅠA族,W与X属于同一主族。下列说法正确的是
A.元素X、W的简单阴离子具有相同的电子层结构
B.由Y、Z两种元素组成的化合物是离子化合物
C.W的简单气态氢化物的热稳定性比Y的强
D.原子半径:r(X)<r(Y)<r(Z)<r(W)
【答案】B
【解析】短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,X为氧元素或S,由于
X的原子序数最小,则X是O;Y是迄今发现的非金属性最强的元素,Y为氟元素;在周期表中Z位于ⅠA族,
Z为钠元素;W与X属于同一主族,W为硫元素。A、O2-有2个电子层,电子数分别为2、8,S2-有3个电子层,
电子数分别为2、8、8,A错误;B、钠和氟均是活泼的金属和活泼的非金属,二者形成的化合物NaF为离子化
合物,B正确;C、非金属性:F>S,非金属性越强,氢化物越稳定,则热稳定性:HF>HS,C错误;D、同周期
2
自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则原子半径:r(F)<r(O)<r(S)<r
(Na),D错误。答案选B。学*科网
7.[2016浙江]短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数是其电子层数的2
倍,X、Y的核电荷数之比为3:4。W−的最外层为8电子结构。金属单质Z在空气中燃烧生成的化合物可
与水发生氧化还原反应。下列说法正确的是
A.X与Y能形成多种化合物,一般条件下都能与Z的最高价氧化物的水化物发生反应
B.原子半径大小:X<Y,Z>W
C.化合物ZY和ZWY 都只存在离子键
2 3
D.Y、W的某些单质或两元素之间形成的某些化合物可作水的消毒剂
【答案】D8.[2016新课标Ⅰ]短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n
是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L–1 r溶液的pH为2,s通常是难
溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是
A.原子半径的大小WX>Y
C.Y的氢化物常温常压下为液态
D.X的最高价氧化物的水化物为强酸
【答案】C
【解析】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的
单质,通常为黄绿色气体,则Z是氯元素,n是Cl;0.01 mol·L–1 r溶液的pH为2,说明r是一元强酸,Cl 与两
2 2
种元素组成的化合物反应会产生两种化合物,其中一种r是HCl,另一种物质q的水溶液具有漂白性,则说明
W是H元素;m是HO,q是HClO;两种元素组成的化合物p与Cl 光照反应产生HCl,同时产生s,s通常是
2 2
难溶于水的混合物,根据转化关系图可知p是甲烷,则s可能是CHCl、CHCl、CHCl 、CCl 中的几种物质。
3 2 2 3 4
因此X是碳元素,Y是氧元素。A.根据元素周期律的原子半径变化规律:同一周期的元素,原子序数越大原
子半径越小,同一主族的元素,原子核外电子层数越多,原子半径越大,则原子半径的大小WZ>X,错误;C.Y元素的氢化物有HO和HO,二者在常温常压下都为液态,正确;D.X
2 2 2
的最高价氧化物的水化物是碳酸,该物质是二元弱酸,不是强酸,错误。学*科网
9.下列说法不正确的是
①质子数相同的粒子一定是同一种元素
②质子数相同且电子数也相同的两种粒子不可能一种是分子,另一种是离子
③电子数相同的粒子不一定是同种元素
④一种元素不可以形成不同的单质
⑤某元素的相对原子质量取整数值就是质量数
A.②④⑤ B.①④⑤ C.②③④ D.①②③④⑤
【答案】B
10.某元素的原子形成的离子可表示为 ,下列说法正确的是
A. 含有的中子数为a+n
B. 含有的电子数为a−n
C. 原子的质量数为a+b+n
D.1个 原子的质量约为 g
【答案】D
【解析】 中a表示质子数,b表示质量数,“n−”表示X原子得到n个电子,则其含有的中子数为b−a,电子数为a+n。1 mol 的质量约为b g,则1个 X原子的质量约为 g。
11.现有五种微粒,分别是 、 、 、 、 ,则它们所属元素的种类有
A.2种 B.3种 C.4种 D.5种
【答案】B
【解析】质子数决定元素的种类。 、 是K元素形成的微粒; 、 是Ca元素形成的微粒; 属
于Ar元素。
12.某粒子用符号 表示,下列关于该粒子的叙述正确的是
A.所含质子数为A−n B.所含中子数为A−Z
C.所含电子数为Z+n D.该粒子比M原子多n个电子
【答案】B
13.我国限制稀有金属对外出口,此举对我国战略安全具有重要意义,稀土元素钕( )是制造导弹合
金材料的重要元素。下列说法中正确的是
A. 和 是同一核素
B.一个 原子的质量约为 g(N 表示阿伏加德罗常数的值)
A
C. 原子的中子数与质子数之差为80
D.14 g 钕元素含有6 mol电子
【答案】B14.下列说法中正确的是
A.随着原子序数的递增,原子的最外层电子数越来越多
B.Li、Be、B的最外层电子数依次增多
C.某元素的原子序数越大,其最外层电子数越多
D.稀有气体元素原子的最外层电子都是8个
【答案】B
【解析】随着原子序数的递增,原子最外层电子的排布呈现周期性变化,即除H、He外,最外层电子数重复出
现从1递增到8的变化,而不是越来越多,A项错误;Li、Be、B的最外层电子数依次增多,B项正确;原子序
数的大小与最外层电子数的多少没有必然关系,C项错误;稀有气体元素原子的最外层电子可能是2个(He)
或8个(其他稀有气体元素),D项错误。
15.下列说法一定不正确的是
A.某些花岗石产生氡( ),从而对人体产生伤害, 的质量数是222
B.Se是人体必需的微量元素, 和 互为同位素
C. 的浓缩一直被国际社会关注, 与 是两种不同的核素
D. -NMR(核磁共振)可用于含碳化合物的结构分析, 的中子数为6
【答案】D
【解析】元素符号左上角的数字表示质量数,A正确;质子数相同,中子数不同的核素,互为同位素,B、C项正
确; 的碳原子中子数为:13-6=7,D项错误。
16.[双选]短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是电子层数的三倍,Y与X可
形成YX 和YX两种离子化合物,Z原子的核外电子数比Y原子多1, W与X同主族,则
2 2 2
A.原子半径:Y< Z < W
B.单质的还原性:Y> ZC.气态氢化物的稳定性:X>W
D.Y和Z两者最高价氧化物对应的水化物能相互反应
【答案】BC
17.某周期ⅡA族元素的原子序数为x,则同周期的ⅢA族元素的原子序数可能为
A.只能是x+1 B.可能是x+10或x+24
C.只能是x+11 D.可能是x+1或x+11或x+25
【答案】D
【解析】如果为第2、3周期,则为x+1;如果为第4、5周期,则为x+11;如果为第6、7周期,则为x+25。
18.元素周期表是学习和研究化学的重要工具。下列是元素周期表的部分信息:
(1)地壳中含量最多的金属元素的原子序数是_________。
(2)分析上表规律,可推知,表中x=__________。
(3) 表示的是(写粒子符号)_________。
(4)写出一个由1、7、17号3种元素组成的常见的化合物的化学式:_________。
【答案】(1)13 (2)16 (3)K+ (4)NH Cl
4
【解析】(1)地壳中含量最多的金属元素是Al,其原子序数为13。(2)由元素周期表可推知x的大小为16。
(3)19号元素为K,核外电子数比核电荷数少1,为K+。(4)l号元素为H,7号元素为N,17号元素为Cl,由1、
7、17号3种元素组成的常见的化合物的化学式为NH Cl。
4
19.用A+、B−、C2−、D、E、F、G和H分别表示含有18个电子的微粒(离子或分子),请回答:
(1)A元素是________,B元素是________,C元素是________(用元素符号表示)。
(2)D是由两种元素组成的双原子分子,其分子式是________。
(3)E是所有含18个电子的微粒中氧化能力最强的分子,其分子式是________。(4)F是由两种元素组成的三原子分子,其分子式是________;电子式是________。
(5)G分子中含有4个原子,其分子式是________。
(6)H分子中含有8个原子,其分子式是________。
【答案】(1)K Cl S (2)HCl (3)F (4)HS
2 2
(5)HO(答PH 也可) (6)C H
2 2 3 2 6
20.已知元素 A、B、C、D、E的结构示意图分别为:
a b c d e
请回答下列问题:
(1)属于同周期的元素是____________(填元素符号,下同),属于同主族的元素____________。
(2)金属性最强的元素是____________,非金属性最强的元素是_______。
(3)上述元素中最高价氧化物对应的水化物碱性最强的是____________。
【答案】(1)Na、Al、Cl F、Cl、Br (2)Na F
(3)NaOH
【解析】(1)弄清原子结构示意图与元素在周期表中的位置关系,即电子层数与周期数相等,所以A、B、C同
周期。主族的族序数与最外层电子数相等,所以B、D、E同主族。(2)同周期从左到右金属性减弱,非金属性
增强;同主族从上到下金属性增强,非金属性减弱。所以Na的金属性最强,F的非金属性最强。(3)金属性越
强,最高价氧化物的水化物碱性越强。
21.[2016海南]短周期元素X、Y、Z、M的原子序数依次增大,元素X的一种高硬度单质是宝石,Y2+电子层结
构与氖相同,Z的质子数为偶数,室温下M单质为淡黄色固体,回答下列问题:
(1)M元素位于周期表中的第______周期、_______族。
(2)Z元素是____,其在自然界中常见的二元化合物是____。
(3)X与M的单质在高温下反应的化学方程式为_________________________,产物分子为直线形,其
化学键属__________共价键(填“极性”或“非极性”)。
(4)四种元素中的____可用于航空航天合金材料的制备,其单质与稀盐酸反应的化学方程式为
________________________________________。【答案】(1)三 ⅥA (2)Si SiO (3)C+2S CS 极性
2 2
(4)Mg Mg+2HCl MgCl +H ↑
2 2
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________
________________________________________________________________________________________