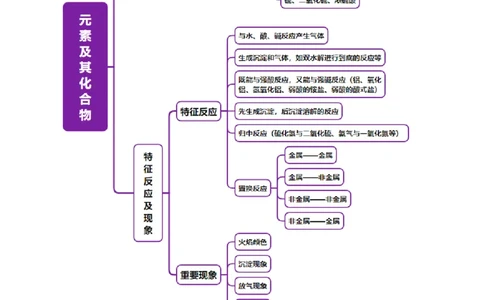
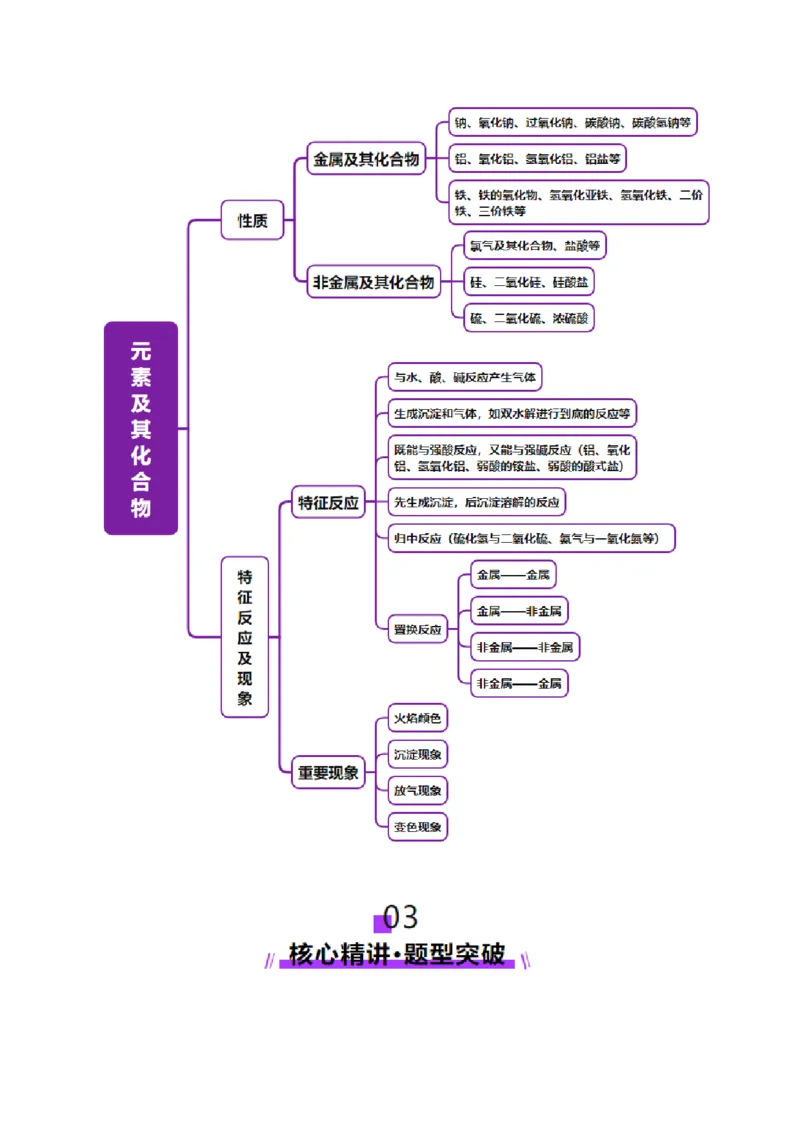
文档内容
专题 01 元素及其化合物的性质与应用
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
题型一 常见无机物的性质与用途...................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.常见金属的性质比较.........................................................................................................................................
2.常见金属的化合物.............................................................................................................................................
3.金属元素及其化合物的重要性质和应用.........................................................................................................
4.常见非金属的性质.............................................................................................................................................
5.常见非金属氧化物的性质.................................................................................................................................
6.常见无机物性质与用途对应关系归纳.............................................................................................................
【命题预测】...........................................................................................................................................................
题型二 常见无机物的性质与转化.....................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】.............................................................................
1.重要元素及其化合物的转化关系..........................................................
2.两种常见金属及其化合物的转化形式......................................................
【命题预测】.............................................................................
考点要求 考题统计 考情分析
常见无机 2024·浙江6月卷,2,3分);2024·山 元素及化合物的性质与应用试题在高考
物的性质 东卷,2,2分;2024·山东卷,5,2 中为必考题型,在各省市及全国卷中均分;2024·浙江6月卷,5,3分;
2024·湖北卷,8,3分;2024·浙江6
与用途 有出现,难度相对简单。元素及化合物
月卷,7,3分;2024·浙江1月卷,
知识,在考查中与基本概念、基本理
7,3分;
论、实验等知识融入越来越深,这也就
要求我们队元素及化合物知识不再是单
纯的记和背了,而是从原理的角度进行
常见无机 2024·江苏卷,10,3分;2024·安徽
掌握,进行整体分析,通过联系、对
物的性质 卷,4,3分;2023•江苏卷,8,3
比、归纳等方法进行解决。
与转化 分;2022•湖南选择性卷,9,3分;题型一 常见无机物的性质与用途
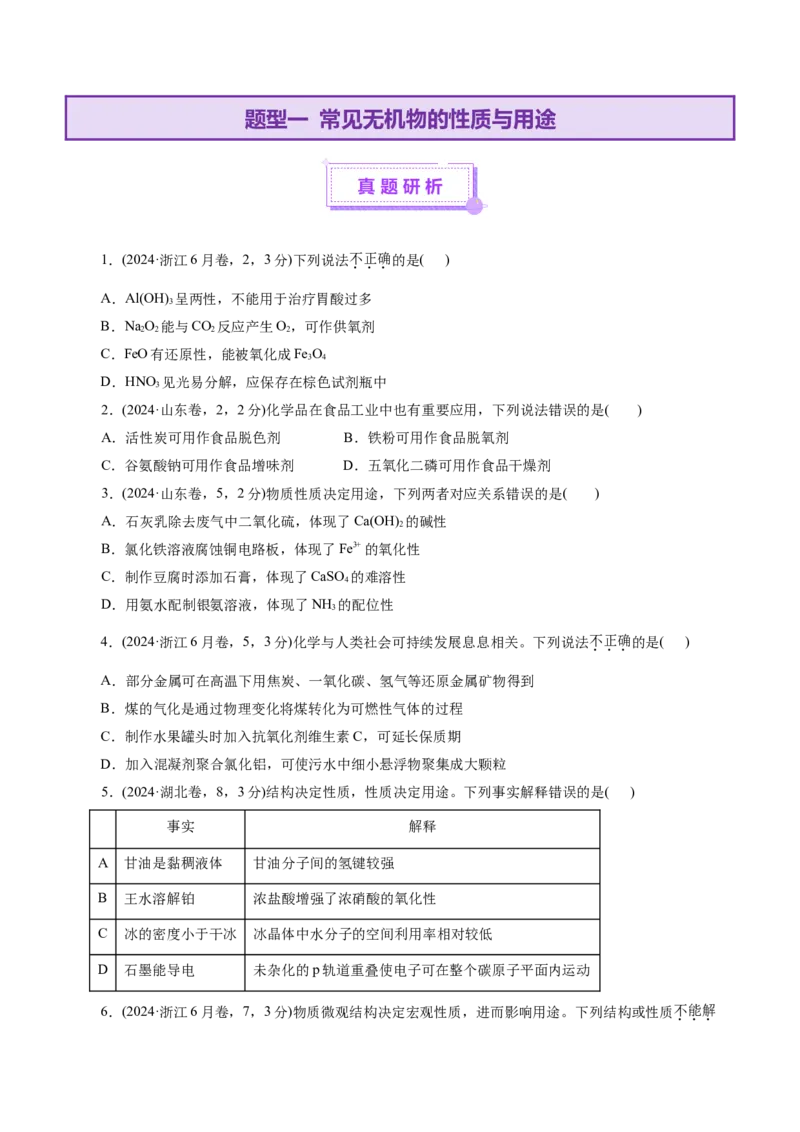
1.(2024·浙江6月卷,2,3分)下列说法不正确的是( )
A.Al(OH) 呈两性,不能用于治疗胃酸过多
3
B.NaO 能与CO 反应产生O,可作供氧剂
2 2 2 2
C.FeO有还原性,能被氧化成Fe O
3 4
D.HNO 见光易分解,应保存在棕色试剂瓶中
3
2.(2024·山东卷,2,2分)化学品在食品工业中也有重要应用,下列说法错误的是( )
A.活性炭可用作食品脱色剂 B.铁粉可用作食品脱氧剂
C.谷氨酸钠可用作食品增味剂 D.五氧化二磷可用作食品干燥剂
3.(2024·山东卷,5,2分)物质性质决定用途,下列两者对应关系错误的是( )
A.石灰乳除去废气中二氧化硫,体现了Ca(OH) 的碱性
2
B.氯化铁溶液腐蚀铜电路板,体现了Fe3+ 的氧化性
C.制作豆腐时添加石膏,体现了CaSO 的难溶性
4
D.用氨水配制银氨溶液,体现了NH 的配位性
3
4.(2024·浙江6月卷,5,3分)化学与人类社会可持续发展息息相关。下列说法不正确的是( )
A.部分金属可在高温下用焦炭、一氧化碳、氢气等还原金属矿物得到
B.煤的气化是通过物理变化将煤转化为可燃性气体的过程
C.制作水果罐头时加入抗氧化剂维生素C,可延长保质期
D.加入混凝剂聚合氯化铝,可使污水中细小悬浮物聚集成大颗粒
5.(2024·湖北卷,8,3分)结构决定性质,性质决定用途。下列事实解释错误的是( )
事实 解释
A 甘油是黏稠液体 甘油分子间的氢键较强
B 王水溶解铂 浓盐酸增强了浓硝酸的氧化性
C 冰的密度小于干冰 冰晶体中水分子的空间利用率相对较低
D 石墨能导电 未杂化的p轨道重叠使电子可在整个碳原子平面内运动
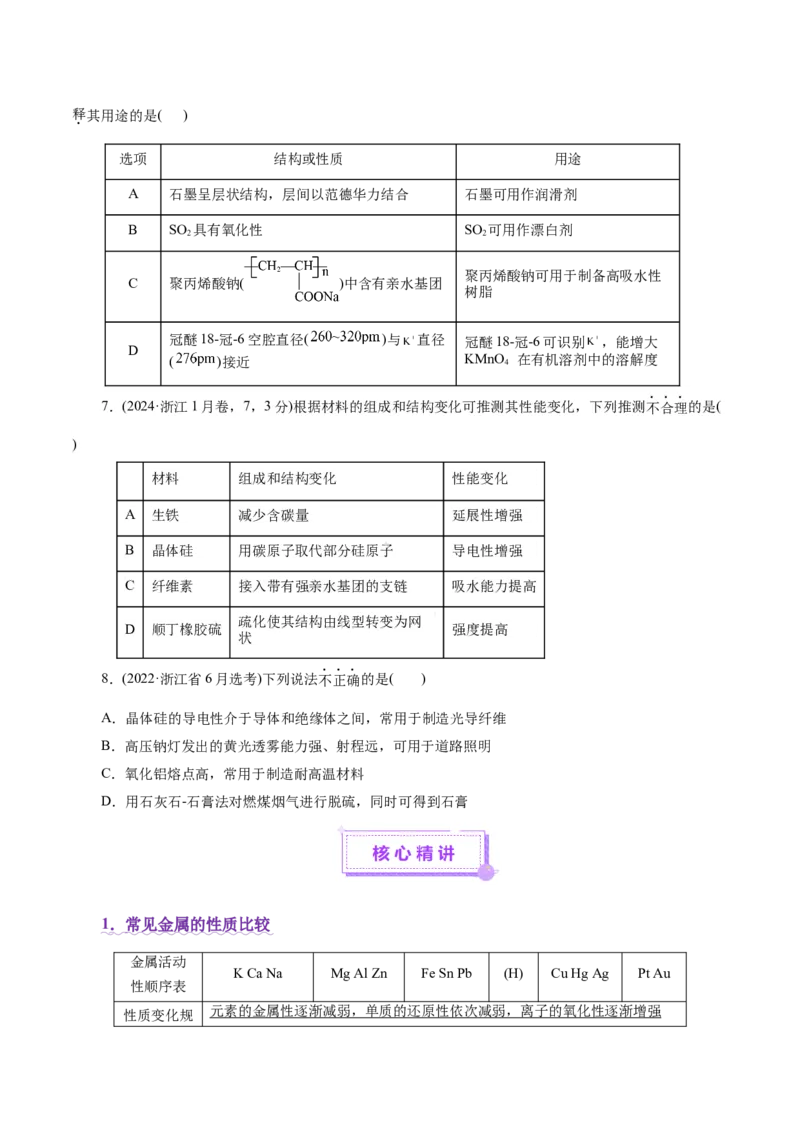
6.(2024·浙江6月卷,7,3分)物质微观结构决定宏观性质,进而影响用途。下列结构或性质不能解释其用途的是( )
选项 结构或性质 用途
A 石墨呈层状结构,层间以范德华力结合 石墨可用作润滑剂
B SO 具有氧化性 SO 可用作漂白剂
2 2
聚丙烯酸钠可用于制备高吸水性
C 聚丙烯酸钠( )中含有亲水基团
树脂
冠醚18-冠-6空腔直径( )与 直径 冠醚18-冠-6可识别 ,能增大
D
( )接近 KMnO 4 在有机溶剂中的溶解度
7.(2024·浙江1月卷,7,3分)根据材料的组成和结构变化可推测其性能变化,下列推测不合理的是(
)
材料 组成和结构变化 性能变化
A 生铁 减少含碳量 延展性增强
B 晶体硅 用碳原子取代部分硅原子 导电性增强
C 纤维素 接入带有强亲水基团的支链 吸水能力提高
疏化使其结构由线型转变为网
D 顺丁橡胶硫 强度提高
状
8.(2022·浙江省6月选考)下列说法不正确的是( )
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明
C.氧化铝熔点高,常用于制造耐高温材料
D.用石灰石-石膏法对燃煤烟气进行脱硫,同时可得到石膏
1 . 常见金属的性质比较
金属活动
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
性顺序表
性质变化规 元素的金属性逐渐减弱,单质的还原性依次减弱,离子的氧化性逐渐增强律
与冷水剧 与沸水缓 高温与水
烈反应 慢反应 蒸气反应
和水的反应 — 不跟水反应
生成氧化
生成碱和氢气
物和氢气
剧烈反应 反应逐渐减缓 不能置换稀酸中的氢
和酸的 与非氧化性酸反应放出H ;与浓硫酸、浓硝 与氧化性
2
— 只溶于
反应 酸及稀硝酸反应,不放出H ,一般产物为: 酸反应(但
2
王水
盐+水+成酸元素的低价化合物 不放出H)
2
金属先与水反
和盐溶液
应生成碱,碱 排在前面的金属可将后面的金属从其盐溶液中置换出来
的反应
再与盐反应
和氧气 常温生成 加热能 加热能 不能被
易被氧化 —
的反应 氧化膜 被氧化 被氧化 氧化
金属氧化物 氧化物跟水剧
对应的水化 烈反应,生成 氧化物不溶于水,也不跟水反应,对应碱的热稳定性逐渐
物及碱的热 碱,碱受热不 减弱
稳定性 易分解
电解法 热还原法 煅烧法 —
金属的 高 温 下 用 CO( 或
冶炼 电解熔融盐或氧化物 Al)从其氧化物中还 — —
原出来
只以游
自然界中存 多以化合态存在,但有极少的游
只以化合态(盐、氧化物)存在 离态存
在的形式 离态
在
2 . 常见金属的化合物
(1)常见金属氧化物
化学式 NaO NaO MgO Al O FeO Fe O Fe O
2 2 2 2 3 2 3 3 4
分 类 碱性氧化物 过氧化物 碱性氧化物 两性氧化物 碱性氧化物碱性氧化物 ——
颜色状态 白色固体 淡黄色固体 白色粉末 白色固体 黑色粉末 红棕色粉末 黑色晶体
反应生成 反应生成 与水缓慢反应
与水作用 不溶于水,也不与水反应
NaOH NaOH和O 生成Mg(OH)
2 2
反应生成钠 反应生成钠 反应生成 反应生成 反应生成 反应生成
与酸作用 盐、水和氧 ——
盐和水 气 镁盐和水 铝盐和水 亚铁盐和水 铁盐和水氧 化 性 除NaO 外氧化性很弱,通常不能用还原剂还原 可用C、CO、Al等还原生成单质铁
2 2
与CO 反应 与CO 生成 与强碱生成 与氧化性酸
其它反应 2 2 与NH Cl溶液 —— ——
生成NaCO NaCO 和O 4 偏铝酸盐 生成铁盐
2 3 2 3 2
(2)常见金属氢氧化物
化学式 NaOH Mg(OH) Al(OH) Fe(OH) Fe(OH) Cu(OH)
2 3 3 2 2
颜色状态 白色固体 白色固体 白色胶状沉淀 红褐色沉淀 白色沉淀 蓝色沉淀
稳定加热 较高温度分解 加热分解成 加热分解成 不稳定易被氧 易分解成CuO
稳 定 性
不分解 成MgO和H 2 O Al 2 O 3 和H 2 O Fe 2 O 3 和H 2 O 化成Fe(OH) 3 和H 2 O
与酸反应 均易与酸反应生成对应的盐,若为氧化性酸则Fe(OH) 还要被氧化
2
与盐反应,与 与NH Cl溶液 与强碱溶液反 新制Cu(OH)
其它反应 4 —— 具有还原性 2
Cl、Al反应 反应 应 被醛基还原
2
(3)重要的盐
盐 NaCO NaHCO FeCl FeCl
2 3 3 2 3
CO+2H+==HO HCO+H+==H O+
2 2
与酸反应 不反应 不反应
+CO↑ CO↑
2 2
HCO+OH-===H O Fe2++2OH- Fe3++3OH-
2
与碱反应 不反应
+CO ==Fe(OH) ↓ ==Fe(OH) ↓
2 3
化
2Fe2++Cl==2Fe3
2
学 氧化还原性 无 无 2Fe3++Fe==3Fe2+
++2Cl-
性
2NaHCO NaCO
质 稳定性 稳定 3 2 3 稳定 稳定
+HO↑+CO↑
2 2
遇KSCN不显血
金属离子检 遇KSCN显血红
焰色反应呈黄色 焰色反应呈黄色 红色,加入氯水
验 色
后显红色
3 . 金属元素及其化合物的重要性质和应用
常见物质 日常应用 利用的性质
钠 核反应堆的传热介质 熔点较低,导热性好
氢氧化钠 制肥皂 与油脂发生皂化反应生成高级脂肪酸钠
调味剂 具有咸味
氯化钠
配制生理盐水(0.9%) 体液替代物
发酵粉、
2NaHCO NaCO+HO+CO↑
碳酸氢钠 膨松剂 3 2 3 2 2
胃酸中和剂 HCO+H+===H O+CO↑
2 2Al (SO )+6NaHCO ===
2 4 3 3
用于泡沫灭火器
2Al(OH) ↓+6CO↑+3NaSO
3 2 2 4
清洗油污 水解,溶液显碱性
碳酸钠
制玻璃 NaCO+SiO NaSiO+CO↑
2 3 2 2 3 2
氧化铝 耐火材料 熔点高
铝制品 表面易生成致密的氧化膜
铝
铝热剂(焊接钢轨) 2Al+Fe O Al O+2Fe(放出大量热量)
2 3 2 3
氢氧化铝 胃酸中和剂 碱性较弱Al(OH) +3H+===Al3++3HO
3 2
在水中生成Al(OH) [或Fe(OH) ]胶体,其可
3 3
明矾、铁盐 净水剂
以和悬浮的泥沙形成絮状不溶物沉降下来
氧化铁 红色油漆和涂料 氧化铁是一种红棕色粉末
硫酸铜 配制农药,杀菌消毒 铜离子(重金属离子)能使蛋白质变性
4 . 常见非金属单质的性质
非金属单质 Cl、Br 、I、O、O、N、H、S、C、Si
2 2 2 2 3 2 2
①气态的有Cl 、O 、O 、N 、H ;固态的有S、C、Si、I ;Br 为液态。
2 2 3 2 2 2 2
物 颜色、状态
②Cl 黄绿色、Br 深红棕色、I 紫黑色、S淡黄色
2 2 2
理
Cl、Br 溶于水;S不溶于水、微溶于酒精、易溶于CS,其他均不易溶于
2 2 2
性 溶解性
水
质]
毒性 Cl、Br 、I 有一定的毒性
2 2 2
①N 放电或高温时反应;②H 、S、C、Si加热或点燃时反应,其他一般
2 2
与O
2
不反应
化
与H ①Cl 光照爆炸;②O 点燃爆炸;③N 在高温高压催化剂条件下反应
2 2 2 2
学
与HO ①Cl、Br 与水反应,既作氧化剂,又作还原剂;②C与水高温下反应
2 2 2
性
与碱 Br 、I 与碱反应,既作氧化剂,又作还原剂
2 2
质
与氧化剂 S、C与强氧化性酸如浓硫酸、浓硝酸反应
与还原剂 Cl、Br 、O、O 与HSO 、NaSO 、HS、NaS、Fe2+、I-等还原剂反应
2 2 2 3 2 3 2 3 2 2
特性及用途 I 使淀粉变蓝、Si作半导体材料
2
5 . 常见非金属氧化物的性质
非金属氧化物 CO、CO、SO 、SO 、NO、NO 、SiO
2 2 3 2 2
色、 ①除 SiO 外,其余均为气体;②除 NO 红棕色外,其他均无色;
2 2
物理
状、味 ③SO 、NO 有刺激性气味;④SO 易液化
2 2 2
性质
毒性 除CO、SiO 外均有毒
2 2
类型 CO、SO 、SO 、SiO 是酸性氧化物;CO、NO、NO 是不成盐氧化物
2 2 3 2 2
化学 与HO ①SO 、SO 、CO 生成相应酸;②NO 生成酸和NO;③SiO 、NO、
2 2 3 2 2 2CO不溶于水
与碱 CO、SO 、SO 、SiO 等酸性氧化物与碱溶液反应生成正盐或酸式盐
2 2 3 2
性质 氧化性 ①SO 能氧化HS;②CO、SiO 能在高温下被C还原
2 2 2 2
①SO 具有较强还原性,能被Cl 、Br 、I 、O 、MnO、Fe3+、HNO 等
2 2 2 2 3 3
还原性
氧化剂氧化为SO;②NO遇空气被氧化为红棕色的NO
2
特性 ①SO 具有漂白性;②SiO 能与氢氟酸反应;③2NO NO
2 2 2 2 4
SO 、NO、NO 、CO均是大气污染物:SO →酸雨、NO、NO →光化学
2 2 2 2
环保
烟雾、CO→有毒气体
6 . 常见无机物性质与用途对应关系归纳
性质 用途
(1) 硅是常用的半导体材料 可作太阳能电池板
二氧化硅导光能力强,并且有硬度和柔韧
(2) 可作光导纤维
度
(3) 4HF+SiO===2H O+SiF↑ 用HF雕刻玻璃
2 2 4
(4) 2C+SiO=====Si+2CO↑ 碳还原二氧化硅制备粗硅
2
(5) 碘酸钾在常温下稳定 食盐中的加碘物质
(6) 氮气的化学性质稳定 作保护气
用浓氨水检验输送氯气的管道是否漏
(7) 浓氨水具有挥发性和还原性
气
(8) 草木灰和硫铵反应生成氨气,使肥效降低 草木灰和硫铵不能混合施用
二氧化硫可用于制作葡萄酒的食品添
(9) 二氧化硫具有还原性
加剂
(10) 氦气化学性质稳定、密度小 可用于填充飞艇、气球
(11) 钠具有较强的还原性 可用于冶炼钛、锆、铌等金属
可用作焙制糕点的膨松剂、胃酸中和
(12) NaHCO 受热分解生成CO,能与酸反应
3 2
剂
(13) NaCO 水解使溶液显碱性 用热的纯碱溶液洗去油污
2 3
(14) NaO 与HO、CO 反应均生成O 作供氧剂
2 2 2 2 2
(15) 肥皂水显碱性 肥皂水作蚊虫叮咬处的清洗剂
(16) 水玻璃不燃不爆 可用作耐火材料
(17) 硅酸钠的水溶液是一种无机黏合剂 盛放碱性溶液的试剂瓶不能用玻璃塞
(18) 锂质量轻、比能量大 可用作电池负极材料
(19) Al具有良好的延展性和抗腐蚀性 常用铝箔包装物品
(20) 铝有还原性,能发生铝热反应 可用于焊接铁轨、冶炼难熔金属
(21) MgO、Al O 的熔点很高 作耐高温材料
2 3
(22) 小苏打与硫酸铝溶液发生双水解反应 可以作泡沫灭火器(23) Al(OH) 有弱碱性 可用于中和胃酸
3
(24) 镁铝合金质量轻、强度大 可用作高铁车厢材料
(25) Fe粉具有还原性 可用于防止食品氧化变质
(26) Fe O 是红棕色粉末 可用作红色颜料
2 3
(27) Cu+2FeCl ===2FeCl +CuCl FeCl 腐蚀Cu刻制印刷电路板
3 2 2 3
(28) CuSO 使蛋白质变性 误服CuSO 溶液,喝蛋清或豆浆解毒
4 4
(29) BaSO 不溶于水,不与胃酸反应 在医疗上用作“钡餐”透视
4
【易错提醒】
(1)CO 通入CaCl 溶液不会产生沉淀。
2 2
(2)高炉炼铁时的还原剂是CO,焦炭的作用是燃烧提供能量和产生CO。
(3)NO 能与水反应生成硝酸,但不是酸性氧化物。
2
(4)SO 和Cl 的混合气体,可能不具有漂白性。
2 2
(5)SO 能使溴水或酸性KMnO 溶液褪色,不是利用SO 的漂白性。
2 4 2
(6)SO 不能漂白石蕊溶液。
2
(7)硅单质可用于制造半导体材料,光导纤维的主要成分是SiO 。
2
(8)Fe、Al能用于盛放浓硝酸是因为“钝化”形成致密的氧化膜,隔离 Fe、Al与硝酸的接
触。
1.下列有关金属及其化合物的说法正确的是( )
A.Na久置于空气中最终生成NaHCO
3
B.金属单质在化学反应中往往体现出还原性
C.铁元素在自然界中都是以化合态形式存在的
D.Al能与任意强酸反应生成H
2
2.[新考法]类推的思维方法在化学学习与研究中经常使用。下列类推结论中正确的是( )
A.NaOH饱和溶液导电能力强,则Ca(OH) 饱和溶液的导电能力也强
2
B.加热时Cu与O 反应生成CuO,则加热时Cu与S反应生成CuS
2
C.BaCl 溶液中通入SO 无沉淀产生,则Ba(NO ) 溶液中通入SO 也无沉淀产生
2 2 3 2 2
D.Al与Fe O 能发生铝热反应,则与MnO 也能发生铝热反应
2 3 2
3.[原创题]物质的性质决定物质的用途。下列说法不正确的是( )
C.二氧化硅具有导光性,可以用作生产光导纤维
A.SO 作为食品添加剂时应注意使用范围和使用的最大限量
2D.苏打和小苏打都是钠盐,均可用作食用碱或工业用碱
D.将氯气通入紫色石蕊溶液中,溶液先变红后褪色,说明氯气具有酸性和漂白性
4.[原创题]下列说法正确的是( )
A.氧化铁在常温下较稳定,常用作油墨和油漆的黑色颜料
B.次氯酸见光易分解,极不稳定,一般情况下只能存在于水溶液中
C.硫化铜具有良好催化活性,一般情况下用金属铜和硫单质加热制成
D.玻璃是重要的建筑材料,其主要由黏土(含水的铝硅酸盐)制成
5.(2025·浙江省天域全国名校协作体高三联考)下列说法不正确的是( )
A.浸泡过KMnO 溶液的硅藻土可作水果的保鲜剂,是利用了它的氧化性
4
B.钠钾合金能用作核反应堆的传热介质,是利用了它熔点低且导热性能好的性质
C.CaCO 是水泥生产中不可缺少的原料,是利用它可以调节水泥的硬化速度
3
D.明矾晶体[KAl(SO )·12H O]可可作净水剂,是利用它能水解形成胶体的性质
4 2 2
6.(2025·浙江省强基联盟高三联考)下列有关物质的结构、性质与用途具有对应关系的是( )
A.在淀粉的主链上再接入带有强亲水基团的支链,可以提高吸水能力
B.浓硫酸具有脱水性,可用浓硫酸干燥SO 、O 等气体
2 2
C.NaO 具有强氧化性,可用作呼吸面具的供氧剂
2 2
D.氮化镓硬度大,可用作半导体材料
7.下列推理正确的是( )
A.铝粉在氧气中燃烧生成Al O,故钠在氧气中燃烧生成NaO
2 3 2
B.铁能从硫酸铜溶液中置换出铜,故钠也能从硫酸铜溶液中置换出铜
C.活泼金属钠保存在煤油中,故活泼金属铝也保存在煤油中
D.钠与氧气、水等反应时钠均作还原剂,故金属单质参与反应时金属单质均作还原剂
8.金属材料在日常生活以及生产中有着广泛的运用。下列关于金属的一些说法中不正确的是( )
A.合金的性质与其成分金属的性质不完全相同
B.工业上金属Mg、Al都是用电解熔融的氯化物制得的
C.金属冶炼的本质是金属阳离子得到电子变成金属原子
D.越活泼的金属越难冶炼
9.C、Si、S都是自然界中含量丰富的非金属元素,下列有关说法中正确的是( )
A.三种元素在自然界中既有游离态又有化合态
B.二氧化物都属于酸性氧化物,都能与碱反应而不能与任何酸反应
C.最低价的气态氢化物都具有还原性,能与O 发生反应
2
D.其最高价氧化物对应水化物的酸性强弱:HSO >HSiO>HCO
2 4 2 3 2 3
10.下列关于常见元素及其化合物的说法正确的是( )
A.NO 与水反应生成硝酸,说明NO 是酸性氧化物
2 2B.SO 能使KMnO 溶液、品红溶液褪色,说明SO 具有漂白性
2 4 2
C.向酸性KMnO 溶液中加入Fe O 粉末,紫色褪去,说明Fe O 中含有+2价Fe
4 3 4 3 4
D.硫与浓HSO 在加热条件下生成SO 和水,说明浓HSO 具有酸性和强氧化性
2 4 2 2 4
11.葡萄酒中常加入亚硫酸盐作为食品添加剂,为检测某葡萄酒样品中亚硫酸盐的含量(通常以酒样中
SO 的量计),某研究小组设计了如下实验(已知还原性:SO 2->I->Cl-)。下列说法不正确的是
2 3
A.葡萄酒中加亚硫酸盐的主要目的是防止氧化,利用了亚硫酸盐的还原性
B.通入N 和煮沸的目的是为了将产生的气体从溶液中全部赶出
2
C.若试剂A选择氯水,则试剂B可选择NaOH标准液
D.若试剂A选择碱液,调节吸收后溶液为中性,则试剂B可选择I 标准液
2
题型二 常见无机物的性质与转化
1.(2024·江苏卷,10,3分)在给定条件下,下列制备过程涉及的物质转化均可实现的是( )
A.HCl制备:NaCl溶液 和
B.金属Mg制备: 溶液
C.纯碱工业: 溶液
D.硫酸工业:
2.(2024·安徽卷,4,3分)下列选项中的物质能按图示路径在自然界中转化。且甲和水可以直接生成
乙的是( )
选项 甲 乙 丙A Cl NaClO NaCl
2
B SO HSO CaSO
2 2 4 4
C Fe O Fe(OH) FeCl
2 3 3 3
D CO HCO Ca(HCO )
2 2 3 3 2
3.(2021•辽宁选择性考试)含S元素的某钠盐a能发生如图转化。下列说法错误的是( )
A.a可能为正盐,也可能为酸式盐 B.c为不溶于盐酸的白色沉淀
C.d为含极性键的非极性分子 D.反应②中还可能生成淡黄色沉淀
一审:审清题意,从题干→问题→框图迅速浏览一遍,尽量在框图中把相关信息表示出来。
二找:找“题眼”即找到解题的突破口。“题眼”主要有:物质的特殊颜色、特征反应现象、特殊反
应条件、特征转化关系、特征数据等。
三析:从题眼出发,联系新信息及所学的旧知识,大胆猜测,顺藤摸瓜,应用正逆向思维、横向纵向
思维等多种思维方式进行综合分析、推理,初步得出结论。
四验:验证确认,将结果放入原题检验,完全符合才算正确。
五答:按题目要求写出答案。
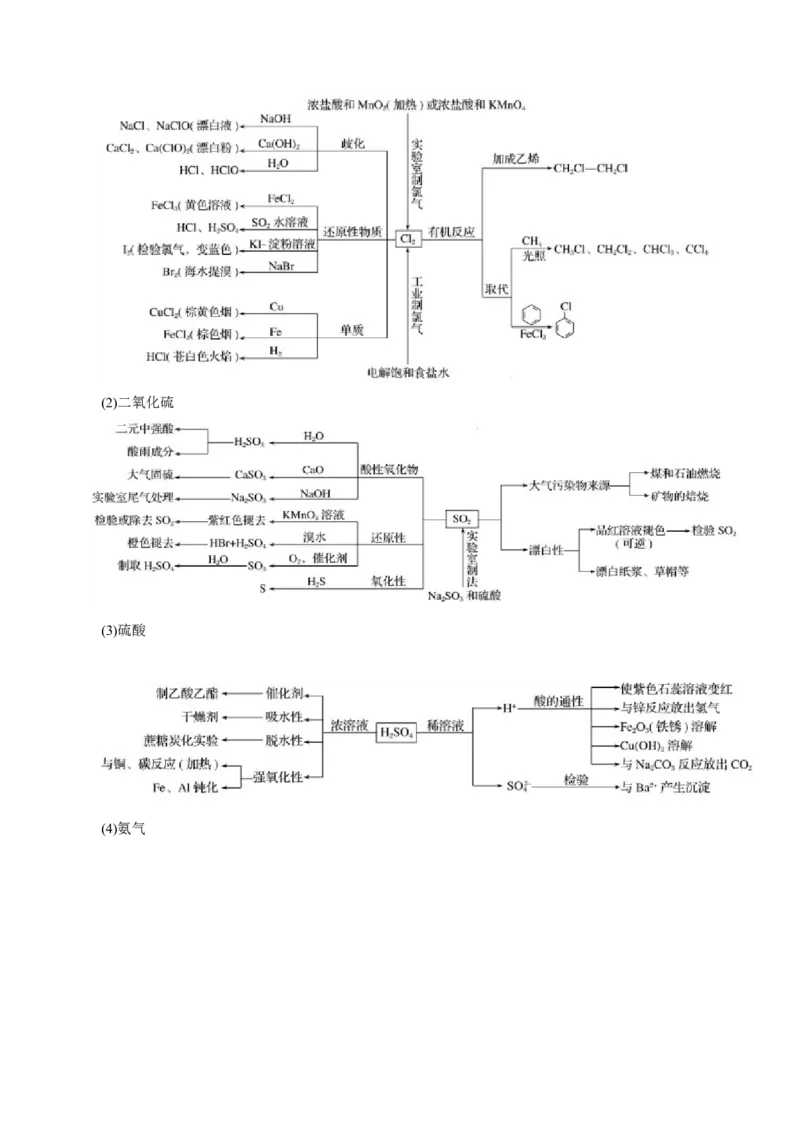
1 .重要元素及其化合物的转化关系
(1)氯气(2)二氧化硫
(3)硫酸
(4)氨气(5)硝酸
(6)二氧化硅
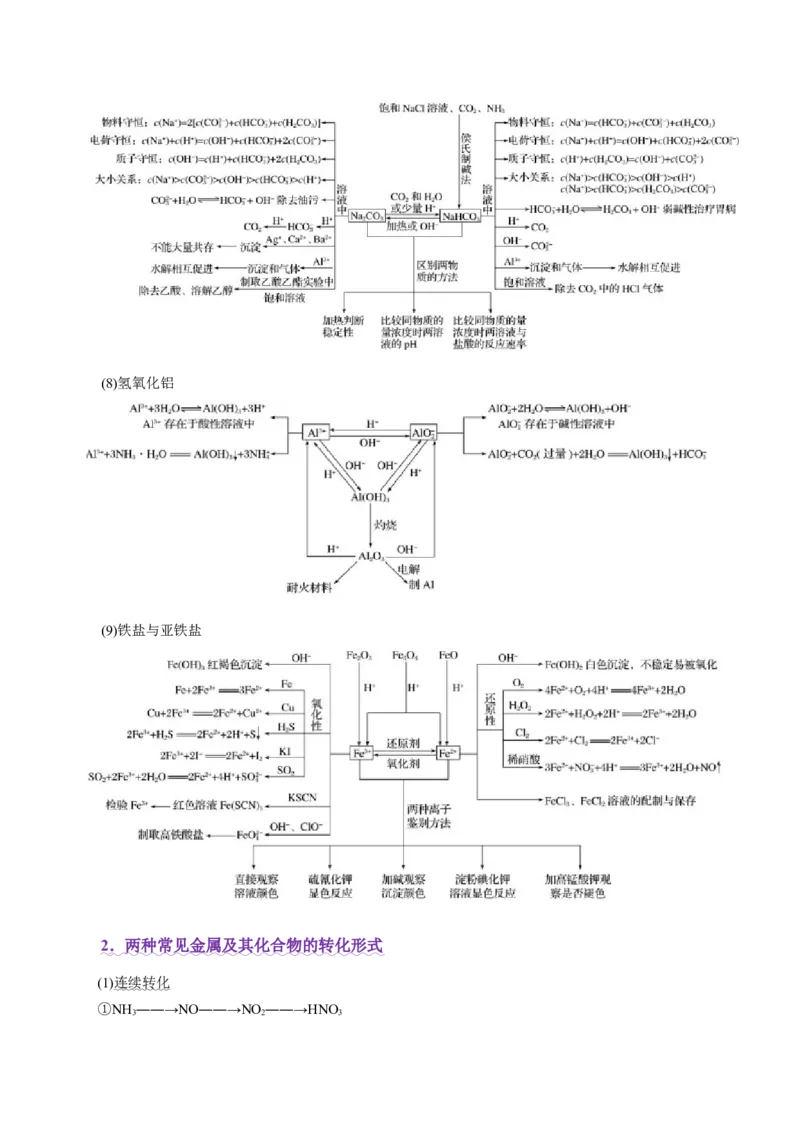
(7)碳酸钠与碳酸氢钠(8)氢氧化铝
(9)铁盐与亚铁盐
2 . 两种常见金属及其化合物的转化形式
(1)连续转化
①NH ――→NO――→NO ――→HNO
3 2 3②HS(S)――→SO ――→SO ――→HSO ;
2 2 3 2 4
③C――→CO――→CO――→HCO;
2 2 3
④Na――→NaO――→NaO――→NaOH。
2 2 2
(2)A――→B――→C转化模式
①A为N、S、C、Na、NH 、HS、CH,D为O。
2 3 2 4 2
②A为Cl,D为Fe,B为FeCl ,C为FeCl 。
2 3 2
③A为Al3+,D为OH-,B为Al(OH) ,C为AlO。
3
④A为AlO,D为H+,B为Al(OH) ,C为Al3+。
3
⑤ A为P,D为Cl,B为PCl ,C为PCl 。
2 3 5
⑥ A为O,D为C,B为CO,C为CO。
2 2
⑦A为CO,D为H+,B为HCO,C为CO。
2
⑧A为SO,D为H+,B为HSO,C为SO 。
2
1.(2025· 江浙皖高中发展共同体高三联考)在给定条件下,下列选项所示的物质间转化均能实现的是(
)
A.N NO HNO
2 3
B.MnO Cl 漂白粉
2 2
C.黄铁矿 SO 硫酸
3
D.CuSO (aq) Cu(OH) Cu O
4 2 2
2.在给定的条件下,下列选项所示的物质间转化均能一步实现的是
A. B.
C. D.
3.[原创题]在指定条件下,下列选项所示的物质间的转化能实现的是( )
A.NO N B.
2
C. D.
4.利用自然资源制备相关化学物质,下列化学工艺不可行的是( )A.提取食盐后母液 含Br 的液体 粗溴 纯溴
2
B.石英砂 粗硅 粗四氯化硅 高纯硅
C.FeS SO HSO HSO
2 2 2 3 2 4
D.铝土矿 Na[Al(OH)]溶液 Al(OH) Al O 铝
4 3 2 3
5.[原创题]下列关于置换反应A+X→B+Y(其中A、B为单质,X和Y为化合物,反应条件已略去)
的描述中,正确的是( )
A.若X是氧化物,则Y也一定是氧化物
B.若X为不含有金属元素的化合物,则B一定是一种非金属单质
C.若A为金属单质,则B一定为一种非金属单质
D.若X为含有金属元素的化合物,则Y一定是一种含有金属元素的化合物
6.[原创题]联氨(N H)可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,其中一种反应机理如图所示。
2 4
下列叙述正确的是( )
A.过程①②③均为氧化还原反应
B.根据过程①,每生成448mLN ,消耗6.4gCuO
2
C.根据上述过程可推知氧化性:O>CuO>Cu O
2 2
D.1 mol N H 可处理锅炉水中0.5 mol O
2 4 2
7.[原创题]已知X、Y、Z、M、N五种常见物质含有同一元素,在一定条件下它们有如下转化关系。
下列推断不合理的是( )
A.若Z为NO,则X可能是N
2
B.若N为HSO ,则Y可能是HS或是单质S
2 4 2
C.若X为单质Fe,N为硫酸盐,则Z可以是FeCl 或FeCl
2 3
D.若Z为NO、X为HO、Y为单质,则Y生成Z的反应一定是化合反应
2
8.[原创题]化合物M(NHCuSO )为难溶于水的白色固体,取少量M进行如下实验,下列推断不正确
4 3
的是( )A.化合物M中Cu的化合价为+1价 B.固体(A)为氧化铜
C.气体G极易溶于水,F能溶于其中 D.加热H会变红色
9.已知甲、乙、丙三种物质均含有同种元素X,其转化关系如下:
的
下列说法错误 是( )
A.若A为NaOH溶液,乙为白色沉淀,则X可能为短周期金属元素
B.若A为硝酸,X为金属元素,则甲与乙反应可生成丙
C.若A为氧气,丙在通常状况下为红棕色气体,则甲可能为非金属单质
D.若乙为NaHCO ,则甲或丙可能是CO
3 2
10.无机物X、Y、Z、M的相互转化关系如图所示(部分反应条件、部分反应中的H.,O已略去)。
X、Y、Z均含有同一种元素。下列说法正确的是( )
A.若X是氢氧化钠,则M不一定为CO
2
B.若Y具有两性,则M的溶液只可能显碱性
C.若Z是导致酸雨的主要气体,则X一定是HS
2
D.若M是用途最广的金属,加热蒸干Y的溶液一定能得到Y
11.元素X的单质及X与元素Y形成的化合物存在如图所示的关系(其中m≠n,且均为正整数).下列
说法正确的是( )
A.X一定是金属元素
B.(n-m)一定等于1
C.由X生成1molXY 时转移的电子数目一定为4N
m A
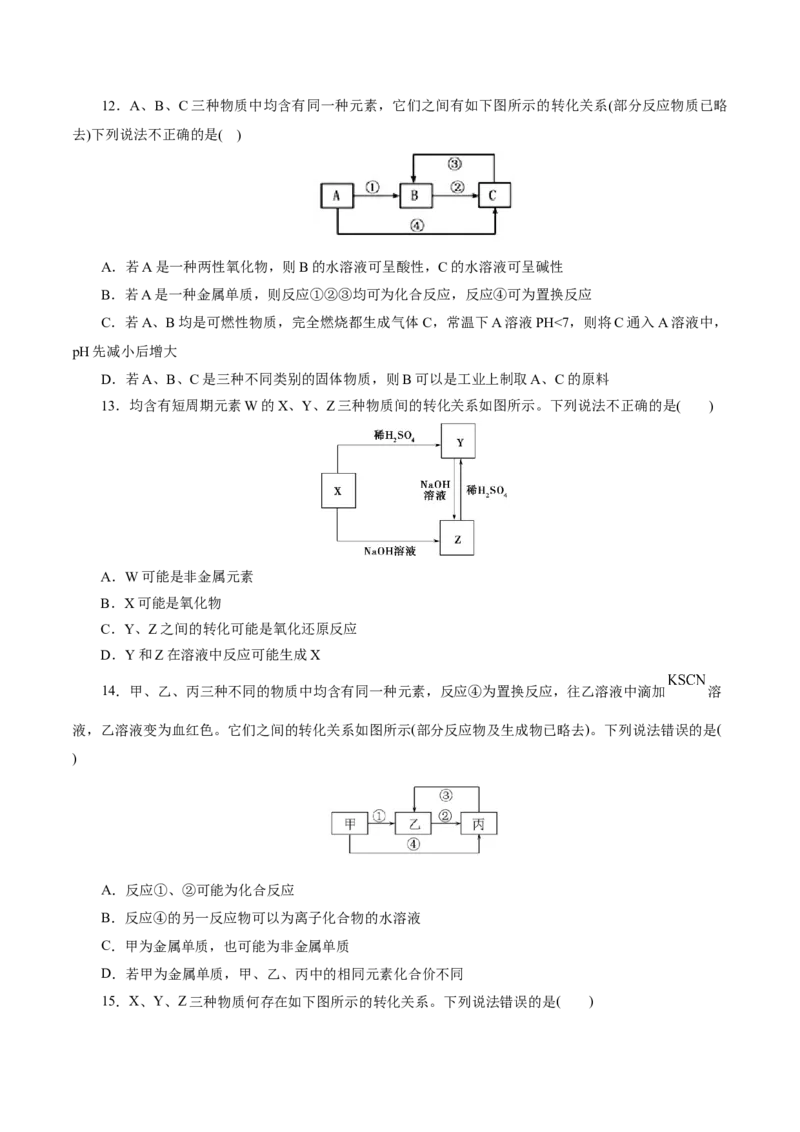
D.三个化合反应一定都是氧化还原反应12.A、B、C三种物质中均含有同一种元素,它们之间有如下图所示的转化关系(部分反应物质已略
去)下列说法不正确的是( )
A.若A是一种两性氧化物,则B的水溶液可呈酸性,C的水溶液可呈碱性
B.若A是一种金属单质,则反应①②③均可为化合反应,反应④可为置换反应
C.若A、B均是可燃性物质,完全燃烧都生成气体C,常温下A溶液PH<7,则将C通入A溶液中,
pH先减小后增大
D.若A、B、C是三种不同类别的固体物质,则B可以是工业上制取A、C的原料
13.均含有短周期元素W的X、Y、Z三种物质间的转化关系如图所示。下列说法不正确的是( )
A.W可能是非金属元素
B.X可能是氧化物
C.Y、Z之间的转化可能是氧化还原反应
D.Y和Z在溶液中反应可能生成X
14.甲、乙、丙三种不同的物质中均含有同一种元素,反应④为置换反应,往乙溶液中滴加 溶
液,乙溶液变为血红色。它们之间的转化关系如图所示(部分反应物及生成物已略去)。下列说法错误的是(
)
A.反应①、②可能为化合反应
B.反应④的另一反应物可以为离子化合物的水溶液
C.甲为金属单质,也可能为非金属单质
D.若甲为金属单质,甲、乙、丙中的相同元素化合价不同
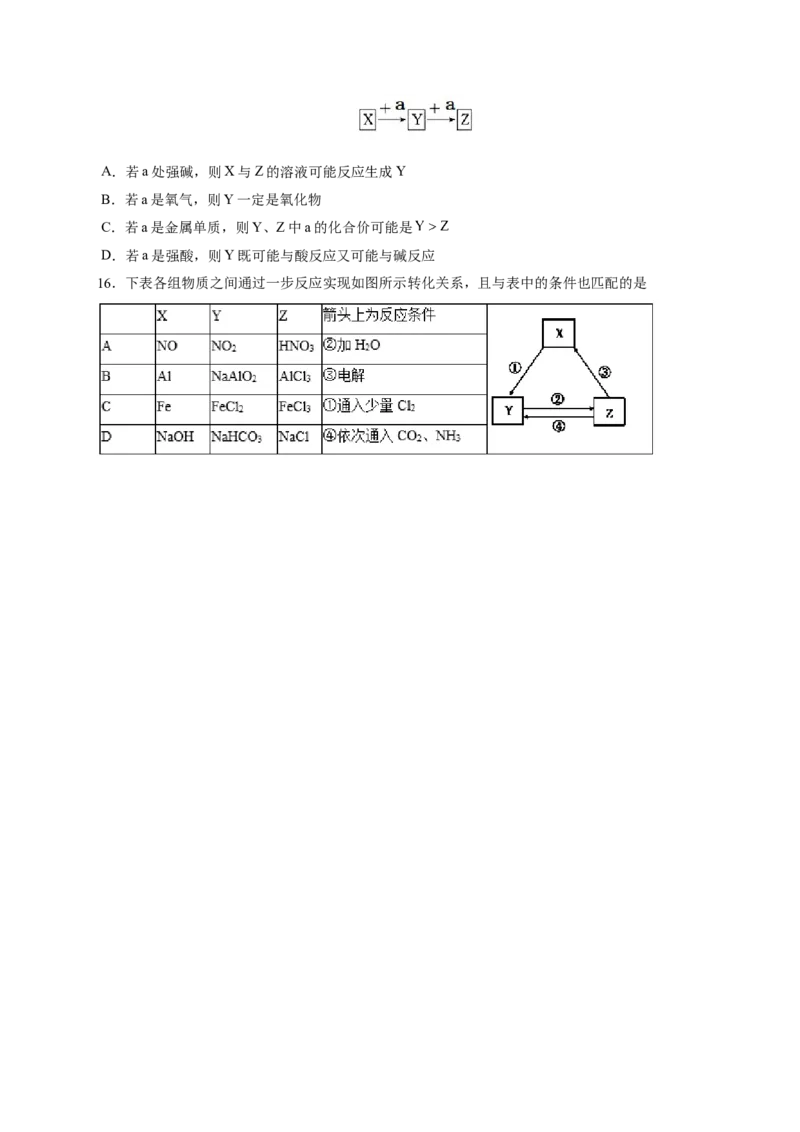
15.X、Y、Z三种物质何存在如下图所示的转化关系。下列说法错误的是( )A.若a处强碱,则X与Z的溶液可能反应生成Y
B.若a是氧气,则Y一定是氧化物
C.若a是金属单质,则Y、Z中a的化合价可能是
D.若a是强酸,则Y既可能与酸反应又可能与碱反应
16.下表各组物质之间通过一步反应实现如图所示转化关系,且与表中的条件也匹配的是